榄香烯对肿瘤恶病质小鼠细胞因子TNF-ɑ IL-6和骨骼肌UPP信号通路的调节作用*
尹爱凝 李宏林 姚娓
肿瘤恶病质(cancer cachexia,CC)是肿瘤患者的常见并发症,其主要表现为不可逆的体质量下降,伴随骨骼肌萎缩。肿瘤恶病质的临床诊断标准为肿瘤患者的体质量下降超过5%、身体质量指数(BMI)<20 kg/m2的患者体重下降超过2%[1]。据估计,在病程后期,60%~80%的肿瘤患者会有恶病质的表现[2],至少20%肿瘤患者的直接死亡原因是肿瘤引起的恶病质[3]。骨骼肌萎缩是肿瘤恶病质的核心症状,骨骼肌质量下降和肿瘤患者生存质量下降明显相关[4],体质量下降,低肌肉质量是肿瘤患者预后不佳的标志,其与总的体重无关[5],减轻骨骼肌萎缩是肿瘤恶病质的重要治疗目标。榄香烯是中药莪术的有效活性成分,具有明显的抗癌活性,可以通过促进肿瘤细胞凋亡以抑制肿瘤细胞增殖[6-7],但目前关于榄香烯对肿瘤恶病质是否有治疗效果鲜见报道,本研究通过构建肿瘤恶病质小鼠模型,检测榄香烯对肿瘤恶病质骨骼肌萎缩的保护作用以及可能的作用机制。
1 材料与方法
1.1 材料
1.1.1 细胞株与动物 小鼠Lewis 肺腺癌肿瘤细胞(Lewis lung cancer,LLC),由上海富恒公司提供;健康雄性SPF 级C57BL/6 小鼠40 只,9 周龄,体重(22±2)g,由大连医科大学动物实验中心提供(合格证号SYXK(辽)2018-0007)。
1.1.2 药物 醋酸甲地孕酮为甲地孕酮纯单体粉末,美国Aladdin公司生产,用蒸馏水配置成浓度为4 mg/mL悬浊液。榄香烯口服乳,批号:H20010338,由大连华立金港药业有限公司生产。置于4℃冰箱备用。
1.1.3 主要试剂及仪器 兔来源一抗MAFBx、MURF-1、β-actin 及二抗均购于中国ABclonal 公司,Western blot 相关试剂盒购于中国Solarbio 公司,白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)酶联免疫吸附(ELISA)试剂盒购于武汉云克隆公司。
1.2 方法
1.2.1 细胞培养 用含有10%胎牛血清和1%青霉素-链霉素双抗的DMEM 高糖培养基将LLC 细胞培养于37℃、CO2体积分数为5%的恒温培养箱中,根据细胞生长情况换液,2~3天进行扩增培养。
1.2.2 小鼠造模 将LLC细胞接种于10 cm平皿,扩增至80%融合后收集细胞,用胰酶消化细胞成单个,细胞计数板计算细胞个数,PBS溶液将LLC细胞浓度调整为1×107/mL,予小鼠右前腋背部皮下接种LLC细胞悬浊液0.2 mL,每天观察肿瘤生长情况,第12 天时,肉眼已可见到小鼠右侧胁肋部肿瘤,小鼠体重和饮食量出现明显下降,根据相关文献提示小鼠进入恶病质状态[8],说明荷瘤模型已建立,开始进行药物治疗。
1.2.3 实验分组及给药 40 只小鼠,通过随机数字表法将其分为健康组、恶病质模型组、醋酸甲地孕酮组、榄香烯组,每组10只。健康组和恶病质模型组小鼠分别给予生理盐水0.2 mL/只灌胃;醋酸甲地孕酮组给予醋酸甲地孕酮溶液0.2 mL/只灌胃(给药剂量以160 mg/kg 计,用生理盐水稀释,浓度4 mg/mL);榄香烯组给予榄香烯口服乳0.2 mL/只灌胃(给药剂量以60 mL/kg计,将榄香烯口服乳用生理盐水稀释1.67倍。每天1 次,连续给药2 周。第14 天后,眼眶取血后处死小鼠,完整剥离皮下移植瘤、腓肠肌及胫骨前肌,完整摘取肝脏。
1.2.4 检测指标及方法 1)饮食量、肿瘤重量、去瘤体重、腓肠肌加胫骨前肌总重量和肝脏重量。在治疗过程中,每天记录小鼠的饮食量。给药14天后,处死小鼠剥离皮下移植瘤,称量小鼠的瘤重及去瘤体重。完整分离腓肠肌及胫骨前肌,并称量其重量。完整摘除肝脏,滤纸吸取表面液体,称取重量,计算肝脏重量占去瘤体重的百分比。
2)HE 染色观察腓肠肌肌丝横截面积形态学变化。分离小鼠腓肠肌后,放入4%多聚甲醛固定。将小鼠腓肠肌依次放入梯度酒精(75%乙醇、80%乙醇、95%浓度乙醇、无水乙醇Ⅰ、Ⅱ)进行脱水,之后放入二甲苯对脱水后的组织进行透明,用石蜡包埋机将肌肉组织进行包埋。包埋结束后进行切片、烤片、脱蜡,进行苏木伊红染色。在光学显微镜下观察各组小鼠腓肠肌肌丝横截面积,并使用Image J 软件进行分析。
3)酶联免疫吸附法(ELISA)检测IL-6 和TNF-ɑ含量。小鼠眼眶取血后,室温避光静置1~2 h,4℃离心,2 500 r/min,30 min,取上清,-80℃保存。按照ELISA试剂盒说明书进行操作,使用酶标仪在450 nm波长处测定其吸光度(OD)。根据标准孔OD值,绘制标准曲线,计算血清样本中TNF-α和IL-6的含量。
4)蛋白质印迹法(Western blot)检测肌肉环状指基因(muscle ring finger 1,MURF-1)、肌肉萎缩盒F基因(muscle atrophy F-box,MAFbx)蛋白表达。取冻存的小鼠腓肠肌组织,提取总蛋白,BCA 法测定蛋白浓度,将样品蛋白浓度调整到均一值,制备蛋白样品。配制10%SDS-PAGE 分离胶,每个泳道上样蛋白50 μg,将蛋白电转到PVDF 膜上。5%的脱脂奶粉室温封闭1 h,兔单克隆抗体MAFBx(1:1 500)、MURF1(1:1 500)、β-actin(1:5 000)4℃孵育过夜。次日,TBST洗膜后,羊抗兔二抗(1:5 000)室温孵育1 h。TBST洗膜,ECL化学发光法显色。条带密度使用Image J软件进行分析。
1.3 统计学处理
采用SPSS 26.0 软件进行统计学分析,组间差异分析采用单因素方差分析,实验结果用()表示,以P<0.05为差异具有统计学意义。
2 结果
2.1 各组小鼠的肿瘤重量、去瘤体重、腓肠肌加胫骨前肌总重量比较
在给药过程中,健康组、恶病质模型组和榄香烯组小鼠各出现1 只死亡。榄香烯组小鼠的肿瘤重量低于恶病质模型组和醋酸甲地孕酮组,但差异无统计学意义(P>0.05)。相对于健康组,恶病质模型组小鼠的去瘤体重及腓肠肌加胫骨前肌总重量显著下降(P<0.05),出现了毛发粗糙、活动量少等恶病质表现;榄香烯组小鼠的去瘤体重、腓肠肌加胫骨前肌总重量较醋酸甲地孕酮组和恶病质模型组小鼠均有所上升,较恶病质模型组上升显著(P<0.05,表1)。
表1 各组小鼠肿瘤重量及去瘤体重、腓肠肌加胫骨前肌总重量 (±s)
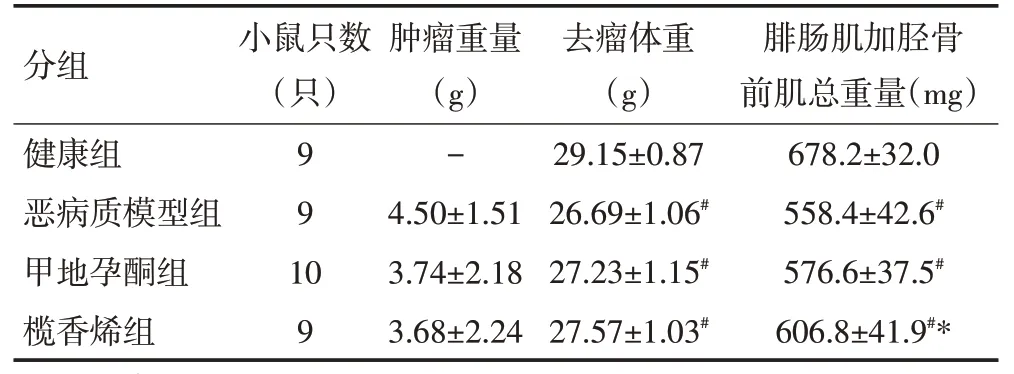
表1 各组小鼠肿瘤重量及去瘤体重、腓肠肌加胫骨前肌总重量 (±s)
#:与健康组比较,P<0.05;*:与恶病质模型组比较,P<0.05
分组健康组恶病质模型组甲地孕酮组榄香烯组小鼠只数(只)9 9 1 0 9肿瘤重量(g)-4.50±1.51 3.74±2.18 3.68±2.24去瘤体重(g)29.15±0.87 26.69±1.06#27.23±1.15#27.57±1.03#腓肠肌加胫骨前肌总重量(mg)678.2±32.0 558.4±42.6#576.6±37.5#606.8±41.9#*
2.2 各组小鼠腓肠肌肌丝横截面积比较
健康组小鼠腓肠肌肌丝横截面积大且较为均匀。相对于健康组,恶病质模型组、醋酸甲地孕酮组、榄香烯组小鼠肌丝横截面积均有不同程度的缩小(P<0.05);榄香烯组小鼠肌丝横截面积相对于恶病质模型组有较大升高,且高于醋酸甲地孕酮组,差异均有统计学意义(均P<0.05,表2)。
表2 各组小鼠的腓肠肌肌丝横截面积 (±s)
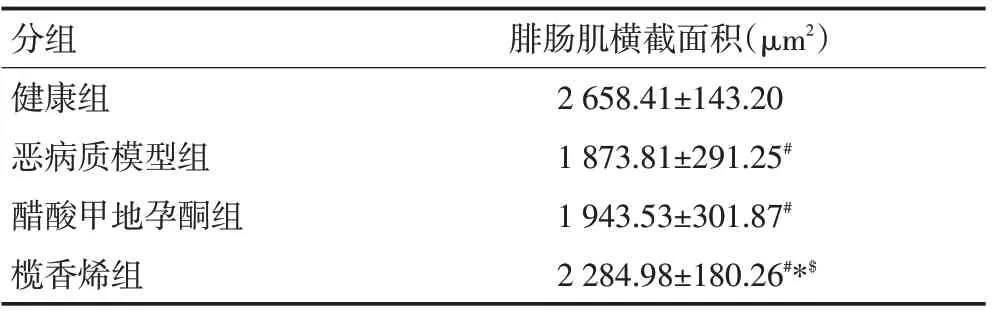
表2 各组小鼠的腓肠肌肌丝横截面积 (±s)
#:与健康组比较,P<0.05;*:与恶病质模型组比较,P<0.05;$:与醋酸甲地孕酮组比较,P<0.05
分组健康组恶病质模型组醋酸甲地孕酮组榄香烯组腓肠肌横截面积(μm2)2 658.41±143.20 1 873.81±291.25#1 943.53±301.87#2 284.98±180.26#*$
2.3 各组小鼠的饮食量及肝脏重量占去瘤体重的比例比较
与健康组相比,恶病质模型组小鼠的饮食量明显下降(P<0.05),但其肝脏重量占去瘤体重的百分比明显上升(P<0.05);醋酸甲地孕酮组小鼠的饮食量明显增加,甚至高于健康组,其肝脏重量占去瘤体重的百分比高于恶病质模型组(P<0.05);榄香烯组小鼠的饮食量和恶病质模型组相近,其肝脏重量占去瘤体重的百分比较恶病质模型组和甲地孕酮组均有所减少(P<0.05,表3)。
表3 各组小鼠的饮食量及肝脏重量占去瘤体重的百分比(±s)
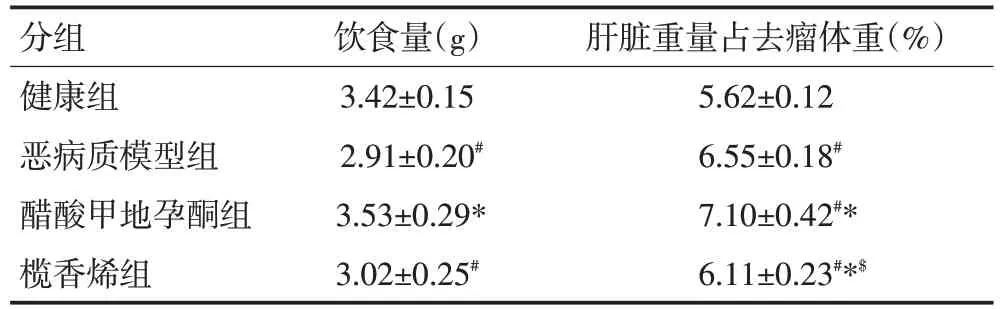
表3 各组小鼠的饮食量及肝脏重量占去瘤体重的百分比(±s)
#:与健康组比较,P<0.05;*:与恶病质模型组比较,P<0.05;$:与醋酸甲地孕酮组比较,P<0.05
分组健康组恶病质模型组醋酸甲地孕酮组榄香烯组饮食量(g)3.42±0.15 2.91±0.20#3.53±0.29*3.02±0.25#肝脏重量占去瘤体重(%)5.62±0.12 6.55±0.18#7.10±0.42#*6.11±0.23#*$
2.4 小鼠血清IL-6和TNF-α含量
恶病质模型组、醋酸甲地孕酮组和榄香烯组小鼠血清IL-6 和TNF-α 含量较健康组明显升高(P<0.05);榄香烯组小鼠血清IL-6和TNF-α含量相对于恶病质模型组和醋酸甲地孕酮组明显下降,差异均具有统计学意义(均P<0.05,表4,图1)。
表4 各组小鼠血清细胞因子IL-6和TNF-α含量 (±s)

表4 各组小鼠血清细胞因子IL-6和TNF-α含量 (±s)
#:与健康组比较,P<0.05;*:与恶病质模型组比较,P<0.05;$:与醋酸甲地孕酮组比较,P<0.05
分组健康组恶病质模型组醋酸甲地孕酮组榄香烯组IL-6(ng/L)43.58±4.33 162.23±19.63#159.45±19.71#117.83±15.37#*$TNF-α(ng/L)68.29±7.51 125.56±14.59#116.23±13.57#93.69±9.20#*$
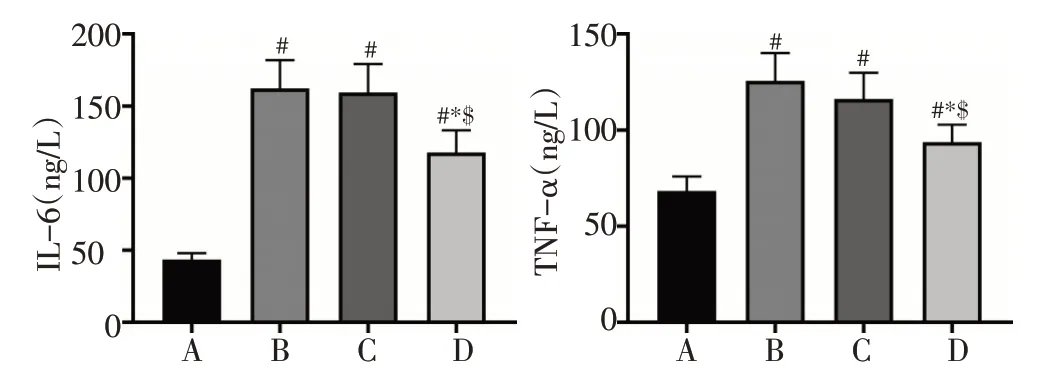
图1 各组小鼠血清IL-6和TNF-ɑ表达水平
2.5 小鼠腓肠肌组织中MAFBx、MURF-1 蛋白表达水平
相对于健康组,恶病质模型组小鼠的腓肠肌中MAFBx、MURF-1 蛋白表达水平明显升高(P<0.05);醋酸甲地孕酮组小鼠腓肠肌组织中的MAFBx蛋白表达水平略高于恶病质模型组,而其MURF-1蛋白表达水平较恶病质模型组降低;榄香烯组腓肠肌中MAF⁃Bx、MURF-1蛋白表达水平相对于恶病质模型组和甲地孕酮组有一定程度下降,且具有统计学意义(P<0.05)(图2)。
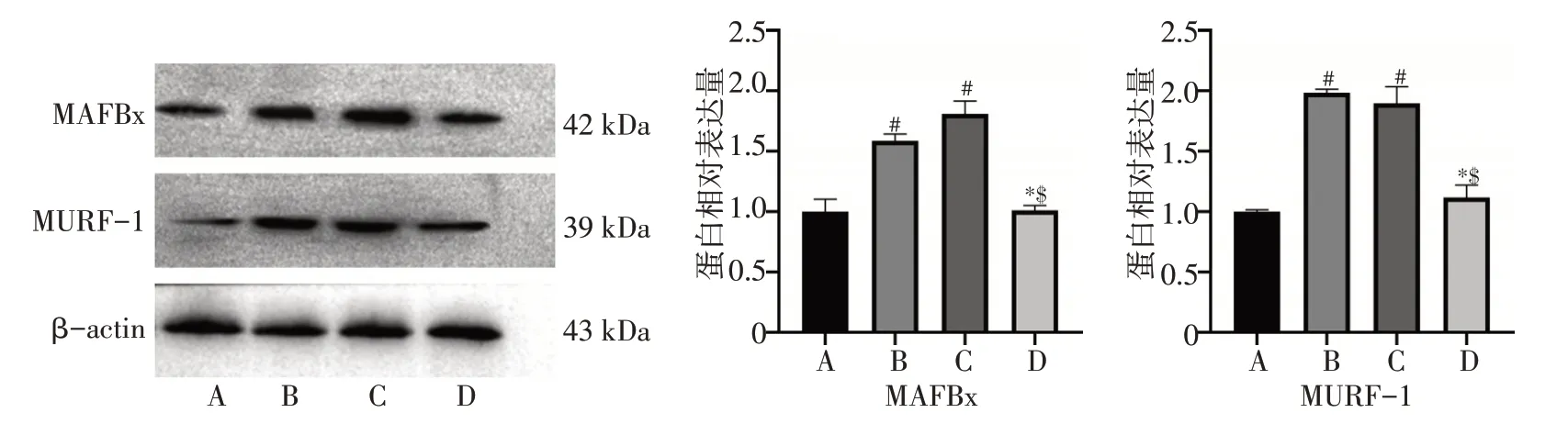
图2 各组小鼠腓肠肌的MAFBx、MURF-1蛋白表达水平
3 讨论
肿瘤恶病质是肿瘤患者常见的并发症,骨骼肌萎缩是肿瘤恶病质的核心症状。本研究在治疗过程中,因灌胃操作不当,健康组小鼠出现1只死亡;恶病质模型组和榄香烯组小鼠在疾病治疗后期,因肿瘤生长速度过快,小鼠的饮食及呼吸受到明显抑制,各出现1只死亡。给药结束时,各组小鼠样本量为9例或10例,差异无统计学意义。研究结果表明,榄香烯组小鼠肿瘤重量低于恶病质模型组及醋酸甲地孕酮组,榄香烯组小鼠的去瘤体重和腓肠肌加胫骨前肌总重量相对于恶病质模型组有一定程度上升,且高于醋酸甲地孕酮组;同时榄香烯组腓肠肌肌丝横截面积相对于恶病质模型组及醋酸甲地孕酮组明显升高,提示榄香烯缓解肿瘤恶病质骨骼肌萎缩效果优于醋酸甲地孕酮。
肿瘤恶病质是一种慢性消耗性疾病,厌食引起的能量摄入减少与异常代谢引起的能量消耗增加导致肿瘤患者负向的能量平衡,是导致肿瘤恶病质的直接原因[9-10]。本研究中,恶病质模型组小鼠的饮食量相对于健康组显著下降,恶病质模型组小鼠的能量摄入减少。研究发现,醋酸甲地孕酮作为一种食欲刺激药,可增加癌症患者的体质量、提高食欲,但其具有增加死亡、水肿、呼吸困难和深静脉血栓形成等不良反应[11-12]。本研究结果显示,醋酸甲地孕酮能明显增加肿瘤恶病质小鼠的饮食量,其饮食量甚至高于健康组,而榄香烯在增加肿瘤恶病质小鼠的饮食摄入量方面低于醋酸甲地孕酮。在能量消耗方面,人体能量消耗包括静息能量消耗、活动能量消耗和饮食生热,占人体总的能量消耗的比例分别为60%:75%,20%:30%和10%[13],静息能量消耗是人体能量消耗的主要成分[14-15]。肝脏、大脑、心脏、肾脏占人体体质量的7%,占人体静息能量代谢的58%,是高代谢器官;而骨骼肌占人体体质量的50%,仅占人体静息能量代谢的22%,为低代谢组织[13,16-17]。肝脏是小鼠重量最大的器官,恶病质患者肝重量的增加与能量消耗增加及线粒体解耦联蛋白表达有关[18],肝脏重量占去瘤体重的百分比升高则小鼠的能量消耗增加。有研究表明,虽然肿瘤恶病质小鼠的体重是下降的,但恶病质小鼠的肝脏重量是上升的[19-21]。本研究结果也表明,恶病质模型组小鼠肝脏重量占去瘤体重的百分比明显升高,导致小鼠的能量消耗增加,但醋酸甲地孕酮组小鼠肝脏百分比较恶病质模型组明显上升,可能与其增加小鼠的能量消耗有关,其机制有待进一步研究,而榄香烯组小鼠肝脏重量占去瘤体重的百分比较恶病质模型组和醋酸甲地孕酮组均有下降,说明榄香烯组小鼠能量消耗减少,榄香烯能够改善恶病质小鼠的能量平衡。
在肿瘤恶病质骨骼肌萎缩的过程中,细胞因子TNF-α与IL-6发挥了重要作用。有报道显示,TNF-α和IL-6在内的几种炎性细胞因子直接影响患者的食欲和代谢,并诱发癌症相关的恶病质综合症[22-23]。TNF-α 结合肌肉细胞表面的TNF 受体,通过NF-κB信号通路诱导MURF-1 和MAFbx 等蛋白的表达,激活泛素-蛋白酶体(ubiquitin-proteasome pathway,UPP)途径进而降解肌肉蛋白[23]。Cai等[24]研究证明,TNF-α、IL-6能够激活NF-κB通路,进入细胞核引起UPP因子的转录,加强UPP信号通路的表达。TNF-α及IL-6 等炎症因子升高能导致厌食,激活骨骼肌蛋白降解,抑制蛋白合成,增强全身的炎症反应,进一步加剧恶病质的进程[25]。因此,TNF-α 和IL-6 水平的升高是癌症恶病质中骨骼肌消耗的重要原因。本研究中,榄香烯组小鼠血清IL-6 及TNF-α 水平较恶病质模型组及醋酸甲地孕酮组明显下降,说明榄香烯在降低小鼠TNF-α及IL-6水平方面优于醋酸甲地孕酮,证明榄香烯缓解恶病质小鼠骨骼肌萎缩效果优于醋酸甲地孕酮。
肌肉萎缩是由于骨骼肌中蛋白质合成减少和蛋白质分解增加所致[26]。已确定UPP信号通路是恶病质状态下骨骼肌萎缩的重要通路[27-28],其能够降解肌纤维和大部分可溶性蛋白,MURF-1和MAFbx是UPP信号通路的限速酶,MURF-1和MAFbx可以降解粗肌丝的肌球蛋白重链等成分[29],MURF-1也能降解细肌丝中的肌钙蛋白Ⅰ和肌动蛋白等有关成分[30-31]。有研究表明,MURF-1和MAFbx的表达增强能够促进底物蛋白的泛素化,从而使更多的蛋白转移至蛋白酶体中进行降解,加重骨骼肌的萎缩[32-33],此外,观察到缺乏MAFbx 或MURF-1 基因的大鼠对肌萎缩具有抵抗性[34]。研究数据表明,恶病质模型组小鼠腓肠肌MURF-1和MAFbx蛋白表达水平明显高于健康组;榄香烯组小鼠腓肠肌MURF-1和MAFbx蛋白表达水平相对于恶病质模型组和醋酸甲地孕酮组有一定程度的降低。因此推测榄香烯可通过降低小鼠腓肠肌泛素-蛋白酶体途径活性,抑制小鼠肌肉组织蛋白的分解代谢,进而减轻恶病质小鼠骨骼肌萎缩。
榄香烯有效缓解肿瘤恶病质的骨骼肌萎缩,其机制与降低机体能量消耗,缓解能量失衡,抑制细胞因子TNF-α 及IL-6 的表达,降低骨骼肌MAFBx 及MURF1 的蛋白表达水平,调节UPP 信号通路的活性有关。此结果为肿瘤恶病质进一步的基础研究提供新的思路,为临床使用榄香烯治疗肿瘤恶病质提供理论依据。
肿瘤恶病质是一种多因素综合征,其发病原因极为复杂,目前大部分研究结果多为动物试验,临床证据较少,因此关于榄香烯缓解肿瘤恶病质骨骼肌萎缩的效果,需要进一步临床试验进行证实。

