CBC与CBC+DIFF模式下全血细胞计数的对比研究*
黄 璨,杨 莉,刘奠忠
西南医科大学口颌面修复重建和再生实验室/西南医科大学附属口腔医院检验科,四川泸州 646000
临床检验在疾病的诊断、治疗、预防中发挥越来越重要的作用,血液常规检验通常包括白细胞计数(WBC)、红细胞计数(RBC)、血小板计数(PLT)及形态等相关参数分析,是医生诊断疾病的常用辅助检查手段之一[1-2]。随着血细胞计数自动化程度不断提高,不仅为临床提供了更可靠的指标,同时也大大提高了工作效率。为保证检验结果的准确度、可靠性、真实性,每日室内质控是必不可少的[3]。《医学实验室质量和能力认可准则CNAS-CL02》要求“实验室应设计质量控制程序以验证达到预期的结果质量”,“同样的检验项目应用不同程序或设备,应有确切机制以验证在整个临床适合区间内检验结果的可比性”,是指通过开展室内质控,建立完善的测评体系和方法,保障医疗质量安全。Sysmex XS-500i 全自动五分类血液分析仪具有全血细胞计数(CBC)和全血细胞计数及分类(CBC+DIFF)两种检测模式,进行血细胞五分类时需配套试剂Sysmex MK-CELLPACK血细胞分析用稀释液、SYS-4DS血细胞分类染色液、SYS-SLS血细胞分析用溶血剂和SYS-4DL血细胞分析用溶血剂。由于CBC+DIFF模式下对白细胞五分类所使用的染液价格比较昂贵,对于每日室内质控而言成本较高,因而考虑仅在CBC单纯计数模式下进行室内质控能否取代CBC+DIFF分类计数模式。参照中华人民共和国卫生部卫生行业标准WS/T 406-2012《临床血液学检验常规项目分析质量要求》(以下简称《要求》)[4],本课题采用质控品对以上两种模式下的全血细胞计数结果进行差异性分析,验证用CBC模式代替CBC+DIFF模式进行室内质控的可靠性,选择既能满足本实验室质控要求,又可以降低检测成本的室内质控方法。
1 资料与方法
1.1仪器与试剂 Sysmex XS-500i全自动五分类血液分析仪、血液混匀器、Sysmex MK-CELLPACK血细胞分析用稀释液、SYS-4DS血细胞分类染色液、SYS-SLS血细胞分析用溶血剂、SYS-4DL血细胞分析用溶血剂、迈克生物血液学质控品。
1.2方法
1.2.1试验准备 按厂家使用说明对Sysmex XS-500i全自动五分类血液分析仪进行日常维护、保养,确保仪器处于良好状态。每日开机后,待仪器自检完毕后,患者标本检测前,用两种不同的计数模式进行质控品检测。每日自2~8 ℃冰箱中拿出质控品,室温放置10~15 min后,再置于血液混匀器上,混匀8~10 min后检测。
1.2.2分组 在CBC和CBC+DIFF模式下进行WBC、RBC、PLT和血红蛋白(Hb)水平计算,检测3次,取平均值。连续检测20 d(同批号质控品)。
1.2.3试验后质控品处理 血液质控品检测完毕后,用柔软的布或纸擦拭试管口和盖子上残留的液体,减少对质控品质量的影响,尽快置于2~8 ℃冰箱内。

2 结 果
2.1WBC检测结果 CBC模式和CBC+DIFF模式下WBC检测结果见图1。CBC模式WBC为(7.93±0.08)×109/L,CBC+DIFF模式WBC为(8.15±0.12)×109/L,两种模式WBC检测结果比较,差异有统计学意义(t=-13.209,P<0.05),相对差异为(2.70±0.90)%<5%,符合行业标准,具有可比性。
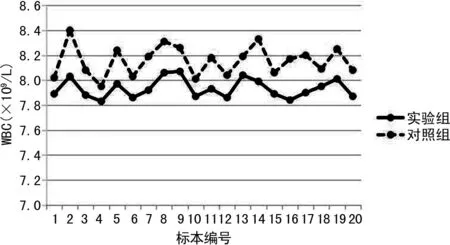
图1 CBC模式和CBC+DIFF模式下WBC检测结果比较
2.2RBC检测结果 CBC模式和CBC+DIFF模式下RBC检测结果见图2。CBC模式RBC为(5.51±0.08)×1012/L,CBC+DIFF模式RBC为(5.53±0.07)×1012/L,两种模式RBC检测结果比较,差异无统计学意义(t=-1.377,P>0.05),相对差异为(1.10±0.50)%<2%,符合行业标准,具有可比性。

图2 CBC模式和CBC+DIFF模式下RBC检测结果比较
2.3PLT检测结果 CBC模式和CBC+DIFF模式下PLT检测结果见图3。CBC模式PLT为(125.85±6.53)×109/L,CBC+DIFF模式PLT为(126.30±6.93)×109/L,两种模式PLT检测结果比较,差异无统计学意义(t=-0.374,P>0.05),相对差异为(3.60±2.10)%<7%,符合行业标准,具有可比性。
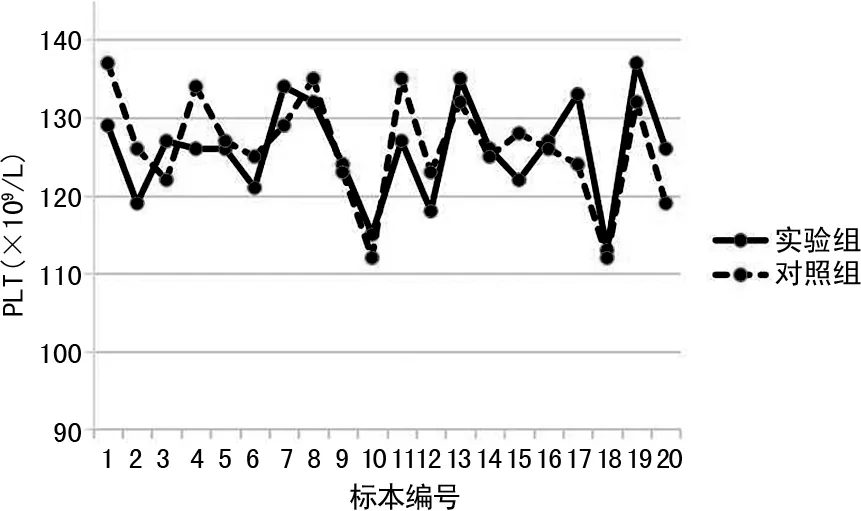
图3 CBC模式和CBC+DIFF模式下PLT检测结果比较
2.4Hb水平比较 CBC模式和CBC+DIFF模式下Hb水平见图4。CBC模式Hb水平为(112.35±1.31)g/L,CBC+DIFF模式Hb水平为(112.80±0.89)g/L,两种模式Hb水平比较,差异无统计学意义(t=-1.528,P>0.05),相对差异为(1.00±0.70)%<2%,符合行业标准,具有可比性。
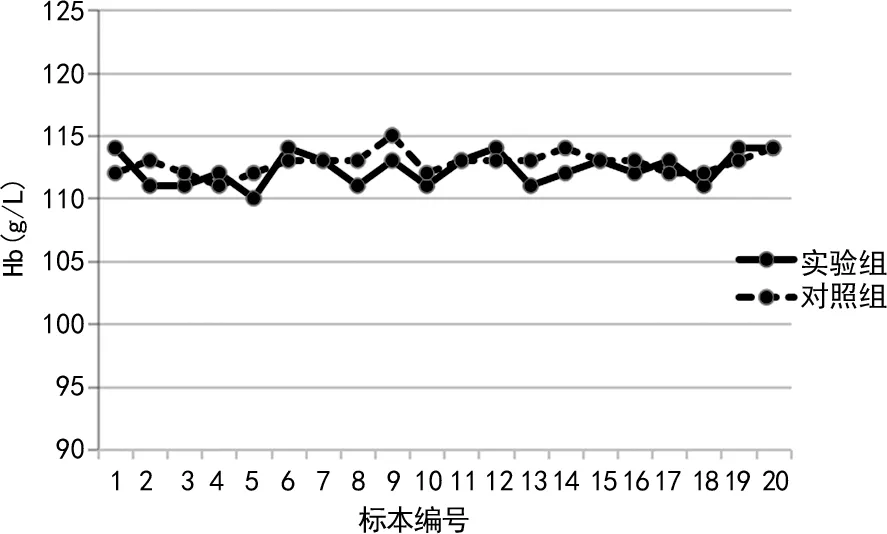
图4 CBC模式和CBC+DIFF模式下Hb水平比较
2.5各种模式s、CV结果 本实验室同批号质控品累计s、CV及CBC模式和CBC+DIFF模式WBC、RBC、PLT、Hb水平的s、CV结果见表1。

表1 各种模式s、CV结果比较
3 讨 论
本实验室使用的XS-500i全自动五分类血液分析仪是Sysmex公司推出的全自动五分类血液分析仪XS系列[5],能利用光检测器模块应用流式细胞计数法执行血细胞分析,主要有CBC模式和CBC+DIFF模式。在血细胞分析中,CBC指的是单纯的计数模式,DIFF指的是白细胞分类模式,可将白细胞分成五分类(中性分叶核粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、淋巴细胞、单核细胞)分别计数。Sysmex MK-CELLPACK血细胞分析用稀释液是一种现成即可使用的稀释液,用于在电阻抗分析和光电分析法中的血细胞分析。SYS-4DL血细胞分析用溶血剂主要用于测定血液标本中淋巴细胞、单核细胞、嗜中性粒细胞及嗜酸性粒细胞的比例,同样在电阻检测和光度检测中对血液标本进行分析。SYS-SLS血细胞分析用溶血剂在检测过程中起破坏红细胞,检测人体Hb的作用。SYS-4DS血细胞分类染色液价格昂贵,主要用于CBC+DIFF模式中对血液标本的淋巴细胞、单核细胞、嗜中性粒细胞及嗜酸性粒细胞进行差别染色。在抽吸标本后,一部分全血标本被SYS-4DL血细胞分析用溶血剂稀释到1∶50,然后再被添加SYS-4DS血细胞分类染色液着色,在一段预定的相应时间后,已着色的标本被送至检测器,进行前向散射光(FSC)和侧向荧光(SFL)强度检测,最后完成5种白细胞的计数和百分比计算。
CBC模式和CBC+DIFF模式WBC检测结果比较,差异有统计学意义(t=-13.209,P<0.05),分析其原因可能是由于两种模式的WBC原理不同,CBC计数模式主要采用流式细胞术和光散射血细胞检测原理[6-9],即利用流式细胞术,单个细胞随着流体动力聚集的鞘流液通过激光照射的检测区时,使光束发生折射、衍射和散射,散射光由光检测器接收后产生脉冲,脉冲的大小与被检细胞的大小呈正比,脉冲的数量则代表被检细胞的数量,也就是说,CBC模式主要通过细胞的大小来计数白细胞;而CBC+DIFF模式则主要采用半导体激光流式细胞计数结合核酸荧光染色原理[6-9],即先用配套染色液对有核细胞进行染色,将染色后的标本导入鞘流式检测系统,被检细胞经半导体激光照射后产生3种信号,其中FSC信号可反映细胞体积大小;SSC信号可反映细胞核的分叶、胞浆颗粒大小、数量、分布均匀程度等信息;SFL强度信号可反映细胞内脱氧核糖核酸水平。通过检测分析FSC、SSC和SFL 3种信号,可实现细胞种类的鉴别。简而言之,CBC+DIFF模式主要以增加SFL强度信号来识别细胞内部结构,从而更加精确计数。从以上分析可知,通过细胞大小来计数的CBC模式与通过识别细胞内部结构来计数的CBC+DIFF模式,最终得到的WBC结果理论上有一定差异。
CBC模式和CBC+DIFF模式RBC和PLT检测结果比较,差异均无统计学意义(P>0.05)。XS-500i全自动五分类血液分析仪的红细胞和血小板检测在RBC/PLT通道中进行,原理为鞘流电阻抗法[10-11],即血液标本稀释后分配到红细胞/血小板检测器内,细胞通过前鞘流检测小孔时,产生一个电阻信号,仪器将这个电阻信号转化为脉冲信号记录下来,脉冲的高度反映了细胞的大小,每个脉冲信号代表一个细胞,通过收集整理大量细胞的脉冲信号,最终得到红细胞和血小板的直方图。由此可见,无论CBC模式还是CBC+DIFF模式,均不影响RBC和PLT检测结果,二者检测结果是一致的。CBC模式和CBC+DIFF模式Hb水平比较,差异无统计学意义(t=-1.528,P>0.05)。XS-500i全自动五分类血液分析仪的Hb水平检测原理为SLS-Hb检测法,即表面活性剂先将红细胞溶解,释放出Hb分子,Hb分子中的Fe2+被氧化为Fe3+,同时SLS的亲水端与Fe3+结合形成稳定的SLS-Hb有色基团,在535 nm有最大吸收峰。因此,无论CBC模式还是CBC+DIFF模式,均不会影响Hb检测水平,二者结果是一致的。
《要求》中对同一台血液分析仪不同模式的结果做出了可比性要求,其中规定WBC检测结果的相对差异应小于或等于5%,RBC检测结果的相对差异应小于或等于2%,PLT检测结果的相对差异应小于或等于7%,Hb检测结果的相对差异应小于或等于2%[6]。可比性是使用不同的检测程序检测某种分析物获得的检测结果间的一致性,结果间的差异不超过规定的可接受标准时,可认为结果具有可比性。因此,能否用CBC模式代替CBC+DIFF模式做室内质控,关键在于验证CBC模式的结果与CBC+DIFF模式的结果之间的可比性[12]。本实验采用质控品作为标本,参照《要求》,20组数据WBC的相对差异为(2.70±0.90)%,RBC的相对差异为(1.10±0.50)%,PLT的相对差异为(3.60±2.10)%,Hb水平的相对差异为(1.00±0.70)%,均符合行业标准要求,可认为结果具有可比性,也就是说,CBC模式下的WBC、RBC、PLT和Hb检测结果与CBC+DIFF模式是一致的。
四川省迈克科技有限责任公司生产的血液质控品的血液学参数较稳定,批内精密度较好,2~8 ℃保存稳定性达6个月以上[13]。CBC模式下质控品RBC、PLT和Hb检测结果与CBC+DIFF模式无差异,WBC虽然与CBC+DIFF模式有差异,但相对差异不超过规定的可接受标准,符合《要求》。由于CBC+DIFF模式对白细胞分类所使用的是SYS-4DS血细胞分类染色液,其价格昂贵,长期使用会大大增加质控成本。加之目前无论是各大厂家的质控品所提供的靶值,还是泸州市及省质控要求,均只要求了WBC、RBC、Hb、PLT等相关参数,未对白细胞分类做出要求。另外,室内质控品、使用方法、质控规则等是否合适取决于是否能监测系统的稳定性,如两种模式下的s、CV、失控率及操作的便捷性等进行比较。表1为本研究CBC模式、CBC+DIFF模式及本实验室同批号质控品累计s、CV结果,可以进行简单的分析,认为CBC模式下质控具有可行性。当然,随着累计标本数量增加,将更全面地讨论此方案的可行性[14-15]。
因此,在本实验室全血细胞分析仪室内质控工作中,结合实际情况,为降低室内质控成本,可考虑用CBC模式代替CBC+DIFF模式,建立适合本实验室的个性化质控方案。