对接受PCI的急性冠脉综合征患者实施基因多态性个体化抗血小板聚集治疗的效果
智勇刚,江 丽,潘蕾羽
(1. 石河子大学医学院第一附属医院药剂科,新疆 石河子 832008 ;2. 石河子第二社区卫生服务中心,新疆 石河子 832008 ;3. 石河子大学医学院第一附属医院,新疆 石河子 832008)
急性冠脉综合征(ACS)是临床上常见的心血管危重症。此病具有较高的致死率。临床调查发现,ACS 患者在发病后1年内的死亡率为15%左右,在发病3 年后的死亡率可升高至25%左右,在发病4 年后的死亡率可升高至39%左右[1]。病理学研究的结果显示[2],ACS 的发生和发展与患者体内血小板聚集的情况有关。进行经皮冠状动脉介入治疗(PCI)是临床上治疗ACS 的主要方法。采用此疗法能够改善ACS 患者的病情,但无法有效地减轻其体内血小板聚集率增高的情况。因此,临床上主张ACS 患者在进行PCI 后,需使用阿司匹林、氯吡格雷等药物进行长期的抗血小板聚集治疗。另有研究发现,对进行PCI 的ACS 患者实施常规的抗血小板聚集治疗,效果并不理想。导致这种情况出现的原因为患者体内的CYP2C19基因存在多态性[3]。本次研究主要探讨对进行PCI 的ACS 患者实施基因多态性个体化抗血小板聚集治疗的效果。
1 资料与方法
1.1 一般资料
本次研究的对象为2019 年1 月至2019 年12 月期间在石河子大学医学院第一附属医院进行PCI 的78 例ACS 患者。这78 例患者的纳入标准为:1)病情符合ACS 的诊断标准[4],并经冠脉造影检查得到确诊;2)年龄≥18 岁;3)在本院进行PCI;4)临床资料完整;5)签署了自愿参加本次研究的知情同意书。其排除标准为:1)在PCI 结束后的24 h 内需要接受溶栓治疗。2)需服用与本次研究无关的抗凝药物。3)患有出血性并发症或存在出血倾向;4)存在凝血功能异常或患有血液系统疾病;5)存在严重的肝、肾功能障碍。6)患有恶性肿瘤或预估生存期少于6 个月。7)在参与本次研究前6 个月内接受过大型手术;8)对本次研究使用的药物过敏或不耐受。使用随机数表法将这78 例患者分为观察组和对照组,每组各39 例。在观察组患者中,有男22 例,女17 例;年龄为46 ~78 岁,平均年龄为(62.48±6.35)岁。在对照组患者中,有男23 例,女16 例;年龄为48 ~76 岁,平均年龄为(62.54±5.98)岁。两组患者的基线资料相比,P >0.05,存在可比性。本次研究获得了石河子大学医学院第一附属医院医学伦理委员会的批准。
1.2 方法
对对照组患者进行常规的抗血小板聚集治疗,方法是:口服氯吡格雷(生产厂家:乐普药业股份有限公司,批准文号:国药准字H20123316,规格:75 mg/ 片),75 mg/d,同时口服阿司匹林(生产厂家:辰欣药业股份有限公司,批准文号:国药准字H37023270,规格:25 mg/ 片),100 mg/d。对观察组患者进行基因多态性个体化抗血小板聚集治疗,方法是:采用核酸芯片杂交法检测患者CYP2C19 基因的多态性。检测用的仪器包括血液基因组提取试剂盒(生产厂家:北京天根生化科技有限公司,目录号:DP318-02)、CYP2C19 基因检测芯片试剂盒、基因芯片检测系统(生产厂家:上海百傲科技有限公司,型号:V 2.0)。具体的检测方法是:抽取患者2 mL 的静脉血,将其置入EDTA抗凝管中充分混匀。按照上海百傲科技有限公司提供的血液基因组DNA 提取试剂盒说明书规定的方法提取和纯化血液标本中的DNA(DNA 的浓度为10 ~60 ng/ml,A260/A280 的比值为1.5 ~2.0)。PCR 的扩增条件为:50 ℃ 5 min ;94 ℃ 5 min;94 ℃ 25 S,48 ℃ 40 s,72 ℃ 30 s,35 个循环;72 ℃ 5 min。使用Baio 基因芯片图像分析软件进行图像扫描和数据分析,并输出检测结果。将检测结果与美国食品及药品管理局的建议相结合,得出患者CYP2C19 基因的分型。对于CYP2C19 基因为快代谢型(*1/*1)的患者,给其口服阿司匹林,100 mg/d,同时口服氯吡格雷,75 mg/d。对于CYP2C19 基因为中等代谢型(包含*1/*2、*1/*3)的患者,给其口服阿司匹林,100 mg/d,同时口服氯吡格雷,150 mg/d;或是口服阿司匹林,100 mg/d,同时口服替格瑞洛,180 mg/d。对于CYP2C19 基因为慢代谢型(包含*2/*2、*2/*3)的患者,给其口服阿司匹林,100 mg/d,同时口服替格瑞洛,180 mg/d。两组患者治疗的时间均为6 个月以上。
1.3 观察指标
治疗结束后,比较两组患者不良心血管事件(再次血运重建、再发性心梗、再发性心绞痛、心源性死亡)的发生率和出血性并发症的发生率。
1.4 统计学方法
采用SPSS18.0 统计软件对本次研究中的数据进行分析,计量资料用均数± 标准差(± s)表示,采用t 检验,计数资料用百分比(%)表示,采用χ²检验,P <0.05 为差异具有统计学意义。
2 结果
2.1 两组患者不良心血管事件发生率的对比
观察组患者不良心血管事件的发生率低于对照组患者,P <0.05。详见表1。
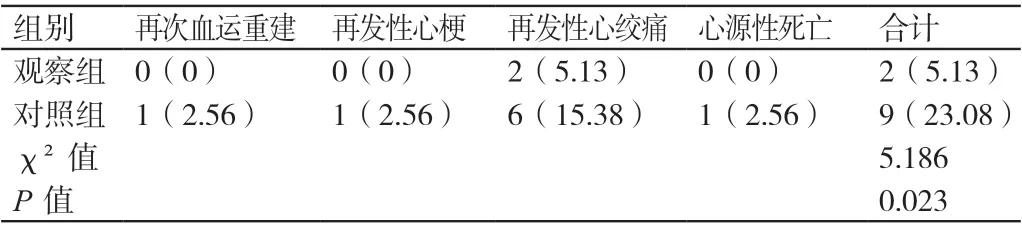
表1 两组患者不良心血管事件发生率的对比[例(%)]
2.2 两组患者出血性并发症发生率的比较
两组患者出血性并发症的发生率大体相当,P >0.05。详见表2。
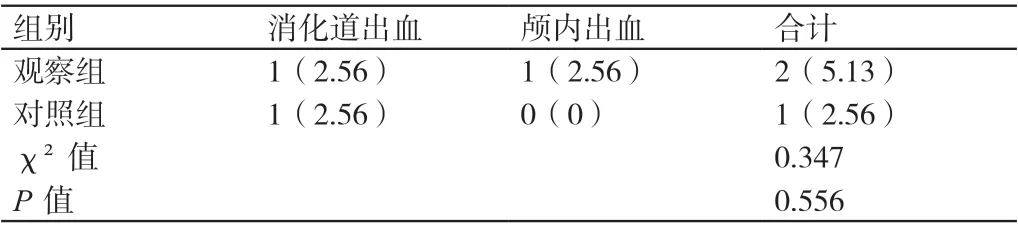
表2 两组患者出血性并发症发生率的比较[例(%)]
3 讨论
氯吡格雷是ACS 患者进行PCI 后常用的抗血小板聚集药。此药的疗效和安全性已经获得了临床上的认可。不过,近年来的药理学研究证实,部分进行PCI 的ACS 患者使用氯吡格雷进行抗血小板聚集治疗的效果并不理想[5]。临床上将这种情况叫做“氯吡格雷抵抗”。导致这种情况出现的原因为患者体内的CYP2C19 基因存在多态性,而不同类型的CYP2C19 基因对氯吡格雷的抵抗作用存在明显的不同。
CYP2C19 基因处在人体的第10 对染色体中,其存在两种突变情况。一种突变情况为CYP2C19 基因第2 外显子的681 碱基位置出现突变,G 变A,从而出现一个异常的拼接位点,导致碱基失去翻译时会使阅读框架出现移动,提前在下游产生1 个终止密码子,促使蛋白质缺失的血红蛋白结合位置失去催化活性。另一种突变情况为CYP2C19 基因第4 外显子的636 碱基位置出现突变,G 变A,出现1 个终止密码子,使得蛋白的生成提前结束,并失去生物活性。上述两种CYP2C19 基因的突变均能使CYP2C19 酶的活性下降或完全丧失,进而影响到氯吡格雷的疗效。
本次研究的结果显示,对进行PCI 的ACS 患者实施基因多态性个体化抗血小板聚集治疗可有效地降低其再发性心梗、再发性心绞痛等不良心血管事件的发生率,而且不会增加其患出血性并发症的发生率。

