加减地黄饮子治疗帕金森病疼痛临床研究
张秀琳,惠 振,王苏雷,肖 婧,陈 清,梁 艳,唐莉莉,徐成成,陈 畅,赵 杨,张臻年
(1.南京中医药大学,江苏 南京 210023;2.南京中医药大学附属南京中医院,江苏 南京 210022;3.江苏省第二中医院,江苏 南京 211005;4.南京市浦口区中医院,江苏 南京 210032)
帕金森病是临床常见的一种中枢神经系统退行性疾病,以中老年患者常见,难以治愈[1]。随着人口老龄化进程的加速,该病的发病率呈逐年递增趋势[2]。其临床表现可分为运动症状和非运动症状,其中超过90%的帕金森病患者会出现非运动症状,且非运动症状的发生早于运动症状。疼痛是帕金森病最为常见的一种非运动症状,可在帕金森疾病病程中的任意阶段出现,甚至能够作为该病的首要表现,且疼痛侧运动症状更为严重,其发生率高达85%,对患者的正常生活及工作造成严重的影响[3]。目前,临床缺乏有效的药物治疗帕金森病,西药常采用多巴胺能药物治疗、阿片类药物治疗等方法治疗,但西药治疗会提高疼痛阈值,且伴不良反应,影响到患者的治疗依从性,具有一定的局限性[4]。因此,如何有效的治疗帕金森病已成为临床研究的热点。近年来,中医中药在治疗帕金森方面获得了满意的疗效,可改善患者早期临床症状,且安全性较高,与西药联合使用不仅能够提高疗效,而且能够减少不良反应[5]。基于此,本研究将探讨加减地黄饮子对帕金森病疼痛的临床研究,以期为帕金森病疼痛治疗提供依据。
1 资料与方法
1.1 一般资料 以自2017年8月至2020年8月于我院收治的68例帕金森病疼痛患者为研究对象,按随机数字表法将所有患者分为治疗组和对照组各34例。治疗组男15例,女19例;年龄48~76岁,平均(56.83±6.59)岁;体重指数(BMI)22.14~25.03 kg/m2,平均(23.87±1.24)kg/m2;病程5~18年,平均(7.19±1.02)年;根据Foed帕金森伴疼痛分类方法:其中静坐不能2例、中枢性疼痛3例、神经根性疼痛8例、运动障碍相关疼痛4例、骨骼肌疼痛17例。对照组男14例,女20例;年龄48~75岁,平均(56.79±6.82)岁;BMI 22.09~25.01 kg/m2,平均(23.79±1.19)kg/m2;病程6~17年,平均(7.08±1.04)年;根据Foed帕金森伴疼痛分类方法:其中静坐不能1例、中枢性疼痛2例、神经根性疼痛9例、运动障碍相关疼痛4例、骨骼肌疼痛18例,两组患者一般资料比较,具有可比性(P>0.05)。本研究符合《世界医学协会赫尔辛基宣言》的相关要求。
西医诊断标准:根据《中国帕金森病的诊断标准(2016版)》[6]及国际疼痛协会(IASP)[7]制定的帕金森疼痛的标准。中医诊断标准:根据《中医老年颤证诊断和疗效评定标准(试行)》[8]中肝肾不足型颤证的诊断标准。主症:头摇肢颤、行动缓慢、腰膝酸软、善忘或神呆;次证:手足出汗、头晕耳鸣、语言障碍、失眠多梦、盗汗颧红、口咽干燥、急躁时颤振加重;大便秘结、小便频数;舌体瘦小,苔微黄,脉细。
病例纳入标准:符合上述诊断标准;Hoehn-Yahra分级≤Ⅳ级者;伴有疼痛障碍,视觉疼痛模拟量表(VAS)评分≥3分及以上,且持续3个月以上;意识清楚,且精神正常者。排除标准:伴有心肝肾等严重器质性病变者;对本研究药物过敏者;患者属于帕金森病叠加综合征;患者超剂量服用美多巴(750 mg/d);伴认知功能障碍者;合并颅内器质性病变或颅脑创伤;孕妇及哺乳期妇女;患者依从性较差;近三个月参加其他研究者;自动退出者。
1.2 治疗方法
1.2.1 对照组:给予抗帕金森西药治疗,口服盐酸司来吉兰片(国药准字H20160342),每天早晨1次,5 mg/次,若患者病情控制不佳可增至10 mg/次;同时给予美多巴(国药准字H10930198)口服,125 mg/次,3次/d;口服度洛西汀(国药准字H20061261),起始剂量为20 mg/d,2次/d;1周后,30 mg/d,2次/d。上述药物均连服10 d。
1.2.2 治疗组:在上述治疗的基础上给予加减地黄饮子治疗。组方:熟地黄、山茱萸、肉苁蓉、当归、天冬、白芍各12 g,巴戟天9 g。辨证加减:便秘、口唇色淡面色无华者加麻子仁、当归;嗳气频作者加大黄、枳实;伴见腹满、便秘、口干口臭者加大黄、麻子仁;伴见喜怒无常、心神不宁、精神恍惚者加小麦、大枣及甘草;伴见口苦干、胸胁胀满、性情急躁易怒者加夜交藤、丹皮、栀子;伴见胸满痞满、善太息、精神抑郁者加陈皮、半夏、佛手;伴见胸满胁痛、情绪不宁者加柴胡、郁金。水煎服,早晚分服,连续服药1个月。
1.3 观察指标 对比治疗前后两组中医证候积分、疼痛视觉模拟量表(VAS)评分、国王帕金森病疼痛评价量表(KPPS)评分及血清单胺类神经递质5-羟色胺(5-HT),去甲肾上腺素(NE)及神经肽Y(NPY)的变化情况,观察两组临床疗效。
1.3.1 中医证候积分:根据《中医老年颤证诊断和疗效评定标准(试行)》[8]制定。根据头摇肢颤、行动缓慢、腰膝酸软、善忘或神呆严重程度将其分为无、轻度、中度、重度,评分为0~6分;根据手足出汗、头晕耳鸣、语言障碍、失眠多梦、盗汗颧红、口咽干燥、急躁时颤振加重将其分为无、轻度、中度、重度,评分为0~3分,得分越高表示患者临床症状越明显。
1.3.2 VAS评分:分别在治疗前后采用VAS评价,采用一条长10 cm的直尺,0端表示无痛,10端表示剧烈疼痛,得分越高表示疼痛程度越明显。
1.3.3 KPPS评分:分别在治疗前后采用KPPS评估[9],该量表包括7个项目如口面部疼痛、慢性疼痛、神经根性疼痛、胀痛、骨骼肌疼痛、症状波动相关疼痛、夜间疼痛共14项内容,评估项目根据疼痛严重程度分为0~3级,根据疼痛频率将其分为0~4级,两项相乘则为0~12分,满分为168分,得分越高表示疼痛程度越明显。
1.3.4 实验室检查:分别在治疗前后抽取患者肘静脉血3~5 ml,离心后保存于-50 ℃冰箱内保存备用。5-HT、NE均采用山西同杰科学器材有限公司生产的Uliti Mate 3000型电化学检测器(高效液相)检测;NPY采用Biometra Tprofessional酶标仪,酶联免疫吸附法测定,酶联免疫吸附法测定,上述试剂盒均购自上海纪宁实业有限公司,需严格根据说明书进行操作。
1.4 疗效标准 根据《中医老年颤证诊断和疗效评定标准(试行)》[8]、帕金森评分量表(UPDRS)Ⅲ[10]及VAS评分[11]评定。显效:临床症状、体征均明显改善,UPDRSⅢ好转率均>50%,VAS评分减轻>50%;有效:临床症状、体征均好转,UPDRS Ⅲ好转率为10%~50%,VAS评分减轻为10%~50%;无效:临床症状、体征均无改善或加重,UPDRSⅢ及VAS好转率<10%,VAS评分<10%。总有效率=显效率+有效率。
1.5 统计学方法 采用SPSS 23.0统计学软件进行分析。计数资料以[例(%)]表示,采用χ2检验;计量资料以均数±标准差表示,采用t检验。P<0.05表示差异具有统计学意义。
2 结 果
2.1 两组中医证候积分比较 见表1。治疗前,两组头摇肢颤、行动缓慢、腰膝酸软、善忘或神呆严重、手足出汗、头晕耳鸣、语言障碍、失眠多梦、盗汗颧红、口咽干燥、急躁时颤振加重评分比较,差异无统计学意义(P>0.05);治疗后,两组评分均较治疗前降低,与对照组比较,治疗组评分均更低,差异有统计学意义(P<0.05)。

表1 两组中医证候积分比较(分)
2.2 两组临床疗效比较 见表2。治疗后,治疗组临床疗效高于对照组(94.12%与73.53%),差异有统计学意义(P<0.05)。

表2 两组临床疗效比较[例(%)]
2.3 两组VAS评分比较 见表3。治疗前,两组患者VAS评分比较,差异无统计学意义(P>0.05);治疗后,两组VAS评分均较治疗前降低,与对照组比较,治疗组VAS评分更低,差异有统计学意义(P<0.05)。
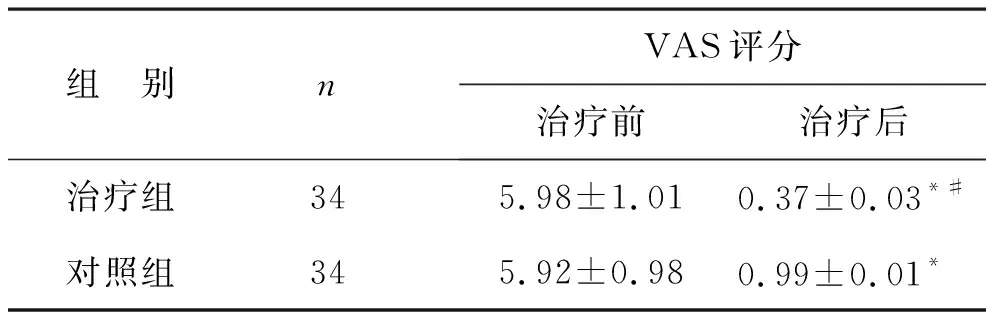
表3 两组VAS评分比较 (分)
2.4 两组KPPS评分比较 见表4。治疗前,两组口面部疼痛、慢性疼痛、神经根性疼痛、胀痛、骨骼肌疼痛、症状波动相关疼痛、夜间疼痛评分比较,差异无统计学意义(P>0.05);治疗后,两组评分均较治疗前降低,与对照组比较,治疗组评分均更低,差异有统计学意义(P<0.05)。

表4 两组KPPS评分比较(分)
2.5 两组血清5-HT、NE、NPY比较 见表5。治疗前,两组血清5-HT、NE、NPY比较,差异无统计学意义(P>0.05);治疗后,两组血清5-HT、NE、NPY均较治疗前上升,与对照组比较,治疗组血清5-HT、NE、NPY均更高,差异有统计学意义(P<0.05)。

表5 两组血清5-HT、NE、NPY比较
3 讨 论
帕金森病与遗传、环境等多种因素密切相关,多种因素会导致机体内黑质纹状体多巴胺能神经元凋亡并诱发神经环路异常,引发肌强直、震颤、运动迟缓等运动症状及情绪障碍、自主神经紊乱、感觉异常等非运动症状[12]。其中疼痛是帕金森患者最为常见的感觉异常,已被认为是中晚期帕金森病患者最痛苦的主要症状之一,对患者的生活质量造成严重的影响。目前,关于帕金森病相关疼痛的发病机制尚不清楚,在临床上部分医师忽略了疼痛对帕金森病患者的影响,其中约50%帕金森病患者合并疼痛并未接受药物或其他疗法治疗[13]。因此,采用积极有效的方法治疗帕金森病,并缓解其疼痛程度,能够提高患者生活质量及治疗依从性,对临床具有重要的意义。
在中医学中将帕金森病纳入“震颤” “肝风”等范畴,最早可见《素问·阴阳应象大论》曰:“年四十而阴气自半,起居衰矣”;《赤水玄珠》曰:“该病壮年鲜有,中年以后乃有之,老年尤多。夫老年阴血不足,少水不能制盛火,极为难治”,故在临床上以中老年为帕金森病的高发人群。该病病因为肝肾不足,加之劳欲过度、五志化火等因素损伤阴精,致使肝肾阴精不足。而肝主筋,阴血不足,难以濡养筋脉诱发拘急痉挛;肾藏精生髓,脑为髓海,肾精不足无以濡养脑髓,脑髓失充;肝肾阴虚动风,同气相求则震颤抖动;日久阻塞经脉,影响气血运行,导致肌肉强直、震颤等症。因此,治当滋补肝肾、益气养血柔肝。笔者根据帕金森病的临床表现及长期服用左旋多巴制剂出现的伤阴症状,我们认为该病基本病机属肝肾阴虚,治疗当养血柔肝,滋阴补肾;遵循张景岳“善补阴者必于阳中求阴”,结合长期的临床经验,我们化裁地黄饮子组成加减地黄饮子,包含熟地黄、巴戟天、山茱萸、肉苁蓉、当归、天冬、白芍共七味中药组成。方中熟地黄具有养血滋阴生津、补精益髓之功效;肉苁蓉具有补肾阳、益精血之功效;巴戟天具有补肾助阳、强筋健骨、祛风除湿之功效;山茱萸具有补益肝肾、涩精缩尿、固精之血、敛汗固脱之功效;配伍熟地黄、山茱萸滋补肾阴,肉苁蓉、巴戟天温补肾精,以上四味共为君药;当归、天冬、白芍养血柔肝为臣药;方中肉苁蓉、巴戟天合用乃取阳中求阴之意,诸药合用,共奏养血柔肝,滋阴补肾之效。于振华[14]通过的研究证实,地黄饮子加减联合针灸能够有效治疗帕金森病;王妮娜[15]通过的研究证实,地黄饮子合芍药甘草汤能够治疗帕金森病患者,效果颇佳。本研究结果显示,治疗后,与对照组比较,治疗组头摇肢颤、行动缓慢、腰膝酸软、善忘或神呆严重、手足出汗、头晕耳鸣、语言障碍、失眠多梦、盗汗颧红、口咽干燥、急躁时颤振加重评分均更低,且临床疗效高于对照组,提示加减地黄饮子能够有效治疗帕金森病疼痛患者,效果显著。
近年来的研究证实[16-17],5-HT、NE、NPY与帕金森病的发展密切相关,其中5-HT属于神经递质,能够调控机体生理功能如痛觉、睡眠、体温;NE是一种神经递质,主要由脑内去甲肾上腺素神经元和交感节后神经元合成和分泌;NPY广泛分布于大脑皮质区、下丘脑、海马区等中枢神经系统,其中浓度最高的是海马区,参与人类记忆功能及学习。已有研究证实[13],5-HT、NE、NPY能够导致通路退化,对疼痛的下行抑制作用减弱,诱发疼痛发生。因此,5-HT、NE、NPY与帕金森病疼痛密切相关,故本研究观察加减地黄饮子对帕金森病疼痛患者5-HT、NE、NPY的影响,结果显示,治疗后,与对照组比较,治疗组血清5-HT、NE、NPY均更高,提示加减地黄饮子能够有效提高帕金森病疼痛患者血清5-HT、NE、NPY水平,调节神经中枢。究其原因如下:经现代药理学研究证实,熟地黄能够抑制下丘脑-垂体-肾上腺(HPA)轴机能亢进,恢复HPA轴机能平衡,发挥益智作用;肉苁蓉具有免疫调节、抗炎、肝保护、抗氧化、抗菌、神经保护、改善认知等多种药理作用;巴戟天具有调节免疫、抗衰老、抗肿瘤、抗抑郁、壮阳等作用;山茱萸具有明显的免疫调节、抗氧化、治疗糖尿病、保护神经系统等作用;当归具有抗血小板聚集,抗炎,增强机体免疫力,对脑缺血损伤的保护,抗肿瘤,调经,平喘等作用;白芍具有抗炎,免疫调节,抗类风湿关节炎和保护内皮细胞的作用;诸药合用保护神经、调节免疫、改善认知、镇痛、解痉、抗炎等作用。盐酸司来吉兰片是一种单胺氧化酶抑制剂,能够抗氧化活性,可增加纹状体内SOD活性,从而缓解多巴胺神经元变性,可阻断多巴胺的代谢,对多巴胺的降解起到抑制作用,能够抑制突触的再摄取,增加多巴胺的作用时间,同时能够保护神经、促进神经成型的作用,改善帕金森病症状[18]。美多巴是苄丝肼与左旋多巴的复合制剂,能够减少左旋多巴的外周不良反应,致使机体内脑多巴胺的浓度提高,以改善帕金森病症状[19]。度洛西汀是一种抗抑郁药,能够有效治疗糖尿病神经痛,其作用机制为选择性双重抑制5-HT及NE再摄取,从而能够对帕金森疼痛发挥双重作用[20]。
综上所述,加减地黄饮子能够有效改善帕金森病疼痛患者临床症状,降低疼痛评分,缓解疼痛程度,升高血清5-HT、NE、NPY水平,发挥神经保护作用。

