56例子痫前期产妇外周血和胎盘中PLGF和sVEGFR-1的临床意义
闵治红 杜巧玲
同济大学附属第一妇婴保健院(上海,201204)
子痫前期(PE)是导致孕产妇和围生儿死亡的重要原因[1]。全球发病率为3%~5%[2],我国发病率可达9%~10%[3]。发病机制尚未阐明[4]。胎盘生长因子(PLGF)主要在胎盘组织中表达[5],参与胎盘形成和发育[6]。可溶性血管内皮生长因子受体-1(sVEGFR-1)主要功能是拮抗血管内皮生长因子和胎盘生长因子[7],sVEGFR-1、VEGF-A 与胎盘生长因子结合可刺激血管生成和改变血管渗透性[8]。目前关于PLGF、sVEGFR-1与子痫前期的关系研究鲜有报道。本研究通过测定子痫前期孕妇胎盘组织和外周血PLGF和sVEGFR-1的表达,分析其与子痫前期的病情和围产期临床结局关系,为子痫前期的防治提供依据。
1 资料与方法
1.1 临床资料
选择2017年1月—2018年12月在本院妇产科住院的轻度(轻度组)、重度子痫前期(重度组)孕产妇各56例,均剖宫产终止妊娠。纳入标准:①孕周≥28周,超声检测孕周与实际孕周相符;②轻度子痫前期和重度子痫前期诊断符合相关诊断标准[9];③单胎自然受孕,月经周期规律;④获得患者和家属知情同意。排除标准:①多胎妊娠或前置胎盘;②生殖道、泌尿道或其他部位感染;③高血压病史或精神异常;④伴随心脑血管、肝脏、肾脏等脏器功能损害,恶性肿瘤,免疫性疾病。选择同期本院就诊正常孕产妇56例(正常组)。本研究经医院伦理委员会批准。
1.2 研究方法
对入选的子痫前期孕产妇和胎儿情况进行连续评测,由主治医生决定住院治疗或在家治疗。对病情严重孕产妇住院治疗;对病情较轻患者在家治疗并按随诊日期定期随诊,进行动态的孕产妇管理。根据监护情况采取提前终止妊娠或待产。孕产妇分娩后统计妊娠结局并测定外周血清和胎盘PLGF和sVEGFR-1 mRNA表达水平。
1.3 PLGF和sVEGFR-1 测定
孕产妇分娩日收集空腹静脉血,酶联免疫吸附试验法检测血清PLGF和sVEGFR-1水平,试剂盒分别购自美国 Bio-Swamp 公司和美国 Biotech 公司。分娩后立即收集胎盘全层组织1 块,预冷生理盐水冲洗后-80℃保存。将-80℃保存的胎盘组织用 4℃预冷的磷酸缓冲液液冲洗,置Cryomill 全自动冷冻研磨仪(德国Retsch公司),加入液氮维持低温,研碎组织成微细颗粒状(5μm), Trizol试剂(天根生化科技有限公司)提取RNA。超微量分光光度计(北京凯奥科技公司)测定260 nm和280 nm的吸光度(A),控制A260/A280在1.8~2.0,RNA电泳检测其完整性。使用逆转录试剂盒(日本TaKaRa公司)将RNA逆转录成cDNA行PCR。采用RT-PRC仪(美国 Applied Biosystems公司)测定IRS-1、PI3K和AKT mRNA的表达水平。PCR反应体系:cDNA、上游引物和下游引物各0.5 μl,2×SYBR Green Super Mix12.5 μl,加入0.1%DEPC-H2O至20 μl。PCR反应条件:50℃2 min,95℃10 min后进入循环(95℃30 s、60℃30 s,循环40次)。RT-PCR产物进行2%凝胶电泳,溴化乙锭成像,采用凝胶成像系统(美国Syngene公司)分析。用PLGF和sVEGFR-1与GAPDH吸光度比值表示目标基因的相对表达量。
1.4 妊娠结局统计
比较两组分娩孕周、胎盘重量、围产儿存活情况、新生儿出生体质量、Apgar评分、宫内生长受限情况、入新生儿重症监护室(NICU)情况、发生新生儿呼吸窘迫综合征等情况。围产期发生以下任一情况判定为妊娠结局不良:①围产儿死亡;②入住 NICU;③出生时极低体重(<1.5kg);④娩出后 5min Apgar 评分<7;⑤宫内生长受限;⑥新生儿呼吸窘迫综合征。
1.5 统计学方法
2 结果
2.1 一般情况
各组孕产妇年龄、孕次、孕周、收缩压、舒张压、体质指数和24h蛋白尿等无差异(P>0.05),收缩压、舒张压以及24h蛋白尿水平存在差异(P<0.05)。见表1。

表1 各组孕产妇临床资料比较
2.2 血清PLGF和sVEGFR-1水平
血清PLGF水平,重度组(57.32±17.64 pg/ml)<轻度组(86.92±19.15 pg/ml)<正常组(113.40±18.54 pg/ml)(P<0.05);sVEGFR-1水平,重度组(1531.37±121.39 pg/ml)>轻度组(1154.61±107.25 pg/ml)>正常组(837.42±94.76 pg/ml)(P<0.05)。
2.3 胎盘PLGF和sVEGFR-1 mRNA水平
胎盘PLGF mRNA水平,重度组(1.76±0.22)<轻度组(2.63±0.27)<正常组(3.56±0.31)(P<0.05);sVEGFR-1 mRNA水平,重度组(2.49±0.27)>轻度组(1.67±0.24)>正常组(0.86±0.20)(P<0.05)。
2.4 子痫前期孕产妇 PLGF、sVEGFR-1与 24h尿蛋白和血压相关性
子痫前期患者外周血清PLGF蛋白、胎盘PLGF mRNA水平与24h蛋白尿、收缩压和舒张压均负相关,sVEGFR-1蛋白、胎盘sVEGFR-1 mRNA水平与24h蛋白尿、收缩压和舒张压均正相关(均P<0.05)。见表2。
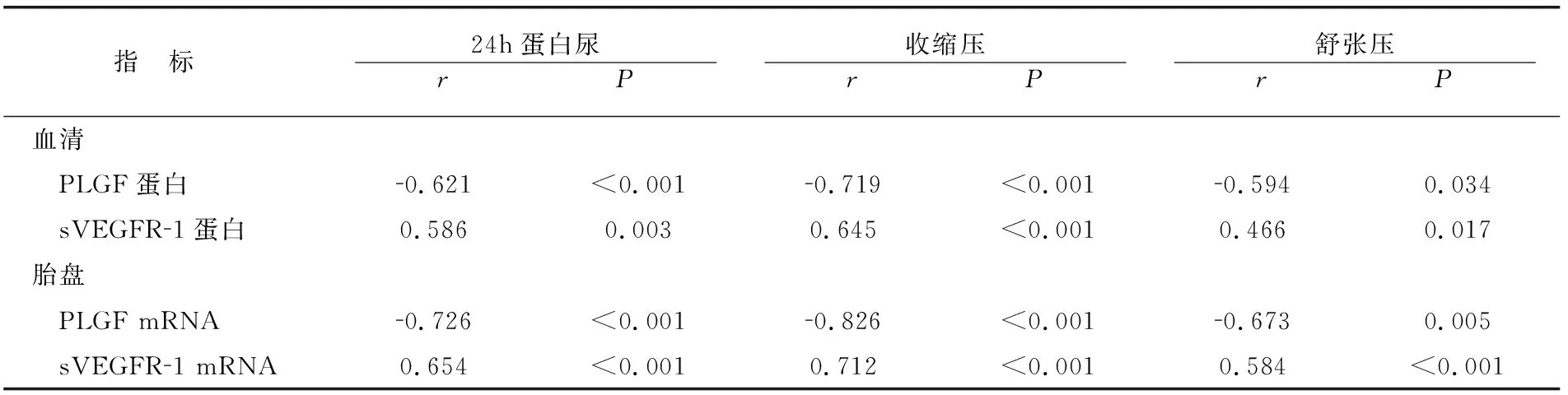
表2 子痫前期孕产妇各指标相关性分析
2.5 各组围生儿妊娠结局比较
正常组、轻度组和重度组围生儿出现临床结局不良存在差异(P<0.05)。见表3。
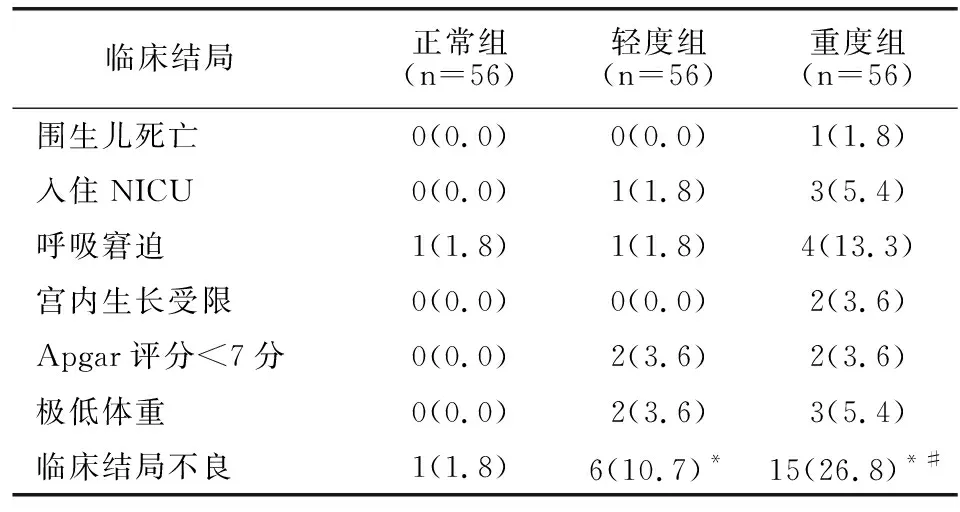
表3 各组围生儿妊娠结局比较[例(%)]
2.6 子痫前期孕产妇不同妊娠结局PLGF和sVEGFR-1水平比较
妊娠结局不良孕产妇外周血清PLGF蛋白和胎盘PLGF mRNA水平均低于妊娠结局正常者(P<0.05),血清sVEGFR-1蛋白和胎盘sVEGFR-1 mRNA水平高于妊娠正常者(P<0.05)。见表4。

表4 不同妊娠结局子痫前期孕产妇PLGF和sVEGFR-1水平比较
3 讨论
子痫前期是导致孕产妇和围生儿预后不良的重要原因,也是引起孕产妇和围产儿发病和死亡的主要原因之一。子痫前期的发病机制仍尚不明确,目前认为子宫螺旋小动脉重铸不足和血管内皮细胞损伤在子痫前期的发病中发挥重要作用[10]。子痫前期孕产妇滋养细胞浸润较浅,引起小动脉重铸不足,导致胎盘组织供血不足从而起胎盘组织缺血缺氧。
PLGF主要由合体滋养层细胞合成的多效细胞因子,具有促血管生成功能[11],病理情况下在多种细胞中表达增加[12]。妊娠期间PLGF水平随着妊娠月份增加水平逐渐升高,在妊娠 28~30 周时达最高,维持胎盘血液供应和胎儿生长发育。VEGF受体sVEGFR-1是强大的抗血管生成因子,可抑制血管生成[13]。 PE 患者存在sVEGFR-1的过度表达,导致抗血管生成与血管生成失去平衡,且sVEGFR-1水平与PE严重程度呈正相关[14],sVEGFR-1水平异常升高促进了 PE 的发生发展[15]。本研究结果显示,随着子痫前期病情的加重,患者外周血清PLGF蛋白和胎盘PLGF mRNA水平升高,sVEGFR-1蛋白和胎盘sVEGFR-1 mRNA水平降低,说明PLGF和sVEGFR-1可能参与了子痫前期的发病。本研究子痫前期患者外周血清PLGF蛋白、胎盘PLGF mRNA水平与24h蛋白尿、收缩压和舒张压均负相关,而血清sVEGFR-1蛋白、胎盘sVEGFR-1 mRNA水平与24h蛋白尿、收缩压和舒张压均正相关,也说明PLGF和sVEGFR-1水平与PE疾病的严重程度密切相关。
在本研究中,正常组、轻度组和重度组分别有1例、6例和15例围生儿出现临床结局不良,说明随着子痫前期病情加重,围产儿的临床预后越差。妊娠结局不良孕产妇外周血清PLGF蛋白和胎盘PLGF mRNA水平均较妊娠结局正常者降低,而血清sVEGFR-1蛋白和胎盘sVEGFR-1 mRNA水平较妊娠正常者升高,说明PLGF和sVEGFR-1水平与PE妊娠结局有关。因此,建议对外周血和胎盘PLGF和sVEGFR-1水平低的子痫前期孕产妇和围产儿应加强监护,随时做好临床医疗支持以改善临床预后。
总之,子痫前期孕产妇外周血和胎盘PLGF和sVEGFR-1可能与PE疾病严重程度及围产儿妊娠结局有关。

