宽场光学相干层析成像技术在眼科学中的研究进展
陶成龙,杨必文,范冉冉,钟会清,苏成康,郭周义,刘智明*
(1. 广州浩康生物科技有限公司,广州 510660;2. 华南师范大学生物光子学研究院,广州 510631)
光学相干层析成像技术(optical coherence tomography,OCT)是集光学、物理学、精密自动控制、电子、计算机图形图像学等多门学科为一体的综合成像技术[1],可通过利用宽带光源的低相干特性,获取物体后向散射光的干涉信号,对其内部微观结构进行检测,从而进行高分辨率断层扫描成像[2]。典型的OCT 成像技术利用血流诱导的信号变化作为内在对比机制区分血管系统和静态组织,具有高分辨率、高精度成像、图像清晰、较高的空间分辨率、高灵敏度、无损检测的特性[3]。该技术早期主要应用于视网膜横断面检查(也是最重要的应用),近年来已逐步渗透到血管内成像[4]、皮肤科[5]、口腔,甚至工业过程的监控[6]。扫描激光眼科成像技术的商业化使简单、高质量的临床宽视野成像成为可能,这简化了相关疾病的成像流程,扩大了其成像范围,更有利于早期诊断。
宽场光学相干层析成像技术(wide-field optical coherence tomography,WF-OCT)则是在典型的光学相干层析成像上进行了改良与优化,其能通过一次扫描完成一个二维平面图像的采集,避免了传统OCT 技术的逐点扫描。通过不同深度的扫描可以获得样品的三维数据集,根据三维图像算法,将三维数据集合成样品的三维图像[7]。三维图像能帮助检测人员从不同角度观察样品的结构和细节信息,为医学的早期诊断、病灶位置的判断以及材料缺陷检测提供有利的依据。
在眼科疾病OCT 临床医学应用中,在了解患者的病史和临床特征的前提下,结合B 扫描(B-scan)图像和其对应层面的横断面(En-face)图像,对玻璃体视网膜交界面、浅层视网膜血管网、深层视网膜血管网、外层视网膜无血管区、脉络膜毛细血管层以及视盘区域视网膜脉络膜进行逐层观察,并根据需要采用软件附带功能进行定量分析,与历次光学相干层析血管造影(optical coherence tomography angiography,OCTA)图像进行纵向比较,最后进行详尽的OCTA 描述[8]。本文介绍了WF-OCT 技术的基本原理,并归纳了最新的技术进展以及其在眼科医学中的应用。
1 WF-OCT 技术
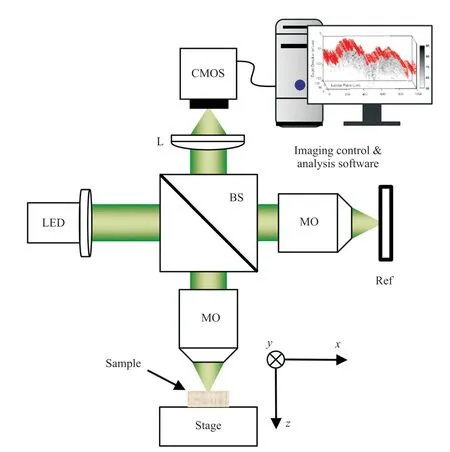
图1 典型的WF-OCT 系统[9]Fig. 1 Typical system of WF-OCT[9]
WF-OCT 系统利用平行光束照射在样品表面,利用二维探测器接收干涉信号获得样品的二维信息,一次性建立样品整个断面的三维图像,且能够在低相干光源下对表面反射率较高的样品的表面和次表面样品进行干涉信号的采集,并且具有大于50°的宽成像视场(field of view,FOV),更大幅度地提高了成像的效率及质量。典型WF-OCT系统的结构如图1[9]所示,主要由光学结构、机械运动以及采集传感三部分组成。由光源激光器发出激发光,经过光导纤维,以平行光束进入光纤耦联器;光纤耦联器将光束分成两束,一束进入包括扫描仪的样品臂进行组织取样,另一束则进入放有反射镜的参考系统。从反射镜返回的参考光和被样品背向反射回来的信号光在分束棱镜相遇。当它们的光程差处于光源的一个相干长度范围内时,会产生干涉信号。干涉信号包括了样品的二维信息,由二维相机检测并传送到电脑主机端。驱动步进电机和压电陶瓷移相器通过移动宏动台和微动台来控制参考镜的移动。在这过程中,扫描系统使从样品不同深度结构反射回来的信号光与参考光产生干涉,仅需要几秒钟的采集时间便可以获取变化数据集,同时计算机软件记录下样品内不同深度的结构特征的信息,据此进行特征提取、图像融合等处理,快速得到样品光谱,进而分析判断样品性能[10]。
2 WF-OCT 国内外发展现状
WF-OCT 技术主要在瞳孔、睫状体等外界伪影[11]、光学像素采集效率[12]以及视网膜曲率的问题上,通过硬件和软件两个方向进行逐步改善与提升。
2.1 WF-OCT 硬件的发展
OCT 的功能拓展有两个实现方法:一是增加光检测元件,直接提升硬件设施得到光谱;二是不改变OCT 系统的硬件配置,编写软件模块,通过对检测到的干涉信号做后期变换和处理来得到光谱信息。早在2011年,Li等[13]运用图像拼接技术将8个6 mm×6 mm的小OCT眼底数据拼接成了50°×35°的完整数据,并同时进行了纵向的运动纠正。2012年,Blatter 等[14]提出了傅里叶域模式激光的OCT 系统,实现了48°视场的眼底扫描。2015 年,Kolb 等[6]又展示了单体超宽场成像,其主要通过设计样品臂实现了单次B-scan 宽度为 85°和100°的WF-OCT 扫描。其中最高视场为100°视场角,并用100°×100°进行拼接,同时,在这种情况下采用了高清晰度、高密度的各向同性采样。研究中,与之前标准60°视场相比,采集受试者在100°视场中视网膜的单体超宽场成像数据几乎将覆盖面积增加了2 倍,提高了临床诊断的观察范围。
同样在2015 年,Zhang 等[15]使用宽场光学相干层析血管造影(wide-field optical coherence tomography angiography,WF-OCTA)对人眼视网膜进行实时眼动追踪。利用商用蔡司三维高清光学相干层析成像仪5000 系统中的慢速运动跟踪能力来演示视网膜微血管的无运动WF-OCT成像。按照一定的顺序连续采集多个2.0 mm×2.4 mm 的小范围区域,对每一个位置重复4 次B-scan 计算血管网,最终实现了12.0 mm×16.0 mm的大范围血管网成像(图2)。为了使数据更加可靠,同时更好地消除运动伪影的影响,系统运用了线扫描系统来辅助实现眼睛的运动追踪,使得采集更连贯,避免了后期大量的拼接计算。运动跟踪在评估和量化黄斑区时提供了良好的重复性和可靠性。这一特征预计在准确量化的纵向变化方面特别有用,可用于视网膜疾病,如糖尿病视网膜病变(diabetic retinopathy,DR)的诊断和治疗监测。直到近期,该研究组已经实现了28.2 mm×28.2 mm的实时眼动追踪拼接采集。
2017 年,Poddar 等[8]利用1.7 MHz、1 065 nm 的傅立叶域激光光源搭建了一套扫频源光学相干层析成像系统(swept source optical coherence tomography,SS-OCT),用于实现眼底5 mm×5 mm和9 mm×9 mm 2 种不同尺寸的光学相干层析血管成像的图像采集。其采用同一位置重复扫描5 次B-scan,通过计算同一位置随时间变化的相位方差来呈现血管网。在光路设计上,扫描场镜和眼底镜都是用光学相干层析成像的2 个非球面镜组合而成。最后同样用4 个5 mm×5 mm 的小视场拼接成了30°的大视场范围。同年,Huang 等[16]将光集成器件运用到了OCT 的样品臂光纤中,利用3 层分光器件将单根样品臂光纤分为8 根光纤,并将其依次纵向排列,相邻光纤的纵向间隔为0.25 mm,光程差为2.50 mm。至此,SS-OCT 就可以通过1 次扫描实现8 个不同位置的信息扫描。这样就间接缩短了扫描的时间,从而为大范围的血管网扫描提供了保障。
2.2 WF-OCT 采用的算法研究
前期的硬件配置已经得到较高水平的优化。考虑到经济成本开销,人们便将视线转移到了算法研究中来。2016 年,Zhang 等[17]利用WF-OCTA 提出了一种新颖的自动运动平行条带算法来校正运动伪影,改善图像质量。通过波长为1 045 nm、频率为200 kHz 的光源搭建了SS-OCT 系统,并对同一位置6 mm×10 mm 的区域连续采集2 次光学相干层析血管成像数据,最终用5 个相邻的6 mm×10 mm 眼底区域拼接成了25 mm×10 mm 的宽眼底视网膜图像。整个眼底的视网膜血管的完整性得到了很大的恢复,整个血管造影相当均匀。

图2 人眼视网膜微血管的WF-OCT 成像[15]Fig. 2 WF-OCT imaging of human retinal microvessel[15]
2017 年,Polans 等[18]搭建了一套单次En-face扫描范围达到70°的WF-OCT 系统,扫描长度约19.28 mm。人眼固有的像差导致视网膜外周区扫描的图像分辨率相比于视网膜中间的黄斑区要低得多,因此他们引入了Hofer 等[19]提出的无波前传感的自适应光学系统来矫正OCT 的成像像差。该方法通过迭代的方式实现了对像差的矫正,单次4.5 mm B-scan 的迭代优化时间为20 ms,4.5 mm×4.5 mm内的所有B-scan的迭代时间为3~10 s。
综上,在对WF-OCT 的应用上可以分为两个方面。第一个方面是用单次B-scan的图像对视网膜的结构进行检测,以此来实现视网膜脱离、视网膜劈裂等需要对视网膜外围的结构进行检测的疾病和需要较大范围测量的DR 等的检测。这种单B-scan的宽场扫描比较易于实现,OCT 系统的扫描速度也完全能够满足这种单次的大范围B-scan的需求。其难点在于视网膜自身的曲率带来的光程弯曲使得视网膜图像超出OCT 图像的视野,以及在扫描视网膜外围时,眼睛本身的像差带来的外围视网膜OCT图像不清晰。第二个方面是将其运用在大范围的光学相干层析血管成像功能上来检测眼底血管网的分布情况。由于系统的采集速度的限制,如果单次采集时间过长就会受到眼动带来的数据不连续的影响。因此各个科研组[6,8,13,15]分别采用正交配准、平行条带配准这种后处理的方式来去除眼动带来的影响,再运用图像拼接技术将不同位置采集的图像拼接成一个较大范围的图像。这种运用数据处理的方法虽然能够解决问题,但由于数据量过大,导致运算时间过长以及在拼接时会出现数据缺失等情况,使得其较难实现商业化。另外还有一种运用硬件来解决该问题的方法,即用一套独立的系统来辅助进行眼动追踪。在光学相干层析血管成像数据采集时如有眼动发生,系统则会及时作出响应,调整光斑到正确的位置。这种方法可以使得操作更连贯,被测者更易于配合,得到的图像更可靠,也更容易实现随访。
3 WF-OCT 在眼科学中的应用
自OCT 被引入眼科学以来,它在成像协议、算法和新参数方面取得了重大进展。这些新参数最大限度地发挥了其在诊断、评估治疗反应和评估各种眼科疾病进展中的潜力[20]。WF-OCT 最常用于眼部疾病诊断,现广泛地应用于DR、青光眼、新生血管型老年性黄斑病变(age-related macular degeneration,AMD)等疾病诊断中。DR 经常伴随着视网膜血管闭塞,甚至新生血管(new vessels,NV)的形成[21];青光眼常常会因视网膜血流量的减少而导致失明[22];AMD 通常有脉络膜NV 生成等不同的眼底病理特性[23]。外周OCT 检查可以清楚地描绘视网膜层,并且能提高对视网膜层分裂与整个视网膜升高的诊断,但视网膜外周区域的局部缺血等症状往往难以被检查到。WF-OCT 技术在系统的成像可见范围、速度和灵敏度方面都有显著提高,对视网膜外周区域的检查、糖网病的早期预判和视网膜外周其他疾病的随访和治疗(如靶向外周光凝)等具有很好的指导价值,已成为目前OCT 领域的研究热点,具有巨大的发展潜力。
3.1 视网膜血管性疾病
视网膜血管性病变[24]是由眼部或全身性血管疾病引起的视网膜出血、渗出、水肿、缺血或梗塞,包括DR、视网膜中央动脉阻塞等。
DR 是糖尿病性微血管病变中最重要的表现,是一种具有特异性改变的眼底病变(图3)[25],是糖尿病的严重并发症之一。You 等[26]探讨了WF-OCTA 在临床上DR 患者中难发现的NV 的检测价值,发现WF-OCTA 可检测出临床检查或彩色照片上未见的小NV,可提高对DR 的临床评价。Yasukura等[27]探讨了DR 的WF-OCTA 图像中各小动脉分割的非灌注区。WF-OCTA 图像显示位于浅层和深层的大小动脉似乎是灌注边界,通过侧支血管介导的重叠灌注可能影响每个分支区域糖尿病的可能性。
Chung 等[28]用基于OCTA 的宽场剪辑技术,对视网膜静脉阻塞患者在改善微血管障碍视网膜分支静脉阻塞治疗后的效果进行了跟踪,发现该技术能够很好地描述在经过抗血管内皮生长因子治疗后患者视网膜分支静脉阻塞相关微血管障碍的改善情况,并有望进一步评估该疾病的治疗进展。
Tian 等[29]应用WF-OCTA 评估视网膜血管炎的中度葡萄膜炎患者的血管改变。WF-OCTA 镜下的中度葡萄膜炎的脉络膜和深层毛细血管丛的改变比浅层毛细血管丛更明显。虽然WF-OCTA 扫描是检测中度葡萄膜炎毛细血管非灌注的可靠工具,但它对确定疾病活动度没有帮助。

图3 不同严重程度DR的WF-OCT 成像[25]Fig. 3 WF-OCT imaging of eyes with different DR severities[25]

图4 脉络膜WF-OCT 成像[30]Fig. 4 WF-OCT imaging of choroid structure[30]
Kakiuchi 等[30]探讨了WF-OCT 获得的图像中的黄斑下和斑周脉络膜结构,发现在OCT 图像中,黄斑区脉络膜管腔的比例变化很小,但在黄斑周区变化很大,提供了关于正常情况和疾病相关改变的重要信息(图4)。
3.2 青光眼及视神经疾病
青光眼是一组以视乳头萎缩及凹陷、视野缺损及视力下降为共同特征的疾病,是导致人类失明的三大致盲眼病之一。Lee 等[31]比较了WF-OCT 的视网膜神经纤维层(retinal nerve fiber layer,RNFL)图与光谱域OCT 图对周前病变和早期青光眼的诊断能力。WF-OCT 的RNFL 厚度图显示了与光谱域OCT图相似的对健康眼周前病变和早期青光眼的诊断能力,在临床中可以有效地检测早期青光眼的变化。
Hood 等[32]评估了一份基于WF-OCT 方案的青光眼诊断报告。通过分析108 例青光眼或疑似青光眼的临床单页报告,再与后期患者的病情相结合,进行病情诊断与分析。这份单页报告包含RNFL 厚度图、视网膜神经节细胞层概率图、RNFL 黄斑和视神经厚度概率图和视神经图像。一份基于WF-OCT扫描的单页报告可以提供极好的早期青光眼诊断所需的敏感性和特异性信息。
进一步,Muhammad 等[33]探讨了利用混合深度学习方法与WF-OCT 相结合,以区分先前被分类为疑似青光眼和轻度青光眼的眼睛。混合深度学习方法的方案在区分疑似青光眼和早期青光眼方面优于标准OCT 临床指标,但应该进一步改进现算法,进而提高筛选的灵敏度与检测准确率。
同样,WF-OCT 在眼底肿瘤方向也有应用。Lim 等[34]采用WF-OCTA 调查了经过放射治疗后脉络膜恶性黑色素瘤伴明显放射性视网膜病变(choroidal melanoma with clinically evident radiation retinopathy,CERR)的发生率,发现在105 位脉络膜恶性黑色素瘤患者中,CERR 的发生率几乎达到50%。WFOCTA 成像显示:与对照组相比,CERR 在整个宽视野和毛细血管周围区域,浅丛和深丛的中心凹无血管区扩大,毛细血管密度(capillary vascular density,CVD)降低;与未发生CERR 患者相比,发生该病变的患者其视网膜表面和深丛的CVD 都减少,毛细血管周围区域以及乳头状黄斑束浅丛的CVD 也减少(图5)。这些发现对早期发现和监测放射性视网膜病变非常重要。
以上研究结果表明,作为一种眼科学诊断辅助光学相干成像工具,WF-OCT 技术在提高疾病信息成像鉴别方面有着巨大的作用。
4 总结与展望

图5 WF-OCT技术在CERR监测中的应用[34]Fig. 5 Application of WF-OCT for CERR monitoring[34]
OCT 广泛应用于生物医学领域,无需标记即可对组织中的深度微结构形态进行成像。WF-OCT是OCT 的全场、高横向分辨率版本。它使用简单的非相干光源、高数值孔径物镜和二维检测器,无需扫描即可获取给定深度下样本的正面视图。在体内组织中,这些动态的技术被认为是在微观结构水平测量弹性组织的有效手段。对于传统成像技术,WF-OCT 有两个主要优势:第一,切片能力能够将散射体的运动排除在相干之外;第二,干涉性质使它们对轴向尺寸的相位变化非常敏感。轴向尺寸的相位变化远小于光轴分辨率,低至十几纳米。总而言之,扩大视野的宽领域扫描可以清楚地发现在临床检查和眼底照片中的漏诊部分。对于多种眼科疾病来说,一般研究视网膜疾病、青光眼、视神经病变、白内障等,WF-OCT 技术有可能使疾病增殖阶段的测定更加可靠和客观,并且该技术更安全、更快、更便宜,更适合于常规监测,特别是在严重的非增殖性DR 或接受抗血管内皮生长因子治疗的黄斑水肿等这些具有较长潜伏期、不易监测早期患病现象而导致错失最佳治疗时间的眼底疾病。然而,从基础研究到临床转化的过程中,发展和优化光检测元件扫描视图范围和数据处理部分以提高监测治疗效果仍是今后WF-OCT 技术研究的重要方向。随着WF-OCT 技术的不断发展与改进,其将在眼科医学领域发挥更大的作用。

