醒脑静注射液联合阿替普酶治疗急性缺血性脑卒中临床疗效的Meta分析*
成知叡 刘福生 王苏妹 孙琛琛 靳 辉 胡 曼 方晓磊△
(1.北京中医药大学,北京 100029;2.北京中医药大学东方医院,北京 100078)
急性缺血性脑卒中(AIS)具有高发病率、高死亡率和高致残率的特点,发病3~4.5 h严重危害患者的健康和生命[1]。目前,重组组织纤溶酶原激活剂阿替普酶(Rt-PA)已被广泛应用于AIS发病3~4.5 h内的治疗[2]。然而,只有20%~30%的患者使用Rt-PA后实现了完全再通,并且阿替普酶可诱发再灌注损伤,包括出血性转化或大量水肿[3]。虽然,阿替普酶溶栓治疗是早期血管再通的主要方法,但由于大动脉闭塞的时间窗严格,再通率低,只有少数患者能获益。因此,有必要探索一种有效而简单的方法来改善这类患者的血管再通。
当前中药已被广泛用作于神经系统疾病的辅助治疗手段。其中,醒脑静注射液是治疗AIS最常用的中成药之一,它是由安宫牛黄丸进行改良后制成的,由麝香、冰片、香姜黄、栀子等成分组成[4]。醒脑静注射液能穿透血脑屏障,直接作用于中枢神经系统,可以促进AIS患者康复、缩短昏迷时间、减少并发症等[5]。既往研究表明,醒脑静注射液可能具有多种神经保护机制,如抑制谷氨酸诱导的凋亡、抑制氧化应激、改善神经行为障碍以及降低梗死灶大小等[6-7]。最近,醒脑静注射液联合阿替普酶溶栓可以显著改善AIS的临床结局,促进神经功能恢复,减少并发症。然而,早期试验受到样本量小的限制,其结果需要进一步确认。因此,本研究的目的是对醒脑静注射液联合阿替普酶治疗AIS有效性和安全性进行系统评价,以期为临床实践提供依据。
1 资料与方法
1.1 文献选择
1)入选标准:(1)试验选择研究依据公认、权威的AIS诊断标准,其诊断符合《中国急性缺血性脑卒中诊治指南2018》[8]中的诊断标准。经CT和MRI检查确诊为急性缺血性卒中的成年患者;(2)公开发表的临床随机对照试验(RCT);(3)干预措施,比较醒脑静+阿替普酶联合治疗与阿替普酶单用对急性缺血性卒中患者的临床疗效;(4)结果指标,主要结局指标为治疗有效率,次要结局指标包括美国国立卫生院卒中量表评分(NIHSS)、蒙特利尔认知评估量表(MoCA)、纤维蛋白原水平(FIB)、凝血酶原时间(PT)、部分凝血活酶时间(APTT)、D-二聚体;(5)发病≤4.5 h;(6)文献中所选患者不合并严重器质性疾病及并发症;(7)试验措施为醒脑静注射液联合阿替普酶静脉溶栓治疗;(8)预期获得的结局判定标准明确。2)排除标准:动物研究;未提供相应结局指标数据;重复发表、出版的研究;无法获得可用数据的研究。
1.2 文献检索策略
计算机检索万方全文数据库(Wanfang)、中国知网(CNKI)、中文科技期刊全文数据库(VIP)和中国生物医学文献数据库(CBM),收集有关醒脑静注射液+阿替普酶联合治疗与阿替普酶单用对急性缺血性卒中患者的临床疗效的RCT研究,检索时间从建库至2020年8月1日。中文检索词:“醒脑静”“阿替普酶”“缺血性脑卒中”“脑卒中”“脑梗死”。英文检索词:“xingnaojing injection”“alteplase”“acute ischemic stroke”“stroke”。
1.3 文献筛选和数据提取
由2名研究员独立筛选文献,并对筛选结果进行交叉核对,如发生分歧则与第3名研究员讨论协商。2名研究人员独立提取数据并交叉核对。资料提取内容包括:第一作者姓名,出版年份,性别、年龄、样本量、实验组和对照组的治疗方式以及结果指标;纳入研究的基本信息:第一作者、发表时间;研究对象的基线特征;干预措施;结局指标。
1.4 评估纳入研究的偏倚风险评价
2名研究员根据Cochrane handbook提供的RCT偏倚风险评估工具对所纳入的研究进行偏倚风险评估,评估结果交叉核对。
1.5 统计学处理
采用Stata12.0软件进行统计分析。计量资料采用标准化均方差(SMD)为效应分析统计量和95%可信区间表示,二分类变量采用风险比(RR)为效应分析统计量和95%可信区间表示。P<0.05被认为差异有统计学意义。研究间的异质性采用χ2检验和I2统计量评估异质性,当I2<50%或P>0.1时,表明研究间具无异质性,采用固定效应模型进行分析。反之采用随机效应模型进行分析。当研究间具有高度异质性时,可采用敏感性分析和亚组分析来寻找异质性的来源。
2 结 果
2.1 文献筛选流程及结果
计算机检索得到84篇文献,经逐层筛选,最终19篇文献[9-27]符合纳入标准,包括1 768例患者。文献筛选流程见图1。

图1 文献筛选流程图
2.2 纳入研究的基本特征与偏倚风险评价结果
纳入研究的基本特征见表1。纳入研究的偏倚风险评价结果见表2。

表1 纳入研究的基本特征

表2 纳入研究的偏倚风险评价结果
2.3 Meta分析结果
2.3.1 治疗有效率 13项研究比较了两组的治疗有效率,包括实验组561例、对照组560例。异质性检验结果显示组间具有同质性(I2=0%,P=0.99),采用固定效应模型。Meta分析结果显示,醒脑静注射液+阿替普酶联合治疗的有效率显著高于对照组,RR=1.24,95%CI[1.17~1.32],P<0.001,见图2。
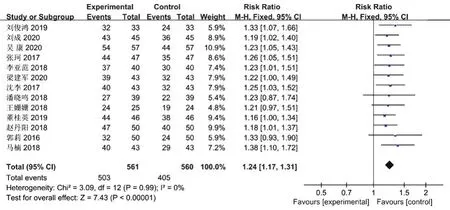
图2 醒脑静注射液联合阿替普酶和单用阿替普酶治疗有效率比较的森林图
2.3.2 NIHSS评分 9项研究比较了两组治疗前后NIHSS评分,包括实验组427例、对照组427例。异质性检验结果显示组间具有同质性(I2=86%,P<0.001),采用随机效应模型。Meta分析结果显示,与阿替普酶组相比,醒脑静注射液联合阿替普酶治疗可以显著改善AIS患者的NIHSS评分,SMD=-1.30,95%CI[-1.70~-0.89],P<0.001,见图3。

图3 醒脑静注射液联合阿替普酶和单用阿替普酶对NHISS改善作用比较的森林图
2.3.3 MoCA评分 5项研究比较了两组治疗前后MoCA评分,包括实验组266例、对照组266例。异质性检验结果显示组间具有同质性(I2=20%,P=0.29),采用固定效应模型。Meta分析结果显示,与阿替普酶组相比,醒脑静注射液联合阿替普酶治疗可以显著改善AIS患者的MOCA评分,SMD=0.97,95%CI[0.79~-1.15],P<0.001,见图4。

图4 醒脑静注射液联合阿替普酶和单用阿替普酶对MoCA改善作用比较的森林图
2.3.4 不良反应 5项研究比较了两组治疗后的不良反应,包括实验组288例、对照组288例。异质性检验结果显示组间具有同质性(I2=0%,P=0.86),采用固定效应模型。Meta分析结果显示,醒脑静注射液联合阿替普酶治疗的不良反应发生率低于对照组,RR=0.4,95%CI[0.22~0.72],P=0.002,见图5。

图5 醒脑静注射液联合阿替普酶和单用阿替普酶不良反应比较的森林图
2.4 纤溶指标与凝血指标分析
见表3。与阿替普酶组相比,醒脑静+阿替普酶联合治疗组能明显改善FIB、PT、APTT和D-二聚体含量。

表3 纤溶指标与凝血指标分析
2.5 发表偏倚
如图6所示,治疗有效率的漏斗图基本对称,表明本研究无明显发表偏倚。

图6 有效率发表偏倚漏斗图
3 讨 论
AIS是世界范围内导致死亡和残疾的主要原因之一。静脉注射Rt-PA溶栓已被证明是治疗AIS最有效的治疗方法。然而,有限的时间窗和出血转化相关的副作用限制了其广泛的应用,50%接受静脉溶栓的患者在90 d后无法实现无残疾。另外,Rt-PA可能由于其纤溶作用而加重脑损伤,并导致血脑屏障破坏,以及其他不良反应[28]。毛细血管内皮功能障碍引起的血脑屏障通透性异常和强烈的炎症反应是阿替普酶治疗后早期脑水肿和缺血脑组织出血性转化的基础[29]。此外,阿替普酶可能会降低细胞外基质的完整性,增加出血性转化的风险[30]。与未接受静脉溶栓的患者相比,出血性转化的风险更高。颅内出血的发生率为9%~27%[31]。因此,通过辅助治疗来提高静脉Rt-PA溶栓的疗效可能是解决这一问题的有效途径。
近年来,醒脑静注射液被广泛用于治疗AIS。研究表明,醒脑静注射液具有降低血脑屏障通透性、减轻脑积水、清除自由基、促进患者康复、缩短昏迷时间、减少脑病并发症等作用,在一定的剂量和时间范围内广泛应用。此外,醒脑静注射液可以为加速出血部位侧支循环构建、增加毛细血管网、降低血管压力的有效药物。临床研究发现,醒脑静注射液作为辅助疗法可以降低血压、维持水/电解质平衡[32]。本研究共纳入了19篇RCT,包括1 768例,这些研究调查了醒脑静注射液联合阿替普酶治疗AIS患者的临床疗效。Meta分析的结果发现,醒脑静注射液联合阿替普酶治疗比单独阿替普酶更有效。此外,与单独阿替普酶治疗相比,醒脑静注射液联合阿替普酶治疗可以显著改善AIS患者神经功能缺损和认知功能。这些结果提示,醒脑静注射液是一种有效的辅助疗法。5项研究报道了醒脑静注射液联合阿替普酶治疗与阿替普酶治疗后不良反应。Meta分析的结果发现,醒脑静注射液联合阿替普酶联合治疗的不良反应发生率低于对照组。综合分析结果发现,与单独阿替普酶治疗相比,醒脑静注射液联合阿替普酶治疗具有抗凝和抑制血小板聚集的作用。
本研究的局限性:1)纳入研究质量不高,许多RCT不采用严格的方法,对分配隐瞒、致盲、治疗意图和退出的报告不足,可能造成选择性报道。2)所有纳入研究均在国内,尚不清楚醒脑静注射液联合阿替普酶对其他人群的疗效。3)纳入的研究未报道醒脑静注射液联合阿替普酶疗法的远期疗效。4)纳入研究的醒脑静使用剂量不一,醒脑静注射液的最佳治疗剂量和疗程需要进一步探索。
综上所述,这些结果发现醒脑静注射液联合阿替普酶可显著提高AIS患者治疗有效率,减少不良反应发生率,改善神经功能缺损和认知功能障碍。然而,由于样本量较小以及研究的局限性,我们的研究结果必须谨慎解释。因此,还需要进行大规模、高质量、多中心的RCT研究予以验证。

