组织学绒毛膜羊膜炎影响因素分析及临床模型构建
吕秀梅
(宁陵县人民医院 产科,河南 商丘 476700)
绒毛膜羊膜炎是胎盘组织感染病球菌或B族溶血性链球菌形成的非特异性炎症反应[1],好发于早产阶段或胎膜早破特别是未足月胎膜早破。绒毛膜羊膜炎分为组织学绒毛膜羊膜炎(histologic chorioamnionitis,HCA)和临床绒毛膜羊膜炎两种。HCA的发生率显著高于临床绒毛膜羊膜炎,患者常无临床症状,仅在胎盘病理检查时发现。既往研究显示,HCA和未足月儿败血症、脑瘫等不良妊娠结局相关,而早期快速、准确诊断HCA对改善妊娠结局具有重要意义[2]。梁海英等[3-5]采用多因素回归模型分析了中性粒细胞、淋巴细胞等炎症指标可以预测早产、胎盘炎症及绒毛膜羊膜炎的发生,但均未建立有效的预测模型。本研究选取2017年2月至2020年5月宁陵县人民医院收治的312例未足月胎膜早破患者作为研究对象,探讨HCA发生的影响因素及构建预测评估模型,为HCA的临床诊疗提供指导。
1 资料与方法
1.1 一般资料选取2017年2月至2020年5月宁陵县人民医院收治的312例未足月胎膜早破患者作为研究对象,最终入组204例未足月胎膜早破患者,根据美国妇产科医师学会(American College of Obstetricians and Gynecologists,ACOG)指南将其分为未足月胎膜早破合并组织学绒毛膜羊膜炎组(HCA组,91例),未足月胎膜早破合并无组织学绒毛膜羊膜炎组(非HCA组,113例),平均年龄(29.51±3.06)岁,平均孕次(2.18±1.25)次,平均产次(1.49±0.86)次。本研究经宁陵县人民医院医学伦理委员会审核批准。
1.2 选取标准(1)纳入标准:①孕周为28~37+6周;②符合2018年ACOG针对未足月胎膜早破发布的第188号实践指南(ACOG指南)诊断标准;③单胎妊娠;④患者签署知情同意书;⑤临床生化检测完整。(2)排除标准:①合并其他精神疾病;②合并生殖系统急性炎症;③合并早产高危症;④胎盘位置异常。
1.3 研究方法收集患者基线资料,包括年龄、孕次、产次、早产史、破膜时间、破膜孕周等资料;采用西森美康XN-1000全自动血细胞分析仪检测红细胞分布宽度、白细胞、中性粒细胞、淋巴细胞;采用日立7180全自动生化分析仪检测C反应蛋白(C-reactive protein,CRP);采用全自动红细胞沉降率分析仪检测红细胞沉降率、中性粒细胞与淋巴细胞比值(neutrophil To lymphocyte ratio,NLR)和血小板与淋巴细胞比值(platelet to lymphocyte ratio,PLR)。

2 结果
2.1 患者基线资料两组破膜孕周、白细胞、CRP、中性粒细胞、淋巴细胞、NLR及PLR比较,差异有统计学意义(P<0.05)。见表1。
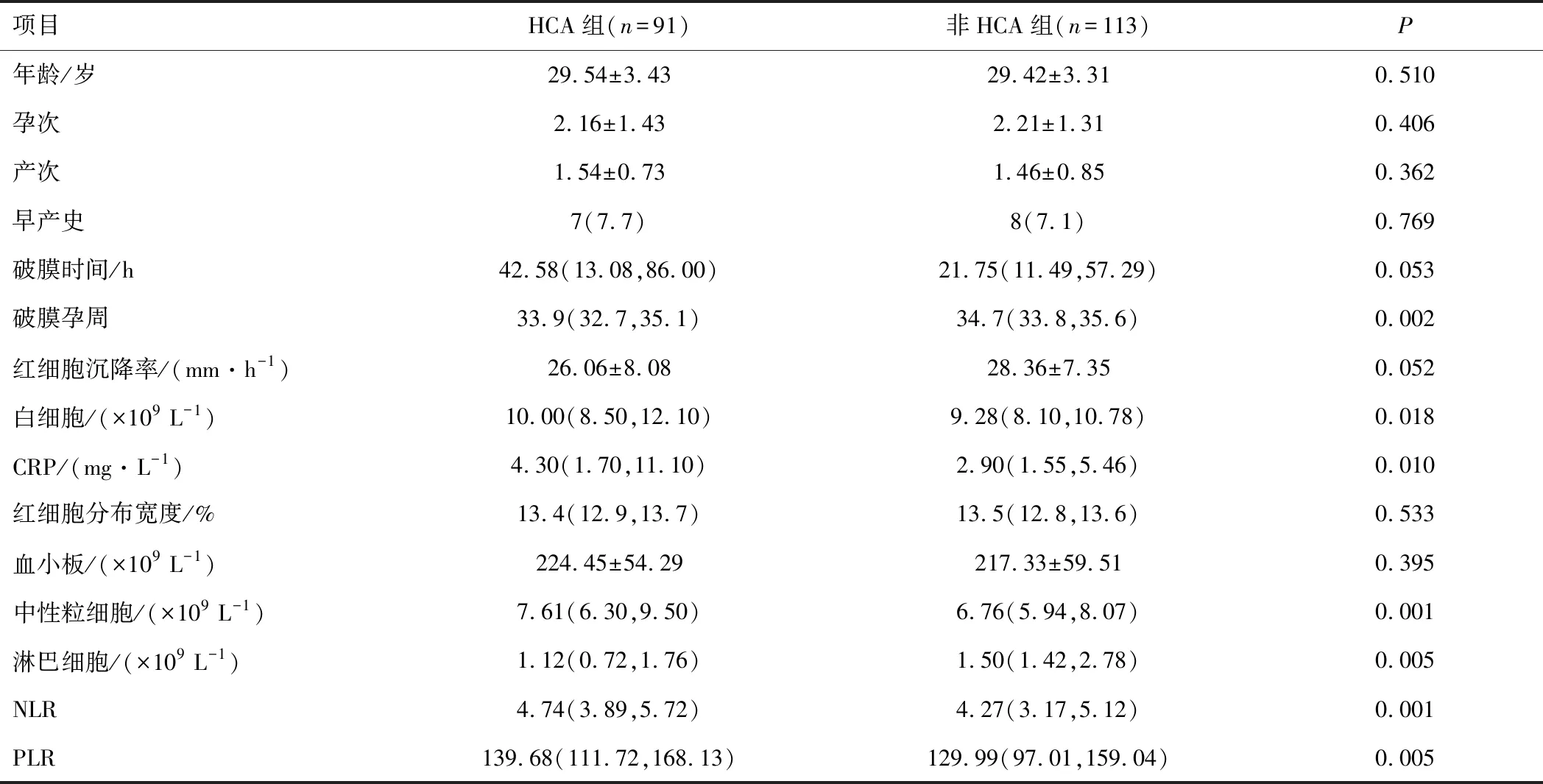
表1 两组基线资料比较
2.2 多因素logistic回归模型分析利用logistic多因素回归模型,采用LR法调整白细胞、PLR、中性粒细胞及淋巴细胞等变量后显示,破膜孕周(OR=0.907,95% CI:0.583~0.962,P=0.019)、NLR(OR =1.092,95% CI:1.003~1.563,P=0.005)、CRP(OR=1.028,95% CI:1.004~1.856,P=0.001)是未足月胎膜早破合并HCA发生的独立因素。见表2。通过模型系数构建预测模型如下:
P=1/[1+exp(-6.086-0.140×α1-0.262×α2+0.334×α3)]。
其中α1为CRP,α2为NLR,α3为破膜孕周。
hosmer-lemeshow模型拟合度显示,预测模型拟合度较好(χ2=2.956,df=8,P=0.920)。
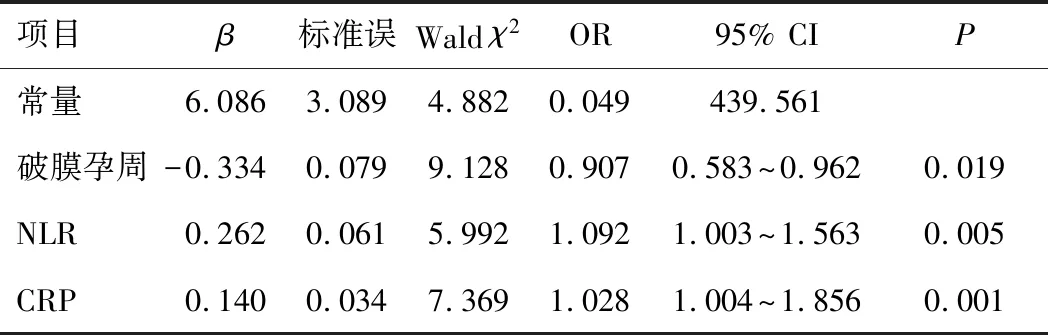
表2 多因素logistic回归模型分析
2.3 模型预测效能破膜孕周、NLR、CRP及模型预测未足月胎膜早破合并HCA的曲线下面积分别为0.626(0.503~0.696)、0.632(0.515~0.653)、0.606(0.515~0.753)及0.705(0.615~0.803),敏感度分别为57.3%、78.6%、38.6%及78.6%,特异度分别为76.8%、33.5%、83.5%、48.1%。
3 讨论
未足月胎膜早破是妊娠<37周产妇的常见并发症,发生率为2%~3%,常合并绒毛膜羊膜炎[6]。未足月胎膜早破合并HCA早期无明显临床表现,产前诊断困难,可引起胎儿窘迫、早产,新生儿败血症、新生儿神经功能及肺功能发育异常,增加产妇和新生儿病死率。目前,羊水穿刺培养和产后胎盘病理检查是诊断HCA的主要手段,羊膜腔穿刺羊水培养可能增加母体感染风险;胎盘病理检查具有滞后性,这导致上述两种诊断方法的临床应用受到限制。研究显示,炎症、感染生化指标可能是早期诊断绒毛膜羊膜炎的潜在生物标志物[3-4]。白细胞介素-6、白细胞介素-8等虽然可以更准确地反映机体炎症状态,但所需实验设备较特殊,无法在基层开展,且检查时间较长。因此,探讨更加简便、快捷、无创的炎症标志物对保证未足月胎膜早破合并HCA患者生命健康具有重要意义。本研究对HCA患者的临床常见外周血炎症指标分析发现,与非HCA孕妇外周血相比较,HCA孕妇外周血中中性粒细胞、CRP、白细胞、NLR、PLR更高,淋巴细胞更低,破膜孕周更早。将上述潜在变量纳入多因素logistic回归分析发现,破膜孕周、CRP和NLR是HCA发生的独立危险因素。基于回归模型进一步建立的联合预测模型可以为HCA的临床诊疗提供指导。研究显示,早产孕妇妊娠时间越晚,破膜孕周越早,宫内感染风险更大[7]。本研究结果显示,破膜孕周越早HCA的发生风险越高,而新生儿脑神经发育和肺功能情况与破膜孕周有关。鉴于目前羊水穿刺培养是产前诊断HCA的唯一方法,本研究为临床指导HCA高危患者提供更多产前信息。
CRP通常应用于临床诊断细菌感染。国外研究早已将CRP应用于预测HCA的发生[8]。本研究亦发现,HCA孕妇外周血CRP水平显著高于非HCA孕妇。NLR是一种新型炎症细胞预测标志物,可以反映机体炎症-免疫平衡,已广泛应用于心血管疾病、血液疾病的预后预测。早有研究发现外周血NLR与宫内感染性早产有关[9]。从炎症机制角度而言,NLR相比CRP更具优势。本研究结果显示,NLR风险系数及曲线下面积均高于CRP,与预期结果一致。另外,联合上述外周血生化指标及临床特征建立预测模型,其受试者操作特征曲线面积为0.705(0.615~0.803),模型预测准确性高于单一指标,且该模型简单、可靠,拟合度较好,可以为临床治疗及预后提供可靠信息。
综上所述,破膜孕周、NLR、CRP是未足月胎膜早破合并HCA发生的独立预测因素,联合检测可以有效提高未足月胎膜早破合并HCA的诊断价值。

