二甲双胍在抗癌领域的研究进展 *
熊惠娟,王宇静,李向华,胡春弟,王小波
(湖北科技学院药学院,湖北 咸宁 437100)
1922年,Werner等[1]合成了二甲双胍及相关的双胍类化合物,为二甲双胍的广泛应用奠定了基础。二甲双胍作为小分子药物,它具有廉价、安全、容易被吸收等特点。多项研究表明,二甲双胍可通过激活腺苷活化蛋白激酶(AMPK),抑制mTOR信号通路和胰岛素样生长因子信号转导来阻碍肿瘤细胞增殖[2-4],能活化抑癌基因p53来阻滞肿瘤细胞周期以及诱导细胞凋亡,还可以通过调节细胞线粒体中的能量供需平衡来达到抑制肿瘤的效果[5-6],这些功能使二甲双胍能够降低由2型糖尿病引起的肝癌、胰腺癌、子宫内膜癌、结肠癌、乳腺癌和膀胱癌等癌症的风险[7]。Bowker等[8]的研究结果表明,接受二甲双胍治疗的糖尿病患者的相关癌症死亡率明显比接受磺脲类降糖药物或胰岛素患者的相关癌症死亡率低。种种实验迹象表明,二甲双胍在降低多种癌症死亡率、延长生存期等方面具有不可磨灭的贡献,目前,对于二甲双胍抗癌活性的作用机制有了一定的认识,但是综合来看,依然只是可见一斑。本文主要从近些年单独使用二甲双胍、与其他药物联合以及结合其他治疗方法在抗癌领域的一些代表性研究成果进行综述。
1 单独使用二甲双胍
在现有的相关试验中[9]已经证明了二甲双胍在对卵巢癌、胰腺癌、大肠癌、急性早幼粒细胞白血病、肝癌、乳腺癌等相关癌症中具有出乎意料的抗癌效果。
1.1 卵巢癌
Hart等[10]通过一系列体外试验证明,二甲双胍可以调节鞘脂变阻器,从而减轻由鞘氨醇-1-磷酸(S1P)引起的卵巢癌吞噬。S1P是鞘氨醇的一种生物活性代谢产物,它可以增强细胞增殖,并在TYKNU和CAOV3卵巢癌细胞中表达,本实验使用qRT-PCR技术、免疫印迹法、MTT检测和集落形成试验证明二甲双胍可以抑制S1P的蛋白表达,并发现S1P变阻器是二甲双胍在卵巢癌中的新靶点,其中SPHK1是鞘氨醇激酶(SPHK)的一种脂质介质,催化鞘氨醇形成S1P,SPHK1水平升高可以增加对二甲双胍的敏感性,SPHK1的水平降低可以增强对二甲双胍的耐药性,对于缺氧诱导的SPHK1尤其敏感,这对于将高度表达的SPHK1作为预测生物标志物也具有重大意义。
1.2 胰腺癌
Boukalova等[11]设计合成了一种线粒体靶向二甲双胍MitoMet(见图1)和它的类似物NorMitoMet,用结晶紫染色法测定了他们对不同胰腺癌细胞株的活力影响。实验结果显示MitoMet比二甲双胍杀死胰腺癌细胞的效率要高四个数量级,而NorMitoMet的IC50值比MitoMet约高20倍,该团队通过高分辨率呼吸测量发现MitoMet和NorMitoMet均通过靶向线粒体复合物I(CI)抑制细胞呼吸,细胞的呼吸频率越高,糖酵解的速度越低,那么胰腺癌细胞对MitoMet和NorMitoMet的敏感性就越高,因此,这是一类十分具有研究价值的抗癌药物,可以大大提高胰腺癌细胞的死亡率,节约成本。
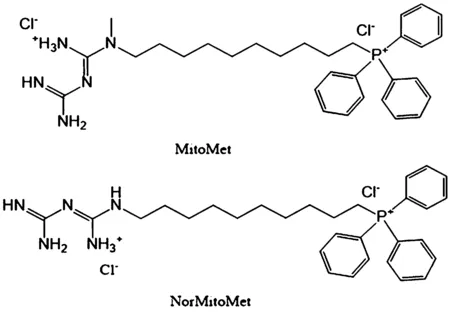
图1 MitoMet和NorMitoMet的分子结构
1.3 结直肠癌
Nguyen等[12]在一项药理性抑制研究中表明,二甲双胍可以通过抑制NADPH氧化酶活性抑制石胆酸(LCA)诱导的活性氧(ROS)产生,从而降低转录因子NF-κB活性,以调控由LCA刺激引起的白细胞介素-8(IL-8)上调,阻止大肠癌细胞(CRC)的增殖和血管生成。LCA已经被证明是CRC的启动子,LCA通过产生ROS破坏胃肠道上皮衬里、诱导癌症干细胞增殖、帮助癌细胞逃过免疫系统的侵袭。该团队在最新的研究中发现,LCA可以诱导CRC细胞中IL-8的表达,使大肠癌细胞增殖和生成血管。该团队对二甲双胍的研究加深了我们对它的抗癌作用的理解,为二甲双胍在CRC治疗中提供了新的思路。
1.4 急性早幼粒细胞白血病细胞
怀磊等[13]设计了一项针对二甲双胍对急性早幼粒细胞白血病细胞系NB4细胞的影响和作用机制的体外试验,使用MTT比色法检测NB4细胞的增殖能力,Western blot检测细胞外信号调节激酶(ERK)磷酸化水平,以此判断细胞凋亡率和粘附力能力的大小。该实验结果表明,二甲双胍以浓度和时间依耐性降低NB4细胞的增殖和分化,加速细胞凋亡,增强细胞与细胞间的粘附能力,防止肿瘤细胞进一步扩散至其他正常细胞和组织中。该团队在探讨二甲双胍这种影响的作用机制中发现,二甲双胍可能通过MEK/ERK信号通路、LKB1/AMPK信号通路、激活caspase-3蛋白酶等方式抑制NB4细胞增殖和分化,促使肿瘤细胞的凋亡和粘附。
1.5 肝癌
Shankaraiah等[14]构建了一种肝硬化背景下CCl4诱导肝癌小鼠模型,旨在探讨二甲双胍与肝肿瘤之间的关联。该小组通过转氨酶分析测定二甲双胍干预的小鼠肝脏的谷丙转氨酶(AST)和谷草转氨酶(ALT)水平,用超声波监测小鼠肝脏的结节生长情况,Western blot分析二甲双胍给药前后影响小鼠肝脏中纤维化的a-SMA蛋白水平,用肝脏组织病理学观察肝细胞中影响肝硬化的指标:脂滴积累。最终研究结果显示,二甲双胍能有效抑制肝星状细胞(HSC)激活,减少肝脏纤维化及肝硬化,预防肝肿瘤发生。此外,该团队还发现二甲双胍对肝癌细胞的抑制作用是通过激活LKB1介导的AMPK通道实现的。
1.6 乳腺癌
Yang等[15]进行了一项关于二甲双胍对乳腺癌细胞作用机制的细胞试验,该团队应用了MTT法、RT-PCR法、免疫印迹分析、荧光素酶报告基因检测以及染色质免疫沉淀分析等常规技术手段验证了二甲双胍对乳腺癌细胞增殖具有显著的抑制作用,降低癌细胞中高迁移率族蛋白2(HMGA2)的启动子、mRNA和蛋白质水平,HMGA2在癌细胞中能促进癌细胞的增殖和扩散,常在乳腺癌、结肠癌或肺癌细胞中表达。该小组研究人员还发现HMGA2启动子的激活可能与转录因子SP1有关,而二甲双胍则通过下调转录因子SP1的数量以达到灭活HMGA2的目的。
2 二甲双胍联合其他抗癌药物
目前临床上用于治疗癌症的主要是一些天然的抗癌活性物质和铂类化合物,它们通常抑制癌细胞的有丝分裂和线粒体呼吸[16],降低线粒体膜电位水平[17],促进细胞色素c释放[18],使细胞产生ROS来阻碍肿瘤生成,诱导凋亡[19]。但这些药物具有毒性大、敏感性差、细胞易耐药等副作用[20],限制它们的临床作用,联合二甲双胍却能有效降低这些副作用。
2.1 联合紫杉醇
Zhao等[21]为了评价二甲双胍和紫杉醇(PTX)联合使用对前列腺癌(PCa)细胞的影响,采用MTT法和显微镜观察二甲双胍和PTX联合应用后PCa细胞的增殖情况,Annexin V和碘化丙啶染色法对PCa凋亡细胞进行流式细胞术检测,并以单独使用MET作为对照组。结果显示,MET和PTX以剂量和时间依赖的方式抑制PCa细胞的生长并增加了PTX对肿瘤细胞的敏感性,方便PTX更好地杀死癌细胞。该团队在对该作用的机制研究中发现,MET和PTX联合可显著提高引起细胞凋亡的蛋白酶caspase-3/7的活性,降低抗细胞凋亡蛋白Bcl-2的表达,促进PCa细胞产生ROS,降低细胞内线粒体膜电位和ATP水平,加快PCa细胞死亡并抑制它的生长,该团队接下来的研究将重点放在雄激素是否会对PCa细胞的ROS水平产生影响。
2.2 联合奥沙利铂
Huang等[22]在探究二甲双胍在奥沙利铂(OXA)治疗结直肠癌(CRC)的作用中发现,二甲双胍可通过降低癌细胞高迁移率族蛋白1(HMGB1)mRNA的表达加强OXA对结直肠癌细胞的毒性,抑制其生长,OXA以剂量依赖性的方式诱导高迁移率族蛋白1(HMGB1)mRNA在细胞中的表达,HMGB1是一种高度保守的核蛋白,它可以在细胞核中结合各种转录因子,修复损伤的DNA双链,增加细胞核DNA的复制、转录和修复过程,还可以增加癌细胞对OXA的耐药性,抑制促进细胞凋亡的蛋白酶caspase-3/7的活性,HMGB1的各种影响阻碍了OXA对CRC患者的治疗。其次,该团队发现,二甲双胍通过抑制ERK和AKT的信号通路和NF-κB活性减弱癌细胞对OXA的抗药性,这个发现对二甲双胍辅助治疗CRC患者和化疗具有重要影响。
2.3 联合顺铂
Moro等[23]设计研究了几项关于二甲双胍联合顺铂(MC)对非小细胞肺癌(NSCLC)细胞KRAS/LKB1基因共突变的影响的体内体外试验,KRAS是一种鼠类肉瘤毒癌基因,它的异常会导致细胞快速增殖,LKB1基因也参与调控生命体的多种基本活动。在体外试验中,该团队将共突变KRAS/LKB1中的CD133细胞作为肿瘤干细胞(CSC)的标志物,通过检测MC组和单独使用顺铂组的CD133富集程度来判断他们的凋亡情况,结果表明,MC相对于顺铂显著降低了CSC水平。接下来该团队为了证明二甲双胍在共突变KRAS/LKB1的NSCLC细胞中的抗肿瘤作用,应用了两种异种移植物(PDXs)模型,分别检测不同剂量的二甲双胍及联合顺铂后对肿瘤大小的影响,试验结果显示二甲双胍可以降低核抗原Ki-67的表达,增加凋亡因子蛋白酶caspase-3的表达,从而抑制肿瘤生长。而且,二甲双胍对于加强顺铂对共突变KRAS/LKB1 NSCLC细胞的敏感性具有不可磨灭的作用。
2.4 联合多柔比星
袁莹莹等[24]发现,二甲双胍以剂量和时间依赖性的方式联合蒽环类抗生素多柔比星比单独使用二甲双胍更能显著抑制急性早幼粒细胞白血病细胞系NB4细胞生长,促进癌细胞凋亡,降低凋亡因子蛋白酶caspase-3和caspase-9的活性;其次,该团队发现二甲双胍可以增强NB4细胞在化疗过程中对多柔比星的敏感性,减轻NB4细胞对多柔比星的抗药性。这在怀磊等[13]的研究基础上更进一步加强了二甲双胍对NB4细胞作用影响的认识,针对二甲双胍的这种特性,越来越多的研究人员将目光放在二甲双胍在恶性肿瘤临床中的辅助治疗。
3 二甲双胍联合其他抗癌疗法
化疗、间歇性禁食等是治疗恶性肿瘤晚期的方法,但化疗给病人带来极大的痛苦,如骨髓抑制和恶心、呕吐等胃肠道副作用[25],限制了它的临床应用,二甲双胍可以减轻由化疗带来的某些副作用且它在血糖低的环境中活性更大。
3.1 联合化疗
Nanni等[26]探讨了一项针对于二甲双胍联合化疗与单独化疗对乳腺癌(metastatic breast cancer,MBC)治疗效果的临床试验,以112名MBC患者为试验对象,将胰岛素抵抗患者指标(homeostasis model assessment,HOMA≥2.5)作为评价患者是否胰岛素抵抗的指标,用无进展生存(PFS)和总生存率(OS)来判断化疗后二甲双胍对肿瘤的影响。该团队的试验结果表明,与化疗相比,二甲双胍联合化疗并没有表现出对乳腺癌细胞的协同抑制效应,因此,没有临床研究价值,但显著的降低了肿瘤的中性粒细胞数量,二甲双胍通过激活腺苷活化蛋白激酶(AMPK)以调节细胞线粒体能量代谢可使患者胰岛素敏感,该团队正在进行另外一项随机试验旨在明确二甲双胍引起的胰岛素敏感变化是否朝着对临床有益的方向进行。
3.2 联合间歇性禁食
Elgendy等[27]在研究二甲双胍协同间歇性禁食对恶性肿瘤影响的在体试验中发现,二甲双胍在接种了人结肠癌细胞并禁食处于低血糖状态下的小鼠中,通过抑制蛋白磷酸酶(PP2A)的癌症抑制因子(CIP2A)和上调催化亚基B56D来活化糖原合成酶激酶3β(GSK3β),减少了抗凋亡蛋白(MCL-1)的表达,诱导癌细胞凋亡,达到抑制肿瘤的目的。该团队认为,在确定该方法的安全性和有效性的前提下,PP2A-GSK3β-MCL-1信号传导通路可以作为二甲双胍治疗癌症的新靶点,并进行下一步的临床试验。
4 展 望
本文综述了二甲双胍近几年在抗肿瘤方面的最新研究进展,总体来说,二甲双胍具有一定的癌症研究价值,但大多研究都指向高剂量的二甲双胍的活性要远大于低剂量的二甲双胍活性,高剂量的二甲双胍在生物体内易累积中毒,如乳酸中毒,胃肠道反应,严重的引起维生素B12缺乏且伴有神经性疾病[28-29]。针对这种现象,近期又有人提出了靶向药物疗法,旨在通过二甲双胍联合单克隆抗体或小分子抑制剂靶向进入癌细胞,促进癌细胞凋亡,增强细胞敏感性[30]。近期的新冠状病毒(2019-nCoV)爆发之际,有人提出了宿主导向治疗2019-nCoV感染,二甲双胍的其中一个作用机制是激活腺苷活化蛋白激酶(AMPK)抑制细胞生长提高人体免疫力,这使得一些研究人员认为二甲双胍也许可以通过提高宿主免疫力来预防2019-nCoV感染,对二甲双胍这个“神奇小分子”来说,无疑又将面临着新的机遇和挑战[31]。

