人参皂苷Rg1缓解免疫抑制小鼠运动性疲劳的作用研究
孔凡秀,董佳萍,杨琪,迟晓星
(黑龙江八一农垦大学食品学院,黑龙江 大庆 163319)
人参为多年生五加科草本植物,由于其具有广泛的药理作用,一直以来被视为百草之王,经现代研究证实,人参具有抗疲劳、增强免疫、抗氧化、增强记忆等功效[1-2]。人参的主要活性成分是人参皂苷、人参蛋白与人参多糖,人参中含有0.4%人参皂苷,人参皂苷由多种皂苷单体组成,其中人参皂苷Rg1是人参总皂苷的主要成分之一[3],具有良好的抗肿瘤活性,对保护神经系统、抑制炎症因子及对糖尿病及其并发症都具有积极作用[4-5]。
运动性疲劳是一种复杂的生理现象,一般表现为肌肉僵硬或伴随疼痛、反应迟钝、注意力不集中、呼吸急促、心跳速率加快等。疲劳的产生伴随着能量的大量消耗,其中包括血糖与肌/肝糖原的消耗,同时伴随着疲劳产物的积累,机体协同机能失调等。免疫低下人群常伴随疲劳感,长期疲劳更易导致免疫低下,但是目前临床上还没有有效的方法解决这个问题。因此,研究副作用小的天然植物提取物对免疫和疲劳的预防和治疗作用尤为重要。目前对于人参皂苷的抗疲劳作用与增强免疫力作用都有相关研究[6-7],但都是基于健康个体或肿瘤动物模型的研究,而人参皂苷尤其是其单体Rg1缓解免疫抑制个体运动性疲劳的作用少有探究,也未见系统报道。本文以人参皂苷Rg1为受试物,建立免疫抑制模型,测定小鼠血清、肝组织及骨骼肌中的抗疲劳相关指标,探讨人参皂苷Rg1的抗疲劳作用和对运动性疲劳的缓解作用。
1 材料与方法
1.1 材料与设备
人参皂苷Rg1(纯度98%,生产批号190315A):南京斯道夫生物科技有限公司;环磷酰胺(纯度95%,批号18041725):江苏盛迪医药有限公司;血清尿素氮(blood urea nitrogen,BUN)、丙二醛(malondialdehyde,MDA)、肝糖原、肌糖原、蛋白定量试剂盒:南京建成生物工程研究所。
5424高速离心机:美国Eppendorf公司;722S紫外可见分光光度计:上海INESA公司;Sunrise酶标仪:奥地利TECAN公司;DRP-9082电热恒温培养箱:上海森信实验仪器有限公司。
1.2 动物与分组
雄性BALB/c小鼠40只,2月龄,体重18 g~21 g,辽宁长生生物技术有限公司,生产许可证号:SCXK(辽)2015-0001。小鼠随机分为5组,每组8只,灌胃给药前,除空白静止组和空白运动组外,其它组小鼠注射环磷酰胺制作免疫抑制模型。
人参皂苷Rg1用生理盐水溶解,通过查阅文献[8]确定人参皂苷Rg1分别以12.5、25 mg/(kg BW·d)剂量灌胃,分别计为L组和H组;空白静止组、空白运动组和免疫抑制模型组按体重以等量生理盐水灌胃,分别记为NCS、NCE、MR组。连续灌胃21 d,在温度(20±2)℃,相对湿度40%~60%,光/暗循环12 h环境下饲养。小鼠采用基础饲粮饲养,基础饲粮组成及营养水平,矿物质预混料与微生物预混料组成参考文献[9]。
1.3 免疫抑制模型的建立
健康小鼠随机分组后,除NCS组与NCE组腹腔注射生理盐水外,其余组腹腔注射环磷酰胺造模,环磷酰胺是较为常用的免疫抑制剂,大量实验证实[10-11]腹腔注射环磷酰胺30 mg/kg,连续7 d可有效抑制小鼠免疫功能,给予受试物灌胃第19天时,环磷酰胺强化造模一次。
1.4 力竭爬杆实验
爬杆架采用长60 cm,直径1 cm的玻璃棒,180目磨砂打磨,下端垂直于地面悬空,距地面40 cm。取每组8只小鼠在灌胃第20天,灌胃30 min后,置于玻璃棒中段,记录小鼠因疲劳从玻璃棒掉落的时间,正式实验前一天进行爬杆训练,实验重复3次取平均值为小鼠爬杆时间[12]。
1.5 血清学指标检测及方法
末次灌胃给药后30 min,除NCS组外,其余组小鼠放入游泳箱中无负重游泳90min,游泳结束后小鼠休息30 min,乙醚麻醉,腹主动脉取血,3 000 r/min离心20min,取上清液。试剂盒测定血清中尿素氮(二乙酰肟比色法)、丙二醛(硫代巴比妥酸微板法)含量。小鼠处死后取肝、骨骼肌等组织用生理盐水漂洗后滤纸吸干,按试剂盒说明测定肌/肝糖原(比色法)及MDA含量。
1.6 数据统计分析
数据采用SPSS 20.0进行单因素方差分析,采用最小显著差异法(least significance difference,LSD)进行多重比较,数据均以均值±标准差(±s)表示,以组间方差分析P<0.05为具有统计学意义。
2 结果与分析
2.1 人参皂苷Rg1对小鼠体重的影响
小鼠的体重变化情况如表1所示。

表1 各组小鼠体重比较结果(n=8)Table 1 Comparision of body weights for different groups(n=8)
小鼠初体重各组间差异不显著(P>0.05);免疫抑制模型建立后,与NCE组相比,MR组、人参皂苷Rg1各剂量组小鼠体重明显下降,差异极显著(P<0.01);末次灌胃后,人参皂苷组、MR组小鼠体重较NCE组下降明显(P<0.01)。
2.2 人参皂苷Rg1对小鼠脏器指数的影响
人参皂苷Rg1对小鼠脏器指数的影响见表2。
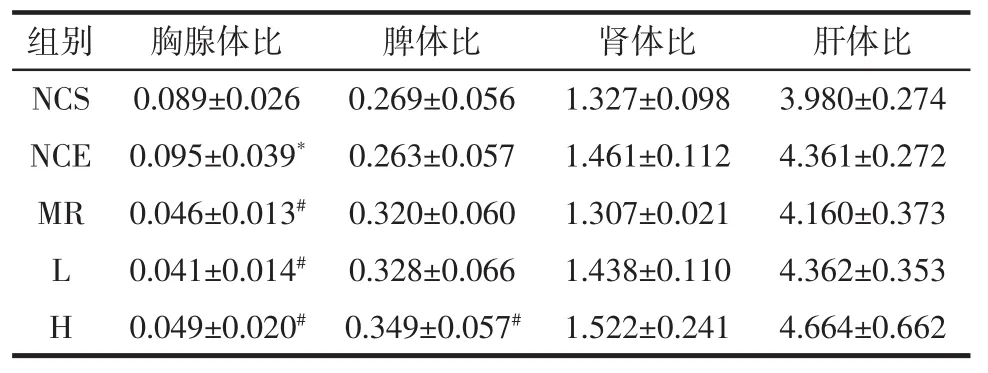
表2 各组小鼠的脏体比(n=8)Table 2 Organ to body weight ratio for different groups(n=8)
如表2所示,与NCE组比较,人参皂苷Rg1各剂量组与MR组小鼠的胸腺体比明显下降(P<0.05);与NCE组比较,H组小鼠的脾体比明显增加(P<0.05);各剂量组小鼠的肾体比、肝体比与NCE组及MR组比较,均无显著差异(P>0.05)。结果表明,人参皂苷Rg1可能对小鼠的胸腺及脾质量存在一定影响。
2.3 人参皂苷Rg1对小鼠爬杆时间的影响
人参皂苷Rg1对小鼠爬杆时间的影响见表3。

表3 人参皂苷Rg1对小鼠爬杆时间的影响(n=8)Table3 Effect of ginsenoside Rg1 on pole-climbing time of mice(n=8)
如表3所示,与NCE组比较,H组小鼠爬杆时间显著增加,时间延长了38.6%(P<0.05),同时H组比MR组小鼠爬杆时间延长了84.1%(P<0.05)。结果表明,高剂量的人参皂苷Rg1可有效延长小鼠的爬杆时间。
2.4 人参皂苷Rg1对小鼠运动后血清中BUN、MDA含量的影响
人参皂苷Rg1对运动后小鼠血清中BUN、MDA含量的影响见图1。
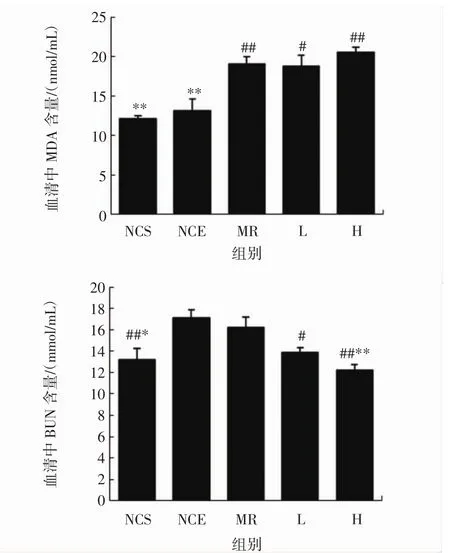
图1 人参皂苷Rg1对运动后小鼠血清中BUN、MDA含量的影响(n=8)Fig.1 Effects of ginsenoside Rg1 on BUN,MDA content in serum of mice after exercise( n=8)
如图1所示,游泳运动后,NCS组与NCE组比较,BUN含量极显著下降(P<0.01);L、H 组与NCE组比较BUN含量均显著降低,其中H组差异极显著(P<0.01);H组与MR组比较BUN含量极显著降低(P<0.01);与NCE组比较,MR、L、H组MDA含量均明显升高。结果表明,人参皂苷Rg1可降低血清中尿素氮含量。
2.5 人参皂苷Rg1对小鼠运动后肝、骨骼肌中糖原和MDA含量影响
人参皂苷Rg1对小鼠运动后肝中糖原、MDA含量影响见图2。
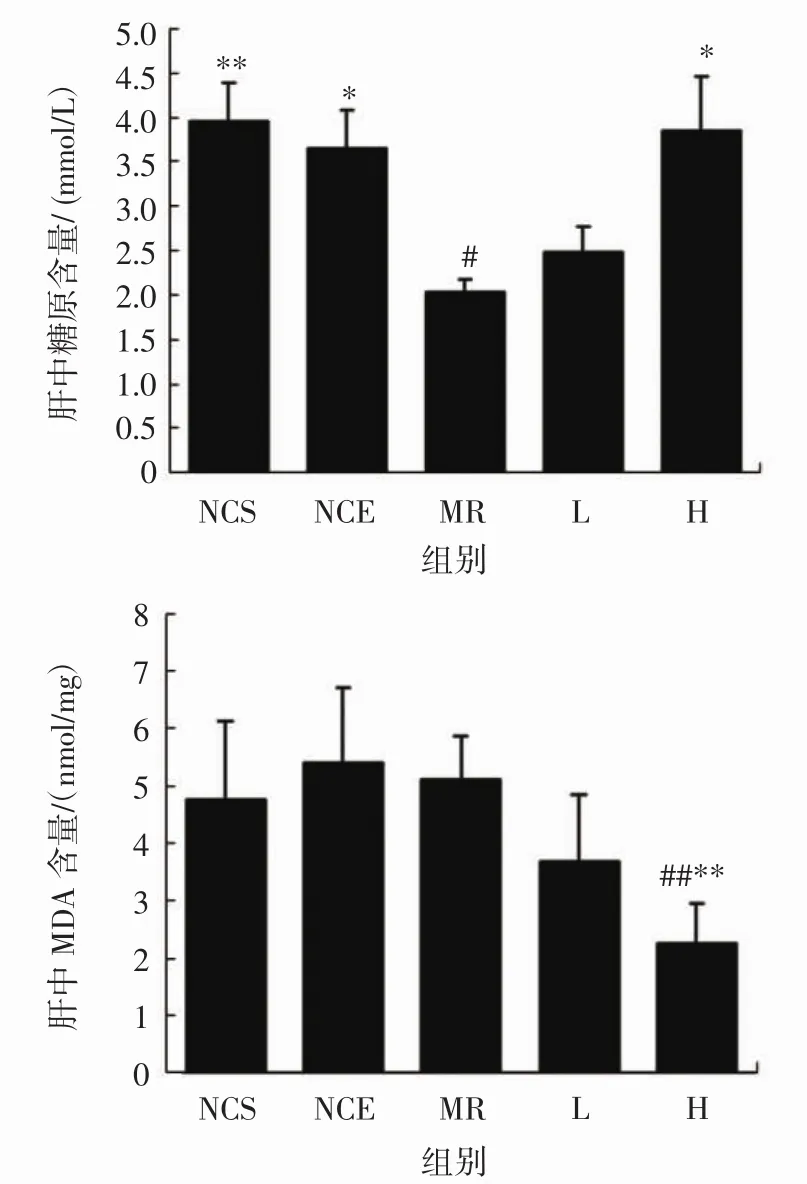
图2 人参皂苷Rg1对小鼠运动后肝中糖原、MDA含量的影响(n=8)Fig.2 Effect of ginsenoside Rg1 on glycogen,MDA content in liver of mice after exercise(n=8)
如图2所示,与MR组比较,NCS、NCE组肝糖原含量显著升高,H组较MR组肝糖原含量显著升高(P<0.05);H组与NCE、MR组比较,肝组织中的MDA含量下降极显著(P<0.01)。结果表明,与MR组比较,高剂量人参皂苷Rg1可增加小鼠肝糖原含量并降低小鼠肝中MDA含量。
人参皂苷Rg1对小鼠运动后骨骼肌中糖原、MDA含量的影响见图3。
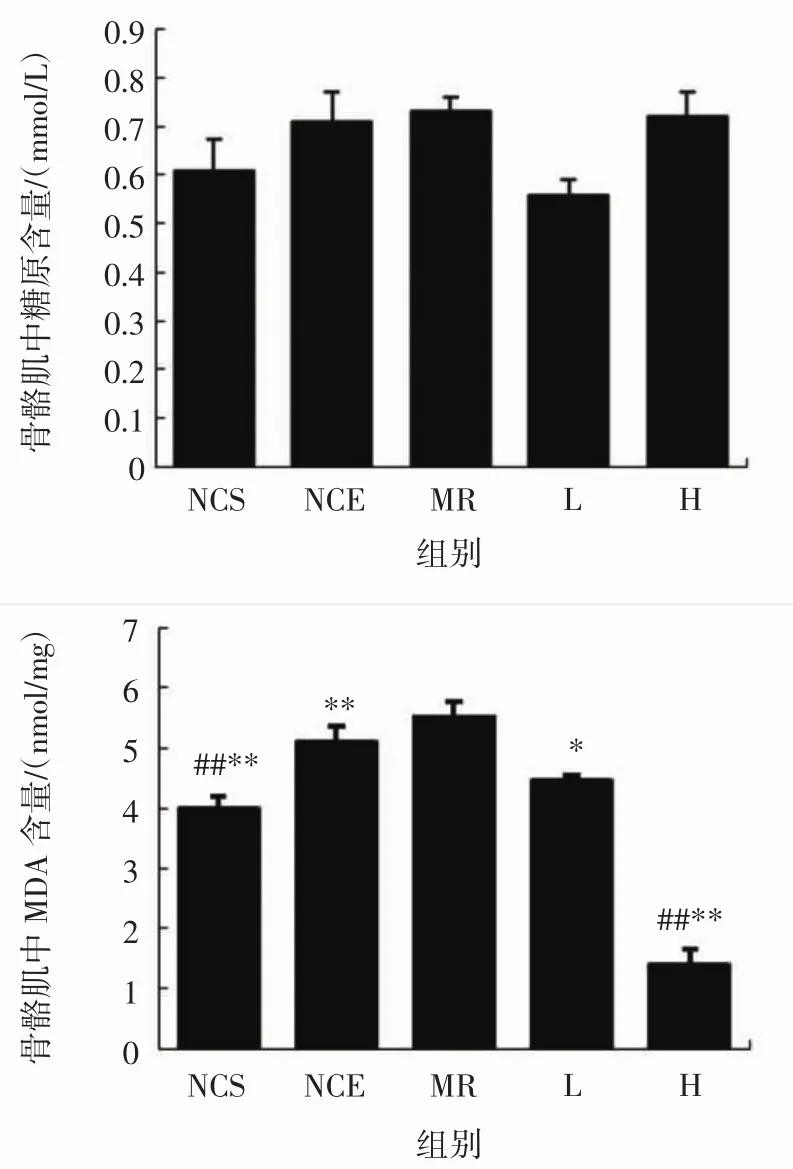
图3 人参皂苷Rg1对小鼠运动后骨骼肌中糖原、MDA含量的影响(n=8)Fig.3 Effects of ginsenoside Rg1 on glycogen and MDA content in skeletal muscle of mice after excercise(n=8)
如图3所示,在骨骼肌中,各组间肌糖原含量无显著差异性;与NCE、MR组比较,NCS组小鼠骨骼肌中MDA含量明显下降(P<0.01);H组与NCE、MR组比较,MDA含量下降极显著(P<0.01)。结果表明,高剂量人参皂苷Rg1组可降低小鼠骨骼肌中MDA含量。
3 讨论
目前广泛认可的是疲劳被分为中枢疲劳与外周疲劳[13],不论哪种疲劳最直观的表征就是运动耐力的下降,因此可以通过动物耐力实验结合生化指标,评价受试物的抗疲劳能力[14]。本实验采用力竭爬杆实验测试小鼠的耐疲劳程度。结果表明,给予小鼠高剂量的人参皂苷Rg1可明显延长小鼠的爬杆时间。
运动初期蛋白质不参与供能,尿素氮含量变化不明显,运动一段时间后,随着蛋白质的加速分解,血清尿素氮含量不断积累,尿素氮含量反映机体疲劳程度[15-16]。本实验小鼠血清指标测定结果表明,空白运动组较空白静止组BUN水平显著升高,提示游泳后运动性疲劳模型建立成功。运动后人参皂苷Rg1低、高剂量组BUN含量显著下降,而模型组BUN含量无显著下降,说明人参皂苷Rg1可有效减少尿素氮的生成,从而有效缓解运动性疲劳的产生。
剧烈运动后,代谢产物丙二醛含量呈现激增,丙二醛作为脂质过氧化的代谢产物,同样反映机体疲劳程度,脂质过氧化过程中对生物细胞膜的损害,将会导致细胞结构与功能的改变,代谢产物MDA含量较少,反应了机体疲劳程度较低[17-18]。有文献报道[19-20],小鼠给予环磷酰胺腹腔注射后,较正常组小鼠肝中MDA含量显著下降,在本实验中,小鼠游泳运动后与正常运动组小鼠比较,肝和骨骼肌中MDA含量并无显著性差异。在给予人参皂苷Rg1后,高剂量的人参皂苷Rg1对肝和骨骼肌中的MDA含量均有降低作用,提示人参皂苷Rg1在较高剂量下(25 mg/kg)可通过有效降低MDA含量,从而减少其对生物细胞的损害,减少运动性疲劳对人体的影响。
高强度运动2 h左右,肌糖原几乎被耗尽,此时为了维持血糖的平衡,肝糖原被消耗,所以肝糖原是衡量机体抗疲劳的重要指标[21-22]。在本研究中,模型组较运动空白组小鼠肝糖原含量下降显著,说明免疫抑制小鼠较正常运动小鼠肝糖原消耗更迅速。给予较高剂量人参皂苷Rg1后,小鼠的肝糖原含量较模型组显著增加,基本可恢复至正常小鼠肝糖原水平,说明人参皂苷Rg1可缓解肝糖原消耗速度,从而缓解运动性疲劳。
4 结论
建立免疫抑制模型后,小鼠耐力、肝糖原含量有所下降。较高剂量(25 mg/kg)的人参皂苷Rg1可显著提高实验小鼠耐力及调节血清和骨骼肌中疲劳相关生化指标的水平,具有较好的抗疲劳功效。

