钾氧电池关键材料研究进展
胡 月 ,郎笑石 ,奚 雪 ,姚传刚 ,蔡克迪,2
(1.渤海大学化学与材料工程学院,辽宁锦州 121013;2.辽宁省超级电容器工程技术研究中心,辽宁锦州 121013)
由于化石燃料的消耗以及其产生的环境问题,人们对于可再生能源的需求在过去十年里日益增长。然而,如何储存和有效利用获取的电能始终面临着巨大挑战。锂离子电池自其1990 年开发至今已被广泛应用于电子产品中,然而其有限的能量密度和高昂的价格限制了其被用于大规模能量储存的可行性。作为锂离子电池的替代品,锂氧电池由于具备极高的理论能量密度而受到了广泛关注。然而由于Li2O2的形成过程产生了高充电过电位以及寄生反应,导致锂氧电池的往返效率低、循环寿命短[1-4]等问题。许多研究团队致力于贵金属催化剂来突破这些挑战,然而这不可避免地带来了高成本问题[5-6]。为了实现可再生资源的大规模利用,开发一种低成本、高效率的储能器件逐渐成为当下研究热点。
基于氧气/超氧化物(O2/O2-)的氧化还原电对可以确保单电子可逆的放电/充电(ORR/OER)反应,这一过程可以有效解决金属空气电池中长久以来的动力学问题。另外,相对于其他不完全稳定的超氧化物(例如LiO2和NaO2),KO2从动力学和热力学的角度来说都是稳定的产物,为电池的长期稳定性提供了可靠依据。地球上丰富的钾、氧元素使得钾氧电池成为了极具希望的下一代能量储存设备,其具备以下优势:(1)钾资源丰富且价格低廉;(2)钾氧电池与锂氧电池工作原理相似;(3)钾金属比锂金属更活泼,具有更低的充放电电位;(4)产物更稳定,循环性能优异。
目前钾氧电池的研究处于起步阶段,近几年,国外的一些科研团队相继开展了钾氧电池的研究工作。美国俄亥俄州立大学吴屹影团队[7]在钾氧电池研究方面取得一系列重要进展,设计的钾氧电池依靠单电子过程有效地解决了钾氧电池中的主要矛盾,在不使用任何催化剂的情况下充放电间的过电势小于50 mV。通过在不锈钢基体上涂层石墨烯等材料制备电极,使用三层膜(聚丙烯-聚乙烯-聚丙烯)组装电池进行测试,结果表明基于还原氧化石墨烯的钾氧电池具有8400 mAh/g 的高比容量(放电速率为1000 mA/g)和超过200 次的循环寿命(限制容量为1000 mAh/g)。
本文从钾氧电池电解质分解、氧气扩散以及负极枝晶堆积等问题出发,归纳总结电解质体系组合、正极超氧化钾稳定存在以及负极保护方面的研究成果,提出相应的解决方案并对钾氧电池的未来发展进行展望。
1 钾氧电池的基本原理
碱金属空气电池的放电始于导电碳电极上氧分子的电化学还原。生成的超氧阴离子与碱金属阳离子(M+)结合形成MO2,根据M 的性质,MO2经历不同的途径,反应原理如表1。
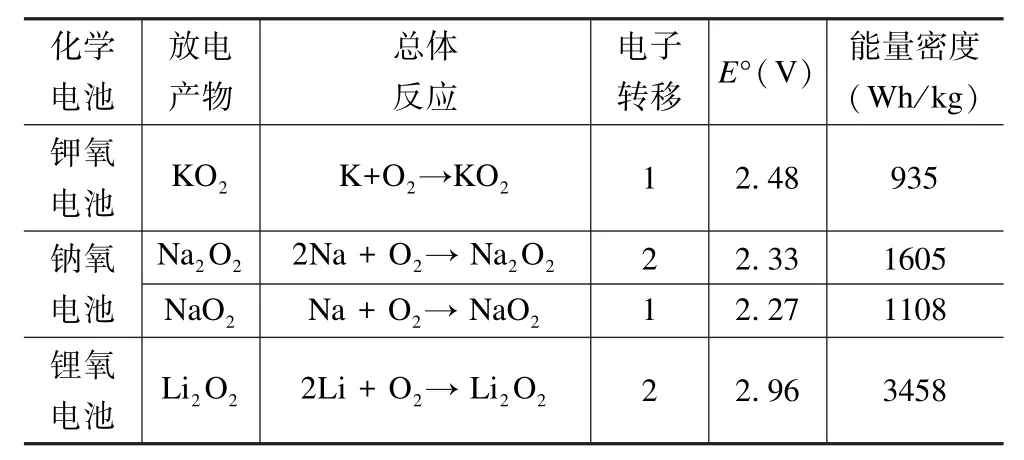
表1 不同碱金属电池中的化学反应原理Tab.1 Chemical reaction principle in different alkali metal batteries
当M 代表Li+时,LiO2在化学上不稳定,是一种寿命短的反应中间体。在电化学还原反应后,Li2O2作为常规锂氧电池的最终放电产物形成。反应如下:
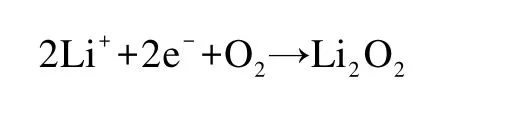
因此,锂氧电池的充电阶段变成了将Li2O2氧化为O2的双电子过程。缓慢的动力学和不可逆的反应机制导致了较大的充电过电位(1~1.5 V),不仅降低了往返能量效率,而且对电解液和电极的电化学窗口提出了挑战。
与之形成鲜明对比的是,K+是一种较重的阳离子,由于晶体堆积结构中阳离子之间的空间排斥作用,它优先形成热力学稳定的KO2而不是K2O2。反应如下:
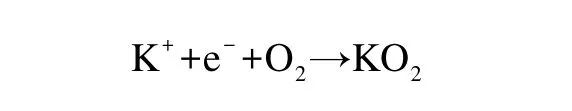
钾氧电池的基本原理可以视为负极碱金属电镀和剥离与氧气在正极还原和生成(ORR/OER) 反应的结合。电池的设计也类似于其他金属空气电池。不同于其他多电子的电化学过程(例如燃料电池和锌氧电池的反应机理为4 电子转移,锂氧电池的反应机理为2电子转移),基于单电子转移的钾氧电池并不需要高昂的电化学催化剂(见图1)。

图1 钾氧电池原理图Fig.1 Schematic diagram of potassium oxygen battery
2 钾氧电池电解液
电解液的选择是钾氧电池研究中最具挑战性的部分。由于钾金属的强还原性,必须依赖于一层稳定的SEI 界面来阻止电解液的持续降解[8-10]。一方面,所选择的电解液需要能有效形成SEI 界面并钝化钾金属表面;另一方面,电解液的成分需要在超氧化物及其自由基的环境中稳定。在基于O2/O2-氧化还原过程的超氧化物电池中,由于其与电解液组分能够发生反应,寻找一种既能稳定碱金属又能稳定超氧化物的电解液仍然具有挑战性。
醚类相对于其他类型的溶剂在超氧化物环境中具有更好的稳定性。研究表明[7]二甲氧基乙烷(DME)相较于其他长链醚类对于钾金属的稳定性更好。Ren等[11]首次采用了六氟磷酸钾-二甲氧基乙烷(KPF6-DME)作为钾氧电池的电解液。研究发现,正极的氧气扩散穿梭到钾金属负极并参与到电解液分解和SEI的形成过程中。这一反应持续腐蚀钾负极并限制了电池的循环寿命。Shrihari 团队[12]通过电化学测试方法比较了使用二甲基亚砜(DMSO)和DME 基电解质的电池的充放电速率,结果表明DMSO 基电解质能够在给定的电流密度下获得较低的过电位。
此外,双(氟磺酰亚胺)酰亚胺(FSI-)被公认为是一种用于碱金属钝化的“神奇阴离子”。Ren 等[13]课题组研究发现使用双(三氟甲基磺酰基)酰亚胺钾(KTFSI)与DME 组成的电解液可在钾负极表面形成溶剂及不渗透保护层。保护层主要由钾金属和KTFSI 盐的反应产物组成,同时也有少量的DME 分解产物。醚类溶剂和氧气分子无法渗透保护层,即使在加压条件下也能有效抑制钾负极的衰变。结果表明,使用KTFSI 电解液的钾氧电池的循环稳定性明显优于未添加保护层的电池,循环稳定性可达60 次以上,是未添加保护层的电池的10 倍以上。这一结果显示了使用KTFSI 电解液能够在钾负极表面形成保护层并且提高电池的稳定性及循环性能,为钾氧电池电解液的选择奠定了基础。
在此基础上Xiao 等[14]对基于KTFSI 和双氟磺酰亚胺钾(KFSI)两种不同钾盐的电解液进行了深入研究。说明了FSI-和超氧化物之间的化学反应,以及在钾氧电池中选取正/负极兼容电解液时所产生的问题。一方面,K 金属负极上S—F 键的断裂形成致密的富有KF-的SEI 膜,导致K 的可逆镀脱;另一方面,较弱的S—F 键使FSI-阴离子易受到O2-及OH-的亲核攻击。KPF6-DME 电解液由于K 金属不稳定,容易受到乙醚溶剂和交叉反应产生的氧气影响,导致循环寿命短。而使用KTFSI-DME 电解液时可以有效钝化K 金属表面,但是这一界面限制了K 离子的传输并且造成了较大的过电势。使用KFSI-DME 电解液时,K 负极的循环效率能得到极大的提高,然而FSI-阴离子对于亲核试剂不稳定,超氧化物和氢氧化物都会造成KFSI盐的分解。Xiao 等[14]通过将KFSI 和KTFSI 盐的优点结合,提出了人造SEI 的方法并取得了至今最好的钾氧电池循环性能,可以循环200 多次(>800 h),库仑效率(CE)保持在100%左右(图2)。尽管目前关于钾氧电池电解液的工作已经取得一系列的研究进展,但现今仍处于初级阶段,氧气对于表面SEI 形成的影响以及循环深度对于钾负极的影响都值得更深入的研究。
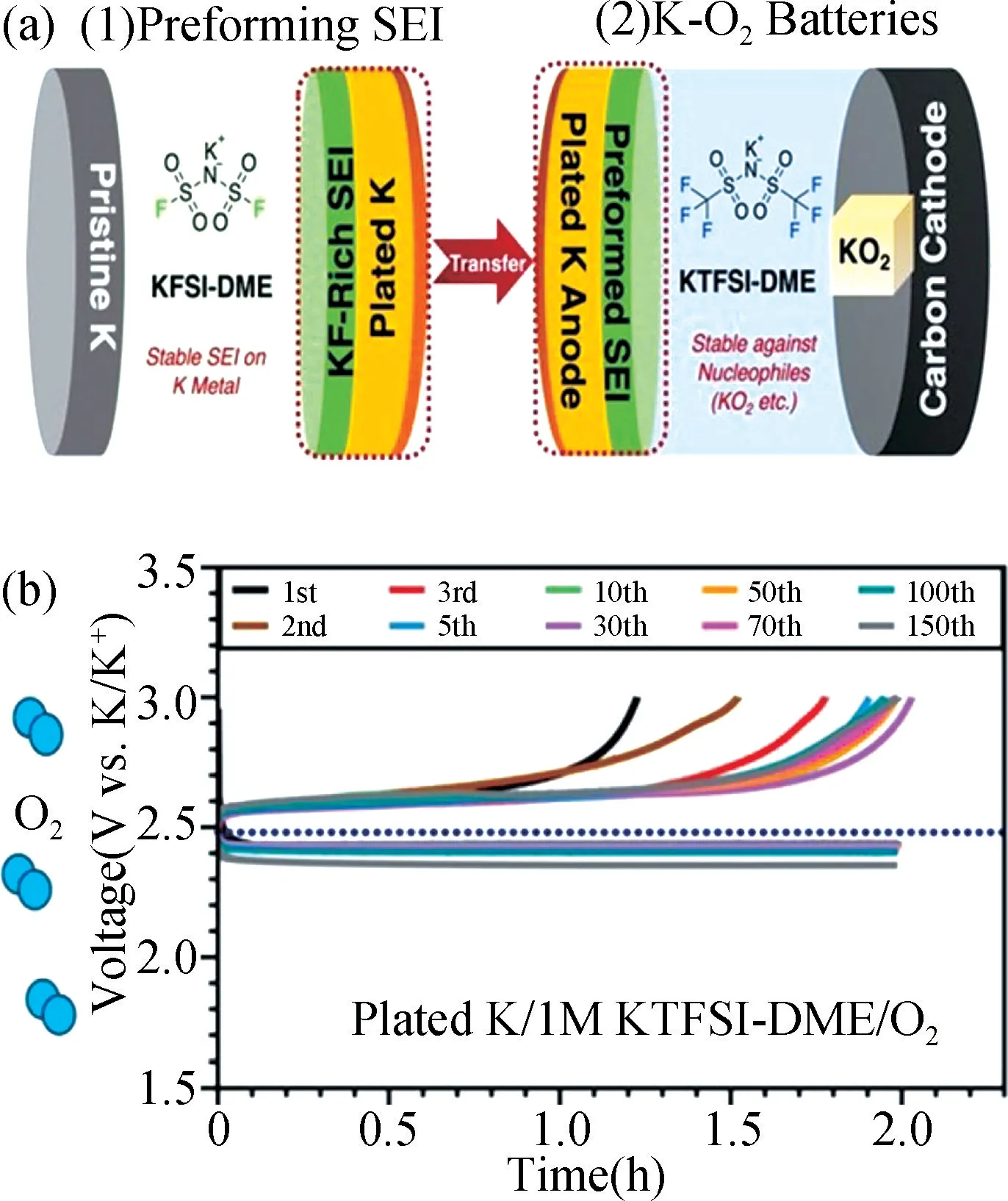
图2 (a)在钾氧电池中应用人工SEI 膜;(b)钾氧电池在KTFSI-DME 电解液中的电压分布[14]Fig.2 (a) Application of artificial SEI film in potassium oxygen battery;(b)Voltage distribution of potassium oxygen battery in KTFSI-DME electrolyte[14]
3 钾氧电池正极
3.1 正极产物:KO2的形成
可充电式钾氧电池因其比容量高而被认为是一种很有前途的储能方案。然而,钾氧电池中超氧化钾(KO2)的反应性和长期稳定性仍不明确。钾氧电池组装后,氧气分子扩散到非水性电解质中,直到氧气浓度达到平衡,溶解氧气产生放电反应,在正极表面还原为O2-阴离子,此时O2-和K+结合产生初始的KO2原子核。
Xiao 等[15]探索了寄生反应并利用离子色谱法来量化微量副产物。通过定量滴定和微分电化学质量光谱法证实了高可逆单电子转移形成98%的KO2产物(图3)。通过研究钾氧电池的电化学反应量化了KO2的可逆性,观察到少量的副产物,有力地证实了KO2的形成。
3.2 KO2的稳定性
对KO2长期稳定性的关注源于两个基本方面:(1)超氧化物是否会自发歧化成过氧化物;(2)超氧化物是否对电解质和碳电极具有高度反应性。
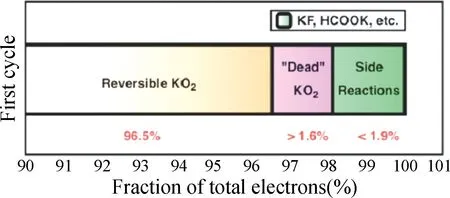
图3 形成可逆的KO2、不可逆的KO2和副反应产物占总电子的比例[15]Fig.3 The ratio of the formation of reversible KO2,irreversible KO2and by-products in total electrons[15]
Luntz 等[16-18]应用微分电化学质谱对锂氧和钠氧电池进行定量滴定。得出结论,产物中的NaO2比Li2O2更能抑制电解质和碳分解。然而,Nazar 等[19]发现NaO2仅占放电产物的90%,处于开路电位下的钠氧电池产生副产物的比例明显增加,导致NaO2在100 h后的比能量降至理论值的43%。许多其他研究小组也证实了NaO2的稳定性低、晶体形态易改变、电荷过电位大等问题[20-24]。
总体而言,NaO2只有在外加电流的情况下才有动力上的优势,与NaO2不同,KO2在动力学和热力学上都是稳定的。Xiao 等[14-15]研究小组已经证明了钾氧电池并不会像钠氧电池中的NaO2自发地通过歧化反应形成Na2O2,而是直接产生KO2放电产物,这与KO2作为放电产物的热力学稳定性有关,KO2的稳定性限制了O2在正极产物中的穿梭效应,抑制了副产物的形成。
Wu 等[25]进一步对钾氧电池产物进行探讨,使用各种分析技术来探测和量化钾氧电池中的副反应,并证明了KO2的长期稳定性。利用核磁共振对循环后的电极进行分析,发现主要副产物为DME 分解产生的甲酸酯(HCOOK)、乙酸酯(CH3COOK)以及KPF6盐分解产生的氟化物(KF)。由于它们在醚类电解质中的溶解度不高,导致副产物堆积在固相钝化电极中。此外,通过离子色谱法来定量副产物,结果表明大部分产物是在首次放电过程中形成的(图4)。
研究表明,钾氧电池中KO2的成核和生长影响其尺寸和形貌,不同的放电速率将影响KO2的晶体大小和他们的分布情况。O2的浓度和扩散速率也是影响KO2生长的重要因素。基于成核理论,放电率低导致O2浓度低及成核缓慢,这进一步促进稀疏多孔的KO2的形成。相反,放电率高会导致氧自由基的过度饱和,与电解质反应后形成一层致密的KO2晶体[7]。基于这些观察,Wu[7,15]提出了KO2的生长机理,并通过使用比表面积大、没有孔径限制、利于O2扩散的正极材料有效提高了钾氧电池的充放电速率和容量。
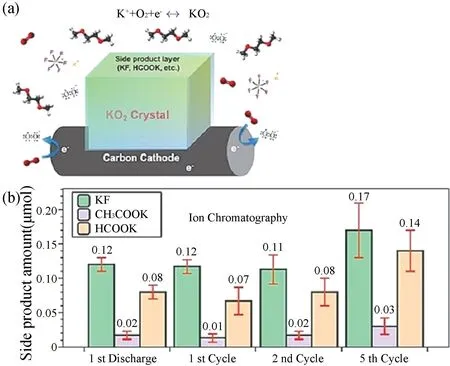
图4 (a)钾氧电池的阴极反应和副产物的表示;(b)离子色谱定量的副产物[7]Fig.4 (a) Cathode reaction and by-product expression of potassium oxygen battery;(b)By products of ion chromatography[7]
目前对KO2在电解质存在下的稳定性以及寄生副反应的研究尚浅,随着人们对锂氧和钠氧电池可逆性的日益关注,对钾氧电池中KO2的电化学反应和化学稳定性进行系统的研究显得尤为重要。
4 钾氧电池负极
自2013 年Wu[7,15]团队研究钾氧电池以来,一直致力于电解液组合和电极设计。在钾负极稳定性、充放电速率、比能量以及循环寿命方面取得了令人鼓舞的进展[24-26]。除钾金属负极之外,作为替代的其他负极材料也值得进一步研究(图5)。Wu[7]团队首先研究了钾-锑(K-Sb)合金作为负极,其可逆比容量高达650 mAh/g。在目前的研究中,空气电池存在的一个关键问题是固体金属负极枝晶生长所引起的安全问题。解决金属负极的枝晶生长问题成为未来空气电池负极的研究热点之一[27-30]。在碱金属空气电池(M-O2)中,通常使用固体碱金属(即Li、Na 和K)作为负极,研究发现用液态负极代替固体负极是一个有效解决枝晶生长的办法。
Zhai 课题组[31]研究了Na-K 合金作为钾氧电池的负极材料,由于其在常温下是液态的属性,这一负极解决了钾金属不均匀沉积和枝晶生长的问题。同时离散傅里叶变换(DFT)显示溶剂和Na-K 合金表面的相互作用相对于钾负极更小,有利于电解液的稳定。
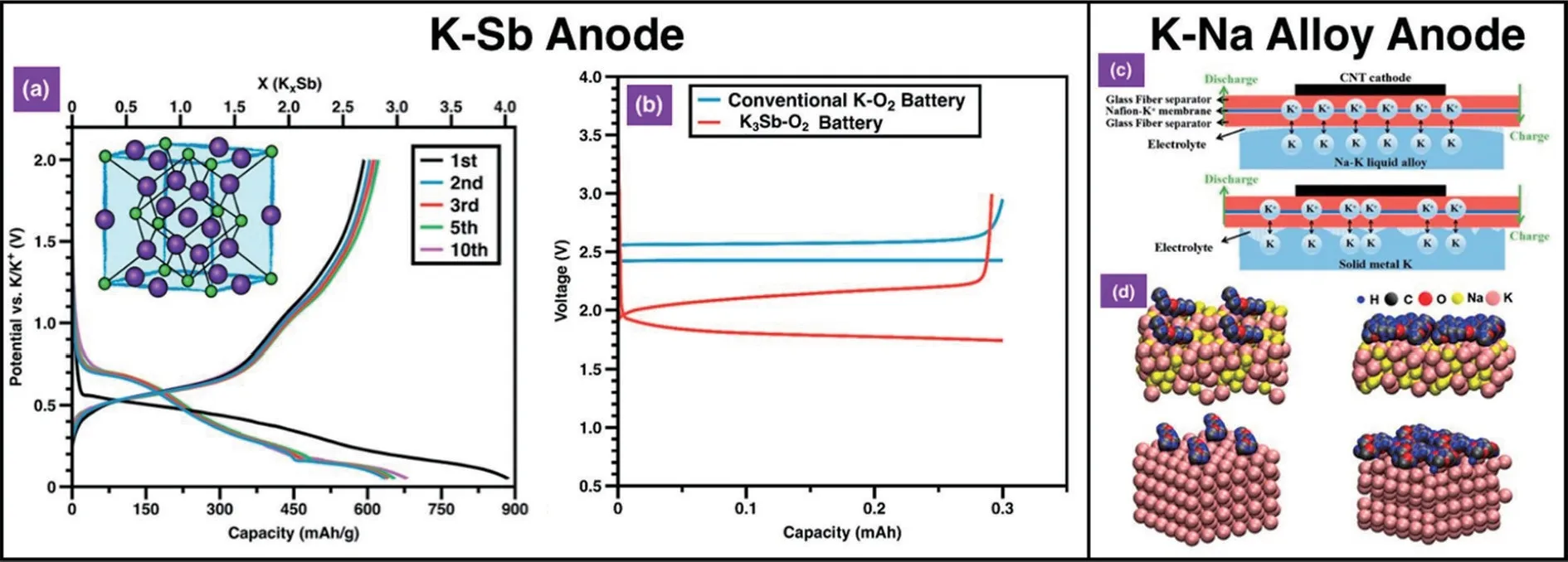
图5 其他已被应用于钾氧电池中替代金属钾负极的材料[25-26]Fig.5 Other materials have been used to replace metal potassium anode in potassium oxygen batteries[25-26]
另外,Zhai 等[31]进一步探究了室温下基于液态Na-K 合金负极的无枝晶钾氧电池。在其合金负极电池中,液态合金和电解液之间独特的液-液连接体系提供了一个均匀稳定的负极电解质界面。同时发现,Na-K 合金只与钾氧电池相容,而不与钠氧电池相容,这主要是由于在放电过程中K 的还原性较强,形成的KO2比NaO2在热力学上更稳定。结果表明,液态合金负极钾氧电池具有很高的循环寿命(超过620 h)和较低的放电电荷过电位(初始循环时约为0.05 V)。此外,对钾氧电池降解机理的研究表明,O2的穿梭效应和乙醚电解质不稳定性是钾氧电池的关键问题。
总之,此研究为解决碱金属空气电池枝晶生长问题提供了一条新的途径。虽然直接使用钾金属可以使能量密度最大化,但为了防止有机电解液的连续还原和交叉反应的影响,需要在钾金属表面形成一个理想的钝化层。因此,钾金属负极的深度循环被认为是实现可逆钾氧电池化学反应的主要挑战。
5 结论和展望
钾氧电池是一种以金属钾为负极、空气中的氧气为正极活性物质的高比能量新型储能设备,属于一种半开放系统。钾氧电池由于其正极可逆的单电子反应和热力学稳定的KO2放电产物在金属空气电池中独具一格。本文针对钾氧电池中充电过电位高、电解质分解、枝晶生长堆积等问题列举了相应的解决办法。其中选用组合电解液体系以及液态金属合金作负极有效提高了负极的稳定性及电池的循环性能。
然而,钾氧电池的研究目前处于探索阶段,尽管在电解液和负极的选择上取得了一些进展,但同时乙醚电解质的不稳定性限制了负极的深度循环,对负极的保护以及安全问题有待解决。提高电池循环性能、抑制枝晶生长是未来钾氧电池的发展方向。
希望未来材料的发展和基础化学的研究能进一步提升其正负极电化学反应的可逆性,并持续提升钾氧电池电化学性能,使其达到商业化的标准。

