均匀沉淀法制备ZnO、Fe/ZnO光催化剂*
富笑男,郭叶飞,陈锦涛
(河南工业大学 理学院,郑州 450000)
0 引 言
近年来,科技的进步和工业的发展给我们带来便利的同时也给我们赖以生存的地球带来了严重的污染。如工业废气对空气的污染、工业废水难以降解的污染物对土壤和水资源的污染等,不仅使自然环境受到破坏,甚至还威胁到人类的身体健康。而光催化技术则能够很好的解决此污染问题,并且与传统处理技术相比,光催化技术有着环保、高效等优势,使其成为目前的研究热点[1-7]。
ZnO为典型的直接带隙宽禁带半导体,其宽带隙(3.37 eV)和较大激子结合能(60 meV)的特点使其成为了光催化剂的代表[8-11]。研究者们通过对ZnO进行掺杂等方法来克服其光生电子-空穴对易复合、量子效率低和可见光利用率低等缺点[12-14]。常见的掺杂方法有过渡金属元素掺杂、贵金属元素掺杂、非金属元素掺杂、半导体负载[15-18]。其中过渡金属元素掺杂优势是在ZnO的能级中引入一个杂质能级,使其能带结构发生变化,引入的杂质能级不仅能够拓宽其光谱响应范围,还能作为捕获中心,减少光生电子-空穴的复合,从而增强ZnO的光催化性能[19]。而Fe作为过渡金属的代表性元素,其半径与Zn相近,更加容易掺杂进入到ZnO的晶格内,从而有效提高ZnO的光催化性能。另外,Fe元素在自然界中极易获取,价格低,所以Fe掺杂ZnO光催化剂不仅光催化性能好,性价比高,适合大规模的应用[20-21]。
在本研究工作中采用均匀沉淀的方法,通过改变Fe掺杂浓度和煅烧温度两个制备条件分别得到了纯纳米ZnO和Fe/ZnO光催化剂。再根据光催化降解甲基橙的实验结果对光催化剂的性能进行表征,从而找到最适的光催化剂制备条件。
1 实 验
1.1 纳米ZnO、Fe/ZnO的制备
1.1.1 纳米ZnO的制备
使用电子天平称取一定质量的锌源Zn(NO3)2·6H2O和沉淀剂CO(NH2)2,并在磁力搅拌器的作用下溶解于去离子水中,超声处理30 min后将混合溶液倒入反应釜的釜芯中,在110 ℃的温度下加热反应2 h得到前驱物,将前驱物用去离子水和无水乙醇分别洗涤数次后放入高温电阻炉中,在500 ℃下煅烧2 h,最终得到纯纳米ZnO样品。我们将样品编号为A1。
1.1.2 纳米Fe/ZnO的制备
用电子天平分别称取一定质量的沉淀剂CO(NH2)2、锌源Zn(NO3)2·6H2O和铁源Fe(NO3)3·9H2O在磁力搅拌器的作用下溶于去离子水中(其中Fe3+∶Zn2+的摩尔浓度比为1.0%、1.5%、2.5%),超声处理30 min后将混合溶液倒入反应釜的釜芯内在160 ℃下反应2 h后,将前驱物分别用去离子水和无水乙醇洗涤数次,再将前驱物在500 ℃条件下煅烧2 h,得到样品纳米Fe/ZnO。样品Fe/ZnO编号分别为B1,B2,B3。选择Fe3+∶Zn2+摩尔浓度比为1.0%的掺杂浓度,改变煅烧温度,分别为400、500、600 ℃得到样品Fe/ZnO编号分别为C1、B1、C2。样品编号和制备条件如表1所示。
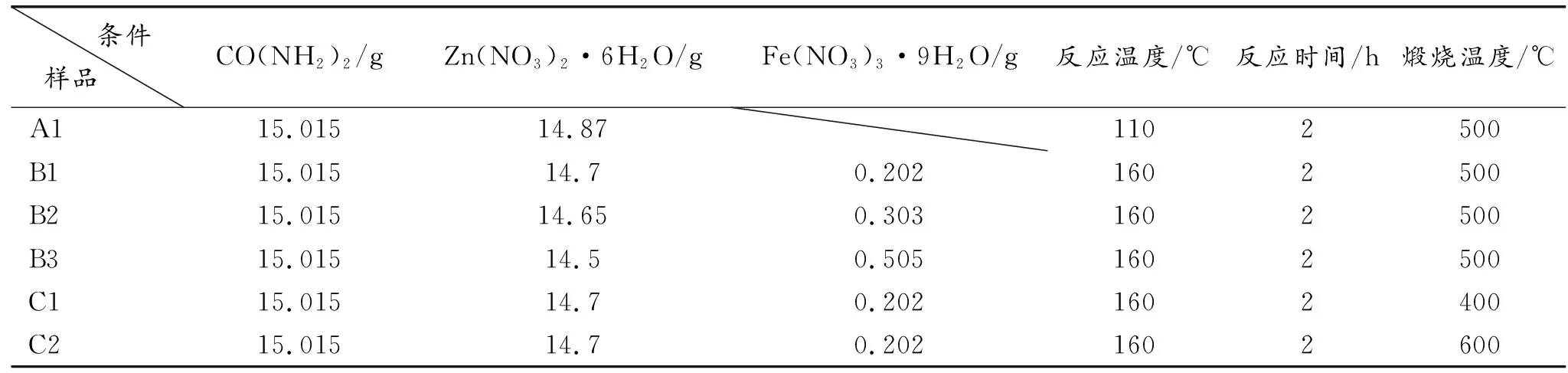
表1 所有样品编号和制备条件
1.2 样品的性能及表征
所有的ZnO、Fe/ZnO样品将通过SEM、XRD进行样品表面形貌、晶体结构的表征和UV-Vis光降解率的测试。所用到的仪器以及规格型号如下所述。样品表面形貌分析用FEI公司QUANTA-FEG-250型扫描电子显微镜(SEM);样品的晶体结构分析采用荷兰帕纳科公司XPert-Pro MPD型X射线衍射仪(Cu Kα,λ=0.154 nm);样品光催化实验的吸光度采用北京普析通用仪器有限责任公司TU-1810型UV-Vis测量。
2 结果与讨论
2.1 XRD分析
如图1所示为所有样品的XRD图谱。所有样品在2θ为31.68°、34.34°、36.16°出现衍射峰,说明样品均为六方纤锌矿结构(对应标准卡片JCPDS,No.99-0111);图中没有出现Fe或Fe化合物的衍射峰,这可能是由于实验中Fe掺杂浓度较低或Fe高度分散导致的。根据图谱可以看出样品衍射峰峰形尖锐,并且没有出现杂峰,说明样品结晶度和纯度较好。
另外,根据XRD测试数据以及谢乐公式可计算出样品的晶粒尺寸。表2为所有样品的晶粒尺寸。
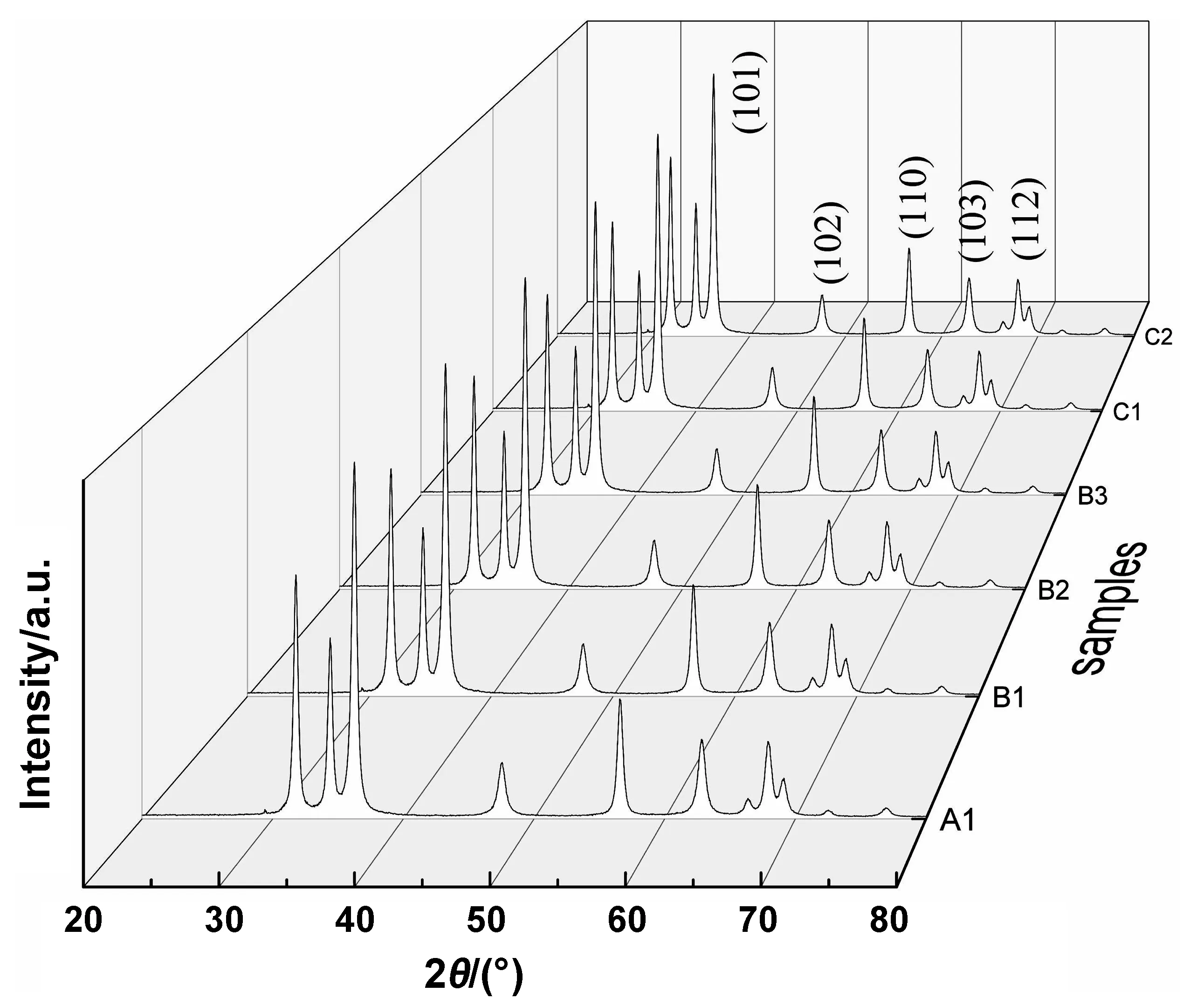
图1 所有样样品的XRD图谱Fig 1 XRD patterns of all samples

表2 所有样品的晶粒尺寸
根据系列B样品的晶粒尺寸可以看出,当制备条件中的反应时间和煅烧温度相同时随着Fe掺杂浓度的增加,晶粒尺寸也随之减小。另外,我们看到纯纳米ZnO样品A1的晶粒尺寸为211 nm,相较于B系列样品的晶粒尺寸要稍大一些;说明在此掺杂浓度范围内,以及在此相同制备条件下,掺杂会抑制晶粒的长大。在Fe掺杂浓度一定的系列C样品和样品B1中,煅烧温度为400 ℃时晶粒尺寸最大,600 ℃时次之,500 ℃时最小,并且3个样品晶粒尺寸相差较大,说明煅烧温度对晶粒尺寸的影响较大,并且随着煅烧温度的升高,晶粒尺寸变化情况为先减小再增大。
2.2 SEM、EDS分析
2.2.1 纳米ZnO的SEM和EDS
图2所示为纯纳米ZnO的SEM图像。图2(a)、(b)分别对应样品A1的低倍和高倍。根据图2(a)可看出样品A1是颗粒平铺而成,形成了有一定平整度并且较为密集的颗粒膜,放大后可以看到并没有很明显的团聚大颗粒,而是众多的小颗粒紧密的连接在一起形成了有一定厚度的完整的颗粒膜。

图2 样品A1的SEM图像Fig 2 SEM images of sample A1
为了对样品进行元素定性半定量分析,我们对样品A1进行了EDS测试,结果如图3所示。从图中可看出样品A1仅由O和Zn两种元素组成,其中在横坐标为2附近出现的小峰为测试时引入的Pt,说明样品为纯纳米ZnO,不含其他杂质。
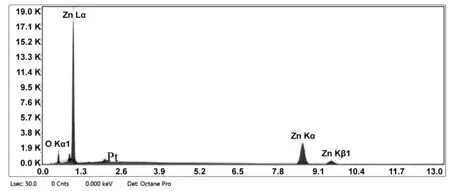
图3 样品A1的EDSFig 3 EDS spectrum of sample A1
2.2.2 纳米Fe/ZnO的SEM和EDS
如图4所示,分别为不同浓度Fe掺杂Fe/ZnO样品B1、B2、B3的SEM图。在低倍数情况下(图4a、c、e)可看出样品B1和B2均有较好的平整度,其中样品B1的平整度最好,样品B3的平整度较差,并且这些样品都有一定的团聚现象。另外,还可以看到样品B2颗粒与颗粒之间有明显的空隙。从放大后(图4b、d、f)看,样品B1团聚形成了无规则大小不一的颗粒,还有一些更小的颗粒附着在这些颗粒表面,颗粒之间较为紧实的堆积在一起;样品B2团聚的颗粒大小基本相同的,而这些颗粒又进一步的团聚成大且无规则的团聚物;样品B3而是很多小颗粒紧密聚集在一起形成了类似A1颗粒膜。
我们对样品B1进行了EDS测试,结果如图5所示。图像结果显示样品仅含有O、Zn、Fe 3种元素,说明制备的Fe/ZnO样品不含杂质。测试结果显示Fe元素的含量为0.91%,实验中实际的掺杂浓度为1.0%,两者相差较小,可能是由于测试误差等造成,可以忽略不计。

图4 样品B1(a、b),B2(c、d),B3(e、f)的SEM图Fig 4 SEM images of sample B1(a, b), B2(c, d) and B3(e, f)
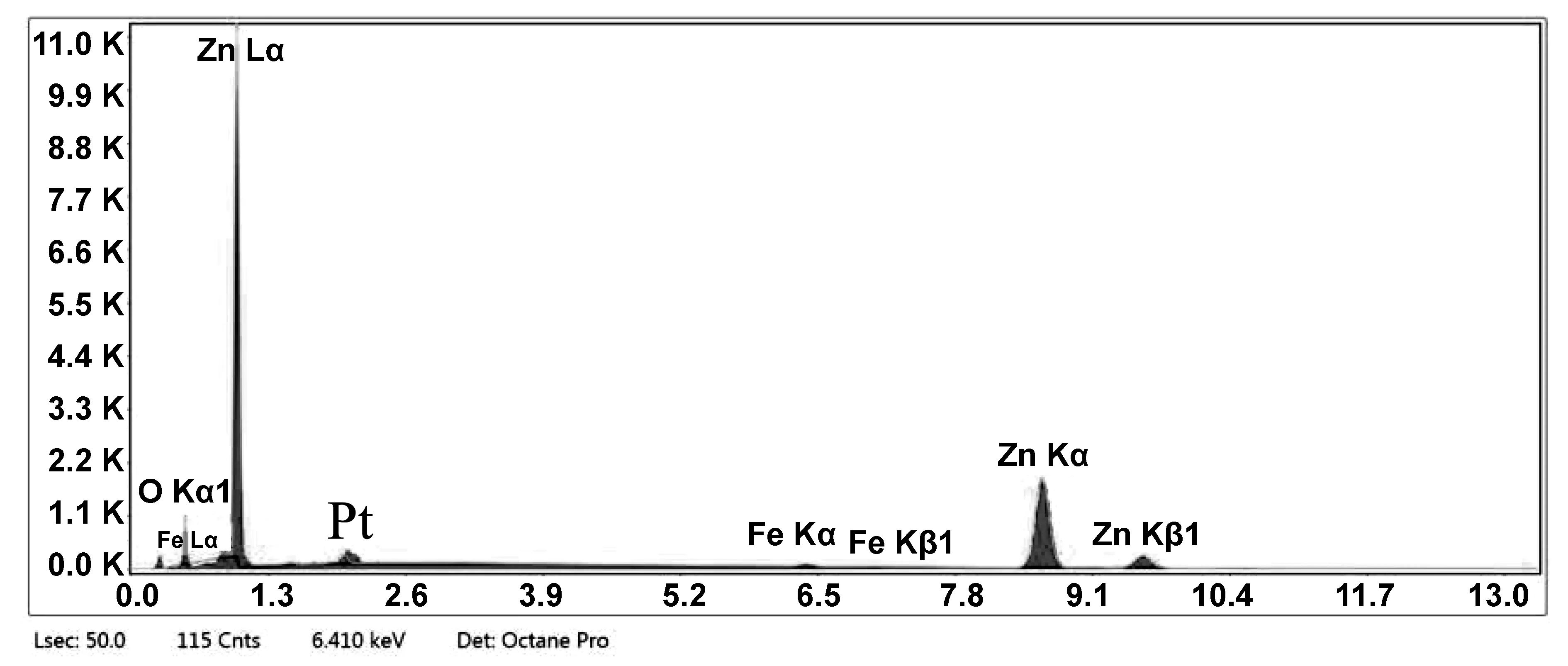
图5 样品B1的EDSFig 5 EDS spectrum of sample B1
不同煅烧温度的Fe/ZnO样品C1,C2的SEM图如图6所示。在低倍数情况下如图6a、c,可看出样品C1平整度较差,而C2平整度较好;两样品都是由许多大小、形状各异的团聚颗粒组成,颗粒之间都有一定较均匀的空隙;样品C1团聚在一起的较大块状颗粒,样品C2也有团聚的块状物,但没有C1那么大。两样品放大之后如图6b、d所示,样品C1颗粒尺寸相差较大,并且团聚现象严重,许多小颗粒附着在较大的颗粒表面,使颗粒之间空隙较少;样品C2颗粒尺寸则较为均匀,没有像样品C1那样,有很多小颗粒附着在团聚颗粒表面,并且颗粒之间也有一定空隙。

图6 样品C1(a、b),C2(c、d)的SEM图Fig 6 SEM images of sample C1 (a, b) and C2 (c, d)
2.3 光降解实验分析
实验所制备的三组光催化剂的光催化性能将通过在高压汞灯照射下降解甲基橙溶液的实验结果进行表征。在黑暗环境下将一定质量的催化剂样品加入到甲基橙溶液中超声处理30 min使其完全溶解,再静置30 min使光催化剂与溶液达到吸附-解析平衡状态。光照开始之前取4 mL溶液离心后用紫外-可见光分光光度计(UV-Vis)测量吸光度作为初始吸光度A0,实验开始后每隔20 min取样一次,离心后测量吸光度A。计算光催化剂的降解率如下:
降解率=(A0-A)/A0×100%
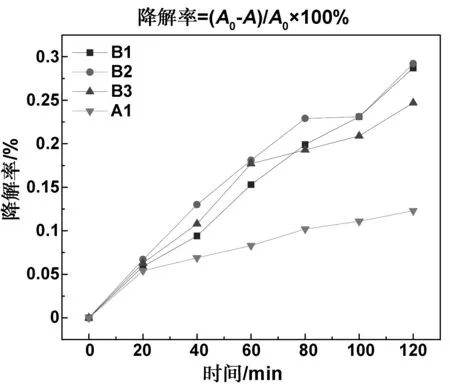
图7 样品A1和系列B样品的降解率图像Fig 7 Photodegradation curves of sample A1 and samples B series
图7为系列B不同Fe掺杂浓度样品和纯纳米ZnO样品A1的降解率图像。可以看出在120 min时降解效果最好的为掺杂浓度1.5%的样品B2,达到了29.2%。其次是与之非常相近的样品B1为28.7%,然后是掺杂浓度为2.5%的样品B3,为24.7%,降解率最低的是无掺杂的纯纳米ZnO样品A1。其中B系列3个样品降解情况的总体趋势基本相同,都是随着时间的增加而增加,并且曲线斜率基本相同;样品A1在最初的20 min降解率曲线斜率几乎和系列B的样品相同,但是20 min后降解率的增长速率明显降低了,并且之后一直保持这样较低的增长速率,达到120 min时为12.3%。
从上面实验结果来看,即使样品A1与B系列样品的晶粒尺寸大致相同,并且A1和B3的表面形貌也大致相同,但是纯纳米ZnO和B系列样品的光催化率还是相差很大的,即Fe掺杂的B系列样品的光催化性能还是明显高于未掺杂的样品A1,这说明在这样的制备条件下样品的晶粒尺寸和表面形貌对其光催化活性的影响并不是起主要作用,而Fe的掺杂则明显增强了ZnO的光催化性能,说明Fe的掺杂对光催化剂性能的提升有着决定性作用。在掺杂样品中,Fe掺杂浓度为1.5%的样品B2光催化性能最好,要高于掺杂浓度1%和2.5%的两个样品B1和B3。说明在一定的掺杂浓度范围内,光催化性能先是随掺杂浓度增大而增大,进一步增加掺杂浓度则反而降低其光催化性能。另外,样品B1和B2最终的降解率相差不多,这可能是因为两样品的形貌和尺寸相差不多所至,但由于样品B2表面较粗糙,颗粒之间有一定空隙,使光催化剂和染料能够更加充分的接触,从而其光催化性能略高于样品B1。虽然从XRD结果看样品B3的颗粒尺寸最小,但由于其团聚现象严重,颗粒之间几乎没有空隙,导致其光催化性能较差。
图8(a)为Fe掺杂浓度为1.0%时,不同煅烧温度下制备样品的光催化实验的降解率以及未掺杂的样品A1降解率图像。最终降解效果最好的样品为B1,达到28.7%,其次是样品C2为21.3%和样品C1为14.7%,A1降解率依然是最小。4个样品在实验前40 min时降解情况基本相同,但在40~60 min时4个样品降解率斜率出现明显不同。样品B1斜率出现了较大的提高;样品C1斜率则减小;样品C2斜率也有提高,但增长幅度小于样品B1;而样品A1斜率则基本没有变化。60~100 min时B1和C2斜率稍有下降,而C1的斜率稍有增加,A1斜率则依然不变。到100 min时后样品B1的斜率又有小幅上扬,C1斜率下落,而C2和A1保持不变。从图8(a)来看C系列样品的光催化性能均要好于样品A1。
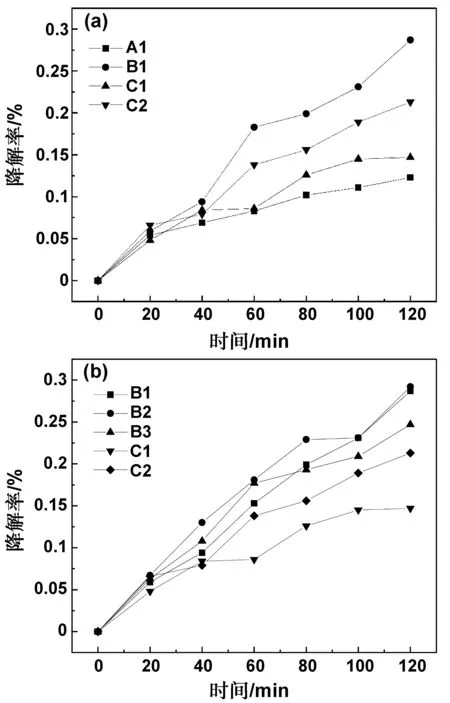
图8 (a)样品A1、C1、C2、B1的降解率图像;(b)B和C系列样品降解率图像Fig 8 Photodegradation curves of sampleA1, C1, C2 and B1 (a); B and C series samples (b)
根据此实验结果分析,Fe/ZnO 3个样品光催化性能均好于无掺杂的样品A1;Fe掺杂浓度相同的Fe/ZnO 3个样品中,煅烧温度为500 ℃的样品B1光催化性能最好,其次分别是600 ℃和400 ℃的样品,三者从40 min之后降解率拉开了距离,说明反应进行到一定时间后,煅烧温度对光催化剂的性能有了较大的影响。另外,根据SEM放大图来看,样品C1的团聚现象比较严重,颗粒之间空隙较小,并且其晶粒尺寸较大为427 nm,这些原因可能导致其光催化性能最差;样品B1和C2的形貌基本相同,都有轻微的团聚现象,但B1由于其样品平整度好、颗粒表面附着有更小的颗粒,并且晶粒尺寸仅为203 nm,这样使更多的样品表面和与染料更充分地接触都使其光催化活性较高,而样品C2的颗粒之间有一定的空隙以及318 nm的晶粒尺寸使其光催化性能要强于C1但弱于B1。
根据上述两组实验结果分析,Fe掺杂和煅烧温度这些制备条件对样品的光催化性能均有影响。首先制备条件影响样品的表面形貌和晶粒尺寸,而这些因素又进一步影响样品的光催化活性。具体分析如下:(1)如图8(b)所示,对比B和C系列样品,B系列3个样品晶粒尺寸均小于C1和C2样品,而光催化实验结果可知B系列Fe/ZnO 3个样品大约在20 min。后光催化性能均高于C1和C2样品,说明较小的晶粒尺寸是有利于光催化性能的提升的。(2)从C系列样品来分析,根据C1和C2样品和样品B1可看出煅烧温度对晶粒尺寸的影响较大。煅烧温度过低的样品C1和煅烧温度过高的样品C2的晶粒尺寸均大于样品B1,并且他们的光催化活性低于样品B1,说明煅烧温度通过影响样品的晶粒尺寸进而影响其光催化活性。其次,Fe掺杂的B、C系列样品的光催化性能均要高于未掺杂的样品A1,这说明Fe的掺杂通过改变样品的晶粒尺寸、表面形貌以及能带结构等有效地提升光催化性能。主要原因如下:(1)在一定的制备条件下掺杂Fe可以使样品的晶粒尺寸发生改变。当反应时间和煅烧温度相同的情况下,Fe的掺杂使样品晶粒尺寸减小,这意味着掺杂的Fe能够抑制晶粒的生长,同时也使光催化剂的比表面积增大;(2)掺杂Fe可使样品的形貌发生改变。纯纳米ZnO样品小颗粒没有形成大的团聚颗粒,而形成了颗粒膜;Fe掺杂的样品大部分形成了大的团聚颗粒聚集在一起,并且相较于纯纳米ZnO样品,掺杂后的样品颗粒之间也有一定的空隙。这可能也是Fe掺杂的样品光催化活性较高的原因;(3)掺杂改变了ZnO的能带结构从而影响其光催化性能[23]。这是因为Fe3+的半径与Zn2+的半径相近,使其能够很容易掺杂进入ZnO的晶格中,在ZnO的能级中引入一个杂质能级,从而改变ZnO的能带结构,而这个杂质能级不仅可以作为一个捕获中心来限制光生电子-空穴的复合,还能够使ZnO价带中的电子通过杂质能级更加容易跃迁至导带从而拓宽ZnO的光谱响应范围,使其在可见光的照射下也能够有较好的光催化活性[23]。
3 结 论
采用均匀沉淀法分别制备了纯纳米ZnO和Fe/ZnO光催化剂样品。通过改变Fe掺杂浓度和煅烧温度两个实验条件研究其对样品表面形貌、晶体结构以及光催化性能的影响。实验结果表明所有样品均为六方纤锌矿结构。在一定的制备条件下,随着Fe掺杂浓度的增加,样品粒径逐渐减小;样品的形貌均为小颗粒聚集在一起而形成的大小、形状不同的团聚物或颗粒膜。光降解甲基橙的实验结果显示Fe掺杂的Fe/ZnO样品的光降解率均在20%以上,当Fe掺杂量为1.5%时的Fe/ZnO样品光催化活性最高。Fe/ZnO样品均比纯纳米ZnO样品光降解率高,即使光催化性能最差的Fe掺杂Fe/ZnO样品和纯纳米ZnO样品相比时,其降解率依然是纯纳米ZnO的两倍。这主要是因为Fe掺杂之后可以使ZnO的能带结构发生了变化,从而抑制其光生载流子的复合,从而增强了对可见光的吸收,所以适量的Fe掺杂能够改善ZnO的光催化性能;其次,掺Fe之后Fe/ZnO样品表面形貌也发生了改变,颗粒之间的空隙相较于纯纳米ZnO样品也有所增加;此外,针对B系列Fe/ZnO样品来说,随着Fe掺杂浓度的增加,样品的晶粒尺寸随之减小,使其比表面积增大,所以提高了污染物与催化剂的接触面积,进一步增强了其光催化性能,对比掺杂浓度相同的B1和C系列样品的光催化实验结果也可进一步说明粒径尺寸小是有利于提升光催化性能的。另外,我们还发现当煅烧温度为500 ℃时,样品的晶粒尺寸最小、光催化性能最佳。综合整个实验结果来看,适当的煅烧温度和Fe掺杂浓度能够有效的改善光催化剂的性能。因此寻找最佳的制备条件对于光催化剂实际应用具很重要的意义。

