发酵法生产利普司他汀的研究进展
李玲,于泳,胡永红
(1 东南大学成贤学院制药与化学工程学院,江苏南京210088;2 南京工业大学生物与制药工程学院,江苏南京211816)
利普司他汀,分子式为C29H49NO5,分子量491.708,CAS 编号96829-59-3,化学名为(2S,3S,5S,7Z,10Z)-5-[(S)-2-甲酰胺基-4-甲基戊酰氧基]-2-己基-3-羟基-7,10-十六二烯酸内酯,淡黄色油状液体,几乎不溶于水,易溶于甲醇、丙酮、乙酸乙酯、正己烷。该化合物含一个β-内酯环、两个链长为6 个碳和13 个碳的脂肪族侧链,13 个碳侧链包含两个独立的双键和一个羟基酯化成N-甲酰亮氨酸(结构如图1)[1-2]。

图1 利普司他汀和THL的化学结构式
1 利普司他汀及其四氢衍生物临床应用概述
利普司他汀能选择性抑制肠道中的胰脂肪酶活性,减少脂肪的水解和吸收,其活性中心为化合物结构中的β-内酯环[2],但其结构中13碳原子的长链含有两个独立双键,该双键的存在导致其稳定性较差。瑞士罗氏(Roche)公司将利普司他汀中两个双键催化加氢, 得到四氢利普司他汀(tetrahydrolipstatin,THL,结构式如图1),即奥利司他(orlistat),于1998 年被美国食品药品监督管理局(FDA)批准作为治疗肥胖症药物上市,是目前上市的唯一非中枢神经系统药物[3-4],现在全球主要地区都已上市。该药物不同于作用于神经传导物质的传统减肥药,无头晕、心悸等不良反应。在胆汁盐的参与下,利普司他汀和胰脂肪酶结合,通过活性部位丝氨酸残基酰化来抑制胰脂肪酶的催化活性,从而降低消化道中脂肪的消化和吸收,该情况下肠道内持续处于油相状态,胆固醇同时也被隔离出来,阻断食物中约30%脂肪的水解和吸收,从而达到控制体重的目的[5-6]。
奥利司他在降“三高”(降血脂、降血糖、降血压)方面疗效显著。临床研究表明,服用奥利司他能有效降低血液中总胆固醇、降低LDL/HDL(低密度脂蛋白胆固醇/高密度脂蛋白胆固醇)比例以及LDL、甘油三酯的水平,还可以降低空腹时的血糖和胰岛素水平,改善血糖耐受性,增加胰岛素敏感性,减少低血糖治疗的需求,另外还可以降低血压,缩小腰围[7-8],能较好地控制或预防高脂血症、代谢综合征、动脉粥样硬化等疾病[9]。
奥利司他为抗肿瘤治疗提供了新思路。脂肪酸合成酶(fatty acid synthase,FAS)是脂肪酸合成中的关键酶,同时在胚胎发育、肥胖症和癌症生物学等领域具有重要功能[10]。Agostini 等[11-12]研究发现,乳腺癌、前列腺癌、口腔癌、肝细胞癌、软组织肉瘤等多种恶性肿瘤中都具有FAS过度表达,这种高度表达与肿瘤的产生、恶化相关。故如能选择性抑制该酶的活性,将会有效遏制恶性肿瘤细胞的蔓延。Knowles 等[13]利用奥利司他抑制乳腺癌细胞MCF-7、MDA-MB-435 和前列腺癌PC-3、LNCaP细胞中FAS 活性,效果显著,导致caspase-8 介导的肿瘤细胞凋亡。Kant等[14]研究发现奥利司他能强效抑制T 细胞淋巴瘤细胞中Bcl-2、HSP-70 表达,导致细胞中活性氧、细胞色素等代谢异常,从而促进肿瘤细胞凋亡。国内学者临床研究发现奥利司他能诱导口腔癌HSC-3 细胞凋亡及细胞周期阻滞[15],还有报道显示对非酒精性脂肪性肝病相关的肝细胞癌的治疗效果显著[16]。
其他应用,如Hahn等[17]研究发现服用奥利司他能抑制寄生虫脂肪酶的代谢,如抑制贾第鞭毛虫,肠道里面的寄生虫。吴宝等[18]将奥利司他与瑞舒伐他汀联合治疗单纯性肥胖伴高脂血症患者安全有效,其减轻体重和改善血脂的效果优于瑞舒伐他汀,且不增加肝肾功能损伤、肌痛风险。近日有学者研究表明,奥利司他除了具有减肥的药理作用外,还可以抑制睾丸氧化应激、炎症和细胞凋亡[19]。
奥利司他不良反应表现为可抑制某些需要羧基酯酶完成的脂溶性维生素(维生素A、D、E、K)的水解和吸收,因此建议在服药时补充脂溶性维生素[20]。在长达两年、数千名患者多项随机、双盲和安慰剂对照临床试验的结果表明,奥利司他除一些胃肠道的不良反应外,总体耐受性良好。常见胃肠道反应发生率约26%,主要表现为胃肠道排气增多、脂肪(油)性大便、大便次数增多和大便失禁[21]。
2 发酵法生产利普司他汀的现状
近年来国内外主要选用毒三素链毒菌(S. toxytricini)生产利普司他汀。Paul 等[22]的专利最早公布了利普司他汀的发酵生产工艺、提取方法,S.toxytriciniNRRL 15443最高发酵效价为6.23mg/L。瑞士罗氏(Roche)公司对毒三素链毒菌进行了诱变选育,随后对利普司他汀进行催化加氢生成四氢衍生物奥利司他,优化了发酵、提取、精制工艺[1-2],同时临床研究取得成功,实现了奥利司他工业化生产[4]。利普司他汀生产效率的提高主要取决于高产菌株的选育和发酵工艺条件优化(含培养基和培养条件),这两方面是相辅相成。Varga等[23]优化了毒三素链毒菌CCM7349 发酵生产利普司他汀的工艺过程,该工艺采用70L 发酵罐补料发酵,约34h时开始补加亚油酸、L-亮氨酸混合溶液,发酵终止效价达3290mg/L。Gasparic 等[24]改良了种子培养基发酵工艺,补料培养基中添加0.3%亚油酸、1%豆油,最优培养条件下培养144h,效价由未补料时的556mg/L 提升至4773mg/L。Fujs 等[25]公布了毒三素链霉菌突变菌株补料发酵工艺,接种20h后补加亚油酸和L-亮氨酸,控制亚油酸体积分数0.3%~0.5%,发酵结束时利普司他汀的发酵效价达4400mg/L。实验条件优化协同数学相关软件工具能显著提高实验效率,如Kumar 等[26]对菌株S. toxytriciniNRRL 15443 的发酵培养基采用Plackett-Burman 设计优化提高利普司他汀效价至1980mg/L。Luthra 团队[27-28]对菌株S.toxytriciniATCC 19813 进行UV 和NTG 联合诱变,随后采用全因子试验设计优化发酵培养条件,发酵培养添加大豆粉35g/L 和豆油25g/L 的条件下利普司他汀效价高达3290mg/L。Kumar 等[29-30]在发酵培养基中添加非常规碳源和调节利普司他汀三羧酸循环(TCA)促进产物合成,结果发现碳氮比2∶3时,添加豆粉40g/L、芝麻油30mL/L、亮氨酸、烟酸、硫胺酸、TCA 循环中间产物烟酰胺腺嘌呤二核苷酸(NADH)和琥珀酸均能有效提高利普司他汀效价,验证试验最终效价提升了2.45 倍,高达2242.63mg/L;同时对毒三素链霉菌菌丝球形成影响因素,发酵动力学参数进行了研究;该研究团队还采用紫外、甲磺酸乙酯、甲基甲烷磺酸盐和NTG 复合诱变技术结合前体物补充,提升效价至2387mg/L[31]。Khushboo等[32]采用N-甲基-N'-硝基-N-亚硝基胍(NTG)和γ射线复合诱变选育并对发酵条件、脂肪酸前体添加进行优化,利普司他汀最高产量为5886mg/L。
上海师范大学王栋海[33]最早通过紫外和微波复合诱变处理毒三素链霉菌菌株,并对其进行培养条件优化研究,发酵效价达663mg/L。浙江工业大学韩俊茹等[34]通过相同的诱变手段得到毒三素链霉菌突变菌株XC-lp-69,并对其进行条件优化确定了补料发酵工艺,效价达1400mg/L;随后该团队对诱变菌株zjut011 采用单因素试验和正交试验法进行了优化,发现L-亮氨酸是最适合lipstatin生物合成的前体,并首次发现二价阳离子Mg2+、Co2+和Zn2+对提高lipstatin 发酵效价有显著作用,确定了最佳工艺条件为:L-亮氨酸45.72mmol/L,辛酸31.1985mmol/L (第6 天添加),Mg2+12mmol/L,Co2+1mmol/L,Zn2+0.25mmol/L,优化后效价高达4208mg/L[35]。王永青[36]采用正交实验法优化了培养条件,并确定了补料培养工艺,于发酵培养36h开始补料,控制亚油酸/辛酸(2∶1)0.35g/(L·h)、L-亮氨酸(8%)0.4g/(L·h);发酵培养72h补加4%的豆油。孙菲[37]研究了溶氧和剪切力对毒三素链霉菌发酵产生利普司他汀的影响,采用10L发酵罐补料工艺发酵效价达到6446mg/L。上海医药工业研究院黄娟等[38]通过紫外-微波复合诱变,突变菌株效价比原始菌株提高3.25倍。刘顺娜等[39]采用紫外和亚硝基胍诱变,获得一株高产突变株,选用葵花籽油作为前体和碳源,并对其进行Box-Behnken中心组合设计优化发酵培养条件,最终发酵效价高达8122.9mg/L。福建省微生物研究所陈洲琴等[40]采用单因素-正交设计实验相结合的方法,优化S.toxytriciniFIM-17-16 发酵培养基和发酵参数,发酵周期短产量高,最高效价达9667mg/L。
以上研究表明,紫外、γ射线、NTG等诱变手段结合数学软件指导的培养条件优化能大幅提升利普司他汀的产量,前体化合物L-亮氨酸、长链不饱和脂肪酸亚油酸的添加也能显著提高利普司他汀效价,另外还发现二价金属阳离子影响效果显著,如表1所示。
3 利普司他汀代谢途径和生物合成机制
链霉菌具有完善的代谢和分泌系统,最为显著的特征是具有丰富的次生代谢途径,而初生代谢和次生代谢之间具有严密的调控体系,目前临床上比较有价值的抗生素几乎都来源于链霉菌属。毒三素链霉菌合成利普司他汀确切的代谢途径和分子机制至今仍未完全阐释清楚。Eisenreich 等[41]研究了毒三素链霉菌合成利普司他汀,起始于C8和C14脂肪酸的Claisen 缩合反应。德国科技大学和罗氏公司对利普司他汀的生物合成机理做了大量研究。Adelbert 等[43-44]运用同位素示综法,用13C 标记培养基中的油脂,采用核磁共振(NMR)法检测,结果排除了利用乙酸等小分子合成利普司他汀烃基链,而是由长链油脂代谢转化而得到[42]。C14部分的唯一来源是培养基中的不饱和脂肪酸,而氢化后的饱和13C-油脂代谢得到C8碳部分和亮氨酸部分,故亚油酸在利普司他汀C14烃基前体的生成过程中有非常重要的作用。基于以上文献结果,推测利普司他汀生物合成路径如图2,亚油酸活化生成亚油酸辅酶A,经过两次β氧化(每次降解2 个碳原子)得到十四烷-5,8-二甲酰辅酶A,和辛酸路径形成的己基丙二酰辅酶A Claisen 缩合形成3-氧代中间体,该中间体经过羟基化与N-甲酰-L-亮氨酸反应合成利普司他汀。Demirev 等[45-46]通过分子生物学研究发现酰基辅酶A 羧化酶(ACCase)复合物(图3)通过催化活化有机酸参与脂肪酸和聚酮类化合物参与了利普司他汀的生物合成,并报道了毒三素链霉菌中酰基辅酶A 羧化酶(ACCase)复合物的两个基因簇,一个基因簇accA1编码乙酰辅酶A 羧化酶复合物(ACC)的α亚基和β亚基,另一个基因簇pccB编码丙酰辅酶A羧化酶(PCC)复合物的α亚基、β亚基、ε 亚基和生物素蛋白连接酶(Bpl)结构域。刘文团队最早研究阐明了利用基因工程技术推测了参与利普司他汀合成的基因[47],近期又报道了一个在利普司他汀生物合成中观察到的例外情况,β-酮酰基载体蛋白合成酶Ⅲ(KAS-Ⅲ)的同系物LstA 和LstB,通过形成一种不寻常的异二聚体来催化C8和C14脂肪酰基CoA 底物的非脱羧Claisen缩合建立利普司他汀的C22脂肪族骨架[48]。
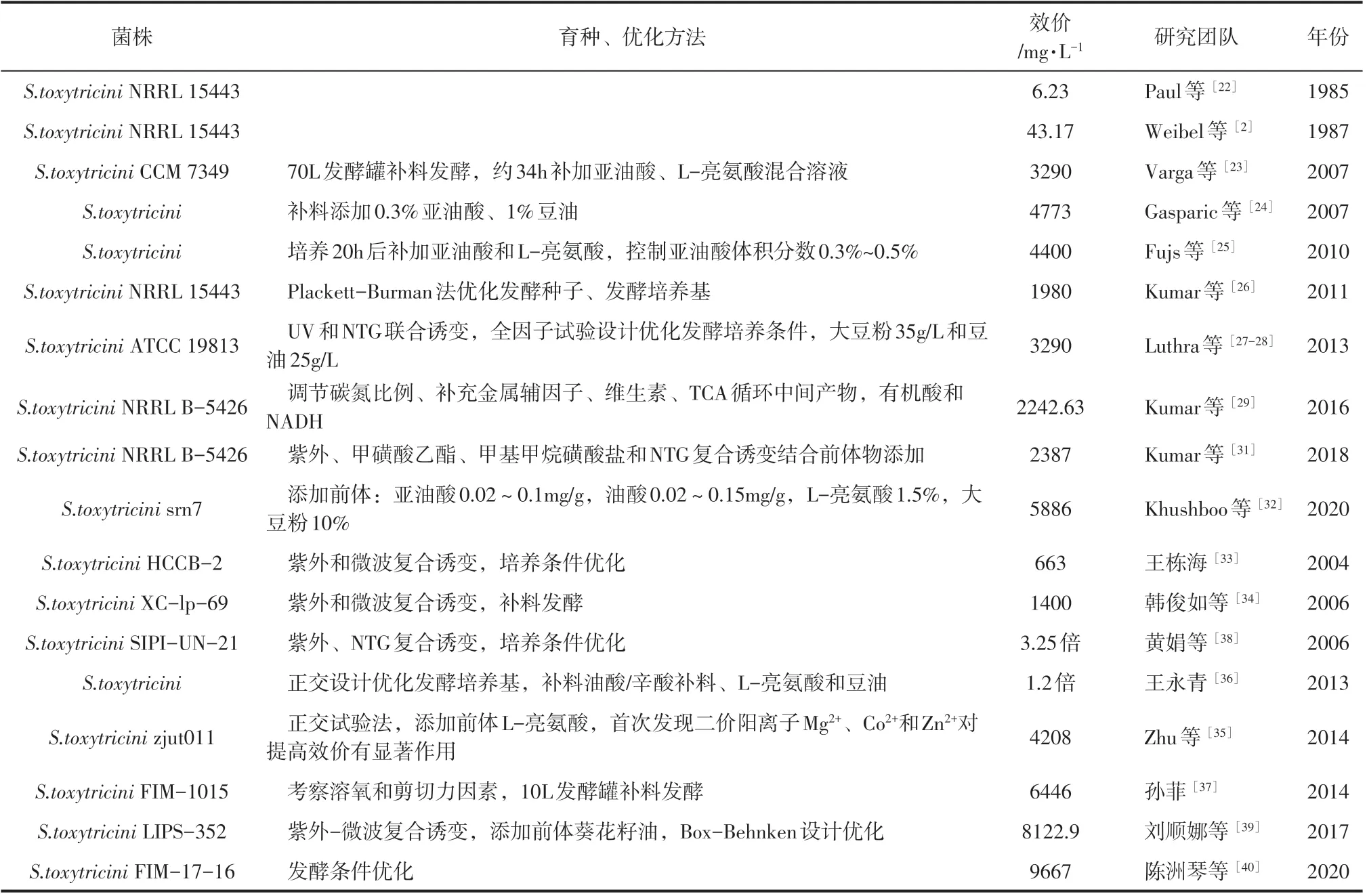
表1 国内外研究团队研究概况
4 结语
近二十年来,全球超重和肥胖的发生率大幅增加,但在发现和开发高效、副作用小的新型抗肥胖药物方面进展不够。药品监管机构因严重的不良反应已经撤销了许多减肥药(如Sibutramine,Rimonabant,Contrive,Phentermine)[10]。奥利司他在减肥药市场中所占比例最大,全球市场2019 年销售规模超30 亿美元,未来五年将会达到60 亿美元。毒三素链霉菌是生产利普他汀的主要菌株,目前科研工作者主要通过诱变育种、优化发酵参数、培养基组成和改变上下游加工因素,将利普司他汀产量提高到9667mg/L。如需进一步增加利普司他汀的产量对研究人员来说是相当具有挑战性的。目前已对利普司他汀生物合成代谢途径、分子机理进行了初步研究,绝大部分研究局限于高产菌株的诱变选育和培养基、培养条件的优化等方面,后续可从以下几个方面展开研究。①代谢路径优化,链霉菌次级代谢产物代谢途径复杂、通路多,可选择性敲除代谢支路,强化目标产物代谢途径,使前体高通量流向目标产物。②基因工程定向改造,利用定向进化的基因工程方法对前体有效性和菌株发展进行研究,结合特异性位点突变和组合突变,通过单独或组合优化关键酶的活性对合成机理进行研究。③数学模型高效调控,对利普司他汀发酵过程进行数学模型描述,精准控制工艺流程;改变链霉菌菌丝体细胞膜通透性,减轻胞内产物的反馈抑制,进一步提高生产水平及产品纯度。

图2 利普司他汀生物合成路径

图3 酰基辅酶A羧化酶(ACCase)复合物

