腹腔镜肝切除术与开腹肝切除术的效果对比及对肝功能的影响分析
蔡育志,高剑,刘丁一,廖海华,张彤
广州市番禺区中心医院消化中心二区,广东广州 511400
肝切除术是指应用外科技术将肝脏的局部病变部位切除,由于肝脏疾病的发病率不断上升,手术切除肝脏的需求也随之增加[1]。 传统开腹肝切除术虽已较成熟,能够开展各种类型的肝切除术,但手术的创伤较大、术后恢复时间久[2]。 随着微创手术及相关器械的发展,越来越多的传统开腹术现已被腹腔镜手术所替代[3]。 腹腔镜肝切除术相比开腹肝切除术能够起到缩短手术时间、减少术中出血的优点已被较多的研究所证实,但对肝功能的影响仍缺乏研究,为此该文方便选择2014 年7 月—2019 年7 月于该院进行肝切除的患者82 例进行研究, 对比腹腔镜肝切除术与开腹肝切除术的效果及对肝功能的影响,现报道如下。
1 资料与方法
1.1 一般资料
方便选择该院进行肝切除的患者82 例,使用随机数字表法将其分为对照组和研究组。对照组41 例,男28例,女13 例;年龄 30~65 岁,平均年龄(43.56±7.33)岁;肝切除病因:胆管癌5 例,肝细胞癌8 例,胆总管结石伴胆管炎7 例,肝良性肿瘤8 例,肝部继发恶性肿瘤13例;平均肝脏体积(1 710.57±129.74)cm3。研究组 41 例,男 27 例,女 14 例;年龄 30~65 岁,平均年龄(43.52±7.31)岁;肝切除病因:胆管癌5 例,肝细胞癌9 例,胆总管结石伴胆管炎8 例,肝良性肿瘤8 例,肝部继发恶性肿瘤 11 例;平均肝脏体积(1 710.52±129.71)cm3。 两组的一般资料比较差异无统计学意义(P>0.05),具有可比性。 该研究已获得医学伦理委员会的批准,所有患者均签署知情同意书。 纳入标准:①Chnd-Pugh 评分为A~B级者,术后残余肝功能可代偿;②肿瘤直径<10 cm 者。
排除标准:①有上腹部手术史者;②肝切除术中转开腹手术者;③肝切除手术禁忌证者。
1.2 方法
对照组采用开腹肝切除术, 于上腹肋缘下切口或者反L 型切口入腹,解剖性肝切除:游离肝周围的韧带及肝叶,采用 Glisson 鞘内或鞘外解剖第一肝门,显示肝缺血线。 解剖第二和第三肝门,将肝静脉段游离、结扎、切断。 采用Pringle 法控制入肝血流,未见肝硬化的患者于常温下阻断入肝血流时间不超过30 min, 根据缺血线、解剖位置、肝段使用超声刀离断肝实质,肝内管道使用钛夹或可吸收的生物夹进行闭合,电凝止血,严重出血者缝合血管,冲洗后观察有无出血,无出血后放置引流管,逐层缝合。 局部肝切除:前期手术操作同上,于距病灶2 cm 处离断肝组织,清除病灶,充分止血后放置引流管,逐层缝合。
研究组采用腹腔镜肝切除术,于脐下开口,插入气腹针,建立二氧化碳气腹,将腹内压维持在13~16 mmHg。主操作孔位于右剑突下,或左锁骨中线肋缘下。 副操位于右腋中线、右锁骨中线,或左剑突下、右锁骨中线。 解剖性肝切除:前面操作同对照组,使用腔镜直线型切割吻合器闭合离断肝蒂和肝静脉,冲洗后观察有无出血,无出血后放置引流管,逐层缝合。 局部肝切除:将肝叶组织游离后, 使用超声刀于距病灶2 cm 处离断肝实质,充分电凝止血后放置引流管,取出标本,逐层缝合。
1.3 观察指标与评价标准
观察两组的手术情况、肝功能情况、并发症情况。手术情况为术中出血量、手术时间、切口长度、肝门阻断时间。 肝功能情况使用全自动生化分析仪检测患者的总胆红素(TBIL)、血清谷丙转氨酶(ATL)的水平。 并发症情况为术后患者发生感染、 出血、 静脉血栓的情况,总发生率=并发症发生总数/患者总数×100.00%。
1.4 统计方法
该研究使用SPSS 20.0 统计学软件分析数据,计量资料用()表示,组间差异比较用t 检验;计数资料采用[n(%)]表示,组间差异比较用 χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组的手术情况对比
研究组的术中出血量低于对照组, 手术时间短于对照组,切口长度小于对照组,差异有统计学意义(P<0.05),两组的肝门阻断时间比较差异无统计学意义(P>0.05),见表 1。
表1 两组的手术情况对比()

表1 两组的手术情况对比()
组别 术中出血量(mL)手术时间(min)切口长度(cm)肝门阻断时间(min)对照组(n=41)研究组(n=41)t 值P 值217.34±34.56 196.64±36.53 2.636<0.05 138.46±35.12 123.37±28.35 2.141<0.05 17.73±1.42 5.48±0.42 2.013<0.05 24.58±8.49 25.31±8.57 0.387>0.05
2.2 两组的肝功能情况对比
研究组术后的TBIL 和ATL 水平均低于对照组,差异有统计学意义(P<0.05),见表 2。
表2 两组的肝功能情况对比()
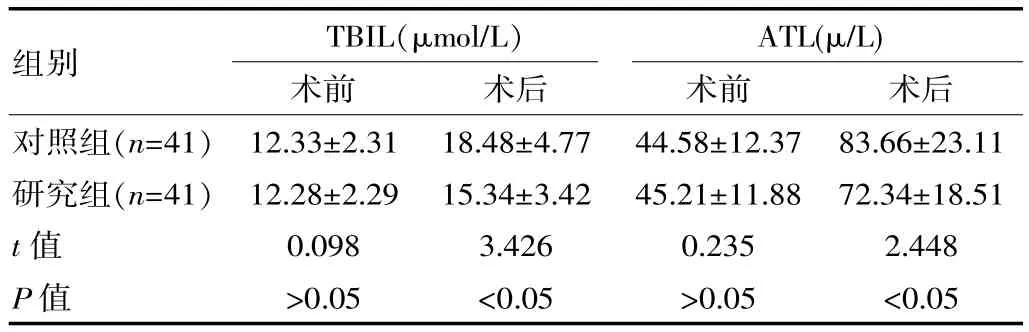
表2 两组的肝功能情况对比()
组别TBIL(μmol/L)术前 术后ATL(μ/L)术前 术后对照组(n=41)研究组(n=41)t 值P 值12.33±2.31 12.28±2.29 0.098>0.05 18.48±4.77 15.34±3.42 3.426<0.05 44.58±12.37 45.21±11.88 0.235>0.05 83.66±23.11 72.34±18.51 2.448<0.05
2.3 两组的并发症情况对比
研究组的并发症总发生率(2.44%)低于对照组的并发症总发生率(14.63%),差异有统计学意义(P<0.05),见表3。
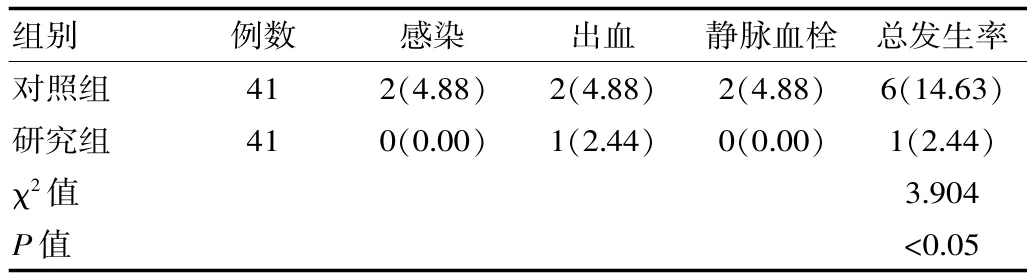
表3 两组的并发症情况对比[n(%)]
3 讨论
肝切除术是治疗肝脏恶性肿瘤、肝脏良性肿瘤、肝囊肿、肝内胆管结石等肝脏疾病的主要方法,我国是肝病大国,肝切除术的需求增加[4]。 传统开腹肝切除术随着百余年的发展,不断改进和完善,治疗效果得到广泛认可,但存在创伤大、恢复慢等缺点[5]。 随着生活水平的不断提高,患者对于手术各方面的要求也越来越严格,通过腹腔镜的微创手术具有创伤小、恢复快的优点,是当下更符合患者需求的手术方式[6]。 肝切除的患者,保留其残存的肝功能是关键, 但由于肝脏的特殊结构和功能,其受手术的影响更加敏感,手术易造成肝功能的损伤[7-8]。 目前对于腹腔镜肝切除术是否会影响患者的肝功能并未获得结论, 因此该文研究腹腔镜肝切除术与开腹肝切除术的效果对比及对肝功能的影响。
腹腔镜肝切除术通过在腹腔镜下进行肝脏的分离、止血、缝合等操作,手术仅需做数个5~10 mm 的孔状切口即可完成, 相比传统的开腹手术10 cm 的切口小得多, 具有更好的美观性。 手术于密闭的腹腔内进行,相比传统开腹手术内环境受影响较小,术后能够快速恢复[8-10]。
该研究中,研究组的术中出血量低于对照组,手术时间短于对照组,切口长度小于对照组(P<0.05),两组的肝门阻断时间比较差异无统计学意义(P>0.05),说明腹腔镜肝切除术的效果优于开腹肝切除术, 能够减少术中出血及手术创伤,缩短手术时间。 分析原因:腹腔镜具有放大的功能,术中的视野清晰,能够清楚地观察到大小血管的分布,避免过度切除而引发的出血,同时能够及时封闭小血管, 手术使用的超声刀也能够起到止血作用。 肝门的阻断技术与传统的开腹手术一致,能够起到控制入肝血流的作用[11]。
TBIL 是直接胆红素与间接胆红素的总和, 胆红素的代谢与肝脏的功能联系紧密,TBIL 升高提示肝功能异常。 ATL 在肝细胞中的含量最多,ATL 升高提示肝细胞受损,该研究中,研究组术后的TBIL 和ATL 水平均低于对照组(P>0.05),说明腹腔镜肝切除术相比开腹肝切除术,对肝功能的影响小。 分析原因:传统开腹手术需充分游离肝组织来获得清晰的手术视野, 对肝组织的损伤较大。 腹腔镜肝切除术通过腹腔镜放大细小组织的功能,切除肝脏的过程较精细,能够减少对肝组织的损伤,对肝功能的影响小[12]。
肝切除术的手术风险较高,术后并发症对患者的病情及预后影响较大。 该研究中,研究组的并发症总发生率(2.44%)低于对照组的并发症总发生率(14.63%)(P<0.05)。 马沛等人[11]的研究中,对照组术后并发症发生率为20.00%(8/40)较研究组术后并发症发生率(2.50%)高(χ2=4.507,P=0.013), 该文的研究结果与马沛等人的研究结果一致。 说明腹腔镜肝切除术能够降低感染、出血、静脉血栓等并发症的发生。 分析原因:腹腔镜肝切除术的密闭性较好, 能够防止空气中的细菌等影响内环境,同时手术的创伤小、恢复快速,患者术后能够尽早下地活动,减少卧床时间,避免静脉血栓的形成[12-14]。
综上所述, 腹腔镜肝切除术的效果优于开腹肝切除术,对患者的肝功能影响小,能够降低感染、出血、静脉血栓等并发症的发生。

