肺癌患者容积旋转调强放疗放射性肺炎发生的影响因素分析
宋丽丽
(佳木斯市肿瘤医院,黑龙江 佳木斯 154002)
肺癌是发病率及病死率较高的恶性肿瘤,因疾病早期无特异性症状,患者常伴有胸痛、咳痰、咳嗽等症状,故早期难以确诊,导致多数患者就诊时为中晚期,不利于预后[1]。目前,临床主要通过靶向治疗、化疗、放疗、手术等方式治疗肺癌患者,而放疗是运用放射线杀灭肿瘤的方式,是晚期肺癌患者的主要治疗手段。容积旋转调强放疗(VMAT)、调强适形放疗(IMRT)等是现阶段运用较广泛的放疗技术,可通过增加剂量以加强局部控制,有效改善预后[2]。但相关研究发现[3],非小细胞肺癌患者在行根治性放疗后,31.35%的患者出现≥2级的放射性肺炎(RP)。因此,如何有效降低RP发生率成为近年来临床关注的重点。鉴于此,本研究探讨肺癌患者VMAT发生RP的影响因素。报告如下。
1 资料与方法
1.1 一般资料
选择我院2018年8月—2019年8月行VMAT的肺癌患者72 例,其中男55 例,女17 例,年龄(62.36±9.74)岁;临床分期:Ⅱ期7 例,Ⅲ期53 例,Ⅳ期12 例;发生RP 18 例(25.00%),未发生RP 54 例(75.00%)。
1.2 纳入和排除标准
纳入标准:经病理学或细胞学确诊者;均为原发灶,且首次行VMAT治疗;放疗后随访≥6 个月;临床及随访资料完整者。排除标准:治疗期间中断放疗≥7 d;存在胸部放疗史;有严重精神系统疾病者;接受其他放疗技术。
1.3 方法
采用问卷调查,记录所有患者一般资料,包括年龄、性别、糖尿病、临床分期、病理类型、吸烟史,并统计双肺平均剂量(MLD)、双肺V5,V20和V30等剂量学参数。RP的诊断:放疗后出现发热、咳痰咳嗽、胸闷等症状,或以上症状加重;照射区域内炎症变化与胸部影像学显示的炎症变化基本相同;排除药物性肺炎、肺梗死、心源性疾病、肺部感染等因素引起的上述症状。记录RP发生率,并分析行VMAT肺癌患者发生RP的影响因素。
1.4 统计学方法
采用SPSS23.0系统软件进行统计学分析。计数资料以百分率(%)表示,采用χ2检验。用Logistic回归方法分析多因素。P<0.05为差异有统计学意义。
2 结 果
2.1 行VMAT肺癌患者发生RP的单因素分析
在年龄、糖尿病和双肺V5,V20,V30及MLD方面,发生RP患者与无RP者对比,差异有统计学意义(P<0.05)(见表1)。
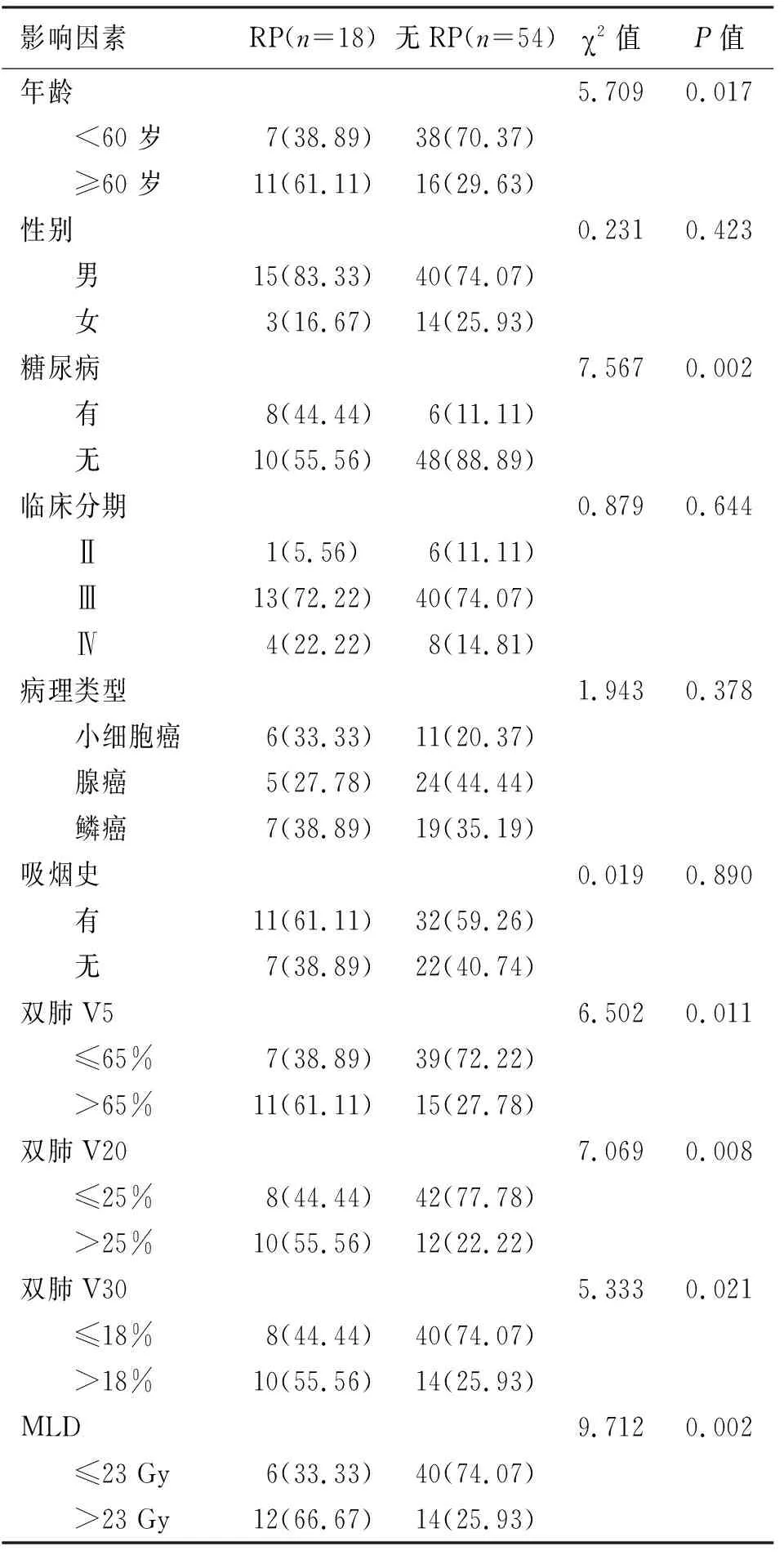
表1 行VMAT的肺癌患者RP发生的单因素分析 例(%)
2.2 行VMAT肺癌患者发生RP的多因素分析
经Logistic回归分析,年龄大、糖尿病、MLD高、双肺V5,V20和V30高是行VMAT肺癌患者发生RP的危险因素(OR>1,P<0.05)(见表2)。
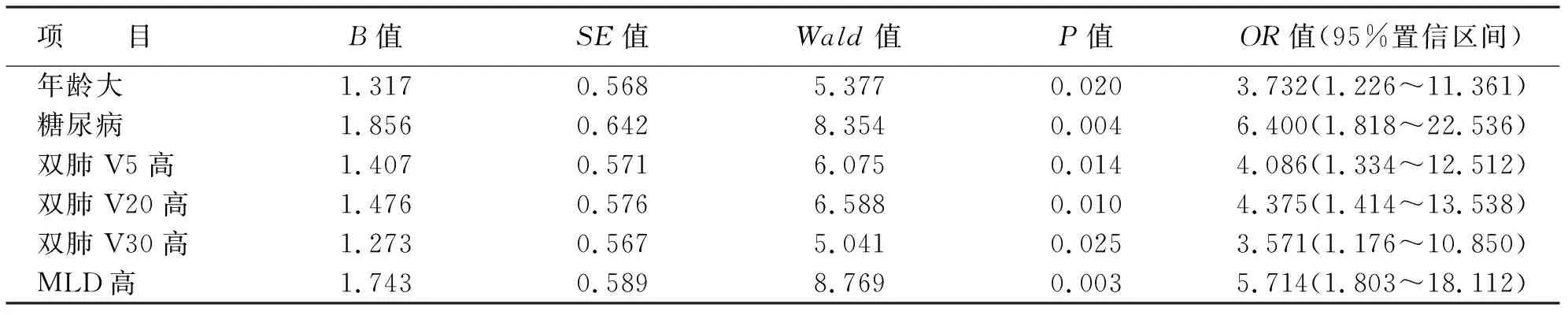
表2 行VMAT的肺癌患者RP发生的多因素分析
3 讨 论
VMAT是目前较为先进的放射治疗技术,因靶区剂量覆盖优势、机器跳数较少、治疗时间短等特点,在肺癌放疗中广泛应用。但RP是肺癌放疗后严重并发症,因肺部对射线的耐受性不高,在放疗治疗中,受到射线照射的肺组织易发生放射性肺损伤,导致低氧血症、咳嗽、劳累后气短等问题,严重者造成放射性肺纤维化,危及患者生命安全[4-5]。本研究结果显示,在年龄、糖尿病和双肺V5,V20,V30及MLD方面,发生RP患者与无RP比较,差异有统计学意义,且经Logistic回归分析,年龄大、糖尿病、MLD高及双肺V5,V20,V30高是行VMAT肺癌患者发生RP的危险因素。可见,年龄、糖尿病与VMAT肺癌患者发生RP有关,这是由于年龄大的患者,其多器官功能衰退,机体免疫力较差,且对外界反应易出现低敏或超敏,多数不能耐受放疗,导致RP发生率较高[6]。而伴有糖尿病的肺癌患者,因自身微循环病变,会阻碍肺部血液循环,进而影响受照射的肺组织修复功能,同时会增加微循环和通透性,造成炎性渗出,并影响患者肺功能,降低放疗耐受性,导致低剂量时诱发RP[7]。剂量学参数包括MLD和双肺V5,V20,V30等与VMAT肺癌患者发生RP有关。V20和V30是指全肺总体积中受到20 Gy和30 Gy等剂量照射的肺体积占比。若肺部某一区间功能单位损伤,不会影响其他功能单位,故放疗后肺功能损伤程度与超出肺耐受剂量的受照体积大小有关[8]。在照射全肺时,RP的阈值较低,仅为6~8 Gy,而在照射部分肺组织时,RP的阈值为20~30 Gy[9]。刘爱华等[10]研究发现,非小细胞肺癌患者在接受低分割放疗后,RP发生率为30.83%,且患肺最大受照剂量≥54 Gy和V20≥12%、有化疗史等是其独立危险因素,与本研究结果一致。因此,肺癌患者在行放疗时,需综合考虑多种临床因素,制订合理的治疗方案,同时严格限定受照体积V5,V20,V30等,依据高危临界值严格控制正常肺组织受量,以降低RP发生风险。

