不同取代位置的萘衍生两亲分子在气/液界面组装膜中的螺旋结构与圆偏振发光
孟 妍,王秀凤,张 莉,刘鸣华
(1.国家纳米科学中心,中国科学院纳米系统与多级次制造重点实验室,北京100190;2.中国科学院化学研究所胶体、界面与化学热力学重点实验室,北京100190)
Langmuir-Blodgett(LB)技术可在二维气/液界面上精确地控制分子之间的排列及堆积方式,从而成为在分子水平上构建有序超薄膜及纳米组装体的有效手段,受到广泛关注[1~3]. 利用LB技术可以设计和合成各种各样的两亲分子,构筑均一有序的超薄单分子层膜,或自下而上地构筑不同的纳米结构[4~8]. 除了常见的经典两亲性分子外,聚合物[9,10]、纳米粒子[11~13]、纳米线[14,15]和纳米管[16,17]等非典型的分子构筑单元均可被铺展到气/液界面上,获得不同形态的纳米结构,在传感电子记忆及场效应晶体管等领域具有潜在的应用价值[18~20].
分子之间通过非共价相互作用形成的手性空间结构或不对称排列所表现出来的超越分子层次的超分子手性现象是连接分子手性和宏观手性的桥梁,也可以模拟生物超分子结构进一步帮助理解生物体中重要功能的表达[21,22]. 超分子手性不仅与分子的本征手性相关,还与分子的组装和排布相关. 二维气/液界面也是表达及产生超分子手性的重要场所,因为界面为两相交界之处,在宏观上是不对称的.界面本身的特性决定了界面上的物理化学过程与体相的物理化学过程不同. 由于两个相对界面分子的作用力不同,界面分子处于一个力场中,不能象体相分子一样自由运动,因而在诱导分子不对称排列、表达超分子手性时有独特优势,表现出界面诱导的非手性分子的对称性破缺[23,24].
具有本征手性的分子在气/液界面的有序排列和堆积是否会促进超分子手性信号的放大是一个值得研究的课题. 本文选择含有发光基团萘环且长链取代基位置不同的手性两亲分子,即含有萘环的N,N′-双十八烷基-α-萘-L-氨基-谷氨酸二酰胺(1NLG)和N,N′-双十八烷基-β-萘-L-氨基-谷氨酸二酰胺(2NLG)(图1),研究了其在气/液界面的铺展、组装行为及转移膜的超分子手性. 研究发现,萘环取代的位置对于界面组装体的结构及性能具有非常明显的同分异构效应. 萘环的取代位置不同,导致两亲分子组装形成不同的纳米结构:1NLG组装形成了均一的纳米带状结构,而2NLG则形成了左手螺旋结构. 与三维体相中的组装相比,界面组装体表现出更明显的超分子手性放大效应,2NLG 的界面组装体表现出圆偏振发光(CPL)性质,其不对称因子[glum,glum=2(IL-IR)/(IL+IR),其中IL与IR分别是指左手与右手CPL值[25,26]]与三维体相组装体(超分子凝胶)相比明显提升,表明界面上分子的有序排列促进了超分子手性的放大.
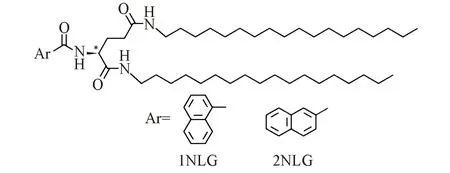
Fig.1 Molecule structure of 1NLG and 2NLG
1 实验部分
1.1 试剂与仪器
Boc-L-谷氨酸(98%)、十八胺(98%)、1-萘甲基酰氯(98%)和2-萘甲基酰氯(98%),美国Alfa公司;氯仿作为溶解和分散试剂,按照标准方法纯化处理;经过Milli-Q装置过滤的去离子水用作亚相,25 ℃导电率(18 MΩ·cm);参照文献[27]方法合成1NLG和2NLG并提纯.
KSV 小型槽(由电脑控制),芬兰KSV 公司,LB 膜槽表面积为273 cm2(364 mm×75 mm);Shimudzu UV-2600型紫外-可见(UV-Vis)光谱仪,日本岛津公司;TENSOR-27型傅里叶变换红外光谱仪(FTIR),德国布鲁克公司,分辨率4 cm-1;JASCO J-815型圆二色谱仪(CD)和JASCO CPL-200型圆偏振荧光光谱仪,日本加司科公司;Empyrean型X射线衍射仪(XRD),荷兰帕纳科公司;Bruker Fast Scan型原子力显微镜(AFM),ScanAsyst模式(智能模式),德国布鲁克公司.
1.2 实验过程
所有测试在室温下进行. 配制1.0×10-4mol/L的1NLG和2NLG的氯仿溶液并分别滴加500 μL到水亚相表面;挥发溶剂20 min后,用滑障以5 cm2/min的速度压缩表面膜,测试表面压-单分子面积等温曲线,即π-A等温线. 利用水平转移法,将分子膜转移到洁净的石英基片上测试其紫外-可见光谱、圆二色光谱、荧光光谱及圆偏振发光光谱;转移到CaF2基片上进行红外光谱测试;转移到硅片基片上测试XRD 谱. 在特定的压力下,以1 mm/min 速度和垂直提拉的方式将分子膜转移到新剥的云母片上用于AFM扫描,AFM的高度和三维图像除了图像整平未进行其它图像处理,以跟踪模式采集512×512像素图像.
2 结果与讨论
2.1 1NLG与2NLG在气/液界面的组装
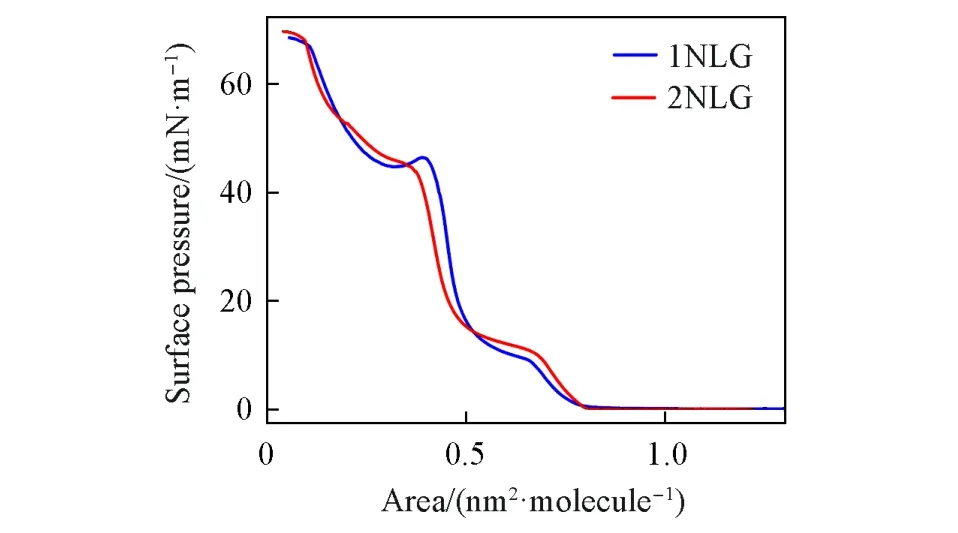
Fig.2 Surface pressure⁃molecular area isotherms(π⁃A)of 1NLG and 2NLG on the water subphase
图2给出1NLG和2NLG分子在纯水亚相上的π-A曲线. 由图2可见,1NLG和2NLG分子均可在水亚相表面铺展并形成相对稳定的Langmuir膜. 1NLG和2NLG表面压的起点分别为0.82和0.80 nm2,随着压缩的进行,表面压力逐渐升高,分别在9和10 mN/m出现转折点,表明液态扩张相向液态凝聚相转变. 继续压缩分子膜,表面压力进一步升高至约46 和44 mN/m,表面压-面积(π-A)曲线出现第2 个转折点,随后呈线性增加. 从π-A曲线推测1NLG 和2NLG 两亲分子分子膜的崩溃压约为46和44 mN/m,继续压缩会导致单层膜到多层膜的转变. 由π-A曲线可推测出1NLG和2NLG分子的极限占有面积分别为0.54 和0.49 nm2/molecule,小于根据Gaussian 09 程序优化的分子头基面积(图3,假设亲水的萘基团和酰胺基团部分接近水的表面,计算得到的单分子面积分别为0.93 和1.01 nm2),表明两亲分子的亲水头基在气/液界面可能采取相对倾斜的方式排列.
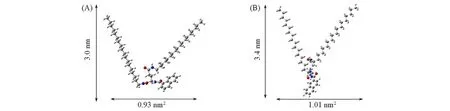
Fig.3 Models of 1NLG(A)and 2NLG(B)calculated by Gaussian 09
2.2 1NLG和2NLG单层LB膜的AFM形貌
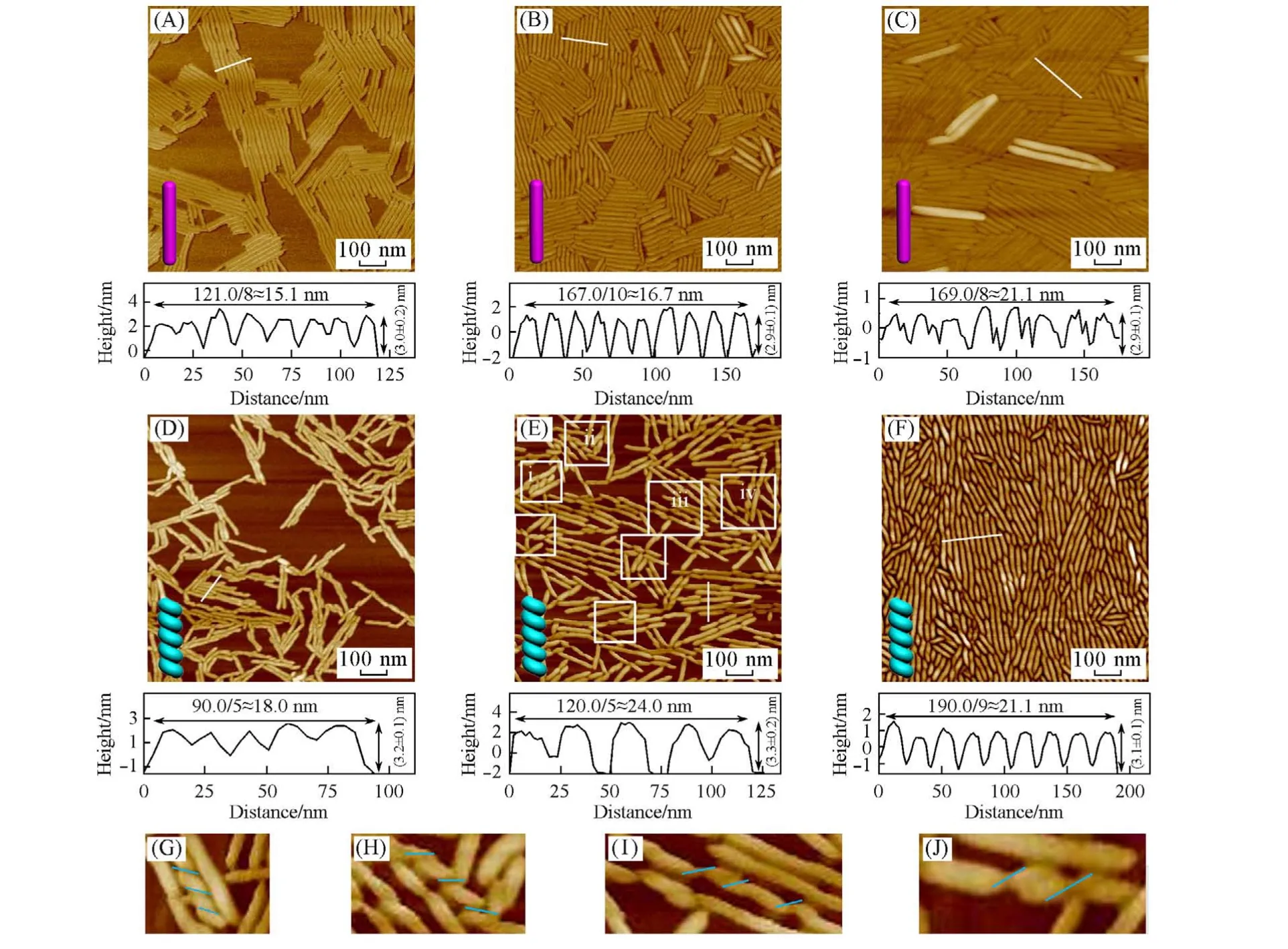
Fig.4 AFM images at various surface pressures of monolayer LB films of 1NLG(A—C) and 2NLG(D—F)and magnified images of the selected regions(i—v)in(E)(G—J)
为了研究1NLG 和2NLG 分子所形成的Langmuir 膜的聚集结构,通过垂直提拉法将界面分子膜转移单层到云母片表面,利用AFM 技术研究膜的表面形貌. 图4(A~C)给出了不同表面压力下1NLG 的LB膜的AFM图像. 当铺展膜在5 mN/m压力下转移时,LB膜形貌为纳米带状结构,直径尺寸均一,约为15.1 nm,横截面的高度均一,约为(3.0±0.2)nm,与Gaussian 09程序优化的分子高度(3.1 nm)基本一致,表明1NLG在水亚相表面形成了相对稳定的单层膜. 当表面压增加到15 mN/m时,1NLG的超分子组装体保持纳米带状结构,直径约为16.7 nm,高度保持不变,约为(3.0±0.2)nm,但微畴之间的空隙明显减小. 继续增加表面压至30 mN/m,1NLG 的LB 膜基本形貌没有发生明显变化,仍表现为均一的纳米带状结构,直径约为21.1 nm,高度约为(2.9±0.1)nm,但纳米带排列更加紧密,空隙进一步减小,并且出现单层膜向多层膜转化的趋势.
图4(D~F)示出了不同表面压力下2NLG的LB膜的AFM图像. 与1NLG的LB膜的纳米带状结构不同,2NLG 在5 mN/m 的压力下转移得到的LB 膜呈现出明显的左手纳米螺旋结构,其直径约为18.0 nm,高度在(3.2±0.1)nm左右,与Gaussian 09程序优化的分子高度(3.4 nm)一致,表明2NLG分子在气/液界面铺展时形成了单层膜. 当表面压从5 mN/m增加到15 mN/m时,所得LB膜的纳米螺旋结构保持不变,直径约为24.0 nm,高度约为(3.3±0.2)nm. 当表面压继续增加到30 mN/m时,纳米螺旋结构之间的堆积更加紧密,直径约为21.1 nm,高度约为(3.1±0.1)nm.
由图4可见,由1NLG和2NLG组装得到的LB膜的纳米结构高度和直径基本相同,但2NLG形成的LB膜具有明显的左手螺旋结构,表明萘环的取代位置影响了分子间的π⁃π堆积及氢键作用,进一步影响了分子的排列,导致组装形成的纳米结构有明显差别.
2.3 界面组装体的超分子手性
为了更好地理解两亲分子1NLG 和2NLG 在界面的排列及组装,采用朗缪尔-谢弗(Langmuir-Schaefer,LS)技术将分子膜转移至石英基片上测试其紫外-可见吸收光谱. 由图5(A)可见,1NLG 和2NLG膜分别在221和217 nm处有一个强的吸收峰,在290和283 nm处有一个相对较弱的吸收峰,分别对应萘基团的1Bb吸收带和1Lb吸收带. 与1NLG和2NLG分子的氯仿溶液相比,LS膜的吸收峰表现出明显的蓝移,分别从单分子态的230 和236 nm 蓝移到221 和217 nm,表明在1Bb的跃迁方向形成了H-聚集. 与1NLG相比,2NLG的LS膜相对于其溶液态表现出更明显的蓝移. 我们推测在气/液界面排列时,2NLG分子之间可能存在更强的π-π堆积作用[28].
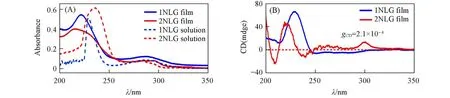
Fig.5 UV⁃Vis absorption(A) and CD(B) spectra of 1NLG and 2NLG in chloroform and 40⁃layer LS films of 1NLG and 2NLG transferred at 15 mN/m
由于凝胶分子含有手性中心,测试了LB膜的圆二色光谱[图5(B)],所有CD测试均通过旋转测试附件消除其线二色性(LD)影响[29]. 尽管1NLG和2NLG都具有本征手性中心,但其溶液均无法得到CD信号,这可能是由于手性中心距离发色的萘基团较远,无法在溶液这一相对自由的环境实现手性从手性碳原子到远端发色团的有效传递. 而将1NLG 和2NLG的界面组装体转移到固态基板上形成的LS膜则可检测到明显的CD信号,分别在229和219 nm处得到正的科顿效应(Cotton effect),与紫外-可见吸收光谱的吸收对应. 这一结果表明,1NLG和2NLG分子在LS膜中实现了手性传递,诱导萘基团产生了超分子手性信号. 同时,1NLG的LS膜在289 nm处没有明显的手性信号,2NLG的LS膜在300 nm处显示出一个正的科顿效应,手性不对称因子gCD=2.1×10-4,表明2NLG分子间的相互作用强于1NLG分子,有利于手性在超分子组装体中的传递.
CPL是手性体系的一个独特性质,可用于评价超分子组装体的激发态手性[30~34],在手性传感和3D显示等领域有重要的应用[35]. 1NLG和2NLG分子同时具有荧光基团和手性中心,满足CPL发光的基本条件,因此本文进一步研究了LS 膜的荧光[图6(A)]及CPL 性质[图6(B)]. 在同等荧光强度条件下,1NLG 的LS 膜基本无法观测到清晰的CPL 信号,而2NLG 的LS 膜在360 nm 处左右显示出正的CPL 信号. 这与CD 光谱得到的信息相吻合,表明2NLG 界面组装体中手性传递的效率明显强于1NLG 组装体. 为了考察二维界面对超分子手性组装体的影响,本文同时测试了2NLG 超分子凝胶的CPL 光谱[图6(B)],发现其在360 nm处也可产生明显的CPL正信号,并且LS薄膜的CPL不对称因子glum为4.8×10-2,明显高于2NLG凝胶体系的glum(2.1×10-3),约为凝胶体系的23倍,表明二维界面分子的有序排布有利于激发态手性的表达,其有序组装体系拥有更高的不对称因子.
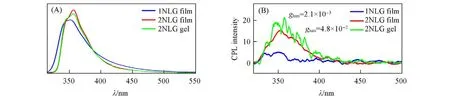
Fig.6 Fluorescence(A)and CPL(B)spectra of LS films fabricated by 1NLG,2NLG and 2NLG gel
红外光谱是表征化合物结构和超分子组装体中驱动力的有效手段,图7(A)示出了LS膜的红外光谱. 由图7(A)可见,1NLG和2NLG在3300 cm-1附近出现N-H的伸缩振动峰;2916与2848 cm-1处强而尖锐的振动峰可归属于长烷基链的CH2不对称及对称伸缩振动,说明尾链是规整的全反式排列,疏水尾链间有很强的范德华力[36]. 另外,酰胺Ⅰ带及酰胺Ⅱ带分别出现在1658~1624 cm-1与1556~1527 cm-1处,说明C=O与N-H之间存在氢键[37]. 1NLG和2NLG的酰胺Ⅰ带明显不同,1NLG分别在1656,1643和1631 cm-1处出现3个振动峰,而2NLG 则在1658和1639 cm-1处出现2个峰,并在1624 cm-1出现一个肩峰. 结果表明,与1NLG分子相比,2NLG的酰胺Ⅰ带向低波数移动,说明2NLG分子间的酰胺键之间的氢键作用更强,更有利于超分子手性的放大和传递[37].
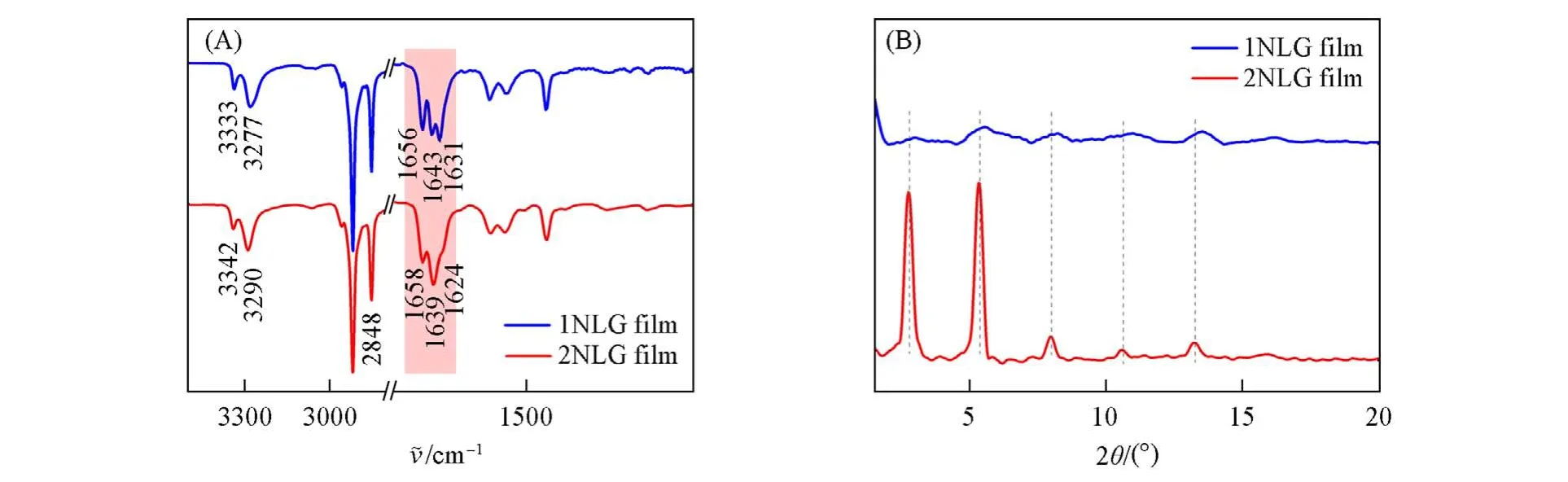
Fig.7 FTIR spectra(A)and XRD patterns(B)of 70⁃layer LS films at 15 mN/m formed by 1NLG and 2NLG
为了进一步理解NLG分子在界面和组装体中的排列方式,测试了LS薄膜的XRD谱图. 图7(B)为1NLG和2NLG的XRD谱图. 1NLG在2θ为2.9°,5.3°,7.9°,10.6°及13.6°处出现衍射峰,根据布拉格方程,层间距计算为3.2,1.7,1.1,0.8,0.6 nm,符合1∶1/2∶1/3∶1/4∶1/5的比例关系,表明形成了层状堆积,层间距约为3.2 nm,与AFM测量的高度和Gaussian 09程序优化拟合的分子疏水链长度基本吻合,证明1NLG的LS膜的基本排布模式为层状排布. 同样地,2NLG在2θ为2.8°,5.3°,7.9°,10.6°和13.2°处出现衍射峰,层间距计算为3.2,1. 6,1. 1,0.8,0.7 nm,层间距对应的比例为1∶1/2∶1/3∶1/4∶1/5,也证实了2NLG组装体的有序层状结构,层间距约为3.2 nm,与AFM测量的高度一致. 比较1NLG和2NLG 可以看出,2NLG 的LS 膜的XRD 衍射峰强度明显强于1NLG 薄膜,表明2NLG 比1NLG 的堆积更有序. 规则紧密的分子排列使得谷氨酸头基间的手性相互作用逐级积聚,从而驱使棒状结构发生弯曲以释放累积起来的手性张力,形成手性螺旋结构.
根据上述结果和1NLG 及2NLG 的分子结构,提出了NLG 分子界面组装体的可能形成模型(Scheme 1). 1NLG分子由于手性中心和疏水长链与萘环基团有一定的角度,在气/液界面上压缩时,由于萘环的空间位阻作用,疏水尾链的靠近没有2NLG分子紧密,从π-A曲线中得到的1NLG分子极限占有面积大于2NLG 的极限面积也印证了1NLG 在界面上的排列相对松散,同时也会影响到分子间的氢键作用和π-π堆积,使1NLG分子不容易像2NLG分子那样形成规则紧密的排列,因而手性相互作用的累积要弱于2NLG组装体,2NLG组装体的手性相互作用在形貌学上和光谱学上的表达更明显.

Scheme 1 Possible formation process of 1NLG and 2NLG interfacial assemblies
3 结论
含有萘基团与十八烷基谷氨酰胺的手性分子1NLG 和2NLG 可在气/液界面可以形成稳定的单层膜. 由于萘基团与疏水尾链的连接位点不同,导致分子排列不同,2NLG的分子排列更利于氢键产生,在π⁃π相互作用和疏水相互作用的有效协同下,手性相互作用不断地逐级累积放大,最后形成螺旋纳米结构,而1NLG 则形成纳米带结构. 1NLG 和2NLG 分子均具有手性中心,并在组装时将分子手性传递给超分子组装体,形成具有手性的超分子膜. 但2NLG所形成的LB膜具有更强的CPL信号,其glum比凝胶体系中的放大了23倍.

