奈达铂联合吉西他滨对比顺铂联合吉西他滨一线治疗晚期肺鳞癌随机对照临床研究
陈胜佳 朱 凯 林金兰 张 晶 徐振武 庄 武 徐海鹏
福建省肿瘤医院 福建医科大学附属肿瘤医院胸部肿瘤内科,福建福州 350014
目前晚期肺鳞癌的治疗进展相对于晚期肺腺癌进展缓慢,一线治疗方式上除了部分肺鳞癌可考虑给予单药免疫治疗和可选择免疫联合化疗外,主要治疗方式仍是以全身化疗为主,传统的铂类因其不良反应,特别是消化道反应发生率高,人们期望探讨新的治疗方案[1]。奈达铂作为一种新型的铂类,目前在多种瘤种治疗中应用[2-3]。为进一步探讨奈达铂在肺鳞癌治疗中的效果,福建省肿瘤医院(我中心)既往联合福州市肺科医院、厦门市第二医院呼吸科、泉州市第一医院呼吸科共4家中心于2012年9月至2013年12月完成101例奈达铂联合吉西他滨与顺铂联合吉西他滨一线治疗晚期肺鳞癌随机对照临床研究,之前报道了奈达铂联合吉西他滨(NDP+GEM)治疗晚期肺鳞状细胞癌的疗效与不良反应[4]。目前更新了OS数据,现报道如下。
1 资料与方法
1.1 一般资料
病例入选标准:①经病理学(或细胞学)和影像学确诊的ⅢB及Ⅳ期的肺鳞癌初治患者,临床分期采用NSCLC AJCC/UICC第7版TNM分期标准;②PS评分0~1分;③临床上至少有1个有可评价病灶;④年龄18~75岁;⑤预计生存期>3个月;⑥至少完成2个周期治疗并完成疗效评价;⑦无法手术治疗及放射治疗,未接受过全身放化疗;⑧无合并严重的全身疾病;⑨治疗前血常规、肝肾功能、心电图等无明显异常。研究设计:多中心、开放性、前瞻性、随机对照临床研究。按照治疗组与对照组随机入组。根据入选标准,研究期间试验组入组69例,对照组入组32例,两组患者一般资料比较,差异无统计学意义(P>0.05)。具有可比性。见表1。
1.2 给药方法
试验组:NDP(捷佰舒,南京先声东元制药有限公司,H20030884)80 mg/m2静脉滴注d1,GEM(泽菲江苏豪森药业股份有限公司,H20030105)1000 mg/m2静脉滴注d1,d8;对照组:DDP 75 mg/m2静脉滴注 d1,GEM(泽菲)1000 mg/m2静脉滴注 d1,d8;奈达铂。给药方法:80 mg/m2静脉滴注,受试者每周期用药一次,奈达铂加入500 ml的生理盐水中,静脉滴注2 h,滴完后继续静滴输液1000 ml以上,每3周重复。药品来源:注射用奈达铂,10 mg/支,由南京先声药业有限公司。本品为白色冻干粉针剂,遮光,密闭,室温保存。注射用吉西他滨:200 mg/支,由江苏豪森制药有限公司。化疗2个周期,对于稳定及有效的病例可以继续应用原化疗方案至4 ~ 6个周期。观察两组患者的疗效及毒副反应。
1.3 疗效评价
根据RECIST 1.1实体瘤疗效评价标准分为:完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。计算 有 效率RR为(CR+PR)/总例 数×100%,临床获益率DCR为(CR+PR+SD)/总例数×100%[5]。无进展生存时间(PFS)是指患者随机入组给药时至任何有记录的病变进展之日或任何原因引起的死亡之日的时间。总生存(OS):从随机化分组开始,至因任何原因引起死亡的时间。自判定疗效有效(CR和PR)或稳定(SD)之日开始,每2个月定期随访1次,以观察有效或稳定患者的PFS和OS[6]。不良反应评价 按照NCI CTC 3.0的毒性指标及分级标准进行评价[7]。
1.4 统计学方法
本研究数据采用专业SPSS 20.0软件进行统计学分析处理,计数资料用[n(%)]表示,采用χ2检验,计量资料以()表示,采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组化疗完成情况比较
两组的大部分患者接受了至少两个周期的化疗,与对照组比较试验组接受化疗的周期略长,但差异无统计学意义(P>0.05),见表2。
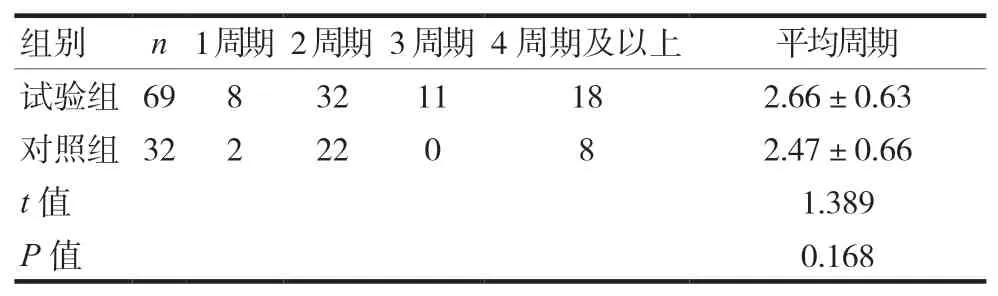
表2 两组一线治疗晚期肺鳞癌完成情况比较
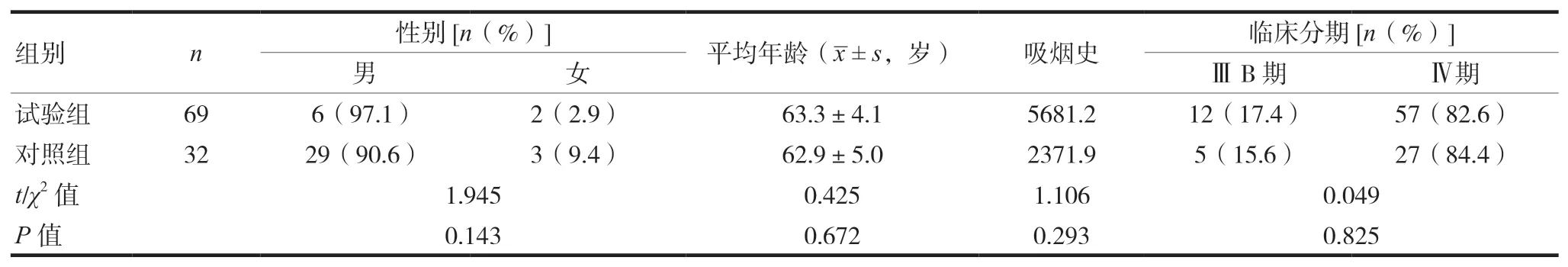
表1 两组临床一般情况比较
2.2 近期疗效
两组的CR患者均为0。两组的RR分别是24.64%和18.75%,与对照组比较,差异无统计学意义(P>0.05)。两组的DCR分别是75.36%和71.88%,与对照组比较,差异无统计学意义(P>0.05)。见表3(渐进性水平检测为1)。
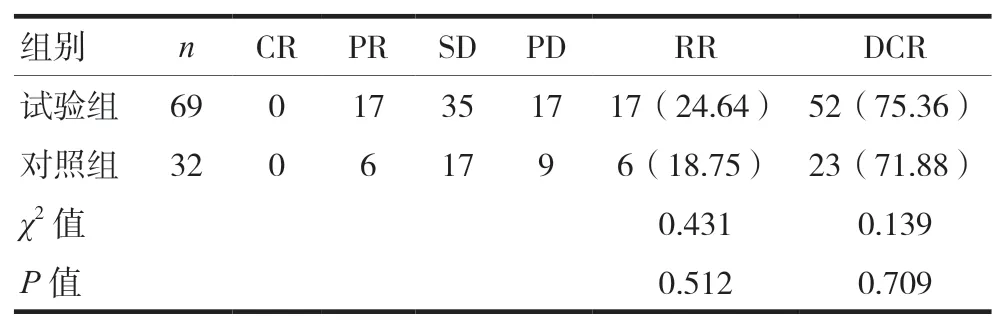
表3 两组一线治疗晚期肺鳞癌近期疗效比较
2.3 两组中位PFS
两组一线治疗晚期肺鳞癌PFS曲线(图1)。试验组中位PFS为4.0个月(95%CI:3.11~4.88个月),对照组中位PFS为4.0个月(95%CI:1.72~6.27个月),两组差异无统计学意义(P>0.05)。
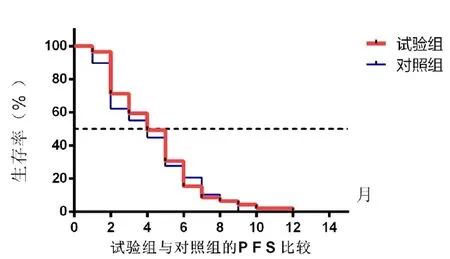
图1 两组的PFS比较
2.4 两组中位OS
两组一线治疗晚期肺鳞癌OS曲线(图2)。实验组中位OS为10.10个月,对照组中位OS为8.05个月,试验组OS比对照组延长了2.05个月,但两组间比较差异无统计学意义(P>0.05)。
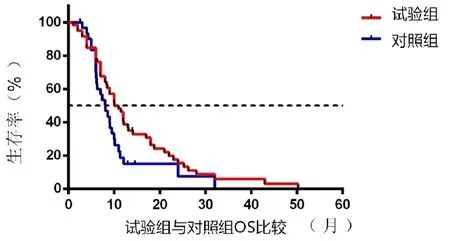
图2 两组的OS
2.5 两组患者不良反应比较
两组患者不良反应主要表现在骨髓抑制,两组差异无统计学意义(P>0.05)。试验组恶心呕吐发生率低于对照组,有显著性差异。试验组有一例于第二周期化疗时出现胸闷,气促,颜面潮红,血压下降等反应,考虑奈达铂过敏反应,予以停药,抗过敏反应处理后缓解。第三周期以后改为顺铂化疗。
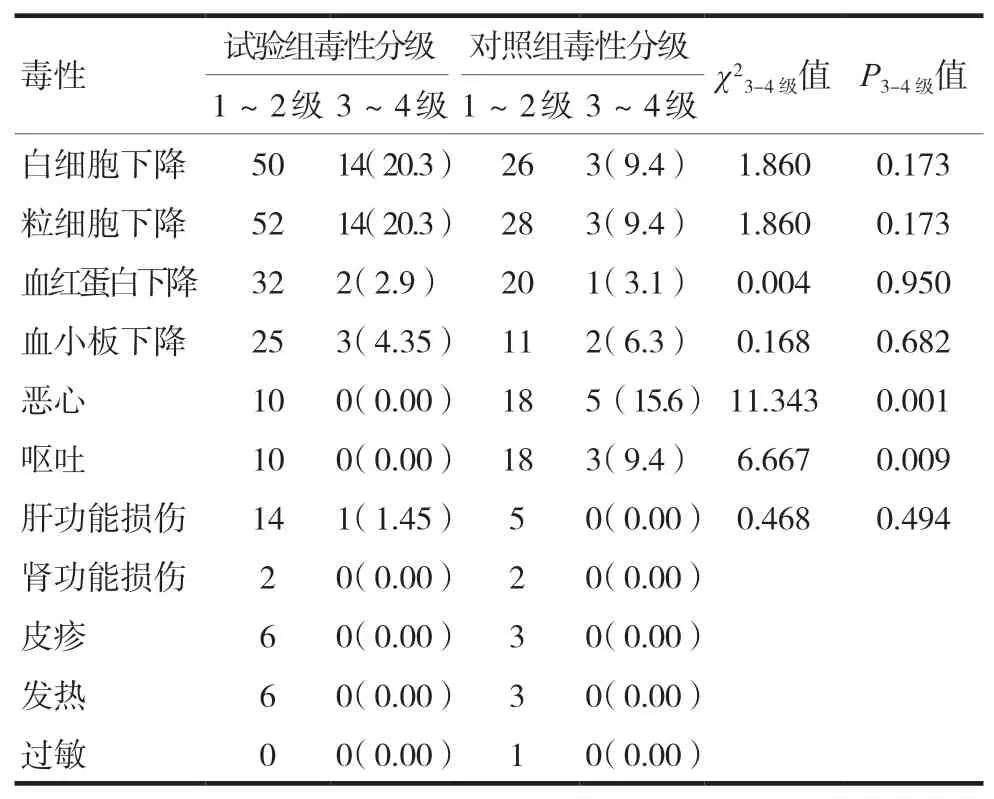
表4 两组一线治疗晚期肺鳞癌不良反应比较
3 讨论
随着分子生物学及药物学的进展,晚期非小细胞肺癌的治疗已经迈入了个体化治疗的时代。根据目前世界卫生组织(WHO)的分类,非小细胞肺癌包括许多病理亚型,主要可分为鳞癌和非鳞癌,非鳞癌中的腺癌可进一步进行分子分型[8-9],但鳞癌目前缺乏相对应的靶向药物,在治疗上,分子分型意义不大。近年来,以PD-1为代表的免疫检查点抑制剂在非小细胞肺癌治疗上取得了一定的进步,特别是缺乏靶向治疗的晚期鳞癌治疗上,这种进步显得尤为重要,目前FDA已经批准了Nivolumab(Opdivo)纳武单抗用于转移性鳞状非小细胞肺癌二线治疗。国家药品监督管理局也批准了纳武利尤单抗注射液用于治疗表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的二线治疗。但由于免疫治疗药物的可及性及昂贵的价格,传统的含铂两药联合方案在晚期肺鳞癌的治疗上依然占有重要的位置。如何优化治疗方案,提高肺鳞癌的化疗有效率,减轻毒性,提高晚期肺鳞癌生存期成为我们面对的难题。
奈达铂自上市以来,适应症为治疗头颈部癌、小细胞肺癌、非小细胞肺癌、食道癌、膀胱癌、睾丸肿瘤、卵巢癌、子宫颈癌等瘤种。因为晚期肺鳞癌有效治疗药物较少,所以前期有不少奈达铂治疗肺鳞癌的临床研究。但大多数临床研究均为小样本的Ⅱ期临床研究,包括一线治疗和二、三线治疗的研究。Masago等[10]报道的奈达铂联合吉西他滨治疗晚期初治肺鳞癌Ⅰ期临床研究中,最大耐受剂量为吉西他滨1000 mg/m2,奈达铂80 mg/m2,推荐的剂量为吉西他滨800 mg/m2d1、d8,奈达铂70 mg/m2d1进入Ⅱ期临床研究。Teramoto等[11]在多西他赛联合奈达铂治疗转移性非小细胞肺癌的Ⅱ期临床研究中发现该方案对鳞癌疗效更佳。Naito等[12]进行的一项研究奈达铂联合多西他赛治疗晚期初治肺鳞状细胞癌,共有21例患者参与研究,其中18例是男性。患者中位年龄为67岁,客观反应率为62%,平均无进展生存时间为7.4个月,平均生存时间为16.1个月,1年生存率为66.7%。最常见的不良反应是中性粒细胞减少(3/4级,86%),非血液毒性相对较轻,该研究认为奈达铂联合多西他赛治疗肺鳞癌活性高。在一项针对老年肺癌的研究中[13],入组了75岁以上的老年初治肺癌35例,予以吉西他滨800 mg/m2,第一天、第八天,奈达铂80 mg/m2,第一天,每三周重复。结果RR为45.7%,MST为14个月,3~4级毒性包括粒细胞减少74.3%,血小板减少48.6%,贫血34.3%,感染2.9%,为治疗相关的死亡。该方案对高龄肺癌有效且耐受性好。本中心关于奈达铂联合吉西他滨治疗晚期复治肺鳞癌临床观察[14],入组26例晚期复治肺鳞癌,总有效率为26.1%,临床获益率为78.3%,PFS 4个月。主要毒性Ⅲ/Ⅳ级粒细胞下降为42.3%(11/26),Ⅲ~Ⅳ级血小板下降30.8%(8/26),Ⅲ级贫血7.7%(2/26)。而最近进行的一项比较大样本的回顾性、随机、对照临床研究显示[15],奈达铂与三代细胞毒药物的联合实验组缓解率(ORR)和疾病控制率(DCR)分别为48.6%和95.2%,较对照联合组为35.1%和89.2%(P<0.01),显著提高。实验组的生存时间较对照组延长(P<0.01)。实验组贫血、肌酐升高、恶心和呕吐发生率较对照组明显降低(P<0.05)。以上研究均表明,以奈达铂为主的两药联合方案无论在一线治疗或二线治疗,亦或高龄患者,治疗晚期肺鳞癌活性高,不良反应可耐受。
本研究选择标准剂量的顺铂联合吉西他滨作为标准对照,根据奈达铂联合吉西他滨Ⅰ期临床研究推荐的剂量,两组用药剂量,入组的年龄、性别、分期、吸烟情况、化疗完成情况、因不良反应减低剂量等均均衡可比。试验组的RR、DCR、PFS与对照组比较,差异无统计学意义,虽然中位OS绝对值延长了2个月,但也未达到统计学差异。不良反应方面,试验组白细胞下降比较明显,但与对照组比较,差异无统计学意义(P>0.05)。而对照组胃肠道反应较为严重(P<0.05)。实验组包括肝肾功能损伤、皮疹、神经毒性等均比较轻微,均能很好耐受。
综上所述,奈达铂联合吉西他滨治疗晚期肺鳞癌有效率高,不良反应轻,相对于标准方案,肺鳞癌的化疗提供了一个等效低毒的选择,可以作为肺鳞癌一线治疗的选择之一。
——再论奈达对翻译本质属性的认知

