多巴胺改性海泡石的制备及吸附性能研究
刘莹,毛增玥,王梓颖,和艳阳,余晶,朱晔
(西南石油大学化学化工学院,四川 成都 610500)
在污水治理中,印染废水具有数量庞大、色度深、有机物含量多、有毒等特点[1]。近年来各种新型染料废水治理技术不断发展,其中吸附法因其设计和处理费用不高、工艺简单、效率较高等特点,成为了染料废水去除的主流技术之一。目前应用较为广泛的吸附剂包括活性炭[2]、活性硅藻土、膨润土[3]和煤渣[4]等。然而部分吸附剂存在成本较高、有毒、耐用性差、再生困难,甚至是无效再生等特点,因此,必须要寻找一种环保高效且再生简单的替代吸附剂。
海泡石(SeP)是一种常见的硅酸盐黏土矿物,具有链层状的特殊结构和高达900 m2/g的比表面积。在物理性质方面,海泡石具有可塑性强、热稳性较好、可做催化剂等特点,目前在重金属离子处理和染料废水治理方面都有广泛应用,与其他大部分吸附剂相比,海泡石具有价格相对低廉、储量丰富、处理工艺简单等优势。然而天然海泡石含有很多杂质,容易堵塞通道,并不能达到良好的去除效果,因此要对其进行一定改性操作。目前对于海泡石改性研究主要包括酸改性、热改性、有机改性等[5]。
多巴胺(DA)是一种沿海常见生物贻贝分泌的黏附蛋白的主要成分,在碱性条件下可以发生自聚反应,形成超强黏性的聚多巴胺层(PDA)。目前DA作为底物与小分子或纳米颗粒之间的联合剂已经应用于许多领域,如固体材料表面改性、生物学分析等[6]。文献[7]报道了一种多巴胺改性海泡石吸附剂的制备方法,采用这一方法改性后的海泡石对重金属的吸附性能有明显的提高。为了进一步增加海泡石吸附剂的回收利用率,笔者在多巴胺改性海泡石的基础上再对海泡石进行磁改性,制备了PDA@SeP/Fe3O4复合材料,这样回收吸附剂时,通过外部磁场的作用能够更快的进行固液分离[8]。实验采用碱性染料亚甲基蓝(MB)模拟废水,探究PDA@SeP/Fe3O4复合材料的吸附性能和可再生性。
1 实 验
1.1 药品及仪器
海泡石、盐酸多巴胺(DA·HCl) 、三羟甲基氨基甲烷(Tris)、FeCl2·4H2O、FeCl3·6H2O、亚甲基蓝(MB),成都市科龙化工试剂厂);氨水、无水乙醇、HCl、NaOH均为分析纯。
V-1800可见分光光度计,上海美谱达仪器有限公司;WQF-520傅里叶红外光谱仪(KBr压片法),北京北分瑞利分析仪器有限公司;X’per Pro MPD型X射线衍射仪,荷兰PANalytical公司;JSM-7500F扫描电子显微镜,日本电子;DF-101S集热式恒温加热磁力搅拌器,巩义市予华仪器公司。
1.2 实验方法
1.2.1 多巴胺初步改性海泡石
海泡石0.5 g,多巴胺0.5 g,分散于250 mL pH=8.5的Tris溶液中,在70 ℃下搅拌反应24 h,真空抽滤之后放入50 ℃烘箱中干燥过夜[8],干燥完毕后研磨成粉末,即得多巴胺初步修饰的海泡石产品。
1.2.2 PDA@SeP/Fe3O4复合材料制备
将0.1 g多巴胺初步修饰的海泡石分散于200 mL去离子水中,搅拌升温至50 ℃,然后加0.04 g FeCl2·4H2O和0.06 g FeCl3·6H2O,剧烈搅拌0.5 h,继续升温至65 ℃,再加入30 mL氨水,之后搅拌0.5 h取出溶液进行沉降分离,用永久性磁体分离合成的复合材料,期间用去离子水洗涤几次之后真空抽滤,然后在50 ℃烘箱中干燥过夜即可制得PDA@SeP/Fe3O4复合材料。
1.3 MB吸附实验
1.3.1 MB溶液的配制
原溶液配置:分别称取0.1、0.2、0.3 g MB粉末溶解于1 000 mL容量瓶中,配置成100、200、300 mg/L的MB溶液。
标准溶液的配制:分别取1~8 mL 100 mg/L的MB原溶液于100 mL烧杯中,加入去离子水稀释成40 mL浓度分别为2.5、5、7.5、10、12.5、15、17.5、20 mg/L的标准溶液,用去离子水做参比溶液,利用可见分光光度计测定不同浓度溶液的吸光度值建立MB标准曲线,其中,MB溶液的最大吸收波长为664 nm。
1.3.2 实验条件的考察方法
1)pH对MB吸附的影响:将10 mg PDA@SeP/Fe3O4复合材料添加到含有40 mL 100 mg/LMB溶液的烧杯中,用1 mol/L NaOH和HCl溶液调节pH值范围在3~11,超声处理3 min后在25 ℃水浴中磁力搅拌3 h,再进行磁分离,分离完成用移液管取4 mL上层清液用纯水稀释至40mL,并用可见分光光度计在MB最大吸收波长664 nm处测定吸光度值,吸附容量按式(1)计算。
2)温度对MB的影响:将10 mg PDA@SeP/Fe3O4复合材料添加到100 mL含有40 mL不同浓度50~275 mg/L的MB溶液的烧杯中,用NaOH和HCl溶液调节pH=10,超声处理3 min,在不同温度(298.15、308.15、318.15 K)的水浴中磁力搅拌3 h至吸附平衡,然后用永久性磁体分离PDA@SeP/Fe3O4复合材料与MB溶液,分离完成用移液管取4 mL上层清液用纯水稀释至40 mL,然后在可见分光光度计中测定其吸光度。吸附容量的计算见式(1)。
3)接触时间对MB吸附的影响:称取10 mg PDA@SeP/Fe3O4复合材料加入到不同浓度的MB样品溶液的烧杯中,用1 mol/L NaOH和HCl溶液调节溶液pH=10,超声处理3 min后在25 ℃水浴中搅拌3 h,设定时间间隔测定MB的剩余浓度,吸附容量根据式(2)计算[9]。
(1)
(2)
式中:qe为平衡时吸附容量(mg/g);c0为MB溶液的初始浓度(mg/L);ce为MB溶液的平衡浓度(mg/L);m为PDA@SeP/Fe3O4复合材料质量(g);v为溶液体积(L);qt为任意时间t的吸附容量(mg/g);ct为任意时间间隔后MB残余浓度(mg/L)。
1.4 PDA@SeP/Fe3O4复合材料再生实验
共进行5次MB循环实验,用无水乙醇解吸复合材料上的MB分子,大致步骤为:将100 mg PDA@SeP/Fe3O4复合材料加到100 mL初始浓度为200 mg/L的MB溶液中,调节pH=10,超声处理3 min,然后在25 ℃水浴中搅拌3 h,测其吸光度,用纯水洗涤,在50 ℃烘箱中干燥,得到吸附后的PDA@SeP/Fe3O4材料;研磨称取吸附后的材料加入50 mL无水乙醇,用盐酸溶液调节pH=3,磁力搅拌1 h后用去离子水洗涤,干燥研磨后用于下一次的循环实验。PDA@SeP/Fe3O4的再生效果通过MB的去除率(η)评价[9],见式(3)。
(3)
式中:co,MB溶液的初始浓度(mg/L);ce,平衡浓度(mg/L)。
2 结果与讨论
2.1 PDA@SeP/Fe3O4复合材料性能表征
2.1.1 红外光谱
图1为试样的红外光谱。由图1可见,在3 633.2 cm-1是海泡石内部中八面体Mg-OH的伸缩振动峰,3 569.6 cm-1的特征峰是海泡石结构内参与配位的羟基弯曲振动;另外,在1 652.7、1 020.1、1 214.9 cm-1处都属于结晶水的伸缩及弯曲振动峰[10],对比用Fe3O4修饰了的海泡石材料,以上特征峰依然存在,只是各峰值有明显的变小,峰宽变窄的现象,且在582 cm-1处出现了Fe-O峰,说明海泡石材料附着有Fe3O4。

图1 试样的FT-IR
2.1.2 X射线衍射
图2为试样的红外光谱XRD曲线。如图2所示,经多巴胺改性的海泡石特征峰数量基本不变,说明PDA的改性并没有改变海泡石的基本结构,2θ=7.36°,20.67°,35.09°处特征峰相比于海泡石原样和多巴胺改性后的材料都有较为明显的峰强度减弱现象,因为改性之后海泡石表面与多巴胺和Fe3O4之间发生物理或者化学作用导致峰强度变化,在2θ=62.93°有的Fe3O4晶体衍射峰,说明Fe3O4成功负载在海泡石表面上[11]。
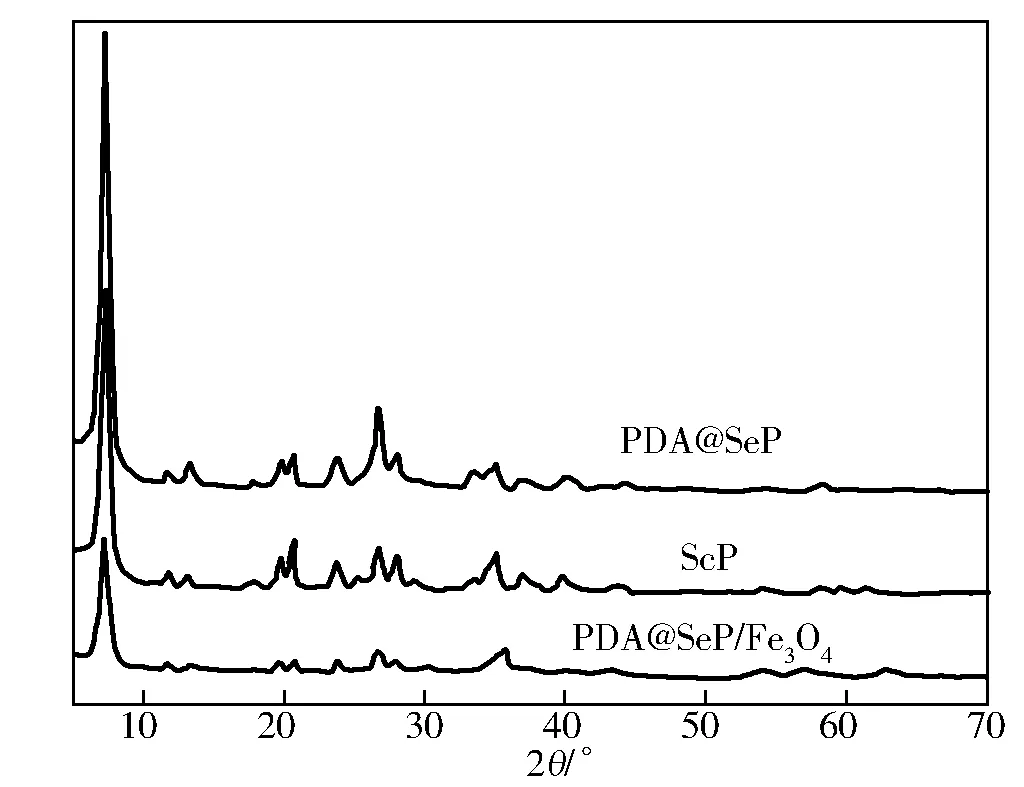
图2 试样的红外光谱XRD曲线
2.1.3 TEM
图3为试样的TEM照片。
由图3可见,经过改性之后的海泡石表面上杂质变少,整体形态更为分散,有明显的纤维状,单个结构更加清晰,并没有成团的现象,这就增大了原样的孔隙率和比表面积,使得海泡石吸附量增大。

图3 试样的TEM照片
2.2 PDA@SeP/Fe3O4复合材料对MB的吸附性能
2.2.1 实验条件对MB吸附性能的影响
1)MB标准曲线。如图4可见,其工作曲线方程为:A=0.068 08C+0.0514 6,拟合度R2=0.998 38,其中A为吸光度,C为溶液质量浓度。

图4 MB标准溶液吸光度与浓度的关系
2)pH值的影响。如图5所示,pH=10时吸附容量最大,可以达到376.01 mg/g。

图5 pH对MB吸附的影响
推测当pH值较低时,溶液中存在很多H+,这些H+使PDA@SeP/Fe3O4复合材料表面质子化,与同为阳离子型染料的MB溶液竞争吸附,使得MB分子吸附位点减少;而在碱性条件下时,溶液中OH-较多,PDA@SeP/Fe3O4复合材料表面去质子化,生成更多带负电荷的吸附位点,此时阳离子型MB可以通过静电吸引力更好地吸附在材料上。
3)温度的影响。如图6所示,温度升高,PDA@SeP/Fe3O4复合材料的吸附容量越大,并且有明显增大的趋势,即使在相同初始浓度的情况下,温度越高,吸附情况越好,45 ℃时有最大的的吸附容量,说明该吸附是一个吸热过程。另一方面,初始浓度越大,PDA@SeP/Fe3O4复合材料的吸附量也越大,并且有较为明显的增加。

图6 温度对MB吸附的影响
4)接触时间的影响。如图7所示,4个不同浓度的PDA@SeP/Fe3O4材料都有相同的吸附趋势,可以判断,改性之后的海泡石给溶液中的MB分子提供了大量的吸附位点,在前0.5 h时吸附容量增加的较快,0.5 h之后虽然也有所增加但大致的趋势不如前0.5 h明显。因为开始时PDA@SeP/Fe3O4材料表面的吸附位点被快速的占据,之后大量分子只能竞争少量的吸附位点。
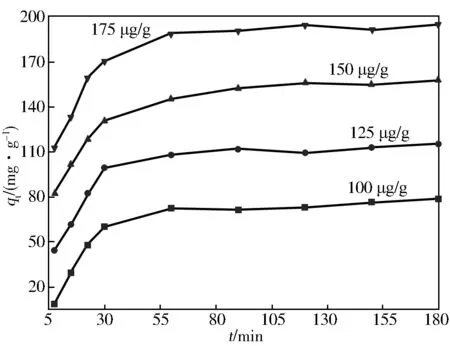
图7 接触时间对MB吸附的影响
2.2.2 PDA@SeP/Fe3O4复合材料的再生性能
对PDA@SeP/Fe3O4材料进行了5次再生性能测试,结果如表1所示。

表1 再生次数对去除率的影响
由表1可见,PDA@SeP/Fe3O4材料的吸附性能逐渐降低,5次循环后,PDA@SeP/Fe3O4对MB的吸附率仍在50%以上,证明PDA@SeP/Fe3O4复合材料在处理MB染料时是可以循环反复进行的,但循环使用次数越多,PDA@SeP/Fe3O4复合材料再生性能越弱。
2.3 PDA@SeP/Fe3O4复合材料吸附机理分析
2.3.1 吸附等温线
吸附热力学主要包括Langmuir模型和Freundlich模型,各自表达式如下[12]。
Langmuir吸附等温式
(4)
Freundlich吸附等温式
(5)
式中:ce为平衡时吸附质浓度,mg/L;qe为平衡吸附量,mg/g;KL为Langmuir平衡常数,L/g;qm为最大吸附容量,mg/g;KF为Freundlich平衡常数,L/g;n为与吸附强度有关的经验参数。
根据式(4)和式(5),可分别利用ce/qe对ce的斜率和截距和lnqe对lnce的斜率截距计算出qm、KL、n及KF的值,另外在Langmuir吸附等温线中可以用另一参数RL来表征吸附过程,具体表达式如式(6)[12],数据拟合结果如表2所示。
(6)
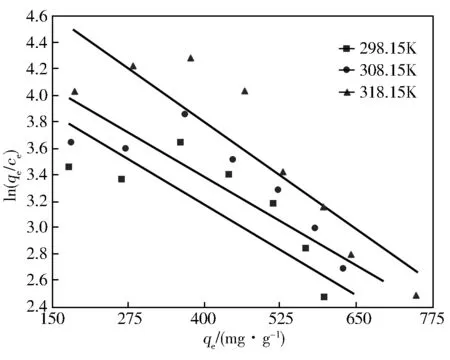
如图1和表2可得,PDA@SeP/Fe3O4复合材料更符合Langmuir模型,相关系数在0.989 3~0.995 3之间,说明Langmuir模型能更好的描述不同温度下该复合材料对于MB染料的吸附性能,这一吸附是单分子层的化学吸附。一般而言,发生化学吸附要吸收热量,因此随着温度的升高,最大吸附容量和平衡常数均增大。根据表2,0 表2 不同温度下吸附等温线参数 2.3.2 吸附热力学 吸附过程的不同热力学参数反应过程的各种基本性质,包括自发性,随机性、吸热性或放热性等,主要参数包括ΔG、ΔH和ΔS,分别通过式(7)和式(8)计算。 ΔG=-RTlnKc (7) (8) 式中:R为阿伏伽德罗常数(8.314 J·mol-1·K-1);T为开尔文温度(K);Kc,平衡常数。Kc值可以根据ln(qe/ce)对qe的线性斜率及截距来计算,结果如图8所示。每个温度对应有其热力学平衡常数K,再根据式(7),以lnK对1/T作图进行线性拟合(图9),可以计算ΔH和ΔS。最后根据公式(6),可计算出不同温度下的热力学参数ΔG。所有结果列于表3。 图8 不同温度下常数K拟合曲线 图9 lnK对1/T的线性拟合 ΔG<0,说明该吸附是自发性过程,不需要外界提供能量,且温度升高反应吉布斯函数△G随之减小,说明温度越高吸附过程进行得更加容易;除此之外,ΔH=7.033 kJ/mol>0,说明该反应是个吸热反应,温度越高吸附容量越大;ΔS=35.514 J/(mol·K)>0,说明整个吸附过程是个混乱度增大的熵增过程,自由度增大[12]。 表3 不同温度下的热力学参数 2.3.3 吸附动力学 从吸附动力学方面来讲,吸附过程可分为三个阶段:颗粒外扩散阶段、内扩散阶段和表面吸附阶段,一般来说,吸附过程总速率由最慢反应速率的一步决定,据经验可知通常是由外扩散和内扩散的过程速率决定。目前,对吸附动力学的研究有很多种模型,本次实验采用准一级、准二级和颗粒内扩散模型进行分析,其表达式如下[14]。 准一级动力学: ln(qe-qt)=lnqe-k1t (9) 准二级动力学 (10) 内扩散模型 qt=kpt1/2+c (11) 式中:qt为MB在任何时间的吸附容量,mg/g;k1为准一级速率常数,min-1;k2为准二级速率常数,g/(mg·min);kp为内扩散速率常数,min-1。 图10 准一级反应动力学拟合曲线 采用动力学准一阶、准二阶模型和内扩散模型对数据进行计算拟合。式(9)中,k1和qe可以通过ln(qe-qt)对t进行线性拟合后图的斜率和截距来计算,具体结果如图10所示。 在进行初步吸附情况模拟之后,采用动力学准二级方程来对过程进一步分析,根据式(10),k2和qe可以利用t/qt对t的线性拟合关系来计算,结果如图11所示,总结情况如表4。 图11 准二级反应动力学拟合曲线 比较两种拟合参数,可知不同浓度下PDA@SeP/Fe3O4复合材料的吸附情况更加符合准二级模型,相关系数R2都在0.922 1~0.999 6之间;并且该模型计算所得理论吸附量和测得的实际吸附量是最为接近的,这说明准二级动力学模型更适合描述PDA@SeP/Fe3O4材料的吸附情况,此时准二级假定的步骤是限速步,即吸附过程由化学吸附控制。 内扩散过程,利用该模型对数据进行拟合计算,具体如式(11),k和c可以利用qt对t1/2的线性拟合关系来计算,结果如图12所示,总结情况如表5。 图12 内扩散拟合曲线 表4 准一级动力学方程和准二级动力学方程拟合参数 表5 不同浓度下内扩散模型相关参数 可见,内扩散吸附过程可分为两部分,第一部分是前30 min,此时吸附速率很快增大,且相关系数R2>0.98,用颗粒内扩散模型可以很好的描述;相比之下,30 min之后的吸附速率较为缓慢,虽然qe也在增加,但明显可以看出吸附进度逐渐趋向平衡,吸附速率减小。另外由图12可以看出内扩散的拟合关系并不是一条过原点的直线,可见在复合PDA@SeP/Fe3O4材料对MB的吸附过程中并不是单纯受内扩散控制,还有外扩散的影响;另外,常数C代表边界层厚度,特别是第二阶段C的数值较大,也对吸附过程有一定影响。所以综上所述,改性海泡石对MB的吸附是不同步骤协同控制的反应。 a.通过对海泡石进行多巴胺改性和磁改性,制得了新型吸附剂PDA@SeP/Fe3O4复合材料,该法操作简单,污染小。PDA@SeP/Fe3O4复合材料在pH=10、45 ℃时吸附性能可达到749.14 mg/g;循环使用5次后,复合材料对亚甲基蓝的去除率仍在50%以上。 b.PDA@SeP/Fe3O4复合材料对MB的吸附是一个吸热过程,温度越高效果越好,且拟合情况更符合Langmuir模型,说明这一吸附过程是化学吸附。另外,整个PDA@SeP/Fe3O4复合材料对MB的吸附过程是动态的,但大体趋势是随着时间推移吸附容量增加;并且模拟结果更符合准二级方程,说明化学吸附占主要作用,根据内扩散模型可知,吸附情况并不是内扩散占主体地位,而是多种吸附共同作用的结果,具体情况还需要做进一步的探究。







3 结 论

