用KV-CBCT对食管癌不同固定体位动态调强分次间摆位误差的研究
徐晓捷,张瑞英,雷亚楠,侯 鹏,李敬霞
食管癌是我国常见的上消化道恶性肿瘤之一,放射治疗是食管癌主要的治疗手段,而调强放射治疗是目前主流的放疗技术。在放射治疗过程中患者的体位重复性十分重要,用锥形束CT可以更好地保证放疗体位的准确性[1-2]。本研究通过对本院行锥形束CT(Cone Beam Computed Tomography, CBCT)位置验证的食管癌患者进行研究,得到分次间的摆位数据,分析不同体位固定下的摆位误差,以指导临床靶区(clinical target volume, CTV)到计划靶区(planning target volume, PTV)的外扩距离。
1 材料和方法
1.1 一般资料来自2019年5月至2020年1月在本院行动态调强的胸段食管癌患者27例,其中体膜固定21例,头颈肩膜固定6例;年龄46~85岁(中位年龄70岁),男15例,女12例。
1.2 设备Philips大孔径16排CT模拟机,瑞典医科达Infinity加速器,计划系统Monaco 5.11,深圳腾飞宇科技热塑膜,头颈肩膜规格605 mm×485 mm×2.4 mm,体膜规格560 mm×460 mm×2.4 mm。
1.3 定位及计划设计患者均采用平静呼吸状态下仰卧位,体膜组(A组)双臂上举双手交叉置于头顶,头颈肩组(B组)合适规格的聚氨酯头枕双臂平放置于体侧,均采用热缩膜固定,配合碳纤维固定架和体位参考金标固定。采用Philips16排大孔径CT扫描,层厚均为0.5 cm。定位扫描的图像传到Pinnacle计划系统。主管医生在CT图像上勾画靶区GTV、CTV,物理师将画好靶区的CT图像传至Monaco计划系统,在Monaco TPS上按照医生的处方要求制作多个放射治疗计划。
1.4 治疗计划实施将审核通过的最优治疗计划传至加速器Mosaiq系统中执行。首次治疗按照患者体膜上的参考金标及患者体表线进行摆位,前3次及每周3次对患者行CBCT扫描,将得到的图像与定位重建得到的DRR图像进行配准。使用自动配准和人工微调相结合,直至结果满意,记录分次间的摆位误差。
1.5 统计方法使用SPSS 23软件进行独立样本t检验,P<0.05为差异具有统计学意义。
2 结果
2.1 摆位误差分析摆位误差频数分析:27例患者总共行CBCT扫描405次,平均每位患者扫描15次,得出平移误差频数数据,可见y轴及患者头脚方向>10 mm者高达8.4%。见表1。
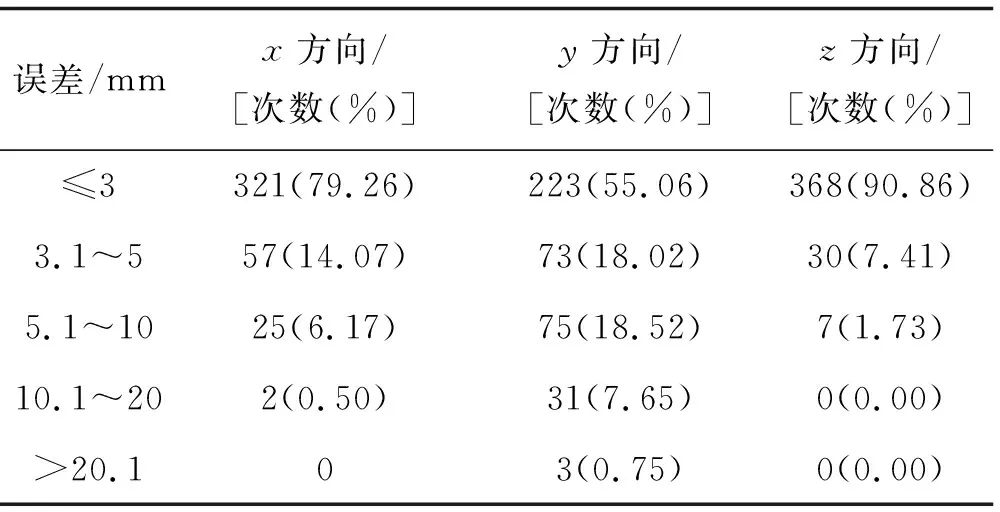
表1 27例405组摆位误差数据频数分析(n=405)
2.2 两组摆位绝对误差比较CBCT数据A组共有315人次,B组共有90人次,A组在x轴和z轴上绝对误差小于B组,在y轴上大于B组,见表2。A组和B组的系统误差和随机误差见表3-4。
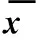
表2 A组和B组三维方向的绝对摆位误差比较(±s) mm

表3 A组和B组系统误差Σ mm

表4 A组和B组随机误差δ mm
2.3 靶区外放边界大小利用Van Herk等[3]提出的由CTV到PTV的外放公式M=2.5Σ+0.7δ(其中Σ表示系统误差,δ表示随机误差)计算A组和B组单纯考虑摆位误差要外放的距离。见表5。

表5 两种体位固定方式在位方向CTV到PTV的外放距离 mm
3 讨论
我国放疗行业已经进入三精治疗时代,即精确定位、精确设计和精确治疗[4]。图像引导的放射治疗(image guided radiation therapy, IGRT)是目前较精准的放射治疗技术,能在保证靶区照射剂量的前提下降低周围正常组织的放射损伤[5]。在多个研究和《肿瘤放射治疗学》一书中均指出患者体位固定方式是影响体位三维精度的重要因素之一[6-8]。与头颈部肿瘤相比,胸腹部的摆位误差相对较大[9]。KV-CBCT能够较清楚地显示软组织等结构,以及肿瘤和危及器官体积变化,是一种较精确的位置验证技术。Huddy等[10]的研究结果表明,CBCT测量摆位误差较电子射野影像装置(electronic protal imaging device, EPID)精确。食管癌调强放射治疗在治疗计划上有靶区内剂量分布均匀、靶区外剂量跌落相对较快的优势,这样的剂量分布特点对摆位精度的要求更高。摆位误差可能导致靶区剂量不够,而周边的危及器官剂量变大或者超标,这将严重影响患者的生存时间和生存质量,因此要尽量减小患者的摆位误差,提高治疗精度[11]。对食管癌摆位误差相关因素进行研究,对提高摆位精度,降低摆位误差都有很好的临床意义[12-14]。
本研究探讨了食管癌不同固定体位的绝对摆位误差以及CTV-PTV的靶区外扩距离的影响。本研究结果显示A组的绝对摆位误差x、y、z轴分别为(1.911±1.641)、(4.386±4.206)、(1.342±1.072) mm,B组分别为(2.738±2.229)、(2.728±2.743)、(1.977±1.348) mm,且3个轴上均P<0.05,差异有统计学意义。
A组固定体位双臂上举双手交叉放于头顶可减少x轴和z轴的绝对摆位误差,这是因为双手上举,胸廓能较舒展地展现一个平滑的曲面,用体膜固定,体膜制作时又相对较紧,这样对整个胸部有更好的固定作用,减小了患者左右方向和前后方向的摆位误差。在y轴上头颈肩膜固定可减少患者上下方向的绝对摆位误差,因为头颈肩膜是从患者头部开始固定,头脚方向头部固定的准确性相对胸部更精确,头颈肩膜用乳胶枕固定了患者的颈部曲度,这样头脚方向固定得更准确,所以头颈肩膜固定的体位在y轴上下方向的绝对摆位误差较小。体膜固定时上界一般在下颌下缘,患者上下的边界依据是患者体表上的标记线,由于患者体表皮肤活动度大,导致上下边界固定有误差。头颈肩固定患者左右位置活动度较大,且头颈肩膜对上胸廓的前后固定度较小,导致头颈肩膜固定的左右和前后方向绝对误差较大。这一结果与惠周光等[15]的研究结果一致,头颈肩膜在减少上下方向摆位误差有优势,体膜在减少左右方向和前后方向摆位误差有优势。
王丹等[16]对中上段食管癌调强放疗进行研究,结果表明在左右、头脚以及前后3个方向的摆位误差分别是(2.02±1.74)、(2.02±1.93)、(2.03±1.89) mm,上段食管癌由CTV到PTV的外放距离为左右4.7 mm、头脚8.5 mm、前后5.6 mm;中段食管癌为左右5.0 mm、头脚11.0 mm、前后6.2 mm。高超等[17]对42例食管癌行三维适形治疗的摆位误差进行研究,结果表明在左右、前后、头脚方向摆位系统误差分别为-2.31、-0.55、-0.16 mm,随机误差分别为4.42、4.35、4.48 mm。摆位误差使食管癌患者GTV 95%体积接受的剂量(D95)与原治疗计划相比降低了32 cGy,CTVD95降低了88 cGy。可见患者在治疗中的摆位误差对靶区剂量的影响明显。因此,为了保证食管癌患者的精确治疗,应尽量保证患者体位有一个很好的重复性和准确性[18-19]。
本研究表明,在x、y、z轴上A组和B组的系统误差分别为0.346、-1.54。-0.616、-1.334;-0.685、-0.748 mm,A组和B组的随机误差分别为2.497、3.186,6.050、3.639,1.576、2.281 mm。系统误差是相对误差的平均值,反映了所有误差的偏向性。本研究显示,在本院Infinity加速器上治疗的食管癌病人,y轴、z轴上误差均偏向下和后方向。A组和B组在患者头脚方向和前后方向均是负值,即分次间的摆位误差更易偏向脚方向和后方向。本研究结果得出A组CTV到PTV的外扩距离x、y、z轴分别为2.613、5.775、2.814 mm,B组CTV到PTV的外扩距离x、y、z轴分别为6.080、5.882、3.467 mm。可见在左右方向和前后方向A组的外扩距离均小于B组,在上下方向B组的外扩距离小于A组,且用单因素方差分析3个轴向的P值均<0.05,有统计学意义,说明体膜固定在x轴和z轴上有明显优势。本研究结果可为本院食管癌患者在放射治疗体位固定方面提供临床参考。建议在本院Infinity加速器上做治疗的、病变在胸中部和胸下部的患者选择体膜固定;而头颈肩膜固定在z轴上有明显优势,建议胸上段的患者选择头颈肩膜固定。
本研究采集分析本科室现有的常规治疗的数据,并非随机分组,两组的样本量不平均,分组中存在偏倚。在实际治疗过程中,不可能对每位患者行自身配对研究,这也使得研究结果有一定的偏差。B组的数据量较A组少,这可能对研究结果存在一定的影响,但B组有90人次的样本量有统计学意义。
食管癌由临床靶区CTV外放到计划靶区PTV时,既要考虑呼吸运动引起靶区运动,又要考虑放射治疗时分次间摆位误差,因此靶区的体积就会增大。随着靶区体积的增大,正常组织肺和脊髓的受量也会相应升高。每个单位均应根据实际的测量数据测算出本单位具体的摆位误差和系统误差。本研究表明,双臂上举体膜固定和双臂放于两侧两种体位固定方式,对摆位误差的影响各有优劣,且误差大小均在可控的范围内,均具有较好的可重复性。对于胸上段食管等肺组织较少的病变部位建议选择头颈肩膜,对于胸中下段的病变部位涉及到肺组织建议选择体膜固定。在临床实践中,可根据患者的具体情况选择合适的体位固定方式。本研究结果可为不同的体位固定三维方向上CTV到PTV的外扩距离提供临床参考依据,本院患者选择头颈肩膜固定的患者CTV到PTV的外扩距离x、y、z轴分别为6.080、5.882、3.467 mm,选择体膜固定的患者CTV到PTV的外扩距离x、y、z轴分别为2.613、5.775、2.814 mm。个性化的外扩距离既可以保证靶区有很高的剂量分布,又能减少正常组织受照剂量,对临床靶区外扩距离有一定的参考意义。

