基于碳酸酯电解液的锂金属负极界面调控
冉 琴,汪靖伦,唐安平
(1.湖南科技大学 理论有机化学与功能分子教育部重点实验室,湖南 湘潭 411201;2.湖南科技大学 化学化工学院,湖南 湘潭 411201)
0 引言
随着锂离子电池在便携式电子设备和电动汽车中的深入应用,迫切需要进一步提高其能量密度[1]。锂金属负极由于具有较高的理论比容量(3860 mAh·g-1)和较低的电化学电位(-3.04 V vs标准氢电极)被认为是下一代储能系统的“圣杯”[2-4]。以锂金属为负极,匹配转换型正极(如S或O2)构成的Li/S和Li/O2电池体系能量密度分别可高达650和950 Wh·Kg-1,匹配插层型高电压过渡金属氧化物正极构成的电池体系能量密度可达440 Wh·kg-1[5]。其中,最新报道的Li/NCM523软包电池能量密度可达340 Wh·Kg-1[6],该电池体系也被认为是实现高能量密度锂金属电池应用的可行途径。
然而,锂金属负极却存在锂枝晶的不定型生长[7]、与电解液的持续反应导致电解液消耗和库伦效率低[8]、体积膨胀导致固态电解质界面(SEI)膜断裂[9]等方面的缺陷,从而导致锂金属电池循环寿命减短和安全问题,使锂金属电池的实际应用面临巨大挑战。近年来,各种策略被报道来提高锂金属负极的性能,如:(1) 设计合成新型电解液和功能添加剂[10,11];(2) 构建人工SEI膜(包括无机SEI膜[12]、有机SEI膜[13]和复合SEI膜[14]);(3) 开发三维锂宿主结构[15,16]和复合电极[17,18];(4) 制备固态电解质[19,20]等。构建人工SEI膜有利于缓解电解液与锂负极的副反应,设计三维锂宿主结构和复合电极在一定程度上可有效抑制锂负极的体积膨胀,但构建人工SEI膜和设计三维锂宿主结构工艺复杂,不利于大规模生产;固态电解质虽然能较好抑制枝晶的形成,但其离子电导率较低[21]。相比较而言,新型电解液和功能添加剂的开发适用于现有电池体系,具有方便和经济的特点,同时有望抑制枝晶的生长、使电池展现出较好的循环性能。
一般而言,电解液体系可分为两类,醚类电解液和碳酸酯类电解液。醚类电解液对锂金属负极有较好的钝化作用,但是在常规锂盐浓度条件下却不能应用于高电压的电池体系;碳酸酯类电解液具有较好的锂盐溶解性、高离子电导率、耐氧化分解性等优点,但其分解产物不能在锂金属表面形成稳定致密的SEI膜。通过电解液和功能添加剂的开发实现锂金属负极界面调控逐渐成为研究热点,界面调控对构建更加坚固、均匀的SEI膜至关重要,而良好的SEI膜可显著增强电池寿命和提高循环效率。采用各种方法和手段构建以下五种界面膜可显著提高锂金属电池的性能:(1) 形成有机/无机复合的SEI膜;其中“硬”无机结构能抑制枝晶的生长,“软”有机结构能提高SEI膜的弹性和坚固性[22,23];(2) 形成含LiF的SEI膜;含LiF的界面不但可有效抑制电解液分解,还能增加SEI膜的强度(剪切模量55.1 GPa)[24,25];(3) 形成含Li3N的SEI膜;Li3N不仅对强还原性的锂金属热力学稳定,同时还具有较好的锂离子传导能力(6 mS cm-1)[26];(4) 形成以无机成分为主的盐-阴离子衍生SEI膜,可有效减少电解液与锂金属的副反应[27];(5) 通过静电屏蔽作用形成锂均匀沉积界面[28-30]。因此,为实现锂金属负极和高电压钴酸锂(LiCoO2)/镍钴锰(LiNixCoyMn1-x-yO2)三元等正极材料构成的高能量密度锂金属电池体系,基于碳酸酯电解液的界面调控显得尤为重要。本文从新型电解液溶剂体系、功能添加剂分子角度综述了其对碳酸酯电解液的锂金属负极界面调控,具体从盐类、功能添加剂、共溶剂体系三个方面介绍其在碳酸酯电解液中的界面调控及对电池性能的影响。最后,根据电解液调控的研究现状,对锂金属电池在碳酸酯电解液中的发展趋势进行了展望。
1 盐类添加剂
1.1 硝酸盐类添加剂
硝酸锂(LiNO3)是锂金属电池中一种“神奇”电解液添加剂,LiNO3的添加有助于形成含快速锂传导性Li3N的SEI膜,从而提高锂金属负极的循环稳定性。但是,LiNO3在碳酸酯电解液中溶解性十分有限,如在1M LiPF6-碳酸乙烯酯(EC)/碳酸二乙酯(DEC)基电解液中LiNO3的溶解度仅为800 ppm(相当于0.012 M)[31],因此,增加LiNO3在碳酸酯电解液中溶解性成为了研究的热点。近年,各种策略被报道用来提高LiNO3在碳酸酯电解液中的含量,其中包括开发助溶剂、共溶剂、吸附缓释等方法,表1中总结了利用上述各种方法在碳酸酯电解液中增加硝酸盐含量后的锂金属电池性能。

表1 硝酸盐添加剂在锂金属电池中的性能


图1 (a)Li/LFP和(b)Li/NCA电池在有/无LiNO3电解液中的循环性能[32];在无(c,d)/有(e,f)Sn(OTf)2和5 wt% LiNO3电解液中,Li沉积形态的俯视图和横截面的SEM图像[33]



图2 (a) EC/DEC和(b) FEC/LiNO3电解液在1.0 mA·cm-2用原位光学显微镜观察的锂沉积过程[34];(c) 锂在铜工作电极上有/无LiNO3电解液的沉积形貌[35]
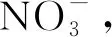
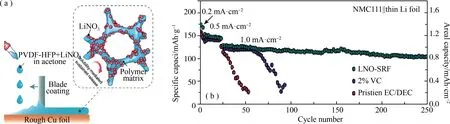
图3 (a) LNO-SRF的制备和工作原理;(b) Li/NMC111电池在0.5 M LiPF6-EC/DEC(pristine EC/DEC)、0.5 M LiPF6-EC/DEC-2%VC或硝酸盐(LNO-SRF)作为添加剂的电解液的循环性能[31]

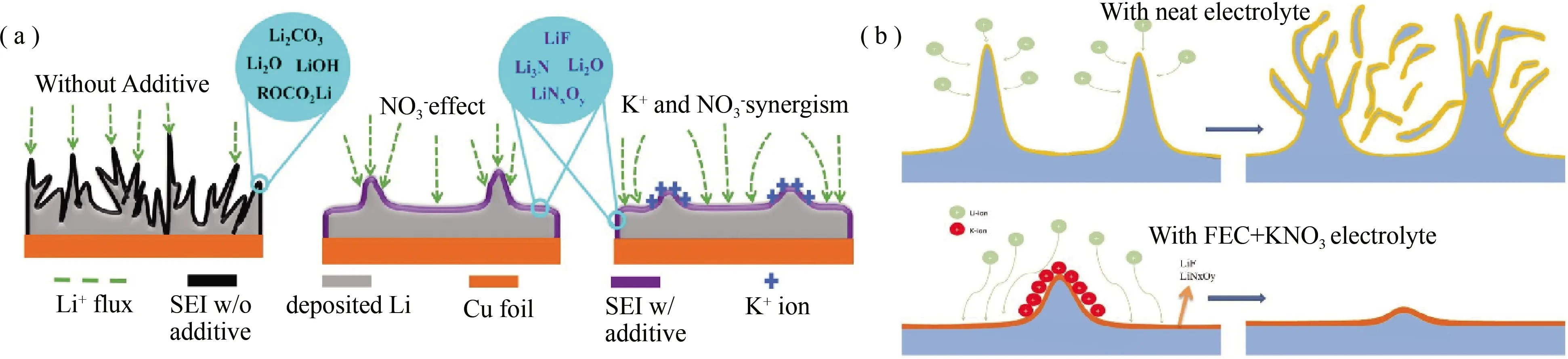
图4(a) 空白电解液和KNO3电解液中锂沉积过程[39];(b) 空白电解液和FEC+KNO3电解液中锂沉积过程[40]
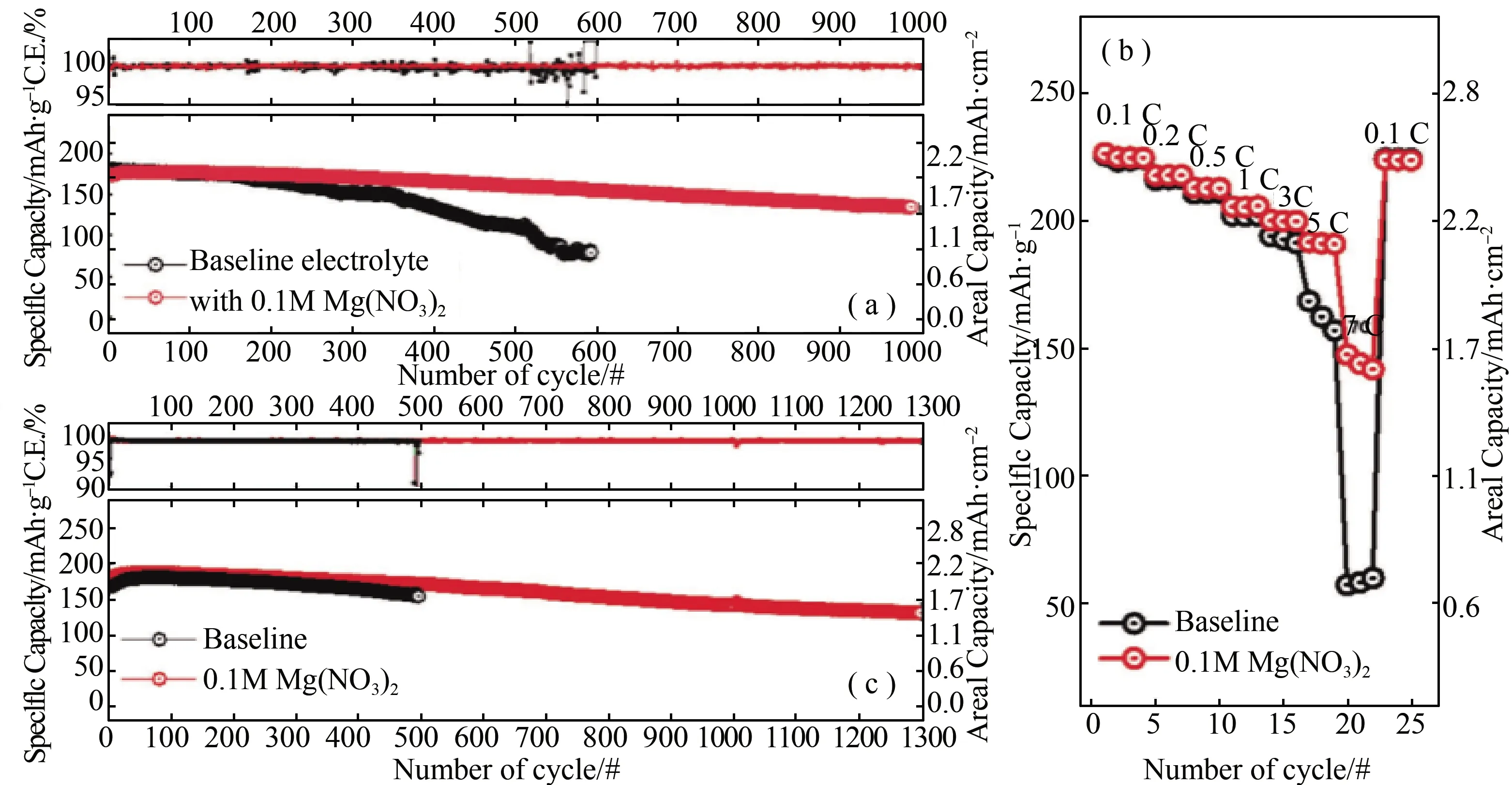
图5 Li/NCMA7扣式电池在基础电解液和0.1 M Mg(NO3)2电解液(a) 循环测试;(b) 不同充放电倍率的电化学性能; (c) Li/NCMA37袋式电池在基础电解液和0.1 M Mg(NO3)2电解液中循环测试[41]
1.2 含氟锂盐类添加剂
含氟锂盐类添加剂大多是可形成含LiF的成膜添加剂,它具有比电解液各组分更低的最低未占分子轨道(LUMO)能级,在充放电过程中能够优先还原参与成膜,从而形成稳定的SEI膜保护锂金属负极和抑制电解液的分解。图6是一些常见的含氟锂盐类添加剂。

图6 含氟锂盐添加剂结构式
Li等[42]利用热稳定的锂盐(LiTFSI,LiDFOB)和高沸点/闪点的有机碳酸盐溶剂(EC,PC)设计了一种新型耐高温电解液。为防止铝集流体腐蚀,还加入了少量的LiPF6。结果表明,新型电解液具有优异的高温性能,通过盐和溶剂的协同作用有效地抑制了锂枝晶的形成。图7(a)中,与空白电解液相比,锂负极在0.8 M LiTFSI-0.2 M LiDFOB-0.01 M LiPF6-EC∶PC(1∶1,by vol.)电解液中浸泡48 h后AFM图像锂表面仅有微小的凸起,证明其形成的SEI更加均匀。利用上述电解液,Li/LiCoO2电池在充放电倍率1 C、测试电压3.0-4.2 V、测试温度80 ℃的条件下,100周循环后容量保持率从4%提升为90%;其在80 ℃高温下的优异性能,克服了传统锂离子电池的工作温度上限(55-60 ℃),有效降低了热失控的风险。
Xu等[43]在0.6 M LiTFSI-0.4 M LiBOB-EC∶EMC(4∶6,by wt.)基础电解液中加入0.05 M LiPF6添加剂,LiPF6用作添加剂不仅在稳定铝集流体方面起着关键作用,而且还诱导产生了一种富含聚碳酸酯成分的坚固导电SEI膜,该SEI膜能有效地将死锂与块状锂金属负极结合起来,从而增强界面稳定性。Li/LiNi0.4Mn0.4Co0.2O2电池在电压2.7-4.3 V、充放电倍率1 C、温度为30 ℃的测试条件下,500周循环后容量保持率为97.1%;在温度为60 ℃的测试条件下,400周循环后容量保持率为90%。而在无0.05 M LiPF6添加剂的电解液中,Li/LiNi0.4Mn0.4Co0.2O2电池在温度为30 ℃的测试条件下,450周循环后容量保持率为74.5%;当温度为60 ℃时,电池在213周循环后终止稳定循环(图7(b)所示)。
Xu等[44]在基础电解液1 M LiPF6-EC∶DEC(1∶1,by wt.)中加入0.15 M 二氟磷酸锂(LiDFP),LiDFP作为添加剂时能够优先还原,在锂金属负极上形成一层稳定的富含LiF和磷酸盐的SEI膜,抑制锂枝晶生长。Li/Li电池在含有0.15 M LiDFP电解液中稳定循环寿命从90 h提升到200 h;Li/Cu电池的平均效率也从84.6%提高到95.2%。此外,含LiDFP添加剂的电解液为提高Li/NCM111电池循环稳定性也有显著效果。

图7 (a) Li负极在不同电解液中浸泡48 h后的AFM图像[42];(b) Li/NMC电池在不同碳酸盐电解质的循环性能,温度30 ℃[43]
Zhao等[45]通过在传统电解液中加入二氟草酸硼酸锂(LiDFOB)和1,1,2,2-四氟乙基-2,2,3,3-四氟丙基醚(HFE)双功能组分,能显著提高电池性能。其中,HFE能提高LiCoO2正极材料的性能;LiDFOB作为成膜添加剂,可以在正极和负极形成稳定的界面。在1.2 M LiPF6-0.15 M LiDFOB-FEC∶DMC∶HFE(1∶1∶1,by vol.)电解液中,Li/LiCoO2电池在测试电压2.75-4.50 V条件下,300周循环后容量保持率可高达84%;而对照电解液在50周循环后的容量保持率低于80%。
1.3 高浓度锂盐
高浓度锂盐电解液通常是指锂盐的浓度超过2 M的电解液体系[46]。与溶剂衍生的SEI膜不同,高浓度锂盐形成的是盐-阴离子衍生的SEI膜由大量的无机成分组成,使锂负极具有高导电性和致密性,在高浓度锂盐的电解液中可以有效地减少电解液溶剂与锂金属负极之间的副反应[47]。另外,在充电过程中,高浓度锂盐提供了更多的锂供应,从而延长了电位跃迁的时间,有利于锂均匀沉积。然而,高浓度锂盐降低了电荷传输动力学,增加了电解液的粘度和成本,阻碍了实际应用。

图8 (a) Cu/LFP电池在1 M和5.5 M LiFSI-DEC/EC电解质的循环稳定性[48];(b) 三电极在1 M、3 M、7 M LiFSI电解液的线性伏安扫描测试[49]
Xie等[48]采用5.5 M LiFSI-DMC/EC或5.5 M LiFSI-DEC/EC电解液(代替1 M LiPF6- DEC/EC电解液)可有效地提高锂金属阳极的库仑效率和速率性能。在5.5 M LiFSI-DMC/EC电解液中,Li/Cu电池在电流密度为0.4 mA·cm-2和6 mA·cm-2时的库仑效率分别为97.0%和94.5%,Cu/LiFePO4电池的容量保持率明显高于1 M LiFSI-DMC/EC(图8(a)所示)。这种性能的提高是由于在高浓度LiFSI电解液中形成了由紧密离子对(CIPs)和离子聚集体(AGGs)组成的三维离子网络,有效地减少了自由溶剂分子的数量,形成含无机组分较多的SEI膜可有效抑制锂枝晶的生长。Li等[49]用三电极测试了高浓度全氟电解液(7 M LiFSI-FEC)的电化学窗口,证明高浓度盐对扩大电化学窗口和抑制铝腐蚀具有明显的效果,在7 M浓度下稳定窗口大于5 V(图8(b))。在5V的Li/LiNi0.5Mn1.5O4锂金属电池中(具有过量锂负极和接近工业要求的高质量负载正极),高浓度全氟电解液不仅与正极有良好的相容性,而且还可使锂金属负极具有更高的可逆性,其能量密度比石墨基LiNi0.5Mn1.5O4电池高30%,比4 V商用石墨基锂离子电池高50%。
1.4 其它盐类添加剂
除了传统的锂盐添加剂,近年来非锂盐添加剂也广泛被报道以提高锂金属电池的性能,如MgCl2[50]、NaPF6[51]等。由于锂表面成核中心和电场不均匀,在电荷初始阶段不可避免地形成金属尖端,非锂盐添加剂大多可以通过自愈性静电屏蔽来影响锂沉积,形成稳定的SEI膜使锂离子均匀沉积。
MgCl2能通过原位反应对锂金属表面进行改性,MgCl2与金属锂反应形成的无机LiCl和金属Mg在界面上共存可有效降低锂表面副反应和界面电阻,促进锂离子扩散和锂均匀沉积(图9(a))。Li等[50]在1 M LiPF6-EC∶DMC∶EMC(1∶1∶1,by vol.)基础电解液加入10 mM MgCl2添加剂,Li/Li电池在在电流密度1 mA·cm-2和容量1 mAh·cm-2时,300 h后的电压为200 mV;而无添加剂的Li/Li电池在200 h后的电压增加到400 mV。此外,Li/Li4T5O12全电池的循环性能也有明显的改善。Cheng等[51]通过在1 M LiPF6-EC/DEC基础电解液中加入0.02 M NaPF6添加剂来稳定锂负极。图9(b)所示,NaPF6的加入使Li+和Na+都聚集在尖端上,Na+通过自愈性静电屏蔽有助于形成光滑致密的无枝晶锂镀层,这种保护作用是通过Na+的缓慢还原来实现的。在含有0.02 M NaPF6电解液中,Li/Li电池在电流密度0.5 mA·cm-2和容量2 mAh·cm-2的条件下,稳定循环寿命从700 h提升到1000 h。Hwang等[52]在1 M LiPF6-EC∶DEC(1∶1,by vol.)基础电解液中加入2 wt% KPF6和2 vol% 三(三甲基硅烷)磷酸酯(TMSP),利用TMSP和KPF6的协同作用来调节锂的沉积和减少电解质的分解。其中,TMSP可在正极表面优先氧化形成保护膜和稳定的界面层,而KPF6通过自愈静电屏蔽机制可阻止枝晶生长。通过使用该电解液体系,Cu/LiNi1/3Co1/3Mn1/3O2电池在20次循环后容量保持率从13%提高到48%,库伦效率从89.1%提高到95.2%。

图9 (a) MgCl2添加剂电解液中SEI形成过程和锂沉积行为示意图[50];(b) 锂枝晶形成、生长和抑制的示意图[51]
2 功能分子添加剂
2.1 含氟类功能分子
氟原子具有较强的电负性,其碳氟键的键能比碳氢键强,所以用氟来取代碳酸酯上的氢原子,可以提高碳酸酯溶剂的热稳定性。氟取代会降低溶剂分子的最高占据分子轨道(HOMO)和LUMO能级,能提高溶剂的抗氧化能力和还原电位[53]。含氟溶剂类添加剂有助于在锂金属负极形成LiF含量较高的SEI膜,从而增加SEI膜的强度、抑制锂枝晶的形成[54,55]。表2中列出了部分含氟类添加剂在锂金属电池中的性能。

表2 含氟类添加剂对锂金属电池性能影响
相比于EC基电解液,锂金属电极在FEC基电解液和1,2-二氟代碳酸乙烯酯(DFEC)基电解液中可形成了富含LiF的SEI。Markevich等[56]比较了FEC基电解质溶液(1 M LiPF6-FEC:DMC(1:4,Merck))和EC基电解液(1 M LiPF6-EC:DMC(1:1,Merck))对Li/Li对称电池在大面积容量、大电流循环条件下的性能影响。实验结果表明,在FEC-基电解液中,Li/Li对称电池在电流密度2 mA·cm-2、容量3.3 mAh·cm-2的条件下可稳定循环1100周;而在EC-基电解液中,Li/Li对称电池在电流密度2 mA·cm-2、容量2.5 mAh·cm-2条件下只能稳定循环200周循环。在电流密度0.5 mA·cm-2、容量1 mAh·cm-2条件下,Li/Cu电池在FEC-基电解质溶液和EC-基电解液中平均库伦效率分别为98.5%和89%(图10(a))。Amine等[57]研究了DFEC参与形成的SEI对锂金属电池循环稳定性的影响。FEC和DFEC基电解液不仅能够形成SEI膜、促进锂的沉积/剥离,而且对NMC正极显示出较强的氧化稳定性。在充放电倍率C/3,测试电压3.0-4.4 V条件下,Li/NMC622电池在1.2 M LiPF6-EC:EMC(3:7,by vol.)、1.2 M LiPF6-FEC:EMC(3:7,by vol.)和 1.2 M LiPF6-DFEC:EMC(3:7,by vol.)电解液中100周循环后容量保持率分别为85.6%、83.3%和94.1%,库伦效率分别为98.35%、99.74%和99.91%;Li/NMC622电池在1.2 M LiPF6-FEC:EMC(3:7,by vol.)和 1.2 M LiPF6-DFEC:EMC(3:7,by vol.)电解液中400周循环后容量保持率为40%和83%(图10(b)所示)。Aurbach等[58]用1 M LiPF6-FEC:DFEC:DMC(1:1:8)作为电解液,可以克服Li/NCM811电池在FEC/DMC基电解液中容量急剧衰减的问题。含有DFEC和FEC的电解液对锂金属表面保护具有协同效应,锂负极SEI膜主要由FEC和DFEC还原产物组成,DFEC还原参与形成表面SEI膜来防止FEC快速消耗。FEC+DFEC的混合电解液代替基于FEC的混合电解液能够将Li/NCM811电池循环稳定性延长到360周。

图10 (a) Li/Cu电池在不同电解液中CE与循环圈数图[56];(b)Li/NMC622在不同电解液中的循环性能[57]
除了氟代碳酸酯,其它含氟类功能分子对锂金属的钝化也有很好的效果,其结构式如图11所示。Feng等[59]在1 M LiPF6-EC:DMC(3:7,by vol.)基础电解液中加入5 wt%(三氟乙氧基)五氟环三磷腈(TFPN),TFPN的加入有利于在锂金属负极表面形成富LiF的SEI膜,具有抑制锂枝晶的能力;此外,加入TFPN的电解液还具有不可燃烧性。在含有5 wt% TFPN电解液中,Li/NCM811电池在电流密度20 mA·g-1、测试电压2.7-4.2 V条件下,100周循环后的容量保持率由为64.1%提高到85.3%。Ma等[60]在1 M LiPF6-EC:DMC(1:2,by vol.)基础电解液中加入2% 硼酸三(2,2,2-三氟乙基)酯(TTFEB),可显著改善锂金属负极的性能。与空白电解液相比,TTFEB可优先在负极表面还原形成含LiF的SEI膜;此外,电解液中由TTFEB衍生的硼化合物可束缚电解液的阴离子和增强Li+迁移数,从而有效地抑制了锂枝晶的生长并使锂沉积均匀(图12(a))。在含有2% TTFEB电解液,Li/Cu电池在电流密度0.5 mA·cm-2条件下,100周循环后的效率从79%提升到91%;Li/Li电池在电流密度2 mA·cm-2条件下的稳定循环寿命从620 h提升到800 h;对Li/LiFePO4电池,使用TTFEB添加剂后同样可取得了良好的循环性能和倍率性能。Yang等[61]在1 M LiPF6-EC:EMC(1:3,by wt.)基础电解液中加入1%三(五氟苯基)硼烷(TPFPB),形成一种同时稳定锂金属负极和LiNi0.5Mn1.5O4正极的电解液体系。密度泛函理论(DFT)计算结果表明,TPFPB分子具有比EC/EMC分子更高的HOMO能级和更低的LUMO能级(图12(b)),从而可在锂电极和LiNi0.5Mn1.5O4电极上优先反应形成稳定的界面层,维持正极材料的结构和抑制锂枝晶的生长。在含有1% TPFPB电解液,Li/LiNi0.5Mn1.5O4电池在测试电压3.5-4.95 V、充放电倍率0.5 C条件下,500周循环后容量保持率由17%提高到90%,效率可达99%。

图11 含氟添加剂分子结构示意图
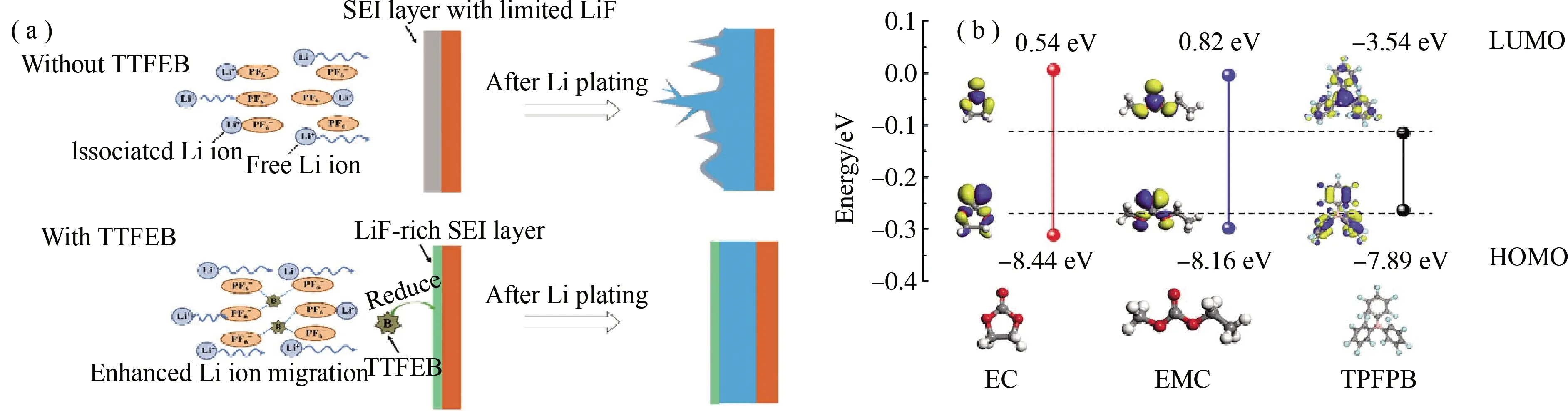
图12 (a) 锂金属负极在有/无TTFEB添加剂的结构变化和电解质性质的示意图[60];(b) EC、EMC和TPFPB分子的HOMO和LUMO能级[61]

图13 在(a)无;(b)有RbF添加剂时锂枝晶生长过程的示意图[62]
此外,无机氟化物如氟化铷(RbF)、氟化铟(InF3)不但可通过静电屏蔽效应调节锂沉积、抑制锂枝晶的生长,还可以形成富含LiF的界面SEI膜。Zhang等[62]在1 M LiPF6-EC:DMC(1:1,by vol.)基础电解液中加入0.05 M RbF,Li/Li电池在电流密度0.5 mA·cm-2、容量1 mAh·cm-2的条件下可稳定循环1000 h;Li/Cu电池在120次循环后库伦效率仍高达90%,而基础电解液的Li/Cu电池在87次循环后效率降至71.8%(图13(a),(b)所示)。Nazar等[63]在1 M LiPF6-EC:DMC(1:1,by vol.)电解液中加入60 mM InF3,可在锂表面原位形成由Li-In合金和LiF组成的稳定双相层。Li-In合金提供了有效的锂迁移通道,使锂沉积在保护层下;而绝缘的LiF相层阻止电子跨层传输,从而显著降低锂金属与电解液的反应。在含InF3的电解液中,Li/Li对称电池在电流密度1 mA·cm-2、容量1 mAh·cm-2条件下可稳定循环400周;Li/ Li4Ti5O12电池在测试电压1.0-2.5 V、充放电倍率5 C条件下,1000周循环后容量保持率可达67%。
2.2 有机功能分子
有机分子由于具有结构可调性,在电池中用作添加剂可参与SEI膜的形成,使SEI膜更好的离子传导性、均匀性和稳定性,以此来提高电池性能.常见的有机分子添加剂如图14所示。
含双键的碳酸酯类分子,如碳酸亚乙烯酯(VC)、乙烯基碳酸乙烯酯(VEC)能通过聚合反应参与成膜,有利于形成均匀且稳定的SEI膜。Wen等[64]在1 M LiPF6-EC:DMC(1:1,by vol.) 电解液中加入2 vol% VC和0.1 M LiNO3添加剂,可在锂表面形成杂化、稳定且有良好导电性的SEI。在含VC+LiNO3添加剂的电解液中,Li/Cu电池可以稳定循环且库伦效率接近100%(首次效率除外),而在空白电解液中的Li/Cu电池库伦效率在不断降低(图15(a)所示)。Zhao等[65]在1 M LiPF6-EC:DEC(1:1,by vol.)电解液中添加10% VEC,可以形成聚碳酸酯和LiF含量更高的SEI膜,形成的膜稳定、表面光滑且能有效抑制枝晶的生长,降低了锂与电解液的副反应(图15(b)所示)。在含10% VEC的电解液中,Li/Cu电池在循环容量1.0 mAh·cm-2、电流密度0.25 mA·cm-2时,100周循环后的库伦效率高达93.2%,空白电解液中Li/Cu电池在50周循环后效率低于80%。

图14 有机添加剂分子结构示意图
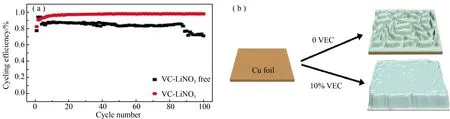
图15 (a) Li/Cu电池在有/无VC-LiNO3添加剂的循环效率图[64];(b) 有/无VEC添加剂在锂金属负极表面形成的SEI[65]
有机硅功能分子用作电解液有着广泛的研究报道[66]。Sun等[67]在1 M LiPF6-EMC:FEC(3:1,by vol.)基础电解液中加入0.1 M叠氮基三甲基硅烷(TSA),通过原位电化学反应,在锂金属表面形成含有富锂、SiOx和LixN(可能是Li3N)化合物的SEI膜。此外,TSA还能稳定负极表面,减少有害的溶剂分解。向电解液中添加TSA后,Li/Li电池在电流密度2 mA·cm-2、容量2 mAh·cm-2的条件下,稳定循环寿命由200 h提高到1200 h(图16(a)所示);Li/Li[Ni0.73Co0.10Mn0.15Al0.02]O2(FCG73)电池在2.7-4.3 V的充放电条件下也表现出优异的循环稳定性和快速充放电能力,300周循环后的容量保持率为82.2%;而空白电解液的Li/FCG73电池在270周循环后的库伦效率突然下降。以端基为甲氧基的液态聚二甲基硅氧烷(PDMS-OCH3)作为电解液添加剂也可以拟制锂枝晶的生长,PDMS-OCH3的分解有利于形成含LiF和Li-Si-O组分的杂化SEI膜,杂化SE膜I的刚性势垒和离子导体性有利于锂的均匀沉积,使锂沉积/剥离的成核和平台过电位同时降低。在1 M LiPF6-EC:DEC(1:1,by vol.)基础电解液中加入8 vol% PDMS-OCH3后[68],Li/Li电池在0.5 mA·cm-2、1.5 mAh·cm-2时的循环稳定性从510 h提高到1800 h,Li/Cu电池在电流密度1 mA·cm-2、容量1 mAh·cm-2条件下循环140周后的效率仍高达90%;无添加剂的Li/Cu电池在70周循环后效率小于60%。

图16 (a) Li/FCG73电池在有无TSA添加剂电解液中的循环性能[67];(b) CTAC加入对锂分解过程影响的示意图[69]
十六烷基三甲基氯化铵(CTAC)被用做一种促进憎锂排斥机制的添加剂,以抑制锂枝晶的生长来实现均匀的锂沉积。在沉积过程中,离子表面活性剂分子可通过静电吸引聚集在突起周围,形成非极性憎锂保护层,该保护层驱使锂离子沉积到相邻区域,从而产生无枝晶的均匀锂沉积(图16(b))。Lai等[69]在基础电解液1 M LiPF6-PC:EC:DEC(1:4:5,by vol.)加入1.2 mM CTAC,Li/Li电池在电流密度1 mA·cm-2、容量0.5 mAh·cm-2的条件下,能稳定循环300 h;Li/ LiNi0.5Co0.2Mn0.3O2电池在测试电压3.0-4.5 V、充放电倍率2 C条件下,300周循环后容量可达127.2 mAh·g-1。
2-(三苯基膦基亚烷基)琥珀酸酐(TPSA)可作为稳定锂负极表面电解液添加剂,TPSA能优先在锂负极表面分解形成稳定的SEI膜,有效地减少了电解液的分解。Wang等[70]在1 M LiPF6-EC:DMC:EMC(1:1:1,by vol.)基础电解液中添加3 wt% TPSA,Li/ LiCoO2电池在测试电压3.0-4.2 V、充放电倍率0.5 C条件下,100周循环后容量保持率可达85%,基础电解液在50周循环后容量急剧下降至0 mAh·g-1。
八苯基聚氧乙烯(OP-10)作为电解质添加剂,在锂负极表面形成稳定的复合层。该表面层不仅促进均匀的锂沉积,而且还促进了交联聚合物的坚固SEI膜形成,改善了Li+的传输并减少了电解质的消耗。Lai等[71]在在1 M LiPF6-PC:EC:DEC(1:4:5,by vol.)基础电解液中添加5 vol% OP-10,电流密度1 mA·cm-2、容量1 mAh·cm-2条件下,Li/Li电池能稳定循环由100 h提高到400 h;在4 mA·cm-2以下具有优异的倍率性能。Li/ LiFePO4电池在测试电压2.5-4.2 V、充放电倍率10 C条件下,1000周循环后显示出约67.1 mAh·g-1的高可逆容量,基础电解液1000周循环后容量为23.1 mAh·g-1。
Wang等[72]在1 M LiPF6-EC:DMC:EMC(1:1:1,by wt.)基础电解液中添加0.15 wt% 丹宁酸(TA),TA分子中的多羟基酚有助于LiPF6的水解反应并形成LiF,多羟基酚的锂盐能与DMC发生酯交换反应而形成交联聚合物,从而形成稳定且均匀的有机/无机复合SEI膜,能显著提高锂金属负极的电化学性能。在含有0.15% TA电解液,电流密度1 mA·cm-2、容量1 mAh·cm-2条件下,Li/Li电池能稳定循环由170 h提高到270 h且拥有较低的滞后电压(图17)。

图17 有/无TA添加剂的Li/Li对称电池(a)循环性能和(b,c)在不同循环后的滞后电压[72]
2.3 沉淀类添加剂
除了可溶性的添加剂之外,不可溶的Al2O3、纳米金刚石(ND)、SiO2等胶粒或纳米颗粒与锂盐之间存在路易斯酸碱作用,可调控胶粒或纳米颗粒的电荷和锂离子传输途径,从而实现锂金属的均匀沉积。Guo[73]等在1 M LiPF6-EC:DMC:DEC(1:1:1,by wt.)基础电解液中加入8 wt% AlCl3,利用AlCl3与电解液中微量水反应形成带正电的Al2O3胶体颗粒(PCCP),PCCP在突出的锂周围形成带正电的静电屏蔽层,诱导锂离子沉积到相邻区域实现均匀无枝晶的锂形态。含有添加剂的Li/Cu电池在电流密度0.5 mA·cm-2、容量2 mAh·cm-2时,150周循环后的库伦效率高达99%。Zhang等[74]通过在1 M LiPF6-EC:DEC(1:1)基础电解液中加入0.82 mg·mL-1ND,锂离子吸附在具有低扩散势垒的ND表面,通过与锂离子的共沉积和静电屏蔽效应实现均匀锂沉积(图18(a))。ND改性电解液可使Li/Li对称电池在2 mA·cm-2/1 mA·cm-2下稳定循环150 h/200 h;在电流密度0.5 mA·cm-2、容量0.25 mAh·cm-2条件下,Li/Cu电池的库仑效率由88%提升为96%;在含有ND电解液,Li/LFP电池在测试电压2.5-3.8 V,充放电倍率1 C条件下,130周循环后容量保持率由85.8%提高到95.1%。Kim等[75]在LiPF6-EC/EMC中加入SiO2纳米颗粒形成纳米粒子分散胶体电解液(NDCE),NDCE能够提高锂离子迁移数并调控成核生长模式和延长Sand's时间来实现较低枝晶的锂镀层。图18(b)所示,Li/NCM811电池在测试电压1.0-2.5 V、充电倍率0.2 C放电倍率0.5 C条件下,15 mg·mL-1SiO2电解液中100周循环后容量保持率可达85%;空白电解液44周循环后容量保持率为80%。

图18 (a) 锂离子在纳米金刚石上的共沉积、柱状锂层的形成和锂沉积/剥离[74];(b) Li/NCM电池在SiO2不同含量电解液中的循环性能[75]
3 共溶剂
如前章节所述,为提高LiNO3在电解液中的溶解性,醚类(乙二醇二甲醚[34])和酯类(γ-丁内酯[35]和磷酸三乙酯[36])共溶剂应用于碳酸酯类电解液体系中取得了不错的电池性能。此外,氟代醚类(HFE[45])共溶剂可提高碳酸酯电解液体系的抗氧化性能。
除此之外,亚硫酸乙烯酯(ES)用作共溶剂也能调控锂离子的溶剂化结构,乙酸甲酯(MA)作共溶剂应用于碳酸酯电解液体系可改善其离子传导速率和低温性能。Wang等[76]制备的1 M LiClO4-EC∶ES(1∶1,by vol.)电解液,Li/Li电池在电流密度1 mA·cm-2、容量2 mAh·cm-2条件下能稳定循环800 h;而在1 M LiClO4-EC∶DMC(1∶1,by vol.)电解液中Li/Li电池只能稳定循环400 h。这是因为在ES的作用下,含硫组分的SEI膜可实现电池的长循环寿命;而EC分子的存在同样可减少电极的副反应。在1 M LiClO4-EC∶ES(1∶1,by vol.)电解液中,Li/LFP电池在测试电压3.0-4.2 V、充放电倍率1 C条件下300周循环后库伦效率为99.9%;相同条件下,Li/LFP电池在1 M LiClO4/ES电解液中30周循环后库伦效率为91.5%(图19所示)。Yang等[77]制备了1 M LiPF6-EC∶FEC∶DMC∶MA(2∶1∶4∶3,by vol.)电解液,Li/Li电池在电流密度3 mA·cm-2、容量1 mAh·cm-2条件下具有显著的循环稳定性,甚至Li/Li电池在电流密度5 mA·cm-2时仍能以较低的过电位运行110 h。此外,由锂负极和LiNi0.8Co0.15Al0.05O2(NCA)正极组成的LMBs具有高容量(200 mAh·g-1)、良好的循环稳定性(300次)、和较好的倍率能力(10 C)和低自放电速率(8.5%);特别是Li/NCA电池在-35 ℃下的容量高达144 mAh·g-1,明显高于无MA电解液中的电池。

图19 Li/LiFePO4电池在1 M LiClO4-EC:ES和1 M LiClO4/ES电解液的循环性能[76]
4 结论与展望
本文基于碳酸酯电解液的配方体系,从锂盐、功能添加剂、共溶剂三方面阐述了可实现锂金属负极界面调控的各种策略和方法。其中,利用含氟的盐类或功能分子和硝酸盐类添加剂,形成含LiF、Li3N和LiNxOy的SEI保护膜对锂金属电池性能的提高有显著效果。此外,利用静电屏蔽效应或共沉淀添加剂也可以调整锂离子沉积和抑制枝晶生长,利用反应性有机分子或共溶剂参与成膜也是提高SEI膜性能的有效方法。然而,高库伦效率和无枝晶锂金属负极的研发,基于碳酸酯的电解液体系的界面调控策略还有以下三方面工作有待进一步开展:(1) 如何提高LiNO3在碳酸酯电解液中的溶解性、并复合其它功能组分形成稳定的SEI膜;(2) 从分子设计的角度入手开发新型功能添加剂和共溶剂调控界面SEI膜的结构和形貌;(3) 从溶剂化结构入手,结合实验研究和理论分析,认清SEI界面膜的形成机理是提高锂金属负极性能的关键。
此外,除了锂枝晶的问题外,面向实际应用的高能量密度锂金属电池还需要考虑的因素较多,如锂片的厚度、电解液的用量、循环过程中体积膨胀、电池系统的外加压力等。因此,从电解液设计的角度实现锂金属界面调控,结合锂三维主体结构和人工SEI膜可有效缓解锂金属循环过程中的锂枝晶问题和体积膨胀问题。此外,锂金属电池的性能不仅与电解液体系的组成有关,还与电解液的用量相关。目前对锂金属电池研究过程中的电解液一般都是大大过量,很少考虑电解液用量对电池性能影响。因此,优化电解液组成以形成更高效和稳定的SEI膜,对锂金属电池在贫电解液条件下保持良好循环性能有着至关重要的意义。

