新型冠状病毒核酸提取方法的性能评价及临床应用
吴永彬,万 颖,蒋红玲,张 晶,辛 杰
广西壮族自治区南溪山医院检验科,广西桂林 541002
新型冠状病毒(SARS-CoV-2)是一种具有包膜结构的正链单股RNA病毒,不仅可感染人类,还能感染其他哺乳类动物和鸟类,可引起呼吸道、肠道、肝脏和神经系统等病变[1]。目前,实时荧光反转录聚合酶链反应检测SARS-CoV-2核酸是筛查和诊断新型冠状病毒肺炎(COVID-19)的重要手段[2],通过对SARS-CoV-2序列中的开放阅读框(ORF)1ab 、核衣壳蛋白(N)及包膜蛋白(E)基因的特异性保守序列设计靶区域来实现标本核酸检测。然而,该方法自临床应用以来仍缺乏可靠的质量控制,已开展SARS-CoV-2核酸检测的实验室或机构大多采用自建体系进行检测,没有形成统一的技术标准。就试剂而言,各厂家推荐的标本前处理方法及核酸提取方法并不统一,试剂之间的差异可能会导致检测结果的不一致。当某项定量检测项目在正式用于标本检测前或检测系统有重大改变后,必须对检测系统的分析性能做出详细、充分的评价,确认检测系统符合临床要求[3]。本研究评价了3种不同的SARS-CoV-2核酸提取方法用于核酸定量检测时的分析性能及临床应用价值,以期为COVID-19的实验室检测和临床诊断提供参考。
1 资料与方法
1.1一般资料 选取SARS-CoV-2核酸检测阳性的COVID-19确诊病例17例,其中男8例,女9例;年龄24~79岁,中位年龄42岁;病程4~24 d;危重型4例,普通型13例。所有患者SARS-CoV-2核酸检测标本于2020年2月12—19日在本院感染性疾病病区收集,其中深咳痰液标本13份,大便标本4份。COVID-19诊断标准参考《新型冠状病毒感染的肺炎诊疗方案(试行第五版)》[4]。本研究经本院伦理审查委员会审核通过(批准文号2020NXSYYEC-003)。
1.2仪器与试剂 电热恒温水浴箱(型号:HH.W21.600S,上海跃进医疗器械有限公司),漩涡混合器(型号:XH-B,江苏康健医疗用品有限公司),全自动核酸提取系统(型号:Natch CS,湖南圣湘生物科技有限公司),荧光定量PCR扩增系统(型号:SLAN-96P,上海宏石医疗科技有限公司)。样本释放剂(批号:S1014,湖南圣湘生物科技有限公司,裂解法),核酸提取及纯化试剂(批号:SDK60102,江苏硕世科技股份有限公司,柱提法),核酸提取或纯化试剂(批号:S1002,湖南圣湘生物科技有限公司,磁珠法),核酸扩增试剂(批号:2020088,湖南圣湘生物科技有限公司,荧光PCR法)。
1.3方法
1.3.1SARS-CoV-2核酸检测 所有标本在检测前先进行56 ℃、30 min灭活,并混匀5~10 s后待检。使用3种SARS-CoV-2核酸提取方法(裂解法、柱提法、磁珠法),按操作说明书提取核酸,最后均提取20 μL SARS-CoV-2核酸液作为扩增模板。在荧光定量PCR扩增系统上选择FAM(ORF1ab)和ROX(N) 通道检测SARS-CoV-2核酸,选择HEX通道检测内标。设置50 ℃、热循环30 min进行反转录;在95 ℃下反应1 min使cDNA预变性;然后按照95 ℃、15 s,60 ℃、30 s循环45次。最后根据扩增信号得出Ct值,并根据核酸扩增试剂说明书判定检测结果。
1.3.2性能验证
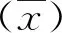

1.3.2.3最低检测限验证 选取低水平且双靶标(ORF1ab、N)Ct值接近的弱阳性标本8份,用阴性对照标本依次按1∶1的比例稀释为8个水平接近试剂盒定量检测下限的标本,分别用3种方法提取SARS-CoV-2核酸并检测,每份标本重复检测4次,连续检测10 d。参考EP7-A2[7],计算阳性检出率及最低检测限。
1.3.2.4临床应用评估 取17份COVID-19确诊病例标本,分别采用3种方法同时提取并检测SARS-CoV-2核酸,每个标本重复检测3次,计算3种核酸提取方法下检测结果的阳性符合率、靶标检出率,分析3种核酸提取方法两两之间检测结果的相关性。

2 结 果
2.1精密度验证结果 3种核酸提取方法下高、中、低水平标本检测结果的CVr和CVi均小于目标CV(5%),符合厂家声明的精密度标准,可满足临床需求。见表1。

表1 精密度验证结果
2.2正确度验证结果 3种核酸提取方法下检测3个水平标本的偏倚均小于允许偏倚,可接受,其中采用裂解法提取核酸时的偏倚较柱提法和磁珠法大,采用磁珠法提取核酸时3个水平标本的检测偏倚均最小。见表2。

表2 正确度验证结果
2.3最低检测限验证结果 3种核酸提取方法下8个水平标本的检出率见表3。Probit回归分析结果显示,模型拟合度均可接受,采用裂解法、柱提法、磁珠法提取核酸时的最低检测限(Ct值)分别是37.42、37.87、39.61,均符合厂家声明的最低检测限。

表3 3种核酸提取方法下的检出率比较[n(%)]
2.4方法学比较 在17份COVID-19确诊病例标本中,有15份标本在3种核酸提取方法下均检测为阳性,其中裂解法和柱提法、磁珠法和柱提法的阳性符合率均为94.11%,裂解法和磁珠法的阳性符合率为88.23%。3种核酸提取方法下的检测结果两两之间均呈良好的线性关系(P<0.05),其中,采用柱提法和磁珠法提取核酸时的检测结果相关性最好(r=0.905,P<0.001)。见图1。

注:A为柱提法与裂解法检测结果的相关性分析;B为磁珠法与裂解法检测结果的相关性分析;C为柱提法与磁珠法检测结果的相关性分析。
2.53种核酸提取方法下的靶标检出率比较 17例COVID-19确诊病例标本中,采用裂解法提取核酸时检出15例阳性,阳性率为88.2%,柱提法提取核酸时检出16例阳性,阳性率为94.1%,磁珠法提取核酸时检出17例阳性,阳性率为100.0%。进一步分析靶标检出率,双靶标(ORF1ab+/N+)检出率最高的是磁珠法,为64.7%(11/17),其次是柱提法的52.9%(9/17)和裂解法的41.2%(7/17);单靶标中,ORF1ab-/N+在3种核酸提取方法中的检出率相当,而ORF1ab+/N-的检出率均较低。3种核酸提取方法下的靶标(ORF1ab+/N-、ORF1ab-/N+、ORF1ab+/N+)检出率比较,差异无统计学差异(P>0.05)。见图2。

注:a为ORF1ab+/N-;b为ORF1ab-/N+;c为ORF1ab+/N+;d为ORF1ab-/N-。
3 讨 论
目前,国内大多数实验室常使用自建检测系统检测SARS-CoV-2[8],对于实验室自建检测系统,我国《临床实验室管理办法》和《医学实验室质量和能力认可准则》均要求需对检验程序的性能进行验证,证实其能满足预期用途后方可用于临床检测。但国内目前对SARS-CoV-2自建检测系统性能验证的具体方法尚未达成广泛共识,本研究对3种核酸提取方法下自建检测系统的精密度、正确度、最低检测限等指标进行了性能分析,并将其用于临床评价。
为使检测结果具有可比性,本研究采取了除核酸提取过程不同外,其余操作均相同的检测方案,整体来看,3种核酸提取方法下自建检测系统检测SARS-CoV-2的精密度、正确度均通过验证,但采用磁珠法提取核酸时的检测偏倚、CVr和CVi普遍比裂解法与柱提法小(除磁珠法低水平标本的CVi和中水平标本的CVr略大于柱提法外),表明与人工操作相比,自动化操作可减少操作误差,提高检测结果的准确度。此外,采用磁珠法提取核酸时的最低检测限(Ct值)稍优于裂解法与柱提法,检测灵敏度更高,这有利于低水平病毒RNA的检出。考虑出现上述差异与试剂提取原理有关,裂解法是一种通过简化的蛋白变性剂和生化试剂混合来抽提核酸的方法,操作简单,标本量仅需10 μL,适合病毒载量高、杂质少的标本,但如果标本不满足上述要求则易漏检,产生“假阴性”结果。柱提法是采用特殊玻璃纤维滤膜高效吸附核酸片段来提取核酸,操作环节较多,易造成核酸丢失,但其最终获得的核酸纯度较高。磁珠法是以磁珠为载体进行分离和转移来实现核酸提取的方法,在保证核酸提取纯度的同时,也保证了模板纯度。
本研究以17例COVID-19确诊病例标本为临床研究对象,比较了3种核酸提取方法下检测结果的阳性符合率及结果间的相关性,结果显示,3种核酸提取方法下检测结果的阳性符合率较高,且结果间两两均呈线性相关。本研究还比较了3种核酸提取方法下靶标的检出情况,结果显示,3种核酸提取方法下的靶标(ORF1ab+/N-、ORF1ab-/N+、ORF1ab+/N+)检出率比较,差异无统计学差异(P>0.05),说明这3种核酸提取方法均可用于SARS-CoV-2核酸检测。但值得注意的是,本研究纳入的临床样本量较少,患者的标本类型、发病时间、病情严重程度、用药情况等因素也不一致,因此结果有待后续的大样本研究进一步验证。
综上所述,本研究评价的这3种核酸提取方法均可满足临床SARS-CoV-2的检测需求,且磁珠法相较裂解法与柱提法具有更好的性能。

