腹腔热灌注紫杉醇联合阿帕替尼、替吉奥化疗对单纯脱落细胞学阳性胃癌患者转化治疗效果
丁平安 杨沛刚 田园 马国斌 郭洪海 刘洋 张志栋 王冬 李勇 赵群
河北医科大学第四医院外三科(石家庄050011)
我国胃癌患者死亡率较高,大部分患者就诊时已处于进展期,同时腹腔内存在隐蔽性转移灶或游离的癌细胞,从而导致预后较差[1-2]。以全身化疗为主的转化治疗模式是晚期胃癌治疗的主要策略,但血浆-腹膜屏障的存在使全身化疗对腹膜种植转移灶的控制效果有限[3]。近年来多项研究发现[4-6],腹腔热灌注紫杉醇化疗(hyperthermic intraperitoneal perfusion chemotherapy,HIPEC)广泛应用于胃癌腹腔转移取得了较好的疗效,尤其针对腹腔内存在游离癌细胞的胃癌患者疗效最佳。同时阿帕替尼作为一种VEGFR-2的新型酪氨酸激酶抑制剂,能够有效抑制血管生成和肿瘤生长从而发挥抗肿瘤作用,已经在多种恶性肿瘤中显示出抗肿瘤活性和可控的毒性[7]。但目前关于HIPEC 化疗同时联合阿帕替尼及替吉奥转化治疗P0CY1胃癌的研究较少,据此本中心开展一项单中心、单臂、前瞻性临床研究(ChiCTR1800014817),旨在探索HIPEC 联合阿帕替尼及替吉奥对P0CY1胃癌患者转化治疗的可能性,并评价其临床疗效性及安全性。
1 对象与方法
1.1 研究对象自2018年2月5日至12月31日于我院收集经腹腔镜探查证实为P0CY1胃癌癌患者进行前瞻性、单中心、单臂临床研究。本研究通过医院伦理审核并在ClinicalTrials 注册,注册号ChiCTR1800014817。纳入标准:(1)初治患者,临床试验开始前未行化疗、放疗或其他抗肿瘤治疗;(2)年龄18 ~70 岁;(3)男性或非妊娠、哺乳期女性;(4)病理确诊为胃腺癌;(5)术中肉眼判断T 分期为T3、T4期,无肉眼远处转移;腹腔灌洗液脱落细胞学检查阳性;(6)血常规符合以下条件:白细胞计数≥3.5 × 109/L,中性粒细胞≥1.5 × 109/L,血小板计数≥100×109/L,血红蛋白≥90 g/L;(7)生化检查符合以下条件:ALT ≤2.5×正常值上限(ULN),AST ≤2.5×ULN,血清总胆红素≤1.5×ULN,血肌酐≤1.5 × ULN;(8)ECOG 体力状况评分:0 ~1;(9)能够遵守研究期间的方案,自愿签署知情同意书。排除标准:(1)5年内有其他恶性肿瘤病史;(2)术中发现存在肉眼可见的转移病灶;(3)同时具有严重或未控制的内科疾患及感染者(包括房颤,心绞痛,心功能不全,射血分数低于50%,难控高血压等);(4)具有精神类药物滥用史且无法戒除者或有精神障碍的患者;(5)严重的或不能控制的精神疾病患者;(6)具有明确的胃肠道出血倾向的患者,包括下列情况:有局部活动性溃疡病灶,且大便潜血(++)不可入组;2 个月内有黑便、呕血病史者;(7)怀孕或哺乳期妇女;(8)根据研究者的判断,有严重的危害患者安全或影响患者完成研究的伴随疾病的患者;(9)研究者认为不适合纳入者。本研究经河北医科大学第四医院院伦理委员会批准(伦理号:2018008),得到全部研究对象或其家属知情同意。
1.2 方法
1.2.1 腹腔镜探查术[8]患者体位为平卧位,以开放法在脐下建立观察孔,并直视下分别于左、右两侧脐锁骨中线处置入5 mm Trocar,置入操作钳进行探查和灌洗。腹腔探查顺序:左右膈下→肝脏、脾脏→腹腔壁层腹膜→盆腔→大网膜、小肠及系膜→横结肠系膜→胃。探查内容:有无腹水,腹盆腔腹膜、肠系膜、大网膜和Douglas 腔有无转移灶,肝表面有无转移,胃周淋巴结是否肿大,胃浆膜面有无浸润,胃壁是否僵硬。腹腔冲洗脱落细胞学检查:以500 mL 灭菌生理盐水分别冲洗左右膈下、腹盆腔腹膜及肠系膜。取头高脚低位于Douglas 腔、肝下及脾窝收集腹腔冲洗液,离心沉渣,细胞学检查有无脱落的肿瘤细胞。对于胃体后壁肿瘤,需要切开胃结肠韧带,探查小网膜囊,包括横结肠系膜和胰腺被膜。
1.2.2 腹腔脱落细胞学结果判定[9]病理科2 名专业医师阅片,胃癌腹腔脱落细胞染色的阳性结果主要包括:核大深染,核浆比例失调;核染色质致密、粗糙,分布不均,排列紊乱;核膜增厚,出现中断或皱折;核仁增多等。若出现腹腔脱落细胞学阳性则定义为CY1。
1.2.3 转化治疗方案HIPEC 化疗第1 疗程在腹腔镜探查术后次日开始,每间隔24 h 进行1 次,连续行3 次HIPEC 化疗,腹腔注药选择紫杉醇(75 mg/m2,加入0.9%氯化钠溶液4 000 mL,灌注速度500 mL/min,水温控制在43 ℃,灌注时间为60 min);HIPEC 治疗结束14 d 后开始进行连续21 d 口服阿帕替尼500 mg/d;同时连续14 d 在早、晚餐30 min 后口服替吉奥80 mg/(m2·d),停药7 d,每3 周为1 疗程。替吉奥剂量根据体表面积(body surface area,BSA)而定:BSA <1.25 m2,80 mg/(m2·d);BSA 1.25 ~1.50 m2,100 mg/(m2·d);BSA >1.50 m2,120 mg/(m2·d),见图1。
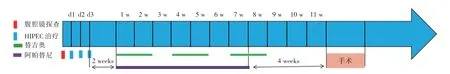
图1 38 例P0CY1胃癌患者转化治疗方案Fig.1 Transformation treatment plan for 38 patients with P0CY1 gastric cancer
1.3 评估标准
1.3.1 化疗不良反应的评估[10]采用常见不良反应评价标准(common term inology criteria for adverse events,CTCAE)3.0 版进行安全性评价,给药开始后每1 周进行1 次安全性评价,内容包括血压检测、实验室检查(血常规、尿常规、肝肾功能和凝血功能)、心电图检查等。所有受试者在最后一次给药结束28 d 内继续接受安全性评估。
1.3.2 疗效的评估[11]所有患者转化治疗3个周期后进行CT 影像学检查,疗效评估采用RECIST1.1标准,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。客观缓解率(ORR)为CR + PR 病例占可评价病例的百分数;疾病控制率(DCR)为CR + PR + SD 病例占可评价病例的百分数。无进展生存期(PFS)定义为本方案转化治疗开始至出现疾病进展时间。3 周期转化治疗结束后再次进行腹腔镜探查联合腹腔脱落细胞学检测评估腹膜转移情况。若术前腹部CT 检查提示有远处脏器转移者、化疗后局部病灶进展者和存在其他严重疾病或全身状况不良者,均不进行再次腹腔镜探查。
1.4 随访方法所有患者经门诊、住院和电话随访等方式收集随访资料。随访时间自发现转化治疗开始,截至死亡终点或2020年10月1日。1年内每月电话随访1次,每2个月门诊复查1次。1年后每3 个月电话随访1 次,每3 个月门诊随访1 次。随访时间为9.7 ~25.9 个月,中位随访时间为16.4个月,随访率为100%。
1.5 统计学方法采用SPSS 21.0对数据进行统计学处理。计数资料采用χ2检验,计量资料采用t检验。采用Kaplan-Meier 法绘制生存曲线,单因素生存分析采用Log-rank 检验,多因素生存分析采用Cox回归模型。以P<0.05为差异具有统计学意义。
2 结果
2.1 临床特征277 例进展期胃癌患者进行腹腔镜探查后,按照入组标准共纳入38 例(13.72%)P0CY1患者。全组患者中男25 例(65.79%),女13 例(34.21%);中位年龄55 岁(95%CI:33 ~69),其中≤50岁11例(28.94%),>50岁27例(71.05%);病灶部位位于贲门14 例(36.84%),胃体4 例(10.53%),胃窦15 例(39.47%),全胃5 例(13.16%);肿瘤病灶直径≥5 cm 者29 例(76.32%),<5 cm 者9 例(23.68%);Borrmann 分型为Ⅰ、Ⅱ型8 例(21.05%),Ⅲ、Ⅳ型30 例(78.95%);肿瘤浸润深度:cT3 期5 例(13.16%),cT4a期27 例(71.05%),cT4b期6 例(15.79%);淋巴结转移:cN1-cN2期有9例(23.68%),cN3a-cN3b期有29 例(76.32%);高-中分化腺癌6 例(15.79%),低-未分化腺癌32例(84.21%)(表1)。
2.2 治疗情况38 例P0CY1胃癌患者均完成3 周期化疗,再次行全腹增强CT 扫描经RECIST 1.1评估局部病灶变化为CR 者2 例(5.26%)、PR 者18 例(47.37%),SD 者14 例(36.84%),PD 者4 例(10.53%),其中ORR 为52.63%(20/38),DCR 为89.47%(34/38)。38 例P0CY1患者均再次进行腹腔镜探查联合腹腔脱落细胞学检测,其中腹腔游离癌细胞转阴(P0CY0)者16 例(42.11%),转阴患者均行R0 手术切除;17 例(44.74%)患者腹腔内仍存在游离癌细胞(P0CY1),术后继续原方案转化治疗;余5 例患者探查发现存在腹膜转移(P1CY1),更换转化治疗方案继续治疗。16 例行R0 手术切除的胃癌患者,术后病理TRG 0 级1 例(6.25%)、TRG 1级8 例(50.00%)、TRG 2 级5 例(31.25%)、TRG 3 级2 例(12.50%)(图2)。

表1 38 例P0CY1胃癌患者的临床特征Tab.1 Clinical characteristics of 38 patients with P0CY1 gastric cancer例(%)
2.3 预后情况38 例P0CY1胃癌患者均获得随访,全组1年OS 为65.79%、中位生存期(median overall survival,mOS)为14.9 个月,1年无进展生存(progression-free survival,PFS)率为50.00%,中位PFS(median PFS,mPFS)为11.7 个月(图3A、3B)。其中再次腹腔镜探查后为P0CY0胃癌患者1年OS为87.50%,1年PFS 为75.00%,而腹腔镜探查为P0CY1、P1CY1胃癌患者1年OS分别为52.94%、40.00%,1年PFS 分别为35.29%、20.00%,三组之间1年OS、PFS 差异有统计学意义(均P<0.05)。见图3C、3D。

图2 38 例P0CY1患者诊治流程图Fig.2 Flow chart of diagnosis and treatment of 38 P0CY1 patients
2.4 治疗期间不良反应全组患者均未出现因HIPEC 紫杉醇化疗及阿帕替尼、替吉奥治疗而死亡。在接受转化治疗的38 例患者中,发生率>10%的不良反应如下:白细胞减少症10.53%、中性粒细胞减少症15.79%、呕吐10.53%、蛋白尿10.53%、高血压10.53%,予以相应治疗后症状均好转。转化治疗过程中4 例患者出现3 级不良反应,包括白细胞减少症(2.63%)、中性粒细胞减少症(2.63%)、呕吐(2.63%)和高血压(2.63%),其中3 例予以对症治疗后症状无好转,首先进行剂量暂停,采取剂量暂停措施2 周内,症状好转继续原方案治疗。全组患者转化治疗期间均未观察到4 级不良反应(表2)。
3 讨论

图3 38 例P0CY1患者生存曲线Fig.3 Survival curve of 38 P0CY1 patients

表2 38 例P0CY1胃癌患者转化治疗期间出现的不良反应Tab.2 Adverse reactions occurred during conversion treatment in 38 patients with P0CY1 gastric cancer 例(%)
最新版NCCN 胃癌临床实践指南中指出,进展期胃癌一旦发现腹腔内游离癌细胞或发生腹膜转移,临床分期即为Ⅳ期,同时也失去了根治性手术的机会;而且也预示着患者预后不佳。有文献报道[12]约10% ~20%的T3期或T4期胃癌患者,在施行根治性手术时,腹腔内已存在游离的癌细胞;有40%~60%的进展期胃癌患者,术后最初复发转移病灶发生在腹膜;而“种子-土壤”学说理论[13]则认为发生腹膜转移最主要原因是术前或术后腹腔内存在游离癌细胞继而形成腹腔种植转移。由此可见,对胃癌患者进一步提高其腹腔内游离癌细胞的防治有着重要的临床意义。
目前对P0CY1胃癌患者的治疗多采用以静脉或口服给药的全身性化疗方式为主,常见的治疗方案包括:铂类联合氟尿嘧啶类、紫杉醇联合氟尿嘧啶类等。但由于“血浆-腹膜”屏障的存在,化疗药物无法透过该屏障而作用于腹腔,因而应用全身性化疗手段治疗P0CY1胃癌患者疗效欠佳。近年来,HIPEC 化疗在临床中的广泛应用给胃癌腹腔化疗提供机会,同时多项研究[1,14]证实针对合并腹腔内存在游离癌细胞的胃癌患者,通过HIPEC治疗取得了较好的疗效,能够明显提高患者预后,延长无病生存期。HIPEC 化疗作为一种新型治疗方案不但可以提高腹腔内药物的有效浓度、增强其局部疗效,而且也降低药物血浆的暴露量,减少了全身性不良反应的发生[15]。同时阿帕替尼作为一种小分子酪氨酸激酶抑制剂,能够竞争性的结合细胞内ATP 结合位点,从而降低VEGFR-2 的表达,通过这种抑制机制从而起到抗肿瘤血管生成以及抗肿瘤活性的作用[16]。研究[17-19]表明阿帕替尼对于晚期胃癌治疗具有一定的客观有效性和明显的生存获益,严重不良反应的发生率低,患者耐受性良好。基于此,本研究(ChiCTR1800014817)首次探索HIPEC 联合阿帕替尼及替吉奥对P0CY1胃癌患者转化治疗的可能性,并评价其临床疗效性及安全性。
KURAMOTO 等[20]开展了一项前瞻性多中心随机对照研究,将88 例P0CY1胃癌患者随机分为HIPEC 组(手术+术中HIPEC)以及对照组(单纯手术),研究结果显示HIPEC组的5年生存率为43.8%,明显高于对照组(4.6%),该研究提示对于P0CY1胃癌患者进行HIPEC 治疗将提高长期生存率,延长患者生存时间。本研究中针对P0CY1胃癌患者通过应用3 次HIPEC 紫杉醇化疗联合阿帕替尼及替吉奥转化治疗3 周期后,经术前CT 检查RECIST 1.1 版本评估发现,ORR 为52.63%(20/38),DCR 为89.47%(34/38);再次经腹腔镜探查及腹腔游离癌细胞检测,发现腹腔内游离癌细胞转阴率达42.11%(16/38),转阴患者均进行R0 手术切除,这较既往研究[21]转化成功率有所提高。本研究中38 例P0CY1胃癌患者转化治疗期间主要不良反应是骨髓抑制及消化道反应,主要以Ⅰ-Ⅱ级不良反应为主,其中出现Ⅲ级不良反应4 例(10.53%),但均给予患者对症治疗缓解,未出现因不良反应而终止治疗,同时本研究中均未出现Ⅳ级不良反应,所有患者未发生因化疗和手术治疗相关的死亡,这与既往研究一致[22]。
综上,HIPEC 紫杉醇化疗联合阿帕替尼及替吉奥是治疗P0CY1胃癌的一种安全、有效转化治疗方案,此治疗方法可显著提高R0 切除率和疾病控制率,延长患者的生存时间,且化疗不良反应可控,因此是具有临床应用前景的转化治疗方法,值得深入研究。
——评《卵巢恶性肿瘤诊疗手册》

