布地奈德联合甘露聚糖肽胶囊治疗AECOPD的疗效及对患者免疫功能、氧化应激水平的影响
任小慧,赵宝莲,任艳阳
陕西省第四人民医院老年病科,陕西 西安 710043
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是因为慢性支气管炎等其他原因导致的细支气管不完全阻塞狭窄,是临床发病率较高且特征为进行性发展的持续性气流受限的肺部疾病。慢性阻塞性肺疾病急性发作期(acute chronic obstructive pulmonary disease,AECOPD)是气道损伤加速而导致的疾病,严重时常常出现呼吸衰竭,甚至导致患者死亡[1]。在AECOPD 的治疗方面,目前主要通过吸氧和使用抗生素、支气管扩张剂、糖皮质激素等药物来达到缓解炎症反应作用,从而有效提高患者的呼吸功能、供氧能力[2]。布地奈德是一种糖皮质激素,其可有效抑制炎症反应,阻止肺功能进行性恶化,是AECOPD 发作治疗的主要药物[3]。除常规治疗方法外,通过其他治疗方式增强机体的免疫功能也是AECOPD 治疗的一种有效方式[4-5]。COPD 患者不管是处在急性发作期还是缓和期,机体都处于氧化和抗氧化失衡的状态,气道氧化应激的失衡被认为是导致COPD 急性发作的原因之一[6]。研究发现,甘露聚糖肽对于呼吸系统感染的治疗效果显著,其能增强黏膜免疫系统的防御能力和创伤修复能力,还具有改善其调节功能的作用,可用于呼吸系统反复感染的治疗中[7]。近年来,有学者对AECOPD 患者在常规通气治疗及抗生素、糖皮质激素、支气管扩张剂等治疗的基础上联合应用免疫功能强化治疗,发现其在改善患者免疫功能和抗感染能力,减少急性期发作次数及促进病情康复等方面具有积极的促进作用[8]。本研究通过布地奈德联合甘露醇聚糖肽治疗AECOPD,探讨其对患者肺功能、炎症反应、免疫功能和氧化应激水平的影响。
1 资料与方法
1.1 一般资料 选取陕西省第四人民医院于2018 年 1 月 至 2019 年 10 月 期 间 收 治 的 120 例AECOPD患者纳入研究。纳入标准:(1)符合《慢性阻塞性肺疾病诊治指南(2007 年修订版)》中的诊断标准[9]:(2)经肺功能、胸部X 线片、心电图等检查证实为AECOPD。(3)年龄18周岁及以上;(4)病程≥1年。排除标准:(1)合并有支气管扩张、支气管哮喘、呼吸衰竭、活动性肺结核者;(2)患有恶性肿瘤、心脑血管疾病及糖尿病等慢性消耗性疾病者;(3)治疗前14 d内使用糖皮质激素类药物者;(4)治疗前3个月应用免疫抑制剂药物者;(5)肝肾功能不全者;(6)对本研究药物严重过敏者;(7)孕妇或哺乳期患者。根据随机数表法将患者分为对照组和观察组,每组60例。对照组中男性31例,女性29例;年龄21~55岁,平均(32.1±3.8)岁;病程5~9年,平均(3.1±0.2)年;临床分级:Ⅱ级22例、Ⅲ级31例、Ⅳ级7例。观察组中男性29例,女性31例;年龄22~45岁,平均(31.9±2.9)岁;病程6~8 年,平均(2.1±0.3)年;临床分级:Ⅱ级19例、Ⅲ级32例、Ⅳ级9例。两组患者的性别、年龄、病程、临床分级等一般资料比较差异均无统计学意义(P>0.05),具有可比性。本研究经我院医学伦理委员会批准,患者均书面告知并签署知情同意书。
1.2 治疗方法 两组患者均给予祛痰、平喘、抗感染及改变水电解质紊乱等常规治疗方案。同时通过雾化给药布地奈德悬浊液(规格:2 mL:0.5 mg,批号:D14200071208,鲁南贝特制药有限公司)、吸入用沙丁胺醇溶液(规格:2.5 mL:5 mg,批号:C14200070695,山东京卫制药有限公司),给药剂量为布地奈德悬浊液2 mL、硫酸沙丁胺醇溶液2.5 mL,2 次/d,7 d 为一个疗程,连续治疗两个疗程。观察组在对照组的治疗基础上增加口服甘露聚糖肽胶囊(规格:10 mg/粒,国药准字:H20103312,天津天士力药业有限公司),10 mg/次,3 次/d,7 d 为一个疗程,连续治疗两个疗程。
1.3 观察指标
1.3.1 肺功能 分别在治疗前和治疗后应用肺功能仪检测肺功能指标,包括第1 秒用力呼气量(forced expiratory volume in 1 second,FEV1)、呼气高峰流量(peak expiratory flow,PEF)和第1 秒用力呼气量/用力肺活量(forced expiratory volume in 1 second/forced vital capacity,FEV1/FVC)。
1.3.2 免疫功能 对两组患者治疗前和治疗后的外周静血中的T 淋巴细胞亚群、自杀伤细胞(natural killer cell,NK)、免疫球蛋白(immunoglobulin,Ig)及血清炎症因子8 (inflammatory factor 8,IL-8)、肿瘤坏死因子α (Tumor necrosis factor α,TNF-α)水平进行测定。取空腹状态下的外周静脉血5 mL,3 mL 通过流式细胞仪进行T 淋巴细胞亚群计数,通过速率散射免疫比浊法对血清(12 000 rmp/min 离心取上清)中的免疫球蛋白A(immunoglobulin A,IgA)、免疫球蛋白M(immunoglobulin M,IgM)、免疫球蛋白 G (immunoglobulin G,IgG)水平测定;通过流式细胞仪对外周静脉血中的CD4+、CD8+T 细胞比例、NK 细胞百分比指标进行测定;剩下2 mL 经过低速离心(3 000 r/min)取上清,通过双抗体夹心酶联免疫吸附法对血清中的IL-8 和肿瘤坏死因子(TNF-α)等炎症因子进行测定,ELISA试剂盒购于南京建成生物工程研究所,检测步骤严重按照说明书进行。
1.3.3 氧化应激水平 在治疗前和治疗后测定血清样本中的超氧化物歧化酶(superoxide dismutase,SOD)活力及丙二醛(malondialdehyde,MDA)浓度:使用硫代巴比妥酸法测定MDA,使用黄嘌呤氧化酶法测定SOD 活力。操作步骤严格按照说明书进行。
1.3.4 安全性 记录患者治疗过程中不良反应的发生情况。
1.4 疗效判定标准 根据监测结果判断治疗效果。判定标准[10]:完全缓解:所有症状都消除,FEV1或PEF 增加≥35%;显效:症状有明显好转,25%≤FEV1或PEF增加幅度<35%;有效:症状有好转迹象,15%≤FEV1或PEF 增加<25;完全无效:症状没有任何好转,FEV1或PEF 水平治疗前后无明显变化。有效率=(完全缓解+显效+有效)/总例数×100%。
1.5 统计学方法 应用SPSS19.0 统计软件进行数据分析,计数资料比较采用χ2检验,计量资料符合正态分布,以均数±标准差()表示,组间比较采用t 检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的临床疗效比较 观察组患者的临床治疗总有效率为96.7%,明显高于对照组的81.7%,差异有统计学意义(χ2=6.988,P=0.008<0.05),见表1。
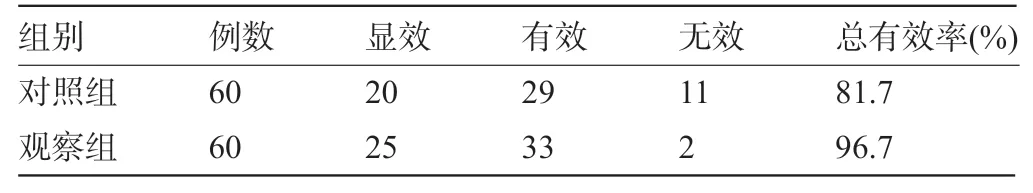
表1 两组患者的临床疗效比较(例)
2.2 两组患者治疗前后的肺功能比较 治疗前两组患者的肺功能指标比较差异均无统计学意义(P>0.05);治疗后,两组患者的FEV1、PEF、FEV1/FVC 较治疗前均明显升高,且观察组患者的FEV1、PEF、FEV1/FVC 明显高于对照组,差异均具有统计学意义(P>0.05),见表2。
表2 两组患者治疗前后的肺功能比较()
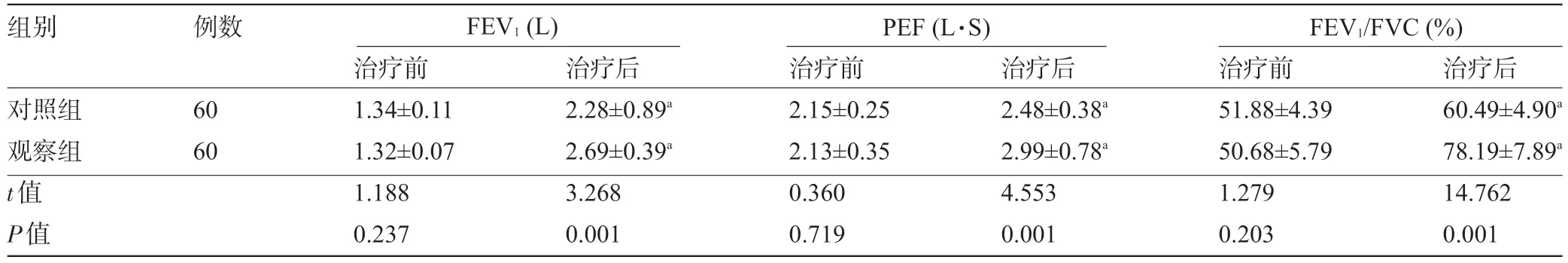
表2 两组患者治疗前后的肺功能比较()
注:与本组治疗前比较,aP<0.05。
组别 例数FEV1(L) PEF(L·S) FEV1/FVC(%)对照组观察组t值P值60 60治疗前1.34±0.11 1.32±0.07 1.188 0.237治疗后2.28±0.89a 2.69±0.39a 3.268 0.001治疗前2.15±0.25 2.13±0.35 0.360 0.719治疗后2.48±0.38a 2.99±0.78a 4.553 0.001治疗前51.88±4.39 50.68±5.79 1.279 0.203治疗后60.49±4.90a 78.19±7.89a 14.762 0.001
2.3 两组患者治疗前后的免疫功能和炎症因子比较 治疗前,两组患者的免疫功能指标和炎症因子水平比较差异均无统计学意义(P>0.05);治疗后,观察组患者的 CD3+、CD4+、NK、CD4+/CD8+和IgG、IgA、IgM 水平较治疗前均明显升高,CD8+、血清 IL-8 和TNF-α水平明显降低,且除CD8+以外,观察组患者治疗后的免疫功能指标和血清炎症因子水平与对照组比较差异均有统计学意义(P<0.05),见表3。
2.4 两组患者治疗前后的氧化应激水平比较 治疗前,两组患者的血清MDA 和SOD 比较差异均无统计学意义(P>0.05);治疗后,两组患者的MDA 明显降低,SOD 明显升高,且治疗后观察组患者的SOD、MOD 水平与对照组比较差异均有统计学意义(P<0.05),见表4。
2.5 两组患者的不良反应比较 治疗期间,观察组和对照组均没有严重不良反应,对照组中1 例患者有短暂恶心,细菌感染1例,观察组中1例患者出现口干,停药后症状缓解。
表3 两组患者治疗前后的免疫功能和血清炎症因子水平比较()

表3 两组患者治疗前后的免疫功能和血清炎症因子水平比较()
注:与本组治疗前比较,aP<0.05。
项目 对照组(n=60)观察组(n=60)t值P值CD3+(%)治疗前治疗后CD4+(%)治疗前治疗后CD8+(%)治疗前治疗后CD4+/CD8+治疗前治疗后IgA(g/L)治疗前治疗后IgG(g/L)治疗前治疗后IgM(g/L)治疗前治疗后NK(%)治疗前治疗后IL-8(ng/mL)治疗前治疗后TNF-α(ng/mL)治疗前治疗后45.95±3.90 52.09±3.98a 47.19±3.88 62.09±2.89a 1.746 15.748 0.083 0.001 28.08±3.82 31.08±2.89a 28.01±3.02 38.01±2.38a 0.111 14.338 0.912 0.001 34.08±5.81 30.07±4.29a 34.01±4.80 29.01±3.19a 0.072 1.536 0.943 0.127 0.82±0.11 1.11±0.20a 0.82±0.21 1.52±0.18a 0.000 11.803 1.000 0.001 2.36±0.38 2.61±0.19a 2.31±0.41 3.21±0.29a 0.693 13.405 0.490 0.001 11.37±1.28 12.01±2.01 11.28±0.99 17.09±1.05a 0.431 17.351 0.667 0.001 1.22±0.20 1.46±0.22a 1.28±0.16 1.71±0.10a 1.815 8.013 0.072 0.001 21.03±4.82 20.01±4.96 20.86±3.94 27.12±3.90a 0.212 8.729 0.833 0.001 394.22±72.89 182.22±61.33a 399.22±91.95 82.23±27.89a 0.330 11.496 0.742 0.001 32.28±8.46 23.19±3.79a 33.29±8.01 16.79±3.47a 0.672 9.647 0.503 0.001
表4 两组患者治疗前后的血清氧化应激水平比较()
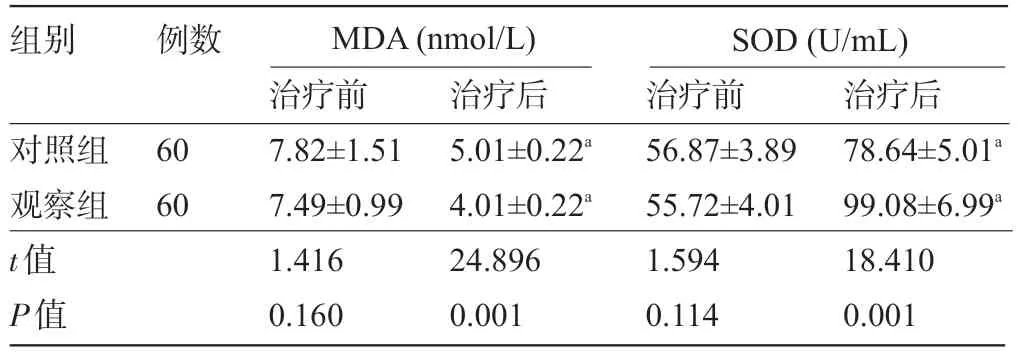
表4 两组患者治疗前后的血清氧化应激水平比较()
注:与本组治疗前比较,aP<0.05。
组别 例数MDA(nmol/L) SOD(U/mL)对照组观察组t值P值60 60治疗前7.82±1.51 7.49±0.99 1.416 0.160治疗后5.01±0.22a 4.01±0.22a 24.896 0.001治疗前56.87±3.89 55.72±4.01 1.594 0.114治疗后78.64±5.01a 99.08±6.99a 18.410 0.001
3 讨论
COPD患者反复多次的急性加重炎症表现会导致肺功能呈进行性下降,加速病情进展,还会使患者死亡风险明显增加[11]。目前,关于AECOPD尚无十分有效的治疗方式,其临床治疗目的在于快速有效缓解症状、缩短病程、促进病情快速转归和尽可能减少并发症的发生[12]。因为免疫功能下降和紊乱,COPD 患者容易出现反复发作且不易彻底被控制的呼吸系统感染,长期的慢性炎症刺激会使大气道大量分泌黏液,从而损伤气道壁,阻塞小气道,对肺实质产生破坏,最终引起气道阻塞和重塑,进而促使COPD 患者病情进展[13]。虽然目前有关免疫功能在COPD发生发展中的具体作用机制还不明确,但对患者在常规治疗基础上联合免疫功能的纠正和提高已经得到广泛认可。氧化应激作为一个新的切入点,也被认为是慢阻肺发生的病机之一[14]。
布地奈德是糖皮质激素的一种,也是目前唯一可以通过气道给药的糖皮质激素[15],其具有良好的抗炎效果,能够显著缓解气道炎症、减少气道高反应,降低细胞因子和肥大细胞对正常气道细胞的损害。但在实际治疗中,单一吸入糖皮质激素治疗对COPD 的疗效有一定的局限性,需联合其他药物配合治疗以达到取长补短、增效减毒达的目的。研究显示,甘露聚糖肽对AECOPD 患者可通过免疫功能和应激能力的调节来达到减轻气道炎症损伤、降低急性发作次数、改善肺功能的目的[13]。本研究对AECOPD 患者在常规治疗和布地奈德雾化吸入治疗的基础上采用甘露聚糖肽辅助治疗,结果发现:观察组有效率为96.7%,明显高于对照组的81.7%,差异有统计学意义(P<0.05)。治疗后观察组患者的FEV1、PEF、FEV1/FVC 均显著高于对照组,差异有统计学意义(P<0.05),治疗后观察组患者的CD3+、CD4+、NK 细胞、CD4+/CD8+和IgG、IgA、IgM 水平均显著高于对照组,差异有统计学意义(P<0.05);观察组治疗后的IL-8、TNF-α均明显低于对照组,差异有统计学意义(P<0.05);观察组患者治疗后其血清MDA 水平明显低于对照组,SOD 明显高于对照组,差异均有统计学意义(P<0.05)。提示对AECOPD患者在布地奈德雾化吸入治疗基础上联合甘露聚糖肽胶囊有利于促进患者肺功能、免疫功能的改善,抑制炎症细胞因子的释放,减轻机体氧化应激水平,从而明显提高患者的治疗效果。
综上所述,布地奈德联合甘露聚糖肽胶囊治疗AECOPD患者更加安全有效,联合甘露聚糖肽胶囊治疗能明显提高患者免疫功能,降低其炎症细胞因子和机体氧化应激水平,能明显改善患者肺功能指标,值得临床推广。

