富钒溶液直接制备高纯V2O5 的实验研究①
张永伟, 宁顺明
(长沙矿冶研究院有限责任公司,湖南 长沙410012)
高纯V2O5主要应用于航空航天、核工业、新能源以及氧化钒基纳米材料及器件行业,是一种高附加值产品。 例如,作为新能源代表之一的钒电池(全钒氧化还原液流电池,VRB)关键组成之一——钒电解液,就是用高纯V2O5来制备的。 钒电池因其有着独特优势[1-3],在绿色环保、储能系统等领域引起了广泛关注,并且已经在新能源汽车、储能系统上得到应用。 钒电池行业对V2O5的纯度有着非常高的要求,传统的化工行业、冶金行业用V2O5已不能满足需求。 我国钒资源丰富,是世界上钒储量和钒矿产量最大的国家[4],尤其是我国特有的矿床——石煤钒矿储量极为丰富[5-9];同时我国也是世界上最大的钒生产和消费国家[10];因此,开发高纯V2O5制备技术在我国具有特殊的资源与市场优势。
一般采用粗V2O5或低纯度成品多钒酸铵(或偏钒酸铵)经碱返溶后再除杂,得到纯净的富钒溶液,再进行铵盐沉钒,经煅烧后得到高纯V2O5。 这种方法综合流程长、能耗高,生产过程产生大量的废水对环境造成严重威胁。 为此有必要开发出能够直接从含钒浸出液中获得纯净富钒溶液的技术,省去沉粗钒及粗钒返溶的操作过程。
1 实验原料
原料为湘西某石煤矿经浓硫酸熟化-水浸-离子交换法获得的含钒富集液,其主要化学成分见表1。

表1 含钒富集液主要化学成分/(mg·L-1)
由表1 可以看出,含钒富集液中主要杂质为Na、S、P、Si、K、Fe、As 等,其中主要杂质S 是石煤矿硫酸熟化时以SO42-的形式进入溶液中的;杂质Na 是在对浸出液进行富集吸附时进入溶液的,它们在沉钒时可通过控制沉钒及洗涤条件将其与钒分离。 这里通过试验确定其他杂质对产品纯度的影响并制定相应的分离方法。
2 实验原理及方法
2.1 实验原理
前人研究成果表明,在净化工序中除P、Si 的同时,亦能有效去除Fe、Ca 等杂质;Na+、K+、Mg2+、SO42-、Cl-可通过控制沉钒和洗涤条件有效除去。
常见的除P、Si 方法有钙盐沉淀法、镁盐沉淀法、铁盐沉淀法、铵镁盐沉淀法等,经过初步对比试验,这里采用磷酸铵镁法除硅、磷,其原理如下:

生成的MgNH4PO4·6H2O 为白色固体,微溶于冷水,溶于热水和稀酸,溶度积常数Ksp=2.5×10-13(25 ℃)[11]。磷酸铵镁法除磷具有渣量少、钒损失率小的特点,而且本文所用原料的pH 值约为10,适于使用磷酸铵镁盐除磷。
除磷时,在溶液中加入氯化铵调节pH 值至8~9 时,硅酸根离子水解沉淀,由于硅酸在水溶液中溶解度很小,因此,在弱碱性溶液中含量很低,可以除得很彻底。
另外,加镁除磷时,由于有Mg2+存在,溶液中存在反应:
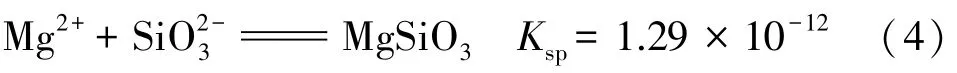
硅酸根离子以硅酸镁沉淀的形式析出。 25 ℃时,如溶液中镁离子的平衡浓度c(Mg2+)=1×10-4mol/L时,溶液中=1.29×10-8mol/L,因此,在净化时适当增加溶液中Mg2+浓度,溶液中硅几乎全部除去。
2.2 实验方法
净化除杂:取一定量含钒富集液,置于恒温水浴锅中加热到指定温度,用硫酸溶液(V(H2O)∶V(浓硫酸)=4 ∶1)或NaOH 溶液(5 mol/L)调节溶液pH 值,然后在搅拌的条件下加入铵盐及镁盐,反应结束后过滤获得净化液。 取样分析净化液中V、P、Si 等浓度,并计算净化除杂操作的钒损失率、除杂率。
制备V2O5:取一定量含钒溶液,置于恒温水浴锅中加热到45 ℃,调节溶液pH 值,然后在搅拌的条件下加入铵盐沉钒,待NH4VO3沉淀析出后,静置、过滤、洗涤、烘干,得到白色的中间产品NH4VO3;最后将干燥的NH4VO3粉末置于马弗炉升温至500 ℃煅烧2.5 h 获得产品V2O5。
3 实验结果与讨论
3.1 除杂剂加入量对除杂率、钒损失率的影响
取含钒富集液100 mL(pH≈10),分别加入1 mL、4 mL、8 mL、12 mL、16 mL 浓度为200 g/L 的氯化镁溶液,按铵镁摩尔比n(NH4Cl) ∶n(MgCl2)=1.3 加入氯化铵,在35 ℃加热搅拌反应60 min,除杂剂氯化镁加入量对除杂效果的影响见图1。

图1 除杂剂氯化镁加入量对除杂效果的影响
可以看出,铵镁法除磷效果较好,而且比较稳定,即使在氯化镁加入为4 mL 时除磷率也能达到96%以上。 随着氯化镁加入量增加,除硅率逐渐增大,当氯化镁加入量进一步增加到16 mL 时,除硅率反而下降。溶液中钒的损失率随氯化镁加入量增加而增大,当氯化镁加入量超过12 mL 后,钒损失显著增大。 其原因有二:一是随氯化镁含量增加,过量的氯化镁与溶液中钒聚合态离子生成复杂的钒酸镁盐沉淀;二是过量的氯化镁在弱碱性条件下发生水解生成Mg(OH)2沉淀,吸附夹杂钒致使钒损失率增加,同时也降低了除杂效果,降低了除硅率。 因此,为了保证较好的除磷、硅效果及较低的钒损失率,选取氯化镁加入量为8 mL。
3.2 溶液温度对除杂率、钒损失率的影响
向含钒富集液中加入氯化镁溶液8 mL,其他条件不变,温度对除杂效果的影响如图2 所示。
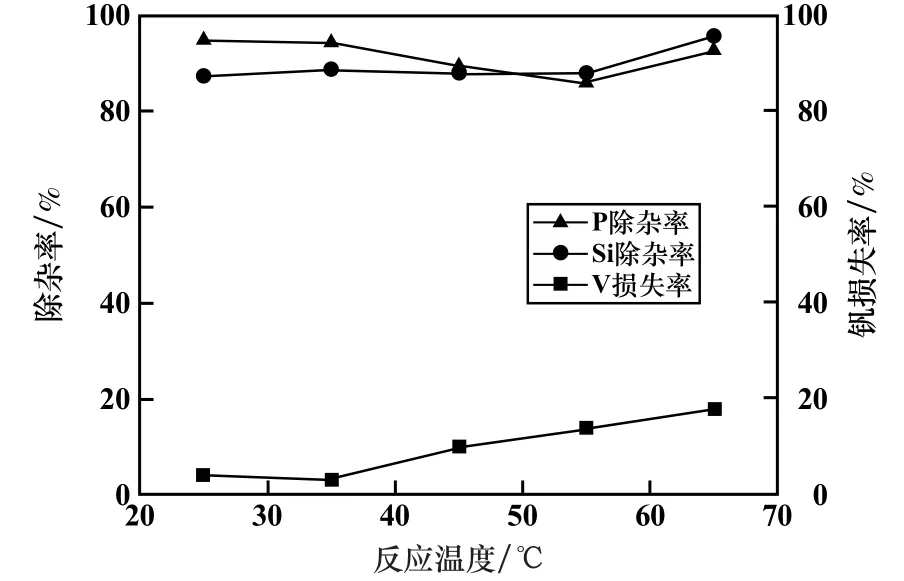
图2 反应温度对除杂效果的影响
由图2 可以看出,随温度升高,除磷率、除硅率均先逐渐下降,至55 ℃时再上升;而钒损失率在反应温度高于35 ℃后显著增大。 这是因为:提高反应温度,磷酸铵镁溶解度也会增大[12-13],从而造成除磷率降低;另外,升温会促进Mg2+水解生成Mg(OH)2,造成除磷率、除硅率降低;继续升高温度,溶液中过量的镁可能生成更难溶的Mg3(PO4)2沉淀,SiO32-水解加剧,使除磷率、除硅率又上升。 另一方面,随温度升高,Mg2+在溶液中水解逐渐加剧,水解产生的胶状Mg(OH)2以及Mg3(PO4)2等沉淀吸附夹杂钒致使钒损失增大。
除杂率和钒损失率在25~35 ℃范围内波动不大,由于除杂反应很快,生成的沉淀物在试验温度下易过滤,滤液清澈透明,不需要通过提高反应温度来改善净化反应速度及过滤性能,所以净化反应温度控制在室温下即可。
3.3 铵镁比对除杂率、钒损失率的影响
室温下净化除杂,其他条件不变,铵镁比对除杂效果的影响如图3 所示。
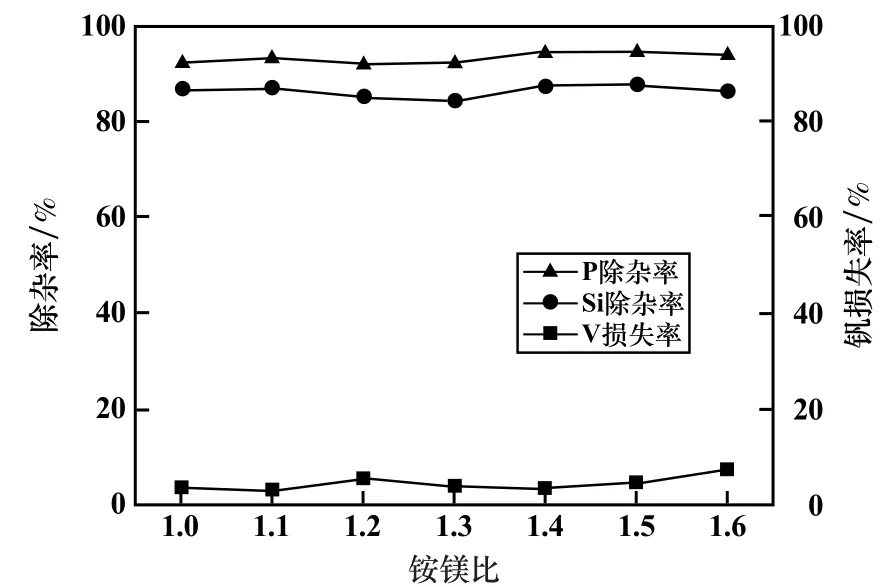
图3 铵镁比对除杂效果的影响
由图3 可以看出,在试验范围内,除杂率变化不大。 但是当铵镁比大于1.4 时,NH4VO3溶解度随NH4+浓度增加而减小[14],溶液中高浓度的钒酸根离子会与NH4+反应生成偏钒酸铵沉淀析出,从而造成钒损失率增大。 在试验过程中可以观察到,铵镁比为1.6 时,加入氯化铵搅拌后溶液会变浑浊,静置后有沉淀生成。因此反应体系铵镁比控制在1.4 为宜。
3.4 溶液pH 值对除杂率、钒损失率的影响
铵镁比1.4,其他条件不变,pH 值对除杂效果的影响如图4 所示。
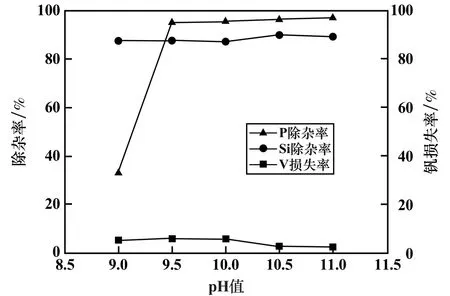
图4 含钒溶液pH 值对除杂效果的影响
由图4 可见,pH =9.0 时,除磷效果很差,除磷率仅为33.35% ,但当pH 值升至9.5 以后,除磷率可达95%以上,且随pH 值增大呈上升趋势。 这可能与磷酸根离子在溶液中存在的形态与pH 值有关。 pH 值较低时,溶液中磷酸根离子主要以HPO42-形式存在,加入除杂剂后生成溶解度较大的MgHPO4(溶度积常数Ksp(298 K)=6.5 × 10-5[15]),降低了除杂效果;随pH 值升高,溶液中磷与铵、镁生成了更难溶的MgNH4PO4,使磷去除率逐渐升高。 在试验pH 值下,除硅效果比较稳定,均能保持在87%以上。 钒损失则在pH 值升至10 后逐渐下降并趋于平稳。 试验中发现,当pH <10.0 时,向溶液加入氯化铵后,溶液会变浑浊,且pH 值越小浑浊现象越严重,而pH >10.0 时却无此现象。 根据有关文献[14],在碱性条件下,偏钒酸铵的溶解度随pH 值增大而增大,当pH >10 时,偏钒酸铵溶解度将快速上升。 因此,当pH<10 时,钒损失率较高的原因可能是在该条件下,偏钒酸铵的溶解度小,溶液中生成了少量偏钒酸铵。
综上所述,pH=10.5 为最佳净化酸碱度。 由于本试验所用含钒溶液pH 值为10.2,与最佳pH 值相差不大,在工业生产中为了降低生产成本,也可不对原液pH 值进行调整直接用于净化反应。
3.5 反应时间对除杂率、钒损失率的影响
含钒溶液pH =10.2,其他条件不变,反应时间对除杂效果的影响如图5 所示。

图5 反应时间对除杂效果的影响
由图5 可以看出,除杂反应速度很快,即使反应时间很短的情况下,除磷率也能达到95%以上,除硅率达到87%以上。 延长反应时间,除磷率及除硅率均有小幅度提高;当反应时间超过30 min 后,除磷率、除硅率不再明显变化,说明除杂反应已经完成。 钒损失率随反应时间延长先上升后缓慢降低,这是因为在前30 min 内随反应时间增加,溶液中过量的除杂试剂与钒逐渐生成了钒酸盐沉淀,造成了钒的损失。 从图5也可以看出可通过延长反应时间来降低钒损失率,但会延长生产周期,降低生产效率,因此净化时间选择30 min 即可。
3.6 优化试验
将含钒富集液在上述最佳条件下进行除杂:取含钒富集液按铵镁比n(NH4Cl) ∶n(MgCl2)=1.4 加入氯化铵和8 mL 浓度为200 g/L 的氯化镁溶液,于室温下搅拌反应30 min 后直接进行过滤,试验结果见表2。由表2 可见,采用磷酸铵镁法除磷、硅效果好,比较稳定,经净化后溶液中磷含量约为2.40 mg/L,硅含量约为6.60 mg/L,而且钒损失率较低。

表2 优化试验结果
将优化条件下获得的净化液与未净化含钒原液在相同条件下制备V2O5,产品分析结果如表3 所示。

表3 净化后产品成分对比/%
由表3 可以看出,经最佳条件净化后制备的V2O5产品中杂质P、Si 含量都明显降低,特别是P,在净化后的产品中未检出。 此外,S、Fe 含量也有显著下降。S、Na、K 等杂质含量与沉钒和洗涤工序关系较大,通过强化沉钒与洗涤工序条件来达到去除偏钒酸铵内夹杂的杂质S、Na、K 等。 杂质含量满足DB 13/T 2059—2014[16]V2O599.9-A 牌号的技术要求,主成分V2O5含量由98.92%提高到99.93%。
4 结 论
采用磷酸铵镁法净化含钒富集液,脱除磷、硅,最佳净化除杂条件为:100 mL 含钒富集液中加入200 g/L 的氯化铵溶液8 mL,按铵镁比(物质的量比)1.4 加入氯化铵,直接使用原溶液(pH≈10.2)于室温(25~35 ℃)下,搅拌净化30 min 后过滤得净化液。 净化液沉钒、过滤、洗涤、烘干、煅烧后获得纯度为99.93%的高纯V2O5,含量满足DB 13/T 2059—2014 V2O599.9-A 牌号的技术要求。 经重复性试验验证,试验样品质量稳定、工艺流程简单,而且生产成本较低。

