柱前衍生-高效液相色谱测定手足口病患者血清中多胺水平
张伟健,谢 琪,,曾今诚,黄明元*(广东医科大学 .东莞市环境医学重点实验室,.东莞市生物活性分子开发与转化研究重点实验室,广东东莞 53808)
多胺是一类含氮的低分子量有机化合物,具有生物活性,一般包括亚精胺(SPD)和精胺(SPM),它们具有促进细胞分化、增生、生长,在调节核酸与蛋白质的合成及生物膜稳定性等方面起着重要的作用[1]。体内 SPD和SPM水平与恶性肿瘤、心血管疾病、脑血管疾病等疾病的发生发展密切相关[2-4]。目前多胺检测在红斑狼疮[5]、恶性肿瘤患者中均有报道[6],主要采用高相液相色谱法(HPLC)[7]。手足口病(HFMD)是一类由肠道病毒感染引起的一种发生于5岁以下儿童中的常见疾病[8]。本实验采用柱前衍生-HPLC测定手足口患儿和健康体检者血清多胺的浓度,旨为临床诊断和疾病预防提供参考。
1 材料和方法
1.1 仪器与试剂
LC-20A高效液相色谱仪、SIL-20A自动进样器、CTO-20A柱温箱、RF-20A xs荧光检测器(Shimadzu),5417R冷冻高速离心机(Eppendorf),氮吹仪REXC100,电动旋涡混旋震荡器 Vortex-Genie2,Milli-Q超纯水仪(Millipore),电热恒温水温箱(精宏公司);亚精胺标准品、精胺标准品和丹磺酰氯均购于sigma公司;乙腈为色谱纯,氨水、高氯酸、NaOH、NaHCO3等均为分析纯。
1.2 标准溶液配制
准确称取亚精胺和精胺标准品100 mg,用超纯水定容至10 mL,放置-20℃冰箱保存;用超纯水分别稀释以上标准品为1 g/L,混合以上单标,再用冷5%高氯酸稀释成终溶度分别为 20、10、4、2、1、0.5、0.1、0.02 mg/L的混合标准溶液,置于 4℃冰箱保存。
1.3 样本收集与前处理
根据中国卫生部于2018年发布的《手足口病治疗指南》和粪便手足口病病毒检测阳性诊断结果,收集手足口病患儿(20例)和同期健康体检者(20例)的血清。
样本前处理:取250 μL血清,然后12000 r/min,4℃,离心5 min,取200 μL血清,加入冷300 μL 5%HCLO4 沉淀蛋白,涡旋,12000 r/min,4℃,离心10 min,转移上清400 μL,放置 4℃待衍生[9]。
1.4 衍生化处理
400 μL的标准液和样品加入200 μL 2 mol/L NaOH和400 μL饱和NaHCO3,然后加上400 μL丹磺酰氯(5 g/L,乙腈做溶剂),在 60℃水浴加热避光反应45 min,反应结束后加入100 μL的氨水终止反应并除去多余的丹磺酰氯。
1.5 衍生物的萃取
加800 μL三氯甲烷萃取,3000 r/min,10 min,吸取下层有机相700 μL,以氮气吹干,残渣用500 μL乙腈复溶,0.22 μm有机滤膜过滤上样检测。
1.6 色谱条件
色谱柱:C18柱 (4.6 mm×250 mm,5μm),流动相:A项为超纯水,B项为乙腈,梯度洗脱,梯度洗脱程序见表1;检测器:荧光检测器,激发波长为340 nm,发射波长为510 nm;流速:1 mL/min,进样体积:10 μL;柱温:40℃。
2 结果
2.1 亚精胺和精胺色谱图。
亚精胺和精胺色谱图见图1。亚精胺和精胺保留时间分别为14.9、18.8 min,分离效果较好。
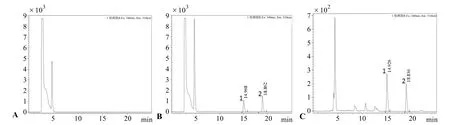
图1 衍生后亚精胺(1)和精胺(2)的 HPLC色谱图
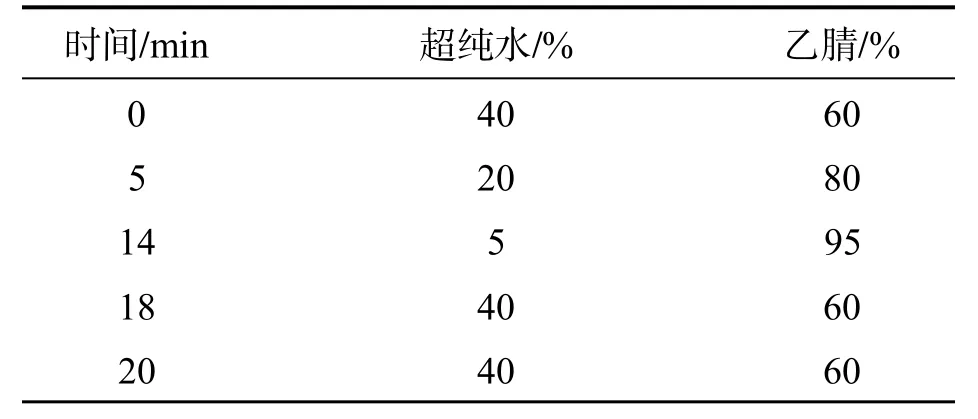
表1 梯度洗脱程序
2.2 衍生条件优化
按“ 1.4衍生化处理”项下方法,考察衍生 pH 分别为9、10、11时多胺的峰面积,结果见图 2A;考察衍生剂用量分别为100、200、400、800 μL时多胺的峰面积,结果见图 2B;考察衍生剂温度分别为30、40、50、60、70℃时多胺的峰面积,结果见图 2C;考察反应时间分别为 10、20、30、40、45、50 min时多胺的峰面积,结果见图 2D。最终确定衍生体系 pH约为 10,衍生剂量为200 μL,反应温度为60℃,反应时间为45 min。
2.3 标准工作曲线
将冷 5%高氯酸稀释成终质量溶度分别为 20、10、4、2、1、0.5、0.1、0.02 mg/L的混合标准溶液,置于 4℃冰箱保存,经衍生化进样测定。以亚精胺和精胺浓度与峰面积采用外标法进行回归得出标准曲线方程,线性方程亚精胺为y=827755x+38250和精胺为y=957264x+34436,相关系数均>0.997,亚精胺最低检测限(LOD)为0.02 mg/L,精胺的最低检测限(LOD)为 0.01 mg/L。
2.4 精密度实验
分别取标准溶液质量浓度 0.1、1、10 mg/L作为低中高质量浓度,于上述色谱条件,1 d内重复检测5次,计算日内精密度和日间精密度。结果见表2,SPD日内精密度(RSD%)为0.18~2.38,日间精密度(RSD%)为0.11~3.14,SPM日内精密度(RSD%)为0.54~0.85,日间精密度(RSD%)为 0.1~1.28。
2.5 稳定性
分别配制低、中、高(0.1、1、10 mg/L)3种质量浓度标准溶液,分别置于-20℃3个月、室温(25℃)24 h、冻融 3次循环以及衍生反应后24 h来考察SPD和SPM的长期、短期稳定性,结果(表 3)表明 SPD和SPM在本实验条件下稳定可测;衍生后 SPD和SPM并不太稳定,提示不能重复检测。
2.6 回收率
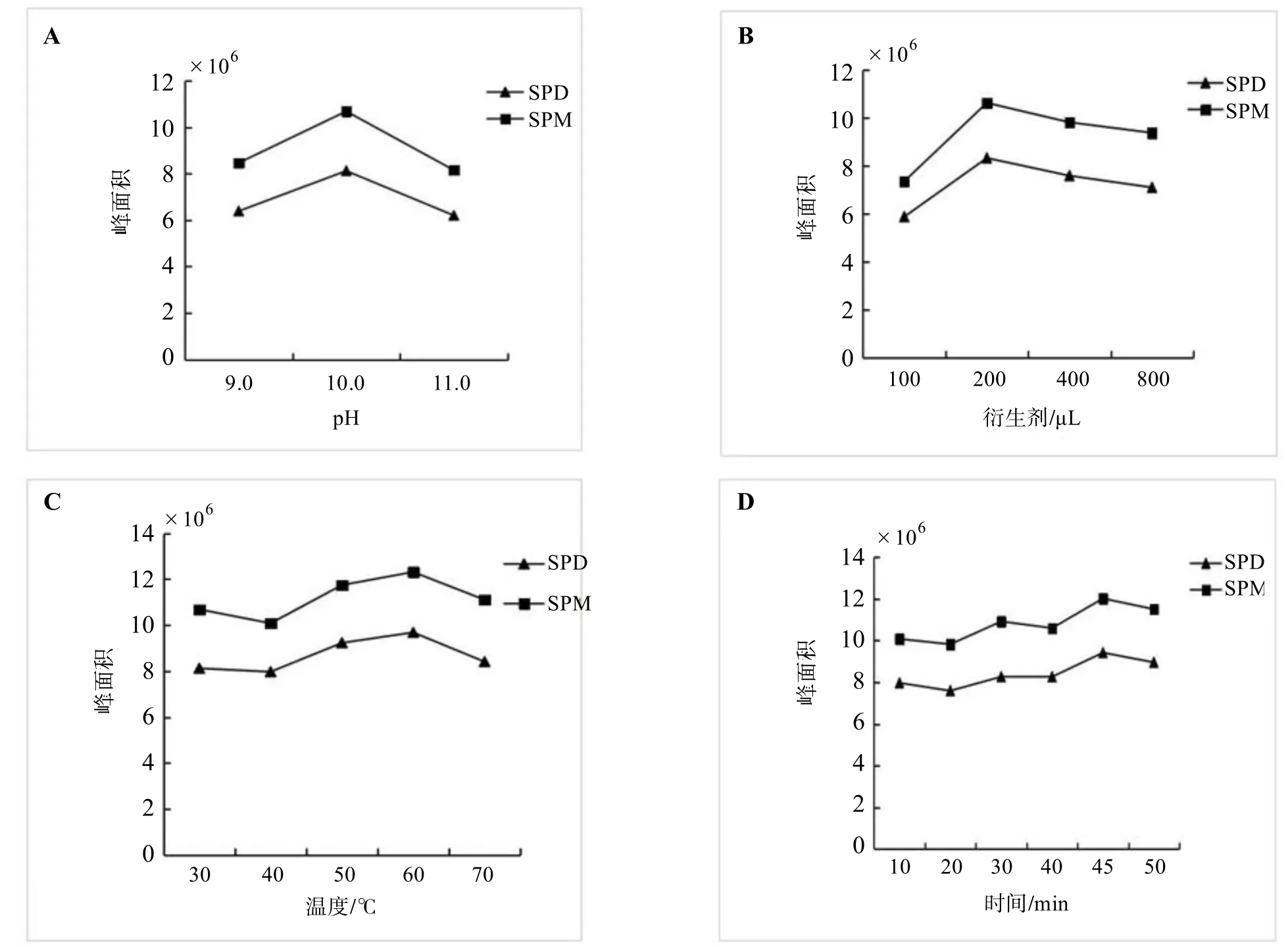
图2 不同衍生条件下亚精胺和精胺的峰面积
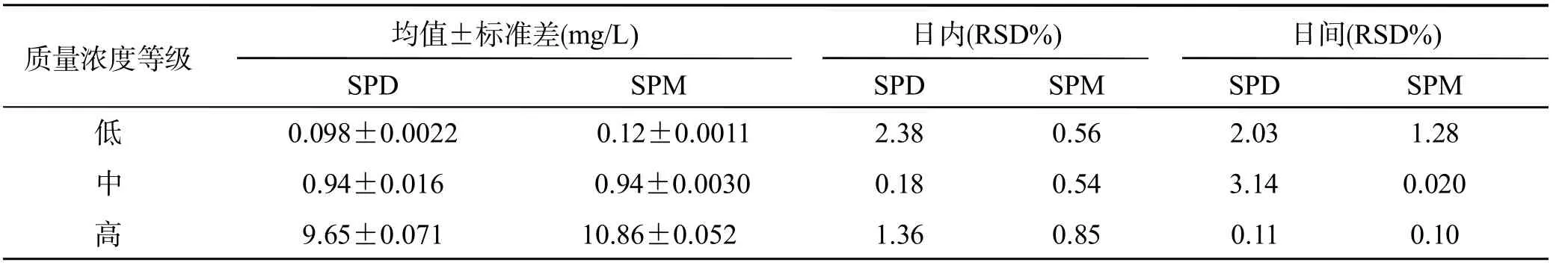
表2 亚精胺和精胺的精密度(n=5)
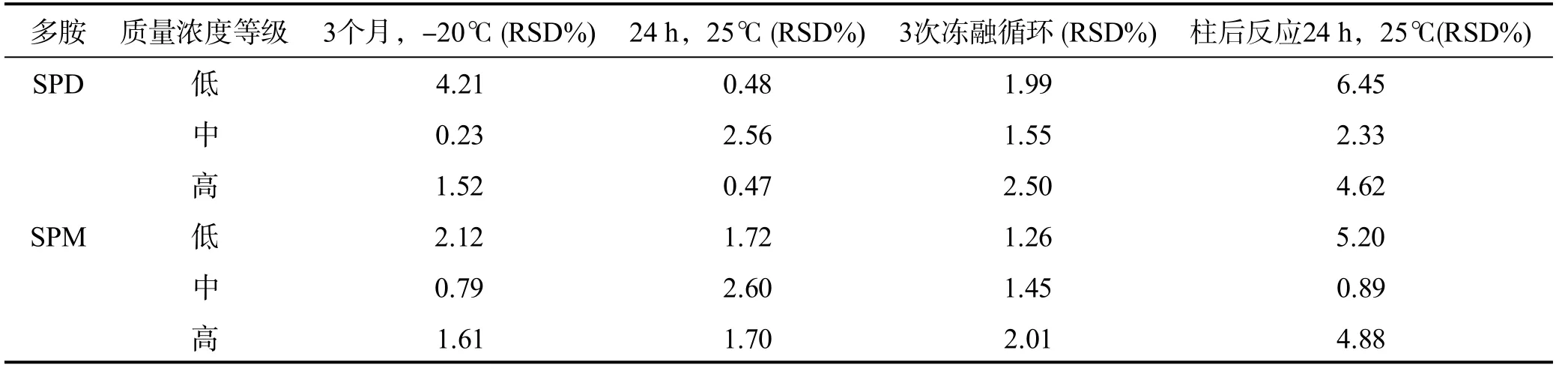
表3 亚精胺和精胺的稳定性(n=3)
配置已知含量(0.5、4、10 mg/L)的质量标准溶液,使用标准添加法,测定回收率。经衍生化处理进样测定,用标准曲线计算,根据测定质量浓度与实际加入质量浓度计算回收率。结果见表4,SPD回收率在87.98%~99.10%,SPM回收率在96.84%~105.15%。
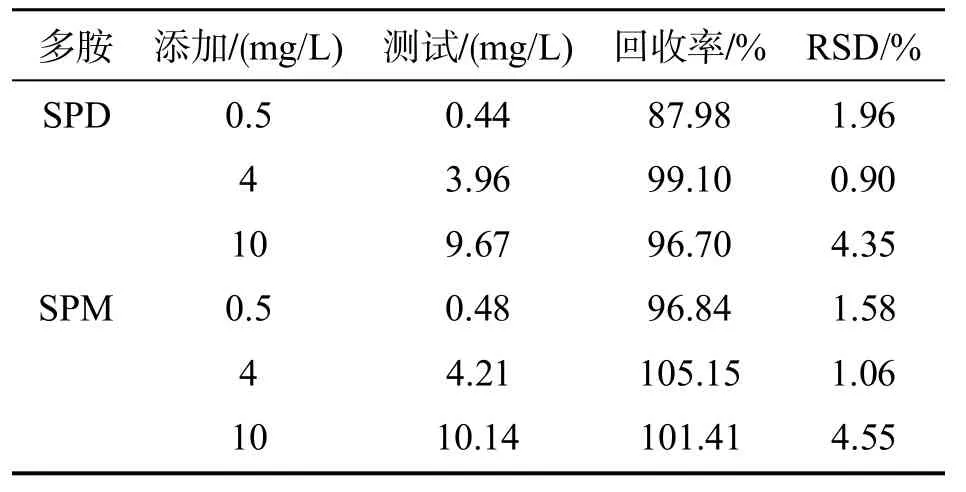
表4 亚精胺和精胺的回收率(n=4)
2.7 HFMD患儿和健康对照者血清中 SPD 和SPM 含量的检测
在优化后的实验条件下,经上述处理,测定20例手足口病患儿及20例健康对照者血清中多胺的水平,SPD和SPM含量见表5。
表5 HFMD患儿和健康对照者血清亚精胺和精胺含量(±s, n=20,mg/L)

表5 HFMD患儿和健康对照者血清亚精胺和精胺含量(±s, n=20,mg/L)
与健康对照者相比:aP<0.01
3 讨论
衍生剂质量浓度在5 g/L时得到最优结果,对衍生剂用量进行优化发现衍生剂量在200 μL时衍生化产物与其他更大剂量相差不大,考虑到成本,确定衍生剂用量为200 μL[10]。有报道发现衍生剂的用量、衍生反应的温度和时间以及衍生体系的 pH值对丹磺酰氯衍生反应影响很大[11],pH值过低会影响衍生反应不完全,过高则会干扰,对 pH进行优化结果表示在10.0左右衍生反应最合适;衍生化温度及衍生时间对实验结果也会有较大的影响,衍生温度过高衍生物易分解,衍生温度过低时衍生反应不完全[5],经反复试验发现,60℃衍生反应45 min吸收信号最强。
应用HPLC检测肿瘤患者生物样本中的多胺已有多篇研究报道。一项研究报道了局灶性脑缺血患者血液中的亚精胺水平升高[12];此外,亚精胺与第48小时的临床结果和第4~6天的梗死体积有关。有趣的是,外源性多胺或多胺抑制剂可以影响一系列的生理活动。例如,亚精胺或精胺预处理显著抑制缺血/再灌注(I/R)细胞的凋亡,抑制caspase-3和caspase-9的表达,抑制细胞色素c 的释放,上调Bcl-2的表达,降低[Ca2+][13]。在一个高血压诱发的充血性心力衰竭模型中,亚精胺的摄入降低了血压,提高了肌氨酸磷酸化水平,防止了心脏肥厚,表明延迟了心力衰竭的进展[14]。在本研究中,我们研究了亚精胺和精胺在 EV71感染的手足口病中的作用,表 5结果显示手足口患者与健康对照中的亚精胺和精胺水平差异均有统计学意义,提示亚精胺和精胺在手足口病,特别是 EV71感染的手足口病中高表达,表明生物多胺与手足口病的进展有关。本研究在已有的研究基础上,优化衍生实验条件,最终建立了衍生体系pH约为 10,衍生剂量为200 μL,反应温度为 60℃,反应时间为45 min的高效液相色谱法以检测手足口患者血清中亚精胺和精胺含量。本方法准确可靠,重复性好,可用于临床监测手足口病患者体内亚精胺和精胺水平,有待提高的地方为应该增加临床样本量和疾病临床分期,更深层次挖掘多胺与手足口病之间的联系,为临床诊断和疾病预防提供参考。

