人工智能:医学发展的新动力
刘志红 陈听雨
创新驱动医学发展,医学的创新需要在学科交叉和前沿汇聚方面抢占制高点。国家“四个面向”的提出进一步昭示,未来中国必将加快生命健康领域科技发展的步伐,加紧补齐生命健康科技研究的短板。医学研究已进入大数据和精准化并行融合时代,我们对数字模型、信息化、材料科学等理论和技术的依赖大幅提升。
大数据、云计算、智能机器人等技术的应用将人类带入了智能时代,而在医学领域,科学进步,技术创新奠定了我们如今数据驱动的医学新时代的基础。在国家“十四五”规划的重点任务中,将人工智能、生命健康、脑科学等作为强化国家战略科技力量的重点瞄准方向。人工智能正以前所未有的速度和广度改变着我们的认知模式和医学研究的范式。目前疾病的规模化前瞻性临床队列和大规模亚健康人群的分子群谱数据越来越多,而个体化医疗信息的获取、分类和储存及医疗信息系统大数据整合与数据库构建都离不开强大的计算,人工智能强大的算力和先进的算法正在推动生物医学走向数据化、计算化和定量化。
随着基因测序、生理和环境检测水平、先进成像和行为跟踪能力的进步,基因组编辑、细胞重编程、组织工程、人工智能等技术的提高,人们能够以前所未有的清晰程度,评估和管理人类健康(high definition medicine)[1]。这种在“生命全周期,健康全过程”的层次上认识生命及健康,需要便携式的生命活动监控体系,“计算+实验”的研究模式,以及“数据分析+经验总结“的积累。人工智能生物学(AI-biology)能够从海量的复杂的大数据中发现人类大脑目前无法分析的数据结构,捕捉到人类可能无法捕捉到的特征,从而解决生物学研究中真正困难、复杂的问题。近期开发的深度学习模型AlphaFold[2]已可以通过基因序列预测出蛋白质的三维结构,其准确性可以与冷冻电镜等实验学解析的三维结构相媲美,这也证实人工智能将成为人类扩展科学知识边界的重要工具之一,可以帮助我们跳出现有的认知范畴,在更深层次上理解和处理生命的复杂信息。
机器学习是人工智能中的重要分支之一,它被定义为使用计算机系统,从样本数据以及过去经验中进行学习的相关算法和统计模型,机器学习不需明确地使用编程来执行特定的任务[3]。机器学习具有识别数据中隐藏模式的能力,可以用来发现两个变量之间的相互关联、按照一定的标准对研究对象进行分类、基于基线特征进行相关结局的预测、识别具有相似模式的对象等。目前较为流行的机器学习算法包括支持向量机[4]、随机森林[5]、梯度增强树[6]和人工神经网络[7]等。人工智能技术已被广泛应用于医学,而在肾脏病领域,人工智能也已开始为肾科医生赋能[8],并在疾病预测[9-12]、患者分群[13-14]、辅助诊断和治疗[15-17]、基因组医学[18]等方向得以应用和发挥作用。
疾病预测
IgA肾病是我国发病率最高的原发性肾小球肾炎,疾病具有高度异质性,且患者预后不佳,我们团队利用人工智能方法,建立了一个可解释且临床实用的IgA肾病患者预后预测系统[12]。研究回顾性分析来自中国 18 个肾脏疾病中心,2 047例经肾活检确诊为IgA肾病患者的基线及长期随访资料,资料涵盖了患者的流行病特征、临床及病理指标等36个变量,据此建立了一个精准预测的机器学习模型及一个临床解释性能佳的风险分层模型(图1)[19],不仅能辅助预测IgA肾病患者的肾脏远期预后,还为临床试验特定患者群的筛选及患者分层管理提供了工具。
狼疮性肾炎是我国最常见的继发性肾小球肾炎,患者临床病理表现多样,治疗反应及预后不一,且患者复发率高,成为影响患者生活质量和远期预后的一个重要因素[20]。同样,使用机器学习方法,我们建立了针对狼疮性肾炎患者的复发预测模型。利用1 694例肾活检确诊的狼疮性肾炎患者的长期随访数据,对患者缓解后5年内的复发进行了预测,模型的预测能力(C统计量)达到0.82。通过该模型,可以准确预测5年内狼疮性肾炎患者的复发风险,并进行风险的分层,从而为个体化治疗和管理患者提供更多的依据[21]。
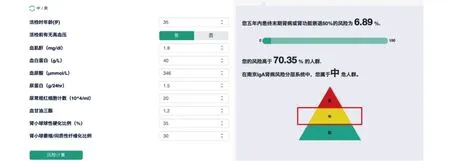
图1 南京IgA肾病风险分层系统的网页计算器在网页计算器中,通过输入患者一般情况、临床及病理的相关指标,点击计算,即可得到患者5年内达到终末期肾病或肾功能下降50%的风险、患者风险在人群中的百分比,以及患者的风险分层(低危、中危及高危)
辅助治疗决策
IgA肾病的发病机制尚未完全阐明,尽管有大量的工作支持其为免疫介导的疾病,但免疫抑制剂在IgA肾病治疗中的疗效仍存在诸多争议。国家肾脏疾病临床医学研究中心及核心单位的多中心随机对照临床实验[22]及重复肾活检研究[23]发现,除常见的临床变量如肾功能、尿蛋白以外,患者的肾脏病理改变对于指导免疫抑制剂治疗亦具有关键作用。故全面结合患者的临床和病理变量,基于人工智能算法,识别接受免疫抑制剂治疗的获益人群,对于指导IgA肾病患者的个体化治疗至关重要。我们收集来自全国24个肾脏病中心4 000多例IgA肾病患者全面的流行病、临床及病理资料,通过人工智能算法自动将人群根据免疫抑制剂治疗的疗效差异分群,并找到使用免疫抑制剂疗效显著的亚群:在肾功能正常的患者中,免疫抑制剂治疗获益随着尿蛋白水平升高而增加,而在肾功能受损患者中,尿蛋白较高且肾脏病理伴有新月体病变的患者接受免疫抑制剂治疗可以显著获益。在以上获益亚群中,免疫抑制剂能够减少50%~70%的终末期肾病发生风险,且研究结果在独立队列中得到了外部验证[14]。
糖尿病肾病是糖尿病的主要微血管并发症,也是终末期肾病的主要原因。国内外制定了多个版本的临床指南以规范糖尿病肾病的诊断和治疗。为明确在真实世界中糖尿病肾病患者治疗的指南符合情况及效果,我们采用《美国糖尿病协会2018年指南》[24]及《中华医学会糖尿病学分会2017年指南》[25],借助大数据分析及人工智能算法,从降糖、降压、调脂三方面详细评估国家肾脏疾病临床医学研究中心的1 128例肾活检确诊的糖尿病肾病患者的治疗及遵循指南的情况,探讨规范治疗与临床指标控制及终末期肾病的关系,并对上述指标控制对糖尿病肾病患者终末期肾病发生的影响进行了分析[17]。结果表明我国糖尿病肾病患者的指南依从性仍存在改善的空间,尤其是血压、血脂的治疗达标率较低。遵循指南治疗方案更有益于糖化血红蛋白、血压水平的良好控制以及降低发生终末期肾脏病的风险。结果还显示控制蛋白尿和低密度脂蛋白水平对改善糖尿病肾病预后具有重要作用。该研究为建立糖尿病肾病患者标准化治疗策略提供了理论依据,且证明源于循证医学和专家经验制定的指南有利于提高临床实践水平,提高临床治疗效果,改善患者预后。
肾脏病理图像识别和分析
肾脏病理不仅有助于疾病的诊断,其在治疗方案的制定、临床预后的评估及科学研究中均发挥重要的作用。人工智能技术被广泛地应用于医学图像识别,特别受到关注的领域是放射学,深度神经网络模型已被证实可以在X线、CT、MRI等得到的各种医学扫描图像中准确诊断骨折[26]、肝脏肿块[27]、颅内出血[28]等多种疾病。长久以来,病理学家们对于病理切片的解释和诊断具有较高的异质性及不一致性,而人工智能模型已经可以对全切片扫描图像进行深度学习,并提高多种肿瘤诊断的准确性和速度[29-31]。人工智能在肾脏病理图像识别中的应用尚处在起步阶段。我们使用12 418张肾小球病理图像训练多种深度学习网络,完成了包含肾小球识别、肾小球病变分类、肾小球内固有细胞识别和定量分析等在内的肾小球基本结构和病变的识别,证实人工智能模型可助力肾脏病理病变的识别和分析。由高年资病理医生对400余例来自国家肾脏疾病临床医学研究中心经病理明确诊断为IgA肾病患者的光镜切片的肾小球病变及结构进行标注,训练多种深度学习模型,最终整合成人工智能肾脏病理识别系统(ARPS系统,图2),该系统可准确识别肾小球基本病变(球性硬化、节段硬化、新月体),精准度92.8%;准确计算肾小球内三种固有细胞的数量,精准度92.2%;并且自动计算系膜区积分。同时,该研究选取220个肾小球中的3万多个固有细胞,将ARPS系统与国家肾病临床医学研究中心的4位初级肾脏病理医生进行人机对照,对比两者在肾小球内细胞识别的精度和速度。最终,ARPS系统识别精准度超越初级病理医生约5%~11%,识别速度更是遥遥领先,是病理医生的50~90倍[15]。该研究证明人工智能病理模型可以对肾脏病理组织中肾小球结构及病变进行准确识别,为未来人工智能助力肾脏病理诊断提供基础,也为肾脏病理走向数字化、定量化迈出重要一步。

图2 人工智能肾脏病理识别系统该系统可在全切片扫描图像中定位肾小球,识别肾小球基本病变(球性硬化、节段硬化、新月体),计算肾小球内三种固有细胞的数量,并且自动计算系膜细胞增生评分
肾脏纤维化程度是慢性肾脏病诊断和治疗选择的重要依据,也是患者肾脏预后预测的主要指标之一。目前,肾脏纤维化的评估金标准仍是肾脏病理,但肾脏活检存在有创和取材片面的缺陷。功能影像学在近几年迅猛发展,其不仅能够反映器官的解剖形态,还可以提供实体器官细胞生物学和病理生理学的相关信息。我们收集了患者肾活检病理评估的肾组织纤维化病变,并对肾脏进行功能影像学检测,纳入指标主要为与肾脏纤维化病理生理机制有关的重要序列,能够反映细胞外基质增生和管周毛细血管减少的程度。基于机器学习,将患者肾脏病理纤维化程度、功能影像学序列以及肾功能[估算的肾小球滤过率(eGFR)]水平一对一进行建模,建立功能影像、肾功能与肾脏病理的映射关联,使得我们得以通过eGFR及功能影像学的指标,推导出患者肾脏纤维化的程度,从而能够可靠地、可重复地评估患者的肾脏纤维化水平[32]。
基因组医学与肾脏疾病
任何生物性状和生理疾病都是基因组结构和功能变化过程的产物,从基因组了解疾病发生发展的规律及其与表型之间的关联,对于系统解读疾病的发生机制和防治至关重要。近几年来,随着基因组学和表型组学的发展,海量医学和遗传学数据的涌现亟需利用人工智能技术构建表型性状与遗传特征的因果关联,最终为认识和防治疾病提供系统的指导(图3)。
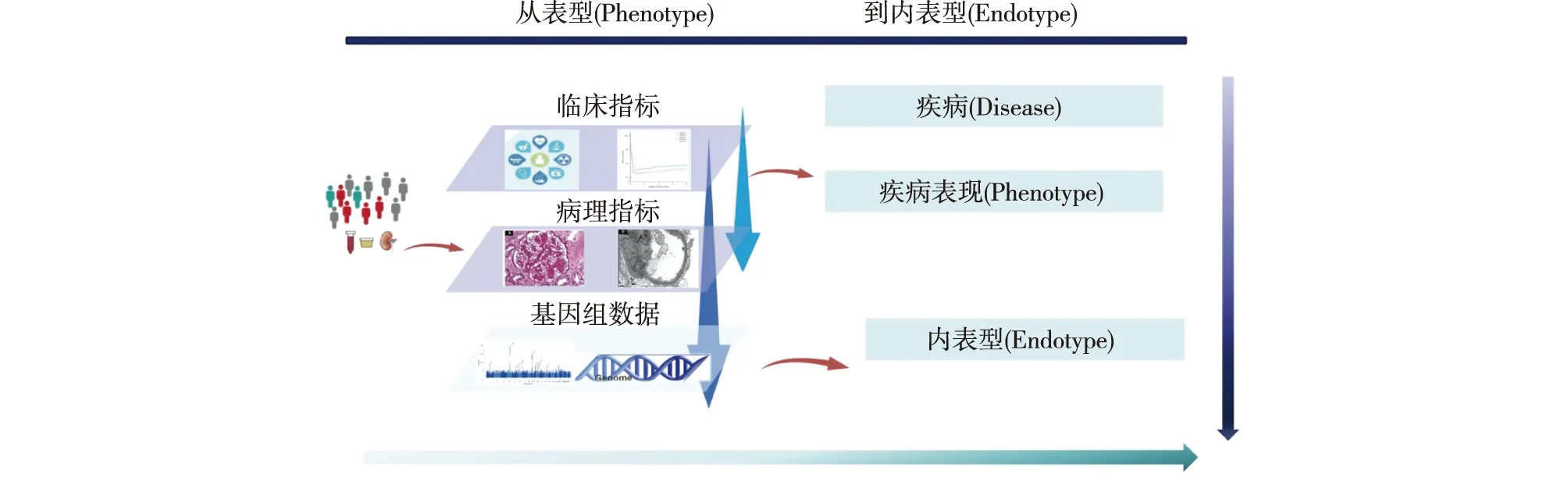
图3 临床表型与基因型的关联在人群中,可通过临床指标和病理指标定义疾病及疾病表型,而从基因组数据了解患者个体化的内表型,并探索基因型与临床表型之间的因果关联,可系统理解疾病的发生机制,并为认识及防治疾病提供指导
传统的观察性研究只能得到相关性的结果,而相关性不意味着因果关联。孟德尔随机化研究可以弥补传统流行病学研究的不足,利用与暴露因素具有密切相关的遗传变异作为工具变量,借助基因组数据推断暴露因素与研究结局之间的因果效应[33]。我们利用孟德尔随机化的研究方法探讨风险因素与糖尿病肾病之间的因果关系,遗传学证据显示BMI与糖尿病肾病之间存在正向因果关联。这为后续糖尿病肾病患者的管理提供重要参考。
近年来,人类疾病遗传性定量分析主要依赖于利用全基因组关联研究(genome-wide association studies,GWAS)来识别常见的遗传变异,而处于“后GWAS时代”的今天,基于疾病风险位点的功能学研究远落后于关联研究[34]。功能学研究包括疾病诊断、人群分层、药物研发、靶向治疗及预后预测等方面[35]。复杂性疾病,如糖尿病,往往是由多个微效基因以及多种环境因素共同导致疾病的发生[36]。基于GWAS构建的多基因风险评分(polygenic risk score,PRS)可以考量每一个遗传变异对表型的影响,并通过加权的方式对许多遗传变异进行综合计算,从而得到每一名患者的遗传风险得分,并对人群进行更加个体化的风险分层[37]。我们针对糖尿病无肾病以及糖尿病肾病患者,基于机器学习方法,从GWAS中筛选多个亚显著性位点(sub-significant SNP)来构建芯片,这项工作将有助于对糖尿病患者发生肾病的风险进行评估。
大规模基因型-表型的研究应包含遗传关联研究,然而,目前大多数的GWAS研究未将这种关联性联系起来,全表型组关联研究(phenome wide association study,PheWAS)[38-40]是GWAS研究的一种补充,其使用的基因型到表型的策略,从一种基因型开始,测试某种基因型与广泛的人类表型及表型组之间的关联性,是了解人类疾病复杂性的一种强大的补充方法。
未来基因组医学研究的新趋势是利用人工智能算法和生物信息学手段,将遗传学、表观遗传学、转录组学、蛋白质组学、代谢组学以及临床表型整合到GWAS研究中[41],这种数据时代的新范式将有利于对发病机制的理解,进一步推动精准医学的发展。
总之,医学研究已进入大数据和精准化并行融合时代,对数学模型,信息材料等理论和技术的依赖大幅提升,人工智能,单细胞图谱,基因组医学的交叉融合,催生了生命科学研究的新纪元。结合生物大数据以及人工智能,我们将能以更高的清晰程度评估人类健康,并构建表型性状与遗传特征的因果关联,为认识疾病本质和个体化防治提供系统的指导,最终重塑人类疾病诊疗体系。

