新生儿败血症相关性胆汁淤积症临床表现及危险因素分析
李惠芳,白岳飞
(1.铜川市妇幼保健院儿科,陕西 铜川 727000;2.西北大学附属神木医院新生儿科,陕西 神木 719300)
败血症是条件致病菌或致病菌侵入血液循环中并扩散和繁殖,释放代谢物与毒素,诱导细胞因子导致严重全身性感染和毒血症情况[1-2]。胆汁淤积症是外源性细菌感染或败血症常见并发症。由于宿主对感染出现免疫应答或细菌产物直接作用导致肝胆系统受到影响,最终影响胆汁分泌和排泄,使胆汁成分反流进入血液出现黄疸现象。相关研究[3-4]显示,败血症和胆汁淤积症具有一定联系,多见于新生儿,细菌感染与败血症占所有引起胆汁淤积症原因的20%左右,而黄疸在早产新生儿的发生率达到20%~60%。导致新生儿败血症相关性胆汁淤积症的原因以厌氧和需氧的革兰阳性与阴性细菌感染为主,多为革兰阴性菌感染。患儿原发部位多数在腹腔内,脑膜炎、心内膜炎、肺炎和泌尿道感染也可诱发胆汁淤积症[5]。鉴于新生儿败血症相关性胆汁淤积症形成原因复杂,临床治疗难度较大,本研究就新生儿败血症相关性胆汁淤积症临床表现与危险因素进行研究,旨在为新生儿败血症相关性胆汁淤积症临床诊治及预防提供参考意见,现报告如下。
1 资料与方法
1.1 一般资料 选取我院2017年10月到2020年10月收治的败血症新生儿100例,其中合并相关性胆汁淤积症38例(观察组),未合并相关性胆汁淤积症62例(对照组)。两组患儿一般资料对比均无统计学差异(均P>0.05),见表1。病例纳入标准:所有患儿均符合败血症诊断标准,且出现休克、腹胀、呕吐、呼吸窘迫、肝脾肿大、黄疸、反应低下、发热或体温不升、哭声低、烦躁不安或嗜睡以及进奶量少等临床表现[6];观察组患儿出现丙氨酸氨基转移酶(ALT)增高或正常,肝脾肿大≥3 cm或质地改变,大便颜色呈浅黄色到白色,血清总胆红素≥85.5 μmol/L[7]。排除标准:发病前无手术史和输血史;药物中毒引发的肝病;病毒性肝炎;代谢性疾病。所有患儿家属对本研究知情并签署同意书。本研究经我院伦理委员会批准。

表1 两组患儿一般资料比较
1.2 研究方法 依照无菌要求对所有患儿血液进行取样后进行细菌培养,应用法国生物梅里埃公司生产的VITEK2 Compact和半自动细菌鉴定仪ATB进行细菌检验,鉴定及药敏卡条均为法国Bio MerieuX公司生产,培养基为江门市凯林贸易有限公司提供,手工药敏纸片为英国Oxoid公司的药物敏感纸片。严格依照相关说明书进行操作。记录患儿出生胎龄、入院日龄、出生时体重、性别、肝功能障碍例数、死亡例数、败血症发作时间、住院天数、有无肠外营养支持、胆汁排秘系统发育是否完善等情况。对患儿入院后进行外周静脉血检测,分别测定患儿总胆红素、直接胆红素和血清内毒素水平。

2 结 果
2.1 两组患儿血液细菌培养结果 观察组38例患儿中血液细菌培养呈阳性者21例,其中大肠埃希菌8例,肺炎克雷伯菌6例,粪肠球菌4例,肺炎链球菌1例,金黄色葡萄球菌2例。对照组62例患儿中血液细菌培养呈阳性者26例,其中大肠埃希菌5例,肺炎克雷伯菌5例,金黄色葡萄球菌8例,表皮葡萄球菌3例,肺炎链球菌5例。
2.2 两组患儿肝功能障碍与病死情况比较 见表2。观察组患儿肝功能障碍及病死情况均高于对照组(均P<0.05)。

表2 两组患儿肝功能障碍与病死情况比较[例(%)]
2.3 败血症相关性胆汁淤积症危险因素单因素分析 见表3。两组患儿败血症发作时间和革兰阳性菌感染情况对比均无统计学差异(均P>0.05)。两组患儿住院天数、肠外营养、总胆红素、直接胆红素、胆汁排秘系统发育、革兰阴性菌感染、血清内毒素水平对比均有统计学差异(均P<0.05)。
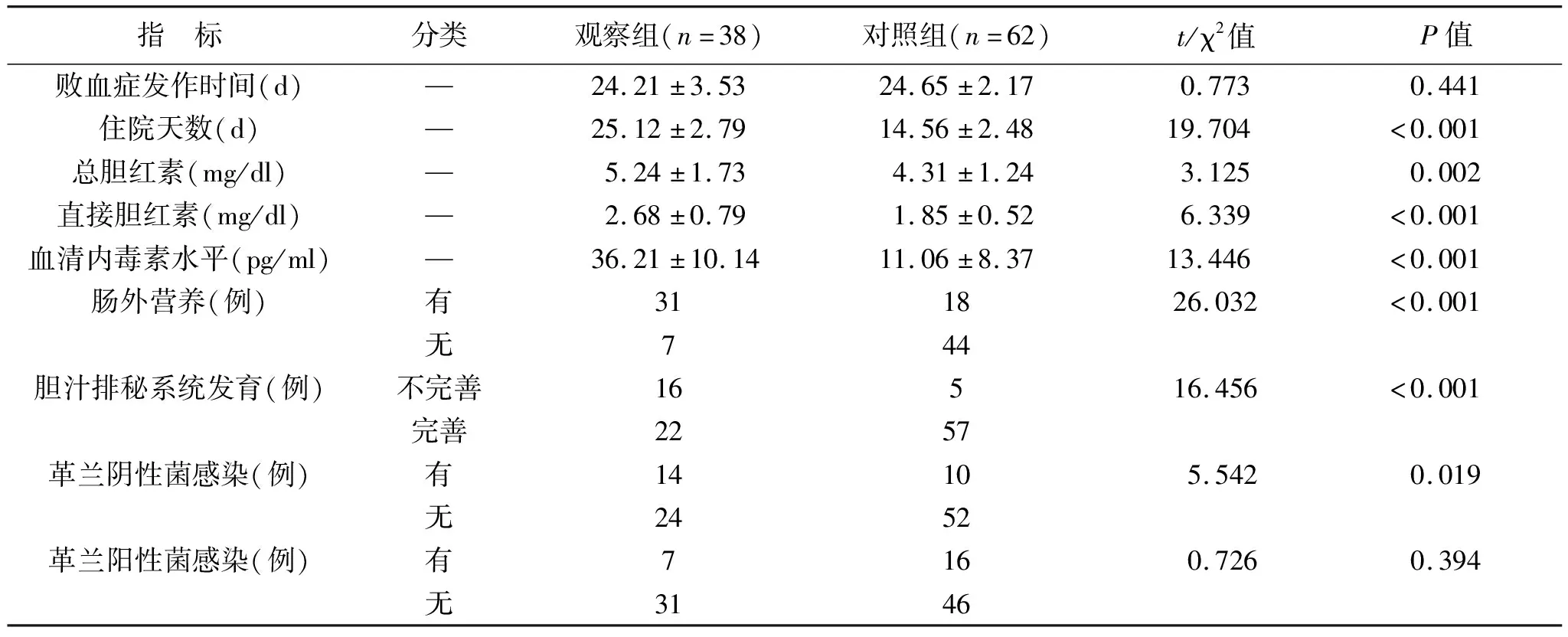
表3 败血症相关性胆汁淤积症危险因素单因素分析
2.4 败血症相关性胆汁淤积症危险因素Logistic回归分析 见表4。将是否发生败血症相关性胆汁淤积症作为因变量(是=1,否=0),以单因素分析具有统计学差异的指标为自变量,进行Logistic回归分析。自变量赋值:住院天数≥63.04 d=1,<63.04 d=0;总胆红素≥2.07 mg/dl=1,<2.07 mg/dl=0;直接胆红素≥14.76 mg/dl=1,<14.76 mg/dl=0;胆汁排秘系统发育不完善=1,完善=0;血清内毒素≥16.31 pg/ml=1,<16.31 pg/ml=0;有革兰阴性菌感染=1,无=0;有肠外营养=1,无=0。结果显示住院天数≥63.04 d、有肠外营养、总胆红素≥2.07 mg/dl、直接胆红素≥14.76 mg/dl、胆汁排秘系统发育不完善和血清内毒素≥16.31 pg/ml为败血症相关性胆汁淤积症的独立危险因素(均P<0.05)。

表4 败血症相关性胆汁淤积症危险因素Logistic回归分析
3 讨 论
当宿主自身免疫力抵不过致病因素的时候,会出现肝细胞受损、胆汁排秘受阻、胆红素代谢紊乱现象,从而出现黄疸[8]。临床研究[9]显示,肝脏中库普弗细胞占网状内皮系统固有组织巨噬细胞的80%~90%。库普弗细胞摄入脂多糖(LPS)、颗粒、细菌之后,会受到刺激释放一些与肝脏损伤相关的产物,如血小板激活因子、溶酶体酶、过氧化物、白细胞介素-6、白细胞介素-1以及肿瘤坏死因子等。而细菌直接入侵肝脏并不是发生败血症相关性胆汁淤积症或者干细胞损伤的主要原因,内毒素增加才是肝脏损伤的主要机制。研究[10-11]已证明,败血症发生过程中干细胞出现功能紊乱可能和炎性细胞因子释放相关。临床组织病理学认为,败血症相关性胆汁淤积症和其他原因所导致的胆内淤积并没有明显差别。但是有学者通过大量尸检和活检肝组织病理对比研究发现,在败血症相关性胆汁淤积症患者的扩张胆管内,胆汁浓缩情况比较突出,所以这类患者病死率比较高[12]。因此,对胆红素较高的败血症伴胆汁浓缩的患者,需要积极寻找病灶根源,从而提升治愈率,降低死亡现象的发生。
本研究结果表明,观察组38例患儿中血液细菌培养呈阳性者21例,对照组62例患儿中血液细菌培养呈阳性者26例,两组患儿细菌感染种类相似,由此证明败血症与败血症合并胆汁淤积症患儿都存在细菌感染现象,而且革兰阴性菌感染最为常见。相关研究[13]显示,引起败血症相关性胆汁淤积症的病原菌主要包含革兰阴性菌与革兰阳性菌,与本研究相符。
本研究中,观察组患儿肝功能障碍发生率和病死率均明显高于对照组。败血症患儿出现相关性胆汁淤积症之后,会出现重度全垂体功能减退、囊性纤维化、甲状腺功能减退等,从而增加患儿肝功能障碍发生率与病死率。两组患儿性别、出生胎龄、败血症发作时间和革兰阳性菌感染情况对比无统计学差异,但住院天数、肠外营养、总胆红素、直接胆红素、胆汁排秘系统发育、革兰阴性菌感染、血清内毒素水平对比均有统计学差异。因此,新生儿败血症相关性胆汁淤积症与住院天数、肠外营养、总胆红素、直接胆红素、胆汁排秘系统发育、革兰阴性菌感染、血清内毒素水平均具有明显相关性。研究[14-15]显示,多数败血症相关性胆汁淤积症与细菌感染、内毒素血症和胆汁排秘系统发育不完善有关。而败血症多由感染导致,因此肠外营养和住院天数均会增加患儿细菌感染概率,导致患败血症相关性胆汁淤积症的概率增加。败血症相关性胆汁淤积症患儿临床表现为总胆红素和直接胆红素升高现象。
本研究Logistic回归分析结果显示,住院天数≥63.04 d、有肠外营养、总胆红素≥2.07 mg/dl、直接胆红素≥14.76 mg/dl、胆汁排秘系统发育不完善和血清内毒素≥16.31 pg/ml为败血症相关性胆汁淤积症的独立危险因素。细菌感染导致胆汁淤积的因素很多,其中包括胆红素排泄障碍、干细胞功能障碍以及溶血引起的胆红素负荷增加等,一般在控制感染后黄疸就能够很快消退。如果患儿受到革兰阴性菌与革兰阳性菌感染,会通过细菌作用和免疫机制损伤红细胞而出现溶血现象,增加胆红素负荷。并且细菌感染过程中会在体内释放内毒素,影响干细胞基底膜有机阴离子运转蛋白和毛细胆管线粒体RNA加工酶2活性,引起胆红素排泄和摄入功能障碍,从而导致败血症相关性胆汁淤积症的出现[16]。因此,细菌侵入并不是败血症相关性胆汁淤积症的主要原因,非特异性内毒素增加才是导致肝脏损伤的主要原因。
综上所述,新生儿败血症相关性胆汁淤积症患儿多与细菌感染有关,细菌感染导致血清内毒素水平升高是合并胆汁淤积症的主要原因。胆汁排秘系统发育不完善、进行肠外营养和住院时间长也会增加新生儿败血症相关性胆汁淤积症的风险。败血症相关性胆汁淤积症新生儿会出现总胆红素、直接胆红素升高现象,导致肝功能障碍发生率与病死率增加。

