非酒精性脂肪性肝病合并2型糖尿病患者血清铁蛋白变化及其临床意义*
孙丽娜,顾 静
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)是慢性肝病的常见类型之一,包括单纯性脂肪肝、非酒精性脂肪性肝炎(non-alcoholic steatohepatitis, NASH)及其相关的肝硬化[1]。2型糖尿病(type 2 diabetes mellitus,T2DM)会导致NAFLD病情恶化,加重NASH和纤维化进展,增加肝细胞癌(hepatocellular carcinoma, HCC)的发生率[2]。铁是人体不可或缺的一种微量矿物质元素,但过量的铁可能刺激机体产生活性自由基,加速机体氧化应激的产生,引起血糖和脂质代谢紊乱,进而导致肝脏内脂肪进一步沉积[3]。铁蛋白是机体储存铁的主要形式,可以作为判断铁负荷是否过量的指标。本研究检测了NAFLD合并T2DM患者血清铁和铁蛋白(serum ferritin,SF)水平变化,现报道如下。
1 资料与方法
1.1 一般资料 2018年1月~2018年12月于华东疗养院体检的NAFLD患者163例(男性113例,女性50例,年龄56.7±9.3岁);NAFLD合并T2DM患者633例(男性559例,女性74例,年龄63.3±10.5岁);T2DM患者163例(男性129例,女性34例,年龄51.4±13.8岁)。T2DM诊断符合1999年WHO糖尿病诊断标准,NAFLD诊断符合2010年中华医学会肝脏病学分会脂肪肝与酒精性肝病学组修订的诊断标准。排除标准:酒精性、血吸虫病性和病毒性肝炎等明确病因引起的脂肪肝、恶性肿瘤和缺铁性贫血或有应用铁剂和急性炎症等可能影响人体铁负荷状态的因素。
1.2 检测与检查 空腹抽取静脉血,使用贝克曼Au5400生化分析仪测定血生化指标;使用普莱默斯Hbp210柔和层析法测定糖化血红蛋白(HbA1C);使用贝克曼DXI800电化学发光免疫分析法测定SF;使用胶乳免疫比浊法(积水医疗)测定超敏C反应蛋白(CRP)等;使用PHILIPS-iu22超声诊断仪行腹部检查。
2 结果
2.1 三组血清指标比较 NAFLD合并T2DM组血清SF水平显著高于T2DM组或NAFLD组,差异有统计学意义(P<0.05,表1),血清UA和CRP水平也显著高于T2DM或NAFLD组(P<0.05,表2)。

表1 三组血清指标比较

表2 三组血清指标比较
2.2 二分类Logistic多元回归分析情况 以是否合并T2DM为因变量,将男性比例、TG、UA、SF、ALT、AST、GGT和CRP作为自变量进行二分类Logistic多元回归分析,结果显示,血清SF和UA是NAFLD合并T2DM的独立预测因素(P<0.05,表3)。
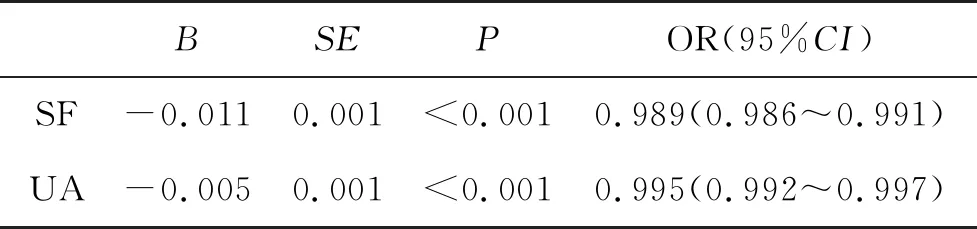
表3 影响NAFLD合并T2DM的二分类Logistic分析
3 讨论
本研究纳入NAFLD人群中T2DM患者,发现合并糖尿病者占比较高。既往研究数据显示,NAFLD患者容易发生T2DM[4]。研究显示,T2DM与NAFLD两者存在共同的发病机制,包括遗传因素、胰岛素抵抗、脂肪组织功能失调、高血糖导致的糖毒性、肠道菌群改变等。本研究发现NAFLD合并T2DM组SF水平相对于单纯T2DM组或单纯NAFLD组明显升高,提示铁代谢异常可能在T2DM和NAFLD的发生发展过程中起着重要的作用。Sumida et al[5]研究发现SF可以预测NAFLD患者脂肪性肝炎。韩国一项包含了2410名健康男性的前瞻性研究也发现,基线SF水平升高是肝脂肪变性的有力预测因子[6]。可能的机制包括铁催化的羟自由基形成使机体氧化应激水平增加,可能导致全身胰岛素抵抗。胰岛素抵抗通过激素敏感脂肪酶增强脂肪组织中甘油三酯的脂解作用,导致了大量游离脂肪酸在肝脏内堆积[7],而代偿性的高胰岛素血症和相对高血糖又促进肝脏的新生脂肪生成和胆固醇的合成,并通过氧化反应减少游离脂肪酸的分解代谢,从而导致了NAFLD的发生和发展[8]。此外,铁在肝脏内的沉积加剧了氧化应激反应,后者消耗ATP、NAD和谷胱甘肽,直接损伤肝细胞内DNA、脂质和蛋白质,从而导致细胞死亡[9]。
Mateo-Gallego et al[10]发现,在家族性高脂血症和高胆固醇血症患者中SF水平升高。Oshaug A[11]发现高铁储存者血清TG水平显著高于低铁储存者,其机制可能是铁储备过高可以影响胰岛素的合成和分泌,引起糖代谢紊乱,从而影响患者的脂质代谢,导致血清TG和TC升高,而HDL-C下降[12]。SF水平升高还与CRP存在显著的相关性,推测SF可能通过炎症因子加重胰岛素抵抗,引起糖脂、嘌呤等代谢紊乱,最终引起血糖、血脂和尿酸的升高。研究发现铁代谢可能与NAFLD严重程度呈正相关,其机制考虑SF升高程度与肝脏脂肪含量相关。
本研究经二分类Logistic多元回归分析显示,SF和UA是NAFLD合并T2DM的独立预测因素。目前,已有大量研究表明,肝脏中铁的蓄积可能导致代谢失衡和肝脏损害。过量铁沉积、炎症信号(IL-6)或内质网应激等多种刺激可能导致铁调素过度表达,从而导致巨噬细胞和肝细胞中铁的滞留增加[13]。有人在前瞻性研究中证实了血清UA是NAFLD发生的独立危险因素[14]。研究还显示,血清UA与NAFLD之间呈线性反应效应,即血清UA每升高1 mg,会导致NAFLD发生风险增加21%[15]。高尿酸血症可能通过加重胰岛素抵抗,激活氧化应激反应和破坏NLRP3炎症小体等机制促进了NAFLD的发生及发展[16]。
综上所述,血清铁蛋白的升高与NAFLD人群发生2型糖尿病存在相关性,血清铁蛋白水平可能可以作为肝脏损伤的预测因子和潜在的治疗靶点。但本研究作为一项横断面研究不能推断出两者的因果关系,且其相关病因及机制较为复杂。因此,我们需要开展更多的临床试验和基础研究来进一步探究。

