半焦催化裂解煤热解焦油模型化合物的研究
韩江则,侯娟敏,薛志伟,李昆杰,赵瑞红,许永权
(河北科技大学 化学与制药工程学院,河北 石家庄 050018)
煤是我国主要的化石能源,然而在煤炭的常规利用过程中产生的焦油严重降低了煤炭利用率[1-2]。煤焦油成分复杂,通常可采用催化裂解的方法将其转化为低沸点的高品质油气[3]。煤热解制得的半焦价低易得、孔隙结构丰富且其所含的金属矿物质都有利于对焦油的裂解[4-7]。因此,采用其作为催化剂用于煤热解焦油的催化裂解具有重要意义,已引起越来越多的关注[8-10]。
本文采用环己烷、正庚烷和甲苯作为焦油的模型化合物,分别代表焦油中的环烃、链烃和芳香烃,考察不同半焦对其催化裂解效果,揭示半焦催化裂解焦油组分的原理。
1 实验部分
1.1 材料与仪器
内蒙褐煤;甲苯、环己烷、正庚烷均为分析纯。
Philips PW 1710型X-射线衍射仪;JSM-7001F扫描电子显微镜;GENESIS能谱仪;NOVA2000型全自动比表面积和孔隙度分析仪;Agilent 3000A气相色谱仪;WQF-510型傅里叶变换红外光谱仪。
1.2 催化剂制备
将内蒙褐煤粉碎、筛分后选取粒径为0.5~1 mm部分作为实验原料。将其在800 ℃氮气气氛下,热解1 h制得实验中采用的催化半焦(C-800)。不同表面结构的半焦催化剂采用水蒸气活化法制备。上述条件所制得的半焦在800 ℃下采用水蒸气(活化每克原料半焦的水蒸气供应量为0.04 g/min),分别活化5~60 min,最终产品分别用AC-5,AC-10,AC-15,AC-30,AC-60表示。
1.3 实验方法
实验流程见图1。反应开始之前向反应管内加入一定量的半焦催化剂,同时将氮气流量调整为100 mL/min,吹扫30 min,以排出反应装置内的空气。之后打开装置进行加热,待达到反应温度后,开始进料。控制焦油模型化合物的进料速率为0.5 mL/min。 液相焦油模型化合物先进入200 ℃的汽化器汽化后,在350 ℃的预热器内与载气混合,进入反应装置发生裂解反应。反应后的液体组分经过冷凝后收集称重,气体用排水法测定气体的体积,整个过程反应时间40 min。

图1 实验流程图Fig.1 Schematic diagram of the adopted experimental apparatus1.恒流泵;2.汽化器;3.预热器;4.电炉;5.热电偶;6.冷凝器;7.气液分离器;8.气体收集瓶;9.量筒
1.4 分析表征
实验中所采用的半焦催化剂采用X-射线衍射仪进行晶相分析。测试条件为铜辐射源λ1为0.154 060 nm,λ2为0.154 439 nm,仪器工作电压为40 kV,电流为30 mA,扫描速率0.42 ℃/s,从10~90°(2θ)对样品进行扫描。催化剂的表面形貌结构采用扫描电子显微镜测试,其表面元素组成采用X射线衍射仪进行测试。不同催化剂表面的金属种类及含量采用能谱仪进行分析。不同半焦的比表面积、孔径、孔容等采用全自动比表面积和孔隙度分析仪(BET)测定,半焦的比表面积由BET方法得到,孔径分布采用BJH方法拟合得到,微孔面积采用 t-法进行拟合。裂解后的气体产物采用气相色谱进行检测分析气体中H2、CH4、N2等含量。液体产物采用傅里叶变换红外光谱仪检测。
本文采用液体收率(%,质量分数)和气体收率(mL/g)等参数考察最终实验结果,具体计算方法分别由式(1)~(2)计算得到。
(1)
(2)
式中W和WL——液体进料量和液体产物的质量,g;
V——热解气的体积,mL。
2 结果与讨论
2.1 不同活性半焦基催化剂对模型化合物催化裂解的影响
制备的不同半焦的表面结构参数见表1。

表1 不同活化时间所得半焦的比表面积和孔径分布Table 1 Pore and surface properties of char prepared from different active time
由表1可知,半焦的比表面积随着水蒸气对其活化时间的延长逐渐增加,且总的孔体积和平均孔径均逐渐增大。但当活化时间超过15 min后,半焦比表面积的增加量逐渐减少,其平均孔径达到介孔范围。此时,可能是由于活化时间的延长,半焦中的微孔逐渐坍塌致使其中更多的微孔向介孔转化。
在反应温度为600 ℃,催化剂用量为5 g,焦油模型化合物为环己烷的条件下。考察不同催化剂对产物气相产品和液体收率的影响,其变化趋势见图2。


图2 不同半焦催化剂对焦油模型化合物催化裂解效果的影响Fig.2 (a) Liquid and gas yield and(b) gas composition varying over different catalysta.气体产率和液体收率;b.不同气体组成
由图2a可知,不同活化半焦对焦油的催化裂解能力有所区别。随着活化时间的增加,液体收率逐渐降低,气体收率逐渐提高;当半焦的活化时间超过15 min后气体收率的增加幅度逐渐较小。由表1可知,随着活化时间的增加,半焦表面的孔道结构更加发达,有利于延长环己烷在其上的停留时间,促进裂解反应的发生。当半焦的活化时间超过15 min后,其表面的孔径逐渐增大,环己烷分子和生成的中间态产物在半焦上的扩散阻力减小,停留时间相应降低,因此裂解反应发生的概率相应减小。图2b描述的是环己烷经半焦作用后所得气体中H2和CH4收率的变化情况。由图2b可知,所得气体中的H2一直处于增加趋势,CH4也大致为增加趋势,尤其是经过催化半焦AC-15,AC-30和AC-60的作用。产品气体中的H2主要来源于裂解过程中的脱氢反应和甲烷裂解反应,CH4主要来源于裂解过程中产生的甲基自由基与氢自由基的相互结合。随着半焦活化时间的增加,不仅使半焦表面的孔道结构逐渐打开,同时半焦内所含的具有催化活性的碱金属和碱土金属组分逐渐暴露出来,从而促进焦油裂解反应的发生,产生更多的气体组分。
2.2 半焦对不同焦油模型化合物催化裂解的影响
采用5 g AC-15催化剂,考察其在600 ℃下对不同焦油模型化合物的催化裂解效果,结果见图3。


图3 AC-15催化半焦对不同焦油模型化合物催化裂解效果的影响Fig.3 (a) Liquid and gas yield and(b) gas composition of different model compounds over the AC-15 catalysta.气体产率和液体收率;b.不同气体组成
由图3a可知,AC-15对3种焦油模型化合物皆有一定催化裂解能力,但对不同焦油模型化合物的裂解能力有所不同。其中,裂解正庚烷、环己烷和甲苯所得的液体产量依次增加,而气体的收率依次降低。由图3(b)可知,正庚烷裂解所得气体中H2和CH4的产率最大,甲苯裂解所得气体中H2和CH4的产率最小。说明AC-15对正庚烷的裂解能力最强,对甲苯的裂解能力最弱。这是因为组成甲苯的甲基和苯环之间形成了一个稳定的共轭体系,最终使得甲苯的裂解需要更多的能量,与环烷烃相比饱和链烃正庚烷更容易被裂解。
2.3 催化剂的XRD表征
对实验所采用的半焦(C-800)和活化半焦(AC-15)催化剂采用XRD进行晶相分析,结果见图4。

图4 不同半焦基催化剂的XRD分析Fig.4 XRD spectra of the char catalysts
由图4可知,半焦的主要衍射峰为(10)和(002),其中(10)衍射峰反映芳香环的平面结构,(002)衍射峰反映焦炭微晶中芳香层的堆积程度。活化后半焦的(10)峰和(002)峰的衍射强度均有所增强,说明碳微晶结构向有序化方向发展。
2.4 催化剂的形貌分析
对实验所用催化剂的表面相貌及元素组成由SEM-EDS进行分析,结果见图5和表2。

图5 SEM-EDS对两种催化剂的表面形貌分析Fig.5 Surface topographies analysis of SEM-EDS for the char catalystsa.C-800;b.AC-15

表2 SEM-EDS对两种催化剂的元素组成分析Table 2 Surface topographies and element composition from SEM-EDS for the char catalysts
由图5可知,活化前半焦的结构紧密,表面平整;活化后半焦的表面质地疏松,空隙结构丰富,且大孔结构明显。因为水蒸气会与焦炭发生反应产生小分子气体,进而产生一系列孔道,最终使其比表面积增大。由EDS分析结果(表2)可知,不同半焦催化剂表面的主要元素为C元素,由于灰分的存在,还有一定量的Fe、Mg、Ca、Na、K等金属元素,且活化后的AC-15催化剂表面活性金属含量得到较大提高。这是由于半焦表面的碳与水蒸气的反应会使其内部的金属物质暴露出来,暴露出来的碱金属和碱土金属对焦油组分有一定的催化裂解作用,从而提高其对焦油组分的催化裂解能力[11]。
2.5 AC-15催化剂催化裂解正庚烷、环己烷、甲苯机理分析
图6描述了不同焦油模型化合物在600 ℃,5 g AC-15催化剂作用下所得产物的红外分析图。



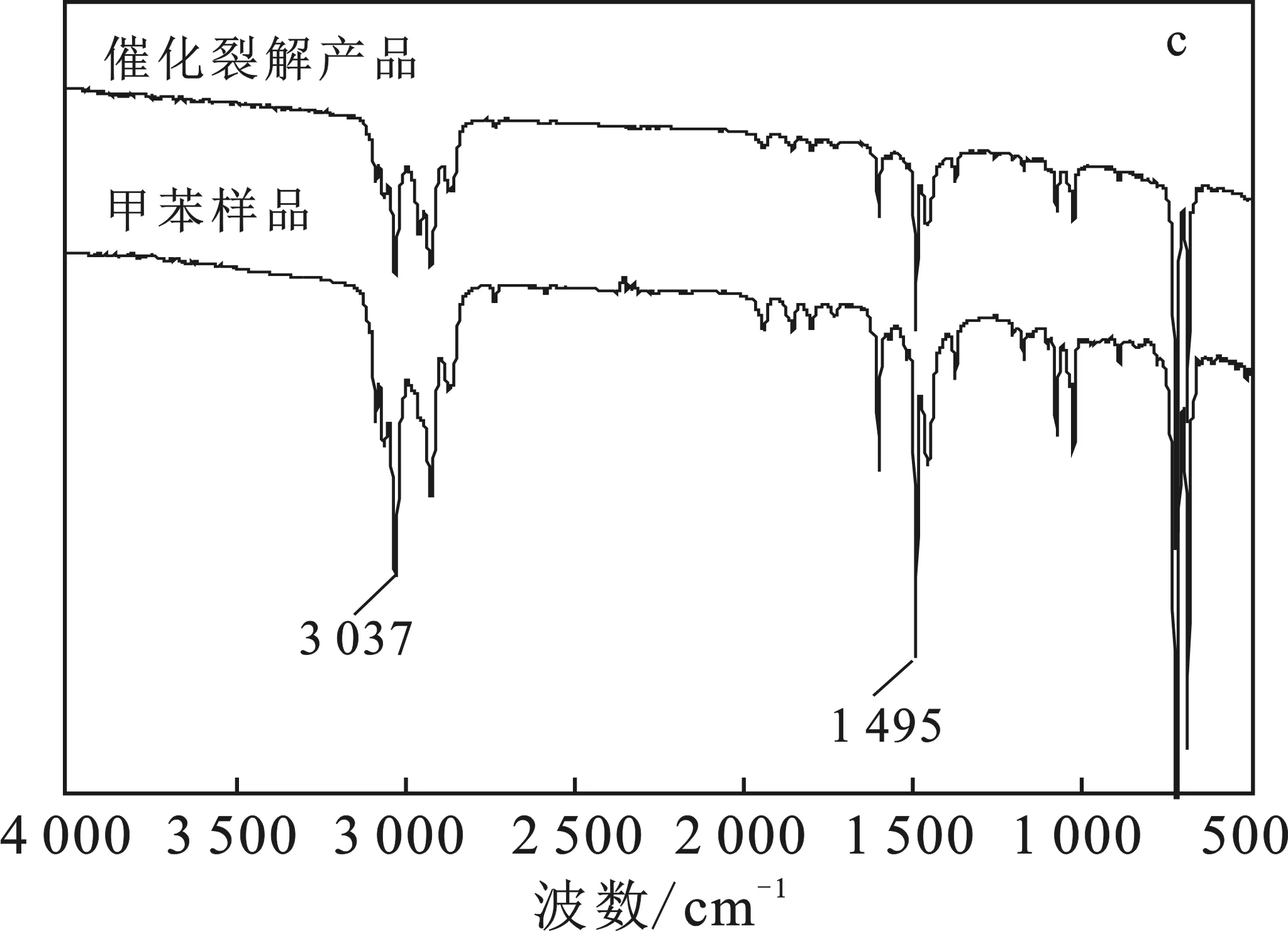
图6 不同焦油模型化合物催化裂解产物的红外分析图Fig.6 FTIR spectra for the catalytic products over AC-15 catalyst
3 结论
本文采用正庚烷、环己烷、甲苯3种模型化合物分别代表生物质焦油中的链烃、环烃、芳烃组分,并在固定床反应器内分别考察了半焦基催化剂对这3种不同的焦油模型化合物的催化裂解效果,得到如下结论:
(1)水蒸气活化后的半焦具有更丰富的孔道结构,且其表面暴露出更多的碱金属和碱土金属物质,从而使其对焦油组分的催化裂解能力增强。
(2)AC-15催化剂对3种不同的焦油模型化合物的裂解能力由强到弱依次为正庚烷、环己烷、甲苯。这是因为相对于链烃,环烃的结构相对稳定;而甲苯由于共轭效应的存在使其难以被裂解。
(3)采用红外光谱仪对3种不同模型化合物经AC-15催化剂作用后所得产物的分析可知,环己烷主要发生了开环反应,正庚烷主要发生了脱氢反应,甲苯被裂解产物的芳香性有所下降,最终生成一系列链烃化合物。

