手外伤感染创面修复治疗中封闭式负压引流技术的应用价值分析
胡建威 吕丰
手外伤是临床常见外科损伤类型,包括手部皮肤、软组织、肌肉、肌腱等组织损伤。由于手外伤可造成组织外露或缺损,暴露于空气中或受到外部刺激,容易并发局部感染、组织坏死,严重者甚至发生局部功能缺陷和外观形态缺损,临床治疗颇为棘手[1]。现代医学认为,手外伤感染治疗的关键在于处理手外伤创面及控制感染,若未得到及时有效的治疗,甚至可发生骨髓炎和全身急性感染[2]。以往临床多采用清创、换药、对创面充分引流等方法进行治疗,以清除感染及坏死组织,促进创面的修复。但对于创面较大、伤口较深者,常无法彻底引流,导致组织深部感染清除不彻底,进而增加了二次手术风险[3]。VSD 是目前临床常用的创面负压引流系统,能够给创面创造一个封闭的环境,能持续引流,预防和控制感染,并给创面提供湿润环境,能加快肉芽组织生长,促进创面愈合,达到显著治疗效果[4]。本研究进一步分析手外伤感染创面修复治疗中VSD 的应用价值,现报告如下。
1 资料与方法
1.1 一般资料 将2020 年1~12 月在本院外科治疗的94例手外伤感染患者,随机分为观察组与对照组,各47例。观察组男30例,女17例;年龄22~58 岁,平均年龄(36.4±9.3)岁;损伤部位:手背11例、手掌14例、手指22例。对照组男31例,女16例;年龄22~58 岁,平均年龄(36.4±9.3)岁;损伤部位:手背10例、手掌13例、手指24例。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。纳入标准:所有患者均符合《外科学》[5]中手外伤感染诊断标准;检查可见手部有开放性软组织损伤,创面伴有炎性或脓性渗出,伤口周围红肿、压痛,创面分泌物细菌培养为阳性;X 线检查显示无骨折,缺损面积在(4 cm×3 cm)~(12 cm×7 cm),平均缺损面积7 cm×5 cm。排除标准合并其他部位外伤;合并糖尿病;结缔组织疾病;治疗依从性差等。
1.2 方法 对照组使用传统每日换药处理,彻底清创,清除炎性及坏死组织,用庆大霉素生理盐水冲洗创面,涂抹红霉素软膏,2 次/d,皮维碘纱布外敷,换药2 次/d,待肉芽组织生长良好后行手术治疗,进行植皮或皮瓣二期修复[6]。观察组使用VSD 治疗,清洗创面,消毒后清除变性、坏死的组织,根据创面裁剪VSD 敷料,安装VSD 引流装置,用生物贴膜紧密包贴钉道口,确保VSD 敷料充分贴合创面,不留缝隙,负压吸引确定装置无漏气、工作正常后,结束手术;术后持续负压吸引,根据创面细菌培养结果选择敏感性抗菌药物,3~5 d 后再次评估病情,查看创面肉芽组织生长情况,决定是否再用VSD 敷料覆盖创面,一般引流8 d,定期更换敷料[7]。
1.3 观察指标及判定标准 比较两组创面修复优良率、治疗时间、各项治疗指标、并发症发生情况及治疗前后VAS、QOL 评分。创面修复判定标准:优:肉芽组织生长良好,碰触易出血,1 周内可进行植皮手术,术后无感染,2 周内拆线,创面愈合良好;良:肉芽组织生长尚可,碰触易出血,治疗1 周后才可进行植皮手术,术后无感染,2 周后拆线,创面愈合尚可;差:肉芽组织生长少,碰触不易出血,治疗2 周后才进行植皮手术,术后发生感染,2 周后才拆线,或创面愈合不佳,需要二次手术[8]。优良率=优率+良率。治疗时间包括抗感染药物使用时间、创面愈合时间、住院时间;各项治疗指标包括一周愈合率、日引流量、换药次数、二次手术、二期植皮时间;并发症包括创面化脓、伤口异常疼痛、创面不愈合;VAS 评分越低疼痛越轻,QOL 评分越高生活质量越高。
1.4 统计学方法 采用SPSS21.0 统计学软件处理数据。计量资料以均数±标准差()表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 两组创面修复优良率比较 观察组创面修复优良率为95.74%,高于对照组的74.47%,差异有统计学意义(P<0.05)。见表1。

表1 两组创面修复优良率比较[n,n(%)]
2.2 两组治疗时间比较 观察组抗感染药物使用时间、创面愈合时间、住院时间均短于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组治疗时间比较(,d)

表2 两组治疗时间比较(,d)
注:与对照组比较,aP<0.05
2.3 两组各项治疗指标比较 观察组一周愈合率、日引流量高于对照组,换药次数、二次手术率低于对照组,二期植皮时间短于对照组,差异均有统计学意义(P<0.05)。见表3。
表3 两组各项治疗指标比较[n(%),]

表3 两组各项治疗指标比较[n(%),]
注:与对照组比较,aP<0.05
2.4 两组并发症发生情况比较 观察组并发症发生率低于对照组,差异有统计学意义(P<0.05)。见表4。
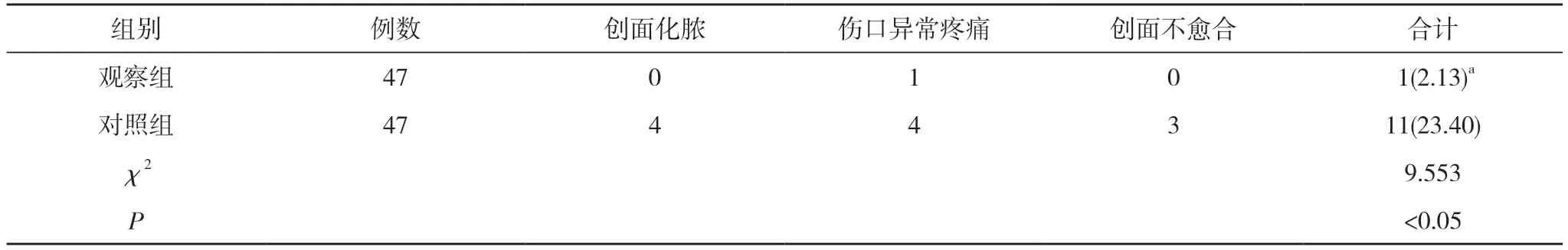
表4 两组并发症发生情况比较[n,n(%)]
2.5 两组治疗前后VAS、QOL 评分比较 治疗前,两组VAS、QOL 评分比较,差异无统计学意义(P>0.05)。治疗后,观察组VAS、QOL 评分均优于对照组,差异有统计学意义(P<0.05)。见表5。
表5 两组治疗前后VAS、QOL 评分比较(,分)
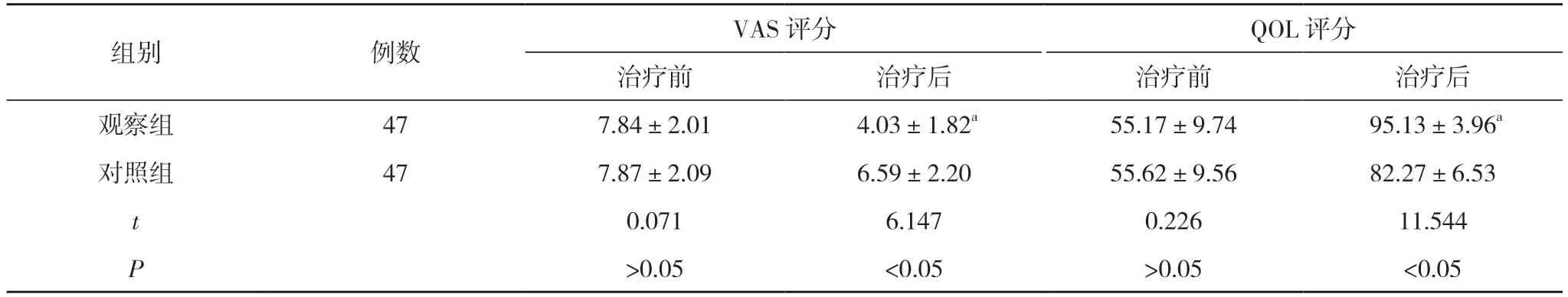
表5 两组治疗前后VAS、QOL 评分比较(,分)
注:与对照组治疗后比较,aP<0.05
3 讨论
手外伤在外科较为常见,复杂手外伤往往伴有皮肤撕脱、软组织及肌腱损伤,导致病原菌容易侵袭而发生创面感染[9]。因此,手外伤创面感染在临床的发病率较高,不仅明显增加了治疗难度,延长创面愈合时间,而且影响手部功能,需要临床给予早期、及时的干预治疗。
手外伤创面感染的处理较为棘手,以往传统换药治疗在清创、用药后用皮维碘纱布外敷,需要每日更换外敷敷料,这使得创面暴露于外界空气中的机会较多,且对创面较大、伤口较深的治疗困难,无法充分引流深部分泌物,需要辅助其他引流工具进行处理,如引流条、引流管等,容易发生引流管堵塞、引流不畅的问题,导致引流不彻底,无法有效清除感染组织及分泌物,增加了二次感染的风险,不利于创面的愈合,使得二次手术几率升高[10,11]。
VSD 是一种封闭负压引流装置,通过将创面密闭于VSD 敷料装置中,进行持续负压吸引,可为创面创造一个完全封闭、湿润的环境,不仅能促进创面渗出液的充分引流,减轻水肿,清除并排出部分坏死组织,彻底清除创面残留的细菌,而且能为创面修复提供适宜的微环境,保持创面局部微湿状态,隔绝创面与外环境之间联系,杜绝感染风险,从而促进创面肉芽组织的生长,加快创面愈合速度,提高创面愈合效果[12]。此外,VSD 还可改善局部血液循环,泡沫敷料与创面症见形成机械应切力,能改变细胞形态和功能,促进新生血管,增进创面供血和供氧,也有助于创面的修复[13]。
与传统引流管相比,VSD 能够在封闭空间内持续负压引流,不受体位约束,也无需经常换药,且采用医用薄膜材料包裹引流管,管腔不易阻塞,能保持较长时间的引流通畅,解决了传统换药、引流所致的引流不彻底、容易再次感染的问题,显示出了较为明显的优越性[14]。同时,VSD 使用生物半透膜封闭创面,具有较好的生物学特性,能使创面与外界形成一道屏障,有效减少外界细菌的侵袭,防止二次感染,还能持续清除创面内部的分泌物和感染组织,吸尽坏死组织,杜绝细菌毒素的滋生,保持创面清洁环境,防止局部炎症引起全身炎症反应[15]。再者,封闭式负压引流可促进创面组织向中心靠拢,减少创面面积,使创面局部环境更加接近生理的湿润状态,还能减少抗生素使用时间,提高创面愈合效果[16]。最后,VSD 属于纯物理治疗技术,有效避免了化学药物治疗的弊端,操作简单易行,对手术条件的要求不高,也避免了患者频繁换药的痛苦,减轻了创面的疼痛感,有助于提升患者的躯体舒适度和生活质量[17,18]。但临床应用VSD 时应注意:①早期合理应用;②彻底清创,不留死腔,重建血运;③术后积极抗感染;④虽然VSD 应用优势明显,但该方法仅能作为过渡治疗手段,最后还需进行二期植皮手术治疗[19,20]。
本研究结果显示,观察组创面修复优良率高于对照组,差异有统计学意义(P<0.05)。观察组抗感染药物使用时间、创面愈合时间、住院时间均短于对照组,差异有统计学意义(P<0.05)。观察组一周愈合率、日引流量高于对照组,换药次数、二次手术率低于对照组,二期植皮时间短于对照组,差异均有统计学意义(P<0.05)。观察组并发症发生率低于对照组,差异有统计学意义(P<0.05)。治疗后,观察组VAS、QOL 评分均优于对照组,差异有统计学意义(P<0.05)。充分证明VSD 应用于手外伤感染创面的治疗获得了良好的效果,能充分引流,消除炎性渗出及坏死组织,刺激肉芽组织生长,明显缩短了治疗时间,降低了二次手术率和并发症发生率,减轻了患者的疼痛感,是一种较为理想的治疗方式。
综上所述,手外伤感染创面修复治疗中VSD 的应用价值确切,感染控制效果好,创面愈合质量高,愈合速度快,并发症发生率低,值得在临床推广使用。

