含能材料合成中的氮链扩增方法
朱 勇,丁可伟,2,肖 川,李陶琦,卜建华,刘 卫,郭松松,葛忠学,2
(1.西安近代化学研究所,陕西 西安 710065;2.氟氮化工资源高效开发与利用国家重点实验室,陕西 西安 710065;3.中国兵器科学研究院,北京 100089)
引 言
全氮材料是一类由氮原子构成的材料,基于氮氮单键(159kJ/mol)、双键(419kJ/mol)和三键(946kJ/mol)之间的平均键能差,由单键或双键组成的全氮材料分解为三键的氮气时伴随着巨大的能量释放[1-4]。与传统的能源材料相比,全氮材料具有高密度、高生成焓、超高能量水平及分解产物清洁无污染等优点。因此全氮材料有望作为新一代超高能材料的候选,在航空航天、武器装备等领域具有广阔的应用前景[5-6]。
全氮材料的制备是一项涉及多学科、多方法的综合性工程[7-11],但化学合成是其中重要的途径或环节。诺贝尔化学奖得主Sharpless教授说化学的核心或本质就两件事:一是CONNECTIONS(连接);二是FUNCTIONS(功能)[12]。目前理论预测了很多具有超高能量密度“功能”的全氮化合物[13-18],但却少有将氮结构单元或原子“连接”成目标化合物的方法。因此,氮氮键成键方法是目前该领域研究的重点。借鉴已有的成键反应,开拓全氮结构的合成方法和理论,分析反应机理,认识产物的稳定规律,逐步形成并完善全氮结构的构建策略。

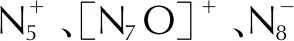
1 氮-卤键叠氮取代反应
叠氮基(R—N3)对N原子上卤素(N—X)的取代反应是合成N—N单键的最常见反应之一,但目标产物的稳定性受底物结构的影响很大,因此这类反应的成功案例并不多见。


图的合成路线

1.2 [N3NFO]+的合成
早在1968年,Christe等[32-34]就发现在F3NO和BF3、AsF等路易斯酸形成的复合物中存在F2NO+离子,并对F2NO+离子进行了详细研究。N5+的成功合成促使人们继续探索HN3与这类离子的反应,2007年,Wilson等[35]发现在-45℃到室温的范围内,[NF2O][SbF6]在无水HF溶液中能和HN3按1∶1化学计量比发生反应,[NF2O]+上一个氟原子被叠氮基取代,生成[N3NFO][SbF6],如图2所示。[N3NFO]+在常温下有一定的稳定性,以一对平面型的顺反异构体形式存在,异构体间能量相差不大。

图2 [N3NFO]+的合成路线
1.3 [N7O]+的合成探索
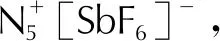

图3 [N7O]+的形成与分解

图4 [N7O]+的分解机理
2 叠氮离子电催化氧化反应


图电催化氧化的装置及可能的机理
3 伯胺重氮转移反应

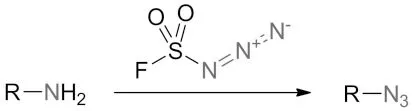
图6 FSO2N3的重氮转移反应
4 氮烯二聚反应
氮烯是一类具有—N=N—、—N=N—N或—N=N—N=N—结构的分子,和烯烃在碳骨架构建中的广泛应用相比,目前氮烯在氮骨架合成中的研究很少。Wiberg[38]于1968年用三(三甲基硅基)肼锂合成了双三甲基硅基二亚胺(BSD),如图7所示,发现其具有极强的反应活性[39]。如图8所示,BSD可以完全或部分进行电子交换,快速完成氧化还原或路易斯酸碱反应,还可以接受自由基。BSD是首个发现的全被硅基取代的二亚胺,由于硅基极易通过N—Si键的酸解而脱去,因此,该类反应在氮骨架构建中有潜在的应用。

图7 BSD的合成路线

图8 BSD可能发生的反应
BSD一般需要在低温、无水无氧环境下处理。0℃以下就能以歧化、二聚和自由基等反应机理分解。其中二聚反应能生成四(三甲基硅基)四氮烯[40],如图9所示。该反应成功将直链氮原子个数由二延伸至四个。西安近代化学研究所丁可伟等[41]用15N标记的对甲苯磺酰叠氮研究了BSD的形成机理,发现叠氮基与肼锂上的锂氮反应,形成长链N5结构,然后分解放出氮气,并消去三甲基硅基-对甲苯磺酰氨基锂形成氮氮双键。对甲苯磺酰叠氮起到了温和氧化的作用,使N—N单键生成N=N双键,而不直接氧化成N≡N三键(即氮气)。进一步的量化计算表明,BSD先异构化为1,1-二(三甲基硅基)二氮烯中间体,然后两个该中间体相互作用形成四(三甲基硅基)四氮烯。
将四(三甲基硅基)四氮烯溶于二氯甲烷中,于-78℃用三氟乙酸处理,可得无色的四氮烯(N4H4)固体[28],如图10所示。与常见氮氢二元化合物、氨(NH3)、肼(N2H4)、二亚胺(N2H2)和叠氮酸(HN3)相比,四氮烯将氮原子构成的直链骨架拓展到了4个。

图10 N4H4的合成路线
5 氨基化及硝化反应
在高氮杂环类化合物的N原子上引入氨基,可以改善一些含能化合物的稳定性[42],且由于增加了N—N单键而提高其能量性能[43],而且,氨基官能团的引入可进一步开展衍生化反应。因此,含N—NH2基团的唑类化合物是重要的含能化合物或其前体化合物。
2012年,Thomas等[43]用羟氨磺酸对含能阴离子进行N—NH2化反应,获得了一系列高性能的中性N—NH2化产物。进一步将该策略扩展到中性的1,5-二氨基四唑,通过羟氨对甲苯磺酸等试剂,合成了1,4,5-三氨基四唑盐[22],如图11所示。1,4,5-三氨基四唑阳离子氮含量达到80%,进一步与硝酸根、5-硝基四唑-2-氧化物阴离子等组合能制备含能离子盐。2012年,Thomas等[29]通过在1-氨基三唑的N3位上引入氨基,合成了1,3-二氨基-1,2,3-三唑阳离子,进一步将其与5-硝基四唑-2-氧化物、5,5′-联(1-氧化四唑)、5,5′-偶氮联(1-氧化四唑)、硝氨基四唑等阴离子组合成含能离子盐[44]。该类高氮化合物由于具有高生成焓、低温室气体排放在火炸药中有重要潜在用途。

图11 氮杂环的N氨基化反应
对氨基进行硝化,既能延长氮链,也能进一步增加化合物的能量密度。2012年,Thomas等[29]将1,3-二氨基-1,2,3-三唑进一步硝化,合成了1,3-二硝氨基-1,2,3-三唑盐,如图12所示,具有7个氮原子直接相连的氮链。该氮链中氮原子上正负电荷交替存在,可能是使该氮链稳定存在的重要因素。

图12 氮杂环上N—NH2的硝化反应
6 氨基氧化偶联反应
氨基的氧化偶联是制备偶氮的常用方法,也是延长氮链的常用手段,尤其是N—NH2的偶联反应,可以用来构建四氮烯结构。偶氮连接基团的引入不仅能大幅提升化合物的生成焓,还能降低某些化合物的感度[45-46]。偶联反应氧化剂、溶剂等的选择都对反应有明显影响。
6.1 酸性氧化剂
1985年,Neunhoeffer等[47-48]将1-氨基吡唑经NiO2及AcOH处理后,意外得到偶联产物1,1′-偶氮吡唑,如图13所示,其N6链结构很快引起人们关注。随后,Nanvyan等[49-51]以Pb(OAc)4为氧化剂,对含不同取代基的1-氨基苯并咪唑的偶联反应进行了系统研究。

图13 氨基吡唑的氧化偶联
1974年,Glover等[52]将3-甲基-1-氨基-苯基三唑盐用饱和溴水氧化,获得了3,3′-二甲基-1,1′-偶氮-苯基三唑盐,如图14所示,构建了N8链结构,但该化合物含有大量非含能基团。2007年,北京理工大学庞思平教授课题组用二氯异氰尿酸钠(SDCI)和乙酸,先后合成4,4′-偶氮-1,2,4-三唑[53]和1,1′-偶氮-1,2,3-三唑[20],后者成功构建了简洁的N8结构,如图14所示,氮含量达到68.3%。

图14 氨基三唑的氧化偶联
2011年,Thomas等[43,54]分别以1-氨基四唑和5-硝基-2-氨基四唑为底物,用类似方法合成了1,1′-偶氮-四唑和2,2′-偶氮-5-硝基四唑化合物,如图15所示,这两个化合物都含有N10链。可见,SDCI氧化偶联试剂的成功使用,使全氮长链的合成取得了可喜的进展。2012年,Tang等[55]用5-甲基-1-氨基四唑为底物,用三氯异氰尿酸(TCICA)为氧化剂,合成1,1′-偶氮-5-甲基四唑化合物,明显降低了感度。

图15 氨基四唑的氧化偶联
6.2 中性氧化剂
以上反应都是在酸性条件下进行的,对于需要避免酸的底物并不适用,目前已经发现了一些在中性条件下也可以偶联N—NH2的氧化剂,典型的如氧化汞、高锰酸钾等。1998年,Porath等[56-57]选择对苯醌、黄色氧化汞等成功氧化偶联N—NH2,设计合成了带羟基的N4链化合物,如图16所示。羟基的引入是希望通过分子内或分子间氢键的形成,探索氢键对N4直链的稳定化作用,不过实验效果并不是十分理想。黄色氧化汞属于剧毒试剂,影响了其在该类反应中的应用。

图16 氧化汞引发的氧化偶联
1966年,Minato等[58]先通过对甲基苯重氮盐与苯基肼的反应制备了1-对甲苯基-3-苯基-四氮烯,进一步利用高锰酸钾在0℃实现了其上N—NH2的氧化偶联,制备了4个苯环取代的N8链化合物,如图17所示。多个稳定的苯环的引入增加了该化合物的共轭作用,但N8链的稳定性仍然很差,极易分解。
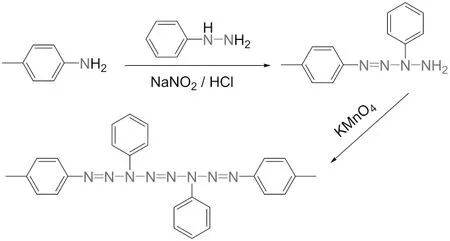
图17 高锰酸钾引发的氧化偶联
7 氨基重氮偶联反应
芳香一级胺和亚硝酸或亚硝酸盐及过量的酸在低温下反应可生成芳香重氮盐,重氮盐在溶液中有一定的稳定性,在有机合成上有广泛的用途[59]。重氮盐正离子是强亲电试剂,在冷的弱酸溶液中,可以和一级芳胺或二级芳胺在氮原子上发生偶联反应,生成重氮氨基结构,如图18所示。这种氨基-重氮盐-重氮氨基策略,也是延长氮氮直链的一种方法。

图18 重氮化反应及重氮盐的偶联反应
如果将芳基选为唑类,利用重氮化及重氮盐的偶联反应就可以合成高氮含量的含能化合物。以5-氨基四唑为例,如图19所示,以其形成的重氮盐继续和5-氨基四唑反应,可生成5,5′-重氮氨四唑[60-62]。该化合物带有3个酸性氢,易被金属离子取代成盐。

图19 5-氨基四唑的重氮化及偶联



图20 1,5-二氨基四唑的重氮化及偶联
8 其他可能合成的氮链结构

图可能的合成路线
8.2 N10的合成


图22 N10可能的合成路线及分解产物
8.3 N12的合成
以含N—NH2的唑类化合物为起始原料,结合氨基化、偶联和硝化等步骤,设计合成具有更长氮链的偶氮唑类化合物,例如合成图23所示的化合物,具有12个氮链的结构,其中硝基在对氮链进行封端的同时,还能起到提高能量和氧平衡的作用。

图23 N12链可能的合成路线
9 结束语
19世纪初,Berzelius等认为人工不可能合成有机物,然而现在化学家合成的新化合物已不计其数,正如有机合成之父Woodward曾说过的:“在上帝创造的自然界旁边,化学家又创造了另一个世界。”传统CHON含能化合物的大量合成与推陈出新正是植根于有机化学上百年的积累。
全氮化学是一个全新的研究领域,已知的氮氮键成键反应非常少,更谈不上系统的全氮结构合成方法和理论。氮链延长反应是该领域最基础的入门技术,目前已取得了一些进展,但还面临诸多挑战,高风险和高回报并存。该领域未来的发展趋势及建议如下:
(1)目前氮链延长方法主要利用叠氮基、胺基、重氮以及氮烯等官能团的取代、偶联等反应,一些具有高反应活性的含氮试剂可能衍生出全新的成键反应,而且电化学等方法日益发挥重要作用,因此,该领域后续研究中应更加重视新型含氮试剂的开发与应用,并充分发挥非传统合成方法的优势;
(2)目前合成的链状全氮结构具有一个共同的特点,它们多含有共轭体系,无孤立的N—N单键,这样避免了全氮结构从键强最弱的一环断裂,从而引起多米诺骨牌效应,导致整个全氮结构崩塌,这对后续新的长氮链结构的设计与合成具有重要借鉴意义;
(3)链状全氮离子或化合物稳定性差,直接合成难度大,宜考虑借助对其具有稳定化作用的客体材料,设计分子间作用力对其进行稳定,进而辅助其合成;
(4)氮链如何向更高阶的全氮结构转化是未来需要研究的重要问题。可以先用含有稳定化单元的氮链为前体,逐步转化为更高阶的全氮结构后再脱去稳定化单元,合成性能更优良的全氮化合物。
- 火炸药学报的其它文章
- Search for Effective Catalysts for the Development of Engines Based on the Products of Catalytic Decomposition of N2O
- DNP/HMX熔铸炸药的流变性能
- 负压环境对炸药爆炸冲击波影响的实验研究
- Synthesis of an Energetic Compound 1,3,5-Trinitrohexahydropyrimidine Based on Carbon-bromine Cleavage Reduction
- 间苯三酚法合成TATB产品中副产物的鉴定及性能表征
- 微量热法研究GAP与BPS固化反应

