高性能LiNi0.7Co0.1Mn0.2O2正极材料合成工艺及电化学性能研究
赵霞妍,雷洋名,王烉然,谢永佳,任小龙,阎雪梅,汪 英
(桂林电器科学研究院有限公司,广西桂林 541004)
引言
2012年以来,锂电池行业保持高速增长并加快了对传统电池的替代。电动汽车用锂离子电池是拉动全球锂离子电池产业增长的主要动力。电动车要求电池具有比能量高、比功率大、自放电少、价格低廉、使用寿命长及安全性好等特性[1,2]。而作为锂离子电池中最为关键部分的正极材料是决定锂离子电池容量、安全性和成本的最核心材料。在动力电池发展早期,磷酸铁锂(LFP)在安全性、成本、高温性能和循环寿命方面具有领先优势,得到了广泛的应用。然而磷酸铁锂较低的能量密度制约了其发展,在乘用车和专用车等领域逐步被三元电池(正极使用三元材料的电池)所取代[3]。近年来受能量密度驱使,我国动力电池逐步由磷酸铁锂电池转向三元电池。
三元材料指以镍钴锰酸锂(NCM)和镍钴铝酸锂(NCA)为代表的层状多元金属复合材料。三元材料能够充分发挥三种金属的优势,电池能量密度较高,是动力电池主要正极材料之一[4,5]。但由于NCA材料在材料生产环境及电池制造上存在更严苛的要求,在安全性上也比NCM更难控制。因此,目前被广泛使用的正极材料主要是NCM。按照镍、钴、锰的构成比例,可以分为NCM111、NCM523、NCM622、NCM811等型号,其放电比容量随着镍含量的增加而升高[6,7],镍含量在60%以上的材料为高镍正极材料。随着能量密度需求的逐渐提高,高能量密度的高镍正极材料将成为行业发展趋势。
采用化学共沉淀法制备了Ni0.7Co0.1Mn0.2(OH)2前驱体,并通过固相烧结法制备LiNi0.7Co0.1Mn0.2O2(NCM712)三元正极材料,系统研究了锂源比例Li/M(M为过渡金属元素总摩尔量)对LiNi0.7Co0.1Mn0.2O2正极材料结构和电化学性能的影响。
1 试验
1.1 材料的制备
以 NiSO4·6H2O、CoSO4·7H2O、MnSO4·H2O 为原料,按比例n(Ni)∶n(Co)∶n(Mn)=7∶1∶2配制成相应浓度的盐溶液。将上述盐溶液与烧碱溶液和氨水同时通入反应釜内,控制共沉淀反应条件得到反应沉淀物。沉淀物经抽滤、洗涤、真空干燥后得到Ni0.7Co0.1Mn0.2(OH)2前驱体。将前驱体粉末与LiOH·H2O按不同Li/M比(1.05,1.10,1.15,1.20)混合均匀,在850℃高温下烧结12 h,得到不同Li/M比的LiNi0.7Co0.1Mn0.2O2正极材料。
1.2 电池组装与电化学性能测试
以不同Li/M比的LiNi0.7Co0.1Mn0.2O2正极材料为活性物质、导电炭黑(super-p)为导电剂、聚偏二氟乙烯(PVDF)为粘结剂,按一定质量比混合,加入N-甲基-2-吡咯烷酮(NMP)制成一定黏度的均匀浆料,采用涂布机涂布、烘干。经辊压机辊压和裁片机裁片后组装成CR2032型扣式电池,负极为金属锂片,静置12 h。采用武汉蓝电电池测试系统在室温下(25℃)进行恒电流充放电性能、循环性能和倍率性能测试,电压范围为2.7~4.4 V。采用法国Claix公司Biologic VSP电化学工作站测试活化后半电池的交流阻抗(EIS)特性,测试频率为0.01 Hz~105Hz。
2 结果与讨论
2.1 不同Li/M比正极材料的晶体结构
图1是不同Li/M比条件下合成的LiNi0.7Co0.1-Mn0.2O2正极材料的XRD图谱。从图1中可知,4种不同Li/M比条件下合成的LiNi0.7Co0.1Mn0.2O2正极材料均具有典型的六方晶系α-NaFeO2型层状结构,衍射峰峰形尖锐,未发现明显杂峰,说明合成的LiNi0.7Co0.1Mn0.2O2正极材料结晶性良好,且无杂质相出现。(006)/(102)和(018)/(110)这两对衍射峰的分裂均比较明显,说明合成的正极材料具有有序的层状结构[8,9]。在六方晶系的三元正极材料中,由于Li+(0.076 nm)和Ni2+(0.069 nm)的离子半径相近,反应过程中容易出现Ni2+占据Li+位置的“阳离子混排”现象,导致正极材料电化学性能下降。通常情况下研究者用(003)峰与(104)峰的强度比I(003)/I(104)来表征阳离子混排程度,这个比值越大表明离子混排程度越低,一般认为I(003)/I(104)>1.2时阳离子混排程度较低[10,11]。根据衍射数据计算得出,4个样品的(003)峰与(104)峰的比值I(003)/I(104)分别为:1.56,1.82,1.65和1.48。Li/M比为1.10的样品I(003)/I(104)的比值最高,此时晶体内部阳离子混排程度最低,说明Li/M比为1.10的样品具有最优的晶体结构。
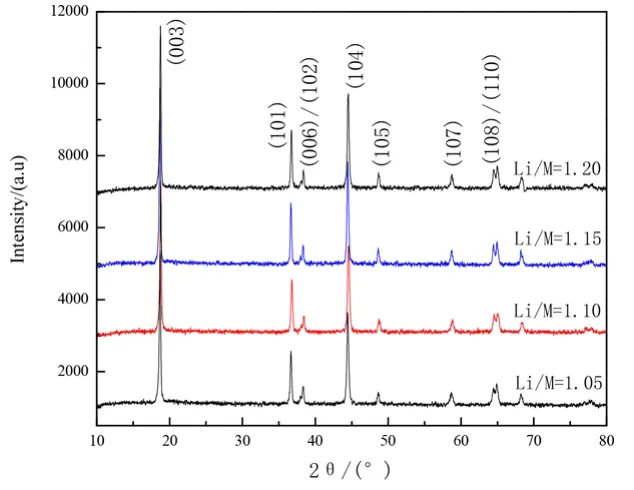
图1 不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2样品的XRD图谱
2.2 不同Li/M比正极材料的微观形貌
图2为不同Li/M比条件下合成的LiNi0.7Co0.1-Mn0.2O2正极材料的SEM图。图2(a)~(d)分别为Li/M比1.05、1.10、1.15和1.20样品的SEM。由图2可见,当材料在相同的高温固相反应条件下合成时,样品的颗粒尺寸和外观形貌没有明显差异,但随着Li/M比的逐渐增大,样品逐渐出现团聚现象。Li/M比为1.15和1.20时团聚现象明显,团聚颗粒之间出现了熔融状物质,当Li/M比增加到1.20时,熔融状物质尤为明显,该物质可能是由于锂源比例过大,颗粒表面出现大量锂残留造成的。该样品在后续的调浆过程中呈果冻状,导致涂布失败。

图2 不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2样品的SEM图
2.3 不同Li/M比正极材料的电化学性能
图3是不同Li/M比条件下合成的LiNi0.7Co0.1-Mn0.2O2正极材料在0.2 C条件下的首次充放电曲线。由图可知,在相同的高温固相反应条件下,LiNi0.7Co0.1Mn0.2O2材料均获得较好的首次放电比容量,随着Li/M比的增加,首次放电比容量呈先升高后降低的趋势。Li/M比为1.05、1.10和1.15的样品,在0.2 C充放电条件下对应的首次放电比容量分别为:196.7 mAh/g、204.0 mAh/g和185.3 mAh/g,Li/M比为1.10样品的首次放电比容量最高。

图3 不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2样品的首次充放电曲线
图4是不同Li/M比条件下合成的LiNi0.7Co0.1-Mn0.2O2正极材料在1.0 C条件下循环充放电50圈的循环性能曲线。由图4可知,随着循环次数的增加,样品的放电比容量均呈缓慢下降的趋势,出现了由于充放电过程中电解液与活性物质之间的副反应和锂离子的沉积造成的不可逆容量损失。随着Li/M比的逐渐增加,1.0 C充放电条件下循环50圈后的放电比容量分别为:180.4 mAh/g,187.0 mAh/g和172.7 mAh/g,容量保持率分别为:96.5%、97.2%和96.2%。Li/M比为1.10样品显示出最优的放电比容量和循环稳定性。

图4 不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2样品的循环性能曲线
图5为不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2正极材料的倍率性能曲线,由图5可知,随着充放电倍率的增加,不同Li/M比样品的放电比容量变化趋势相似,比容量均随电流密度的增大而减小。在不同倍率下,Li/M比为1.10样品均具有最高的放电比容量,Li/M比为1.15样品的放电比容量最低。经过12圈不同倍率的充放电循环后再重新以0.2 C进行充放电时,不同Li/M比样品的放电比容量均能恢复到初始0.2 C充放电时的比容量值甚至还有所提高,其放电比容量分别为:194.9 mAh/g,203.4 mAh/g和187.7 mAh/g。
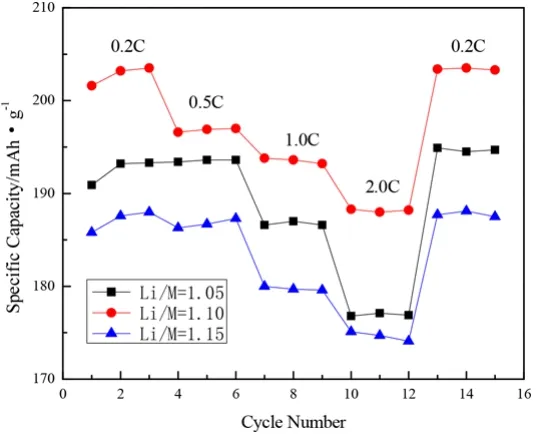
图5 不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2样品的倍率性能曲线
图6为不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2样品的EIS图谱,曲线主要由3部分组成,分别对应于电解液与电极表面反应形成SEI膜阻抗RSEI的高频区的大半圆,对应于电荷传递阻抗Rct的中频区小半圆弧以及对应于离子扩散阻抗(Warburg阻抗)Zw的低频区直线[12]。由图6可知,Li/M比为1.05和1.10样品具有相似的EIS曲线,均由高频区的半圆和中频区的圆弧组成。Li/M比为1.15样品中频区的半圆弧不明显,但低频区的直线异常明显。随着Li/M比的增加,高频区的半圆的半径先减小后增大,Li/M比为1.10时高频区的圆弧半径最小,说明Li/M比为1.10时LiNi0.7Co0.1Mn0.2O2材料的界面阻抗最低,这一结果与图4的循环稳定性以及图5的倍率性能结果相一致。
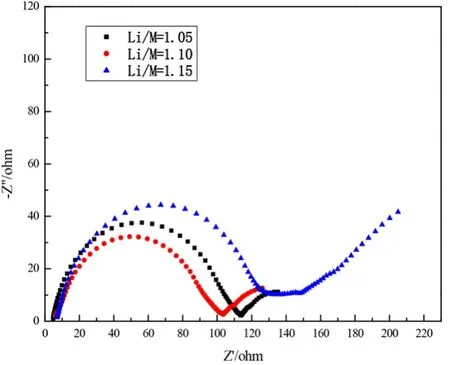
图6 不同Li/M比条件下LiNi0.7Co0.1Mn0.2O2样品的EIS图谱
综合图3~图6的结果可知,Li/M比为1.10的样品具有最优的电化学性能,由此可以确定1.10为最佳的锂源比例。而Li/M比为1.05样品电化学性能较低的原因可能是由于1.05的锂源比不足以补充样品在长时间的高温煅烧下损失的锂,从而出现了锂缺陷,Ni2+进入Li+位发生离子混排,并最终影响到材料的电化学性能。当Li/M比增加到1.15以上时,一方面由于团聚现象的出现导致颗粒堆积过于紧密,电解液未能完全浸润到活性物质表面,导致参与反应的金属离子比例减小;另一方面由于锂源量过多,锂未完全参与反应,样品表面出现锂残留,残留的锂被氧化成杂质Li2O,而Li2O易吸收水分和CO2生成Li2CO3导致材料表面pH值过高,同时Li2CO3的存在使电池循环过程中产生气体,造成电池膨胀从而影响电池的电化学性能[13-15]。
3 结论
在850℃下煅烧12 h的固相反应条件下合成的不同锂源比的LiNi0.7Co0.1Mn0.2O2三元正极材料,均具有典型的六方晶系α-NaFeO2型层状结构,材料结晶性良好,无明显杂质相;材料表面形貌无明显差异,但随着锂源比的增加,材料发生团聚,且表面出现残锂。当Li/M比为1.10时,材料的离子混排程度最低,颗粒未发生团聚,且未发现材料表面有锂残留。电化学性能测试结果表明,Li/M比为1.10的LiNi0.7Co0.1Mn0.2O2正极材料的界面阻抗最低,首次放电比容量、循环稳定性以及倍率性能均最优。在0.2 C充放电条件下的首次放电比容量达到204.0 mAh/g,在1.0 C充放电条件下循环充放50圈后放电比容量为187.0 mAh/g,容量保持率达到97.2%。当倍率由0.2 C增大到2.0 C时,放电比容量从201.6 mAh/g降到188.3 mAh/g,再次进行0.2 C充放电测试时放比容量仍然达到203.4 mAh/g。

