消银解毒饮通过cdc7抑制角质细胞增殖作用的动物实验研究
韩 露 周 扬 段行武 陈 兵 方如男 李建红
北京中医药大学东直门医院,北京,100700
银屑病是一种以红斑、鳞屑为主要表现的慢性炎症性皮肤病,其特征性病理改变为持续性炎症以及角质形成细胞(keratinocytes,KCs)增殖失控和分化障碍[1]。银屑病皮损组织中KCs的增殖速度是正常表皮的2倍,而其细胞周期缩短到正常周期的1/8[2],可见KCs的异常增殖与细胞周期紊乱密切相关。细胞分裂周期蛋白(cell division cycle protein,cdc)7是细胞周期中最重要的调节因子之一,TAK-931则是一种cdc7选择性抑制剂,具有显著的抗增殖活性[3]。尽管目前没有cdc7与银屑病发病的相关报道,但有皮肤肿瘤方面的研究显示cdc7在黑素瘤组织中高表达,而TAK-931可有效抑制黑素瘤进展[4],提示我们cdc7在皮肤组织中发挥重要作用,且与表皮角质细胞增殖密切相关。银屑病是KCs过度增生性疾病,我们先期的预实验也发现,在银屑病体内外模型中cdc7呈过度表达,提示 cdc7可能与银屑病 KCs 异常增殖之间有密切联系。
消银解毒饮根据东直门医院金起凤教授创立的经验方“消银解毒汤”研制,临床应用多年,治疗银屑病血热证疗效确切[5]。先期研究显示消银解毒饮可以通过抑制KCs增殖治疗银屑病[6,7],然而其抑制KCs增殖的作用是否通过对细胞周期的调控仍需进一步研究。本实验拟建立咪喹莫特(imiquimod,IMQ)诱导的小鼠银屑病模型,观测用药前后小鼠银屑病皮损表现、表皮病理改变、皮肤组织cdc7表达情况,从动物实验水平探讨消银解毒饮通过cdc7抑制角质细胞增殖的作用机制。
1 材料与方法
1.1 动物 SPF级健康雄性BALB/c小鼠20只,8周龄,体重20 g,购自辽宁长生生物技术股份有限公司,许可证号:SCXK(辽) 2020-0001。
1.2 药物 院内制剂消银解毒饮(水牛角30 g,生地15 g,丹皮12 g,土茯苓30 g,苦参10 g,紫草15 g,生甘草6 g等)由北京中医药大学东直门医院颗粒药房提供。按照小鼠剂量(20 g体重)=9.1×成人剂量(70 kg体重),得到小鼠灌胃剂量为23.4 g/kg,双蒸水溶解,4℃保存备用。
1.3 试剂 cdc7抑制剂TAK-931(MCE,货号:HY-100888);5%咪喹莫特乳膏(明欣药业,货号:74969);异氟烷(瑞沃德,货号:217180101);苏木素(Sigma,货号:H9627);伊红Y(水溶性)(国药集团,货号:71014544);无水乙醇(国药集团,货号:10009218);二甲苯(国药集团,货号:10023418);包埋石蜡(国药集团,货号:69019361);中性树胶(国药集团,货号:10004160);正常山羊血清(博士德生物,货号:15GO6AC9);Dako免疫组化试剂盒(安捷伦,货号:K5007);重组Anti-CDC7抗体(abcam,货号:ab229187)。
1.4 仪器 病理切片机(德国Leica,型号:RM 2016);脱水机(武汉俊杰,型号:JT-12J);组织摊烤片机(武汉俊杰,型号:JK-6);显微镜(奥林巴斯,型号:BX53)。
1.5 分组及造模
1.5.1 建立动物模型[8,9]将20只小鼠适应性饲养7天后,随机分为4组,每组5只:①对照组;②银屑病模型组;③消银解毒饮组;④TAK-931组。实验前所有小鼠予异氟烷吸入麻醉,除去背部毛发,形成约2 cm×3 cm皮肤暴露区域。②③④组每只小鼠每日涂抹含5% IMQ的膏霜50 mg,①组小鼠只进行等量凡士林涂抹处理,连续涂抹5天。
1.5.2 实验给药 ①②组小鼠蒸馏水灌胃;③组每天进行消银解毒饮灌胃处理(每次23.4 g/kg);④组每天进行TAK-931灌胃处理(每次2 mg/kg)。所有动物给药容量是每次10 mL/kg,每天2次,造模当天开始给药,连续5天。
1.6 检测指标及方法
1.6.1 小鼠银屑病皮损面积和严重程度评估 第1~5天涂抹IMQ前及第6天,每天对小鼠背部皮肤暴露区域进行单独拍照处理,动态观察皮损进展情况,依据银屑病皮损面积与严重程度指数(psoriasis area and severity index,PASI)评价办法[10],对小鼠皮损处红斑、鳞屑及浸润增厚程度进行评分,评分标准为:0分(无);1分(轻度);2分(中度);3分(重度);4分(极重度)。将三者相加得到总积分,对各组小鼠的总积分取均值后绘制趋势图。
1.6.2 HE染色观察小鼠皮肤组织形态学改变 于造模第6天,处死小鼠取其背部皮肤组织,经脱水、透明处理后,进行石蜡包埋,制成4 μm厚的切片。切片脱蜡,入苏木素染液染色5 min,冲洗后入1%水溶性伊红染液染色5 min,以中性树胶封片。显微镜下采集图像,观察各组小鼠皮肤组织病理学变化,并采用ImageJ软件测量表皮厚度。
1.6.3 免疫组化检测小鼠皮肤组织中cdc7表达 皮肤组织切片脱蜡、水化、抗原修复后,滴加3%过氧化氢阻断内源性过氧化物酶,以正常山羊血清封闭30 min,cdc7抗体(1∶100)4℃孵育过夜,酶标二抗37℃孵育30 min,DAB显色,苏木素复染,脱水后以中性树胶封片。显微镜下采集图像,检测各组小鼠皮肤组织cdc7表达情况。
1.7 统计学方法 采用GraphPad prism软件进行统计分析,计量资料采用均数±标准差表示,PASI评分采用秩和检验(Kruskal-wallis)进行组间比较,表皮厚度、cdc7阳性细胞计数采用单因素方差分析(one-way ANOVA),组间两两比较采用LSD进行比较,P<0.05表示差异有统计学意义。
2 结果
2.1 消银解毒饮对小鼠银屑病模型皮肤的影响 从每日皮损变化观察得到,对照组小鼠皮肤无红斑、无鳞屑、无增厚改变;造模后小鼠皮肤逐渐出现红斑,且皮肤不断增厚,第3天出现鳞屑表征,第6天时,背部皮肤红斑明显,布满层状鳞屑,易脱落,皮肤高度增厚;与银屑病模型组相比,消银解毒饮组和TAK-931组皮损进展较慢,鳞屑明显减少,红斑面积较小、颜色较淡,皮损肥厚程度不明显,见图1。
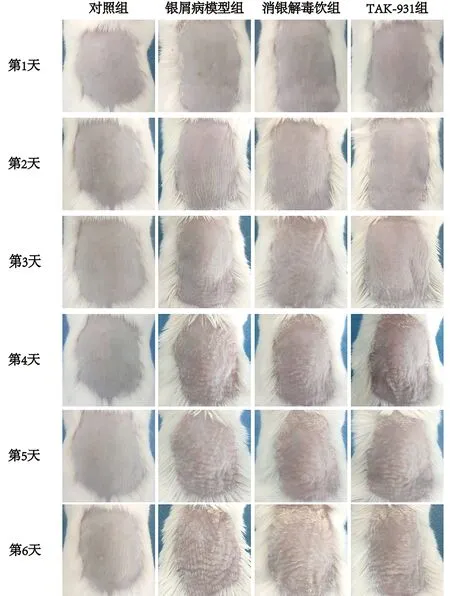
图1 各组小鼠背部皮损表现
PASI评分结果表明,与对照组相比,模型组小鼠第2天起即有皮肤增厚表现,随抹药天数的增加,总评分呈上升趋势,表明皮损不断加重,其中第2~3天及第4~5天评分上升幅度最大;与模型组相比,消银解毒饮组和TAK-931组总评分明显减低,增高速度缓慢,表明消银解毒饮组与TAK-931组皮损进展较慢,红斑、鳞屑、皮损增厚程度较轻,见图2。

图2 各组小鼠皮损PASI评分
2.2 消银解毒饮对小鼠银屑病模型皮肤组织形态学影响 HE染色结果显示,对照组小鼠表皮层薄,无增厚改变,细胞浸润少;银屑病模型组小鼠表皮增生明显,同时存在角化过度与角化不全,棘细胞层增厚,角质层可见Munro微脓肿,真皮层有大量炎性细胞浸润;与银屑病模型组相比,消银解毒饮组和TAK-931组皮损区域表皮增生较轻,真皮层炎性细胞数目较少,见图3。
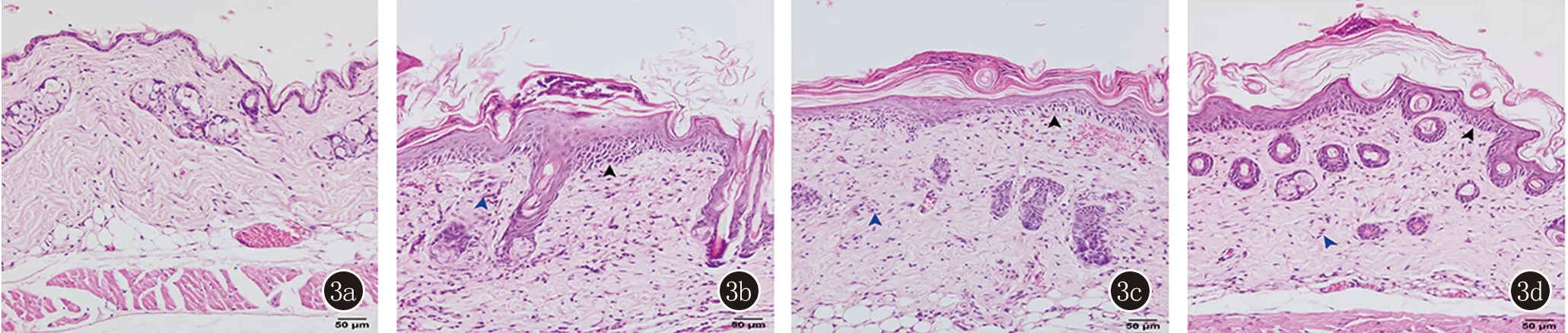
3a:对照组;3b银屑病模型组;3c消银解毒饮组;3d:TAK-931组;黑色箭头:表皮增生;蓝色箭头:炎性细胞浸润(HE,×200)
使用ImageJ软件测量HE染色后各组表皮厚度,银屑病模型组明显较对照组表皮增厚(P<0.01),消银解毒饮组(P<0.01)和TAK-931组(P<0.05)表皮增厚程度均低于模型组,其中消银解毒饮组对表皮增生的改善作用更明显,但二组相比差异无统计学意义,见图4。
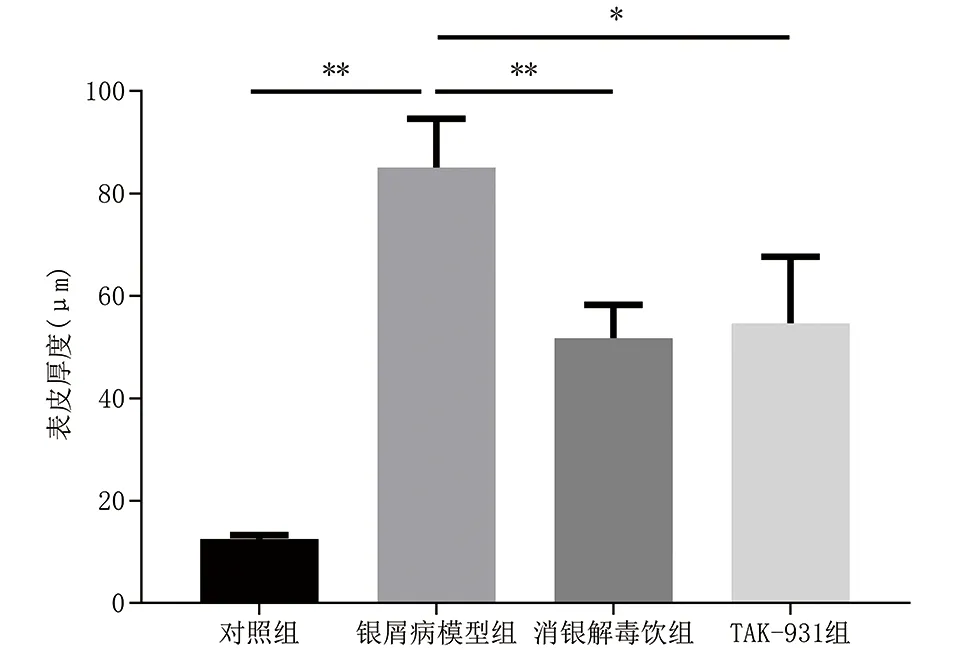
(**表示P<0.01,*表示P<0.05)
2.3 消银解毒饮对小鼠银屑病模型皮肤组织中cdc7表达的影响 免疫组化检测结果显示,对照组表皮较少见cdc7阳性细胞;与对照组相比,模型组表皮cdc7阳性细胞显著增多(P<0.01),主要分布于基底层,棘层亦有分布;消银解毒饮组表皮cdc7阳性细胞数较模型组明显减少(P<0.05),见图5、6。
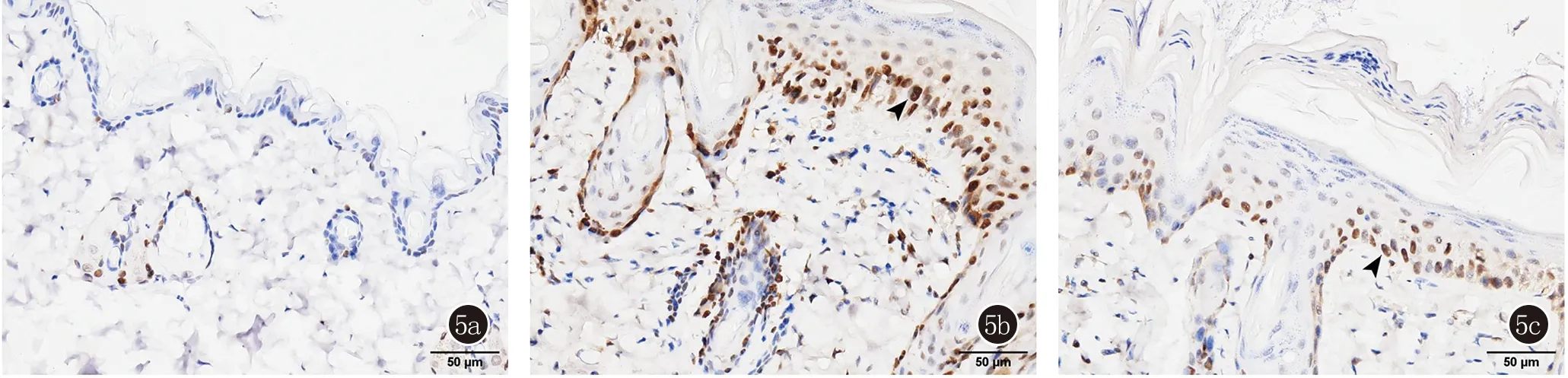
5a:对照组;5b:银屑病模型组;5c:消银解毒饮组

(**表示P<0.01,*表示P<0.05)
3 讨论
银屑病的发病机制尚不清楚,目前较为公认的发病模型认为,当皮肤感染或损伤时,角质细胞释放抗菌肽并与自身遗传物质相结合,激活树突状细胞,产生TNF-α、IL-23等细胞因子,介导Th17细胞的分化。成熟的Th17细胞分泌IL-17、IL-22、IL-23等炎性反应因子激活KCs的增殖。KCs过度增殖又分泌多种细胞因子、趋化因子和抗菌肽等物质趋化Th17等炎症细胞至皮肤,从而形成了促进银屑病发生发展的正反馈环路[11,12]。由此可见,KCs过度增殖在银屑病的发生和维持中都起重要作用。
cdc7是细胞周期中必需的一种激酶,特别调节细胞周期的G1/S相变,而G1/S相变是细胞增殖的基础。cdc7在与其调节亚基DBF4结合后形成活性激酶复合体(DBF4-dependent kinase,DDK),使其下游效应分子微小染色体效应维持蛋白(mini chromosome maintenance protein,MCM)2-7磷酸化,从而激活解旋酶活性,开启DNA复制的第一步[3,13]。而KCs的异常增殖与细胞周期紊乱密切相关[2],依此推测cdc7对细胞周期DNA复制起始的调控可能参与银屑病KCs异常增殖的病理过程。
在本次研究中,与对照组相比模型组小鼠皮肤经IMQ诱导后出现红斑、鳞屑、皮肤增厚改变,同时HE染色观察小鼠皮损组织形态学变化,发现模型组小鼠表皮增生明显,棘细胞层增厚,真皮层有炎性细胞浸润,以上均符合银屑病临床及病理表现。在应用cdc7抑制剂TAK-931后,对小鼠皮损PASI评分有较为明显的改善作用,HE染色结果显示,TAK-931可以减轻银屑病模型表皮增生程度,减轻炎症细胞浸润。说明cdc7对细胞周期的调控作用可以促进银屑病KCs的异常增殖,通过抑制cdc7可以有效干预小鼠银屑病模型进展。
我院制剂消银解毒饮由水牛角、生地、牡丹皮、赤芍、金银花等药物组成,有凉血清热、解毒化斑、泄湿止痒的作用,临床研究显示,其治疗银屑病血热证的总有效率为91.8%,疗效确切[5]。我科前期研究采用药理血清的方法,以角质形成细胞株 COLO-16为研究对象,观察消银解毒饮及拆方后各组药物血清对KCs增殖的影响,发现消银解毒饮可直接抑制KCs过度增殖以及诱导其凋亡,并且可以抑制角质形成细胞分泌血管内皮生长因子(VEGF),从而发挥对银屑病的治疗作用[6,7,14]。本研究使用消银解毒饮干预小鼠银屑病模型,发现消银解毒饮可以明显改善小鼠皮损PASI评分及组织病理形态学表现;免疫组化法检测结果显示,消银解毒饮可以显著降低小鼠银屑病模型表皮cdc7阳性细胞的水平。
综上所述,cdc7可以促进银屑病KCs的异常增殖,消银解毒饮可能通过下调cdc7表达,抑制KCs的过度增殖,发挥对银屑病的治疗作用。然而,本研究尚处于消银解毒饮通过cdc7抑制角质细胞增殖研究的初级阶段,关于其作用机制尤其是具体信号通路的具体调控过程仍亟待进一步阐明。

