rtPA静脉溶栓治疗伴HMCAS急性脑梗死患者的效果及对神经功能评分与预后的影响
黄镇
(南召县人民医院 神经内科,河南 南阳 474650)
急性脑梗死主要由大脑动脉闭塞引发血液循环障碍,出现脑组织梗死所致,会导致神经元受损,造成神经功能障碍,严重影响患者的正常生活[1-2]。大脑中动脉高密度征(HMCAS) 是脑梗死患者早期常见的颅脑CT征象,对临床诊疗急性脑梗死病例具有重要的意义。伴有HMCAS 的急性脑梗死患者脑梗死面积较大,神经缺损风险高,常规抗血小板聚集、脑保护、调脂等疗法治疗,疗效欠佳。重组组织型纤溶酶原激活剂(rtPA) 是一线应用广泛的静脉溶栓药物,但当前对rtPA 静脉溶栓治疗合并HMCAS 患者的预后仍存在争议。为了探讨行之有效的治疗方案,本文就南召县人民医院收治的84 例伴HMCAS 的急性脑梗死患者进行研究,现报道如下。
1 资料与方法
1.1 一般资料
选取本院2017年7月至2019年7月收治的伴HMCAS 的急性脑梗死患者84 例,采用蓝白双色球法将其随机分成对照组和观察组,各42 例。对照组男26 例,女16 例;年龄39 ~86 岁,平均年龄(69.25±2.37)岁;病程1 ~5 h,平均病程(3.04±0.95) h。观察组男25 例,女17 例;年龄41 ~85 岁,平均年龄(69.37±2.59)岁;病程1 ~5 h,平均病程(3.16±0.87) h。两组上述数据对比,无统计学差异(P>0.05)。本次研究经医院伦理委员会批准,且参与本研究的患者及其家属均获知情权。
纳入标准:满足急性脑梗死的诊断标准[3],经CT 检查确诊为HMCAS;发病至入院时间在6 h 以内;患者及其家属同意配合研究。
排除标准:HMCAS 假阳,由非栓塞或血栓引发的双侧或单侧HMCAS 者;接受过动脉溶栓、去骨瓣减压术、机械取栓等治疗者;合并恶性肿瘤者;药物过敏者;血液系统疾病者;严重器质性功能障碍者;精神病者;呼吸系统疾病者;妊娠或哺乳期女性;营养不良、贫血者。
1.2 方法
对照组采用常规治疗。予以患者依达拉奉注射液( 吉林省辉南长龙生化药业股份有限公司,生产批号20170523)30 mg,配以0.9% 生理盐水100 mL,静脉滴注,2 次/d;硫酸氢氯吡格雷片( 深圳信立泰药业股份有限公司,生产批号20170415)25 mg,口服,1 次/d;阿司匹林肠溶片( 河北瑞森药业有限公司,生产批号20170627)100 mg,口服,1 次/d;结合患者病情,予以20% 甘露醇注射液( 安徽丰原药业股份有限公司,生产批号20170319)1 g/kg,静脉注射。治疗期间,降低患者颅内压,维持水和电解质平衡,积极控制感染。
观察组在对照组基础上予以rtPA( 德国Boehringer-Ingelheim,生产批号20170416) 静脉溶栓治疗,使用剂量0.8 mg/kg,确保每日最大剂量≤70 mg,先予以患者总剂量的10%,静脉注射,5 min 内完成注射,剩余90% 的剂量配以0.9% 生理盐水250 mL,静脉滴注,1 h内滴注完毕,1 次/d。治疗期间密切关注各项体征指标、出血情况。
两组均治疗14 d。
1.3 观察指标
根据美国国立卫生研究制定的脑卒中量表(NIHSS)[4]评价患者治疗前后的神经功能。评价内容包括最佳语言、意识水平、最佳运动等十五项,评分0 ~42分,得分越高表明神经功能越差。参照Barthel 评定量表(BI)[5]评价患者治疗前后的日常生活能力,包含控制排便、修饰等十项评价条目,使用4 级评分法,按照百分制评价,得分越高提示患者生活独立性越强。
治疗3 个月后,参照改良RANKIN 量表(mRS) 评价患者的疗效,完全无症状,记0 分;有症状,却无明显功能障碍,可完成全部的日常工作及生活,记1 分;轻度残疾,无法完成发病前的各项活动,但无需帮助仍可照料自身的日常生活,记2 分;中度残疾,需要帮助,尚可独立步行,记3 分;中重度残疾,无法自己行走,在生活中需要他人辅助,记4 分;卧床,大小便失禁,重度残疾,生活依靠他人,记5 分。根据评价结果判断疗效:①预后良好:3 ~5 分;②预后不良:0 ~2 分。预后良好率= 预后良好例数/ 总例数×100%[6]。
统计两组患者的并发症发生率,并发症包括颅内出血、血管再闭塞、消化道出血。
1.4 统计学方法
将数据录至SPSS 23.0 软件,以χ2检验计数资料[n(%)],以t检验计量资料(±s),P<0.05 表明有差异有统计学意义。
2 结 果
2.1 两组NIHSS 和BI 评分比较
治疗后,观察组的NIHSS 评分显著低于对照组,BI评分显著高于对照组,差异显著(P<0.05)。见表1。
表1 两组NIHSS和BI评分比较(± s)单位:分
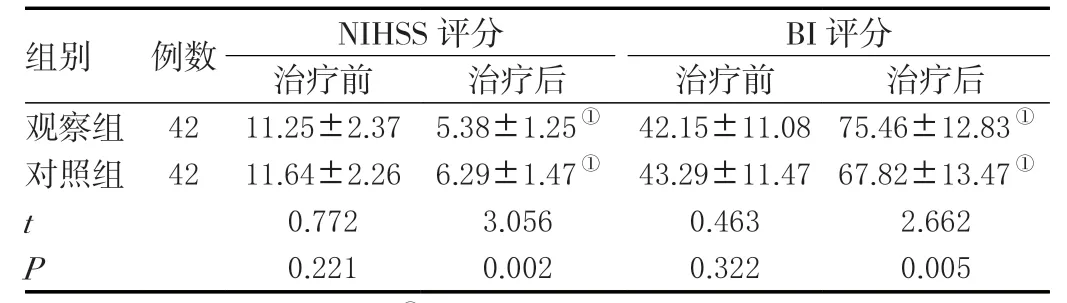
表1 两组NIHSS和BI评分比较(± s)单位:分
注:与同组治疗前比较,①P <0.05。
组别 例数 NIHSS 评分 BI 评分治疗前 治疗后 治疗前 治疗后观察组 42 11.25±2.37 5.38±1.25① 42.15±11.08 75.46±12.83①对照组 42 11.64±2.26 6.29±1.47① 43.29±11.47 67.82±13.47①t 0.772 3.056 0.463 2.662 P 0.221 0.002 0.322 0.005
2.2 两组疗效比较
观察组预后良好率显著高于对照组,差异显著(P<0.05)。见表2。

表2 两组疗效比较[n(%)]
2.3 两组并发症发生率比较
观察组并发症发生率低于对照组,但组间比较,无显著差异(P>0.05)。见表3。

表3 两组并发症发生率比较[n(%)]
3 讨 论
有效溶解堵塞血管的血块、促进血管再通是临床治疗急性脑梗死的关键。急性脑梗死患者大脑中动脉粥样硬化会导致邻近脑组织出现缺氧、缺血现象,造成动脉血供障碍,而HMCAS 是急性脑梗死病例早期典型影像学表现,伴有此类征象的患者预后较差[7]。因此有必要探讨行之有效的治疗方案。相关报道显示,在急性脑梗死患者的溶栓治疗中使用rtPA 可促使脑动脉再通,改善梗死局部血供,疗效较好[8]。
本次研究结果显示:治疗后,观察组的NIHSS 评分显著低于对照组,BI 评分显著高于对照组;观察组预后良好率显著高于对照组,说明观察组疗效更加卓越,患者神经功能、日常生活能力改善效果更加理想。分析后可知,伴有HMCAS 的急性脑梗死患者MCA M1 段存在闭塞情况,而MAC 供血范围较大,当出现主干闭塞后会引发大范围脑组织缺氧、缺血,继发神经功能缺损问题,影响预后。而采用rtPA 静脉溶栓治疗患者可有效溶解血块,促使闭塞血管顺利恢复通畅,改善缺血脑组织区域血运状态,使得缺血半暗带处的血液循环得以恢复,且避免大量神经元细胞发生坏死,从而改善患者的神经功能,提升预后,提高患者的日常生活能力。
本次研究显示,组间并发症发生率无明显差异,说明在常规治疗基础上予以患者rtPA 静脉溶栓治疗并未显著增加患者不良事件发生风险,治疗安全性可靠。研究后发现,rtPA 作为一种非选择性纤维蛋白溶解剂,是临床应用广泛的静脉溶栓药品,可激活体内纤维蛋白溶解系统,加快血栓溶解,且对体内的纤溶酶具有较高的亲和力,能够积极发挥特异性梗死局部溶栓效用。rtPA 现已被西方国家多中心推荐用于急性脑梗死的治疗。且在临床应用中,rtPA 并不会显著影响机体的凝血系统,无抗原性,颅内出血风险较低,支持临床反复、多次使用。因此,采用rtPA 静脉溶栓方案治疗患者安全性可行。
综上所述,予以伴HMCAS 的急性脑梗死患者rtPA静脉溶栓治疗,能够改善患者的神经功能缺损情况,提高疗效,安全可靠,值得临床应用。

