新生儿坏死性小肠结肠炎与输血相关性研究附3例报告
朱彦虹 胡晓琳 陈玲
随着新生儿重症监护病房(neonatal intensive care unit,NICU)救治技术发展,早产儿存活率大大提高,但坏死性小肠结肠炎(necrotizing Enterocolitis,NEC)仍然是早产儿最常见的严重胃肠急症,死亡率高,并发症多,故早期认识和积极治疗是改善预后的关键。NEC的病因复杂,除了主要的早产、低出生体重、感染、喂养方式不当、缺血缺氧及肠道黏膜屏障损伤等因素[1],近来一些回顾性研究发现输血可能是导致NEC的危险因素之一[2-4],早期诊断、积极治疗及预防是提高患儿生存率的必要方法。本文通过分析总结我院3例输血相关性坏死性小肠结肠炎(transfusion associated necrotizing enterocolitis,TANEC)患儿临床资料,并对相关文献进行复习,探讨该病的临床特点及相关发病机制,以便临床医生提高对NEC认识并有利于早期防治NEC。
临床资料
1 病例一 患儿母亲系G4P1,孕26W,患儿于我院剖宫产娩出,出生体重780 g,出生Apgar评分1分钟4分,5分钟6分。患儿出后予以肺泡表面活性物质治疗2次(120 mg/次),有创呼吸机支持7 d,CPAP辅助呼吸23 d。生后第3 d开始母乳喂养,加奶顺利,于第16 d加用母乳强化剂,第20 d(体重980 g,奶量20 mL/次,每3小时喂养1次)出现频繁血氧饱和度下降并腹胀,腹部平片显示部分肠管积气、扩张(图1);血常规显示白细胞17.26×109/L,红细胞2.79×1012/L,血红蛋白91 g/L、红细胞压积26.9%;C反应蛋白<0.5 mg/L。予以输注悬浮红细胞20 mL、给氧、开塞露灌肠及继续母乳喂养(20 mL/次,每3小时喂养1次)的治疗后患儿腹胀明显好转。患儿于生后43 d(纠正胎龄32 W+1,体重1460 g),达全肠道喂养(全强化母乳,26 mL/次,每3小时一次),因血常规提示贫血(白细胞6.82×109/L、红细胞2.65×1012/L、血红蛋白84 g/L、红细胞压积 25.6%),予以输注悬浮红细胞20 mL/kg纠正贫血。第2天(输血后13 h)发现频繁呼吸暂停、腹胀、腹部听诊肠鸣音消失并排鲜血样大便1次,行动态腹部平片(图2)提示肠腔积气、肠壁间隙增宽、部分肠袢固定。诊断为坏死性小肠结肠炎,予禁食、胃肠减压、抗感染(美罗培南、替考拉宁、奥硝唑)及对症支持治疗。患儿腹胀不能缓解,腹围持续增长,于第4天行手术治疗(回肠单筒造瘘术),术中诊断:结肠穿孔,弥漫性腹膜炎,术后病理回报:(乙状结肠)肠肌间及黏膜下神经丛数量略少,节细胞数量略少且不成熟。术后腹胀缓解,于生后96 d,纠正胎龄39 W +6,体重2.49 kg(3rd~10th),达全肠道喂养后,带造瘘口出院。出院后患儿按计划至我院门诊随访,纠正月龄3月NBNA评分39分,身高、体重、头围每次均在3rd~10th百分位。于2019年9月27日行回肠造口闭合术,术后病理提示“肠神经元发育不良”。
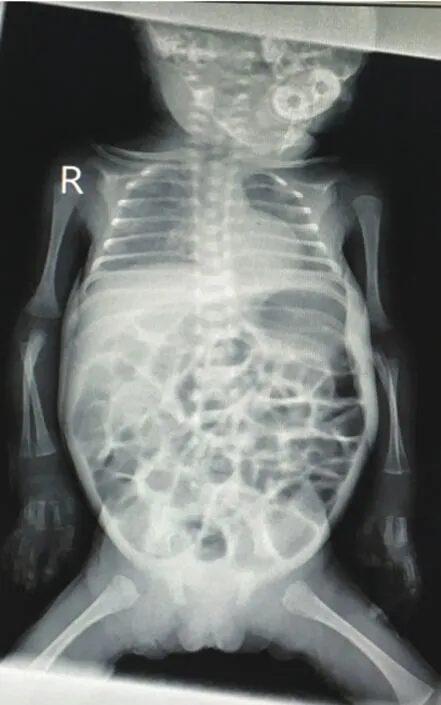
图1 病例一患儿生后20 d腹部平片

图2 病例一患儿生后43 d输血后24 h腹部平片
2 病例二 患儿母亲系G1P2,孕27 W+4,双胎,患儿于我院顺产娩出,出生体重1200 g,出生Apgar评分1分钟6分,5分钟6分。患儿出后立即予以肺泡表面活性物质治疗2次(分别为240 mg和120 mg),有创呼吸机支持2 d,CPAP辅助呼吸12 d。生后第2天开始母乳喂养,第15天加用母乳强化剂,生后第26天达到全肠道母乳全强化喂养(体重1810 g,奶量34 mL/次,每3小时1次)。当天血常规提示:红细胞2.88×1012/L、血红蛋白92 g/L、红细胞压积29.4%;予以输注悬浮红细胞35 mL(20 mL/kg),次日(输血后24 h)患儿出现频繁血氧饱和度下降及呕吐大量不消化胃内容物;腹部立位平片显示腹部肠管积气较多,未见明显肠管扩张及宽大气液平面,双侧膈下未见明显游离气体(图3),诊断为NEC。治疗:予以禁食15 d、静脉营养及抗感染(美罗培南)等积极内科治疗,腹胀好转,再开始母乳喂养,过程顺利,于生后第52天出院(纠正胎龄35 W,体重2.49 kg(50th~90th))。

图3 病例2生后26 d(输血后24 h)腹部平片
3 病例三 患儿母亲系G1P1,孕29 W+4,患儿于我院剖宫产娩出,出生体重1140 g,生后Apgar评分1分钟7分,5分钟8分。生后第3天开始早产奶喂养,加奶过程顺利。生后第11 d(奶量17 mL/次,每3小时1次)患儿无明显诱因出现腹胀,查血常规:白细胞12.71×109/L、红细胞2.81×1012/L、血红蛋白98 g/L、红细胞压积30.9%;予以输注悬浮红细胞25 mL(18 mL/kg),静脉输注,5 mL/h,输血后2 h患儿出现反应差、反复呼吸暂停、腹胀加重、皮肤苍灰、四肢花斑等循环障碍表现。腹部彩超显示:上腹部肠腔积气,肠蠕动慢;腹壁少量积液;门脉少量积气。立即予以呼吸机辅助通气、禁食、抗感染(美罗培南+替考拉林)及支持治疗,患儿病情无好转,患儿家属拒绝手术治疗并放弃治疗后死亡。
讨 论
早在1987年McGrady等在病例对照研究中发现,红细胞输注是新生儿坏死性小肠结肠炎发生的高度相关危险因素,82%的患儿在发生NEC之前至少有1次输血[5]。随着对输注红细胞及NEC研究的深入,多项回顾性研究[4,6-15]报道了输注红细胞与NEC之间的相关性,且输血相关性坏死性小肠结肠炎一般发生于输注红细胞48 h内[16]。这与本文报道病例的输血后发病时间符合。2012年MOHAMED和SHAH等通过对4项研究分析认为NEC发生与输注红细胞有关(OR 2.01,95% CI 1.61~2.50)[17]。由KIRPALANI和ZUPANCIC进行的研究表明输血可以增加NEC的发生率(未校正OR 7.48,CI 5.87~9.53)[18]。然而,2017年GARG[19]和HAY[20]通过对观察性研究分析指出:没有可靠的证据证明输注红细胞与NEC有关。但值得注意的是,由GARG等在对17项已经报道的观察性研究数据进行分析发现,其中4项队列研究的数据显示:输注红细胞可以降低NEC的发生风险率(OR=0.51,95%CI 0.34~0.75)且不同研究间异质性较低,而作为对比的同时,研究者对13项病例对照研究数据分析时发现NEC与输注红细胞无关(OR 1.20,95%CI 0.58~2.47)且相关研究具有较高的异质性。上述荟萃分析之间结论的差异可能是由于发表偏倚所致。因此,在缺乏高质量数据的情况下,输注红细胞是否为NEC的独立危险因素需要进一步的动物试验及前瞻性的临床研究来证明。
1 TANEC可能存在的发病机制 NEC的发生是由多种病因共同作用的结局,其发病机制主要集中在肠道黏膜屏障功能完整性的破坏和炎症反应等。目前,一些动物试验及临床研究已经提出了输注红细胞可能引起肠道损伤。
1.1 缺氧和肠系膜血流异常:新生儿肠道血流阻力低,其有利于血管扩张,增加血管血流速率及O2的运输,严重的贫血可能会改变新生儿肠道血管阻力,导致肠道持续的低流量灌注及缺氧[21],有假说提出缺氧可以导致肠道黏膜的损伤和愈合能力下降[22,23]。新生儿的肠道组织是随着肠道的延长和粘膜的增生而发育的,在代谢活动中及肠粘膜增生中,血管因子的主动表达可以保证血管发育伴随之肠道组织的发育。而发育相对薄弱的小血管可能在结构上比较脆弱,一旦暴露于输血、缺氧、血压及血流改变等情况下,这些脆弱的血管就容易受损伤[15,21,24]。缺血再灌注损伤被认为是输血相关性NEC的原因之一,邹芸苏等研究发现在输血过程中,肠道的氧饱和度变动范围较大[25],表明输血可影响肠道局部组织血流,在输注红细胞的过程中可改变早产儿肠道血流动力学,早产儿因肠道发育不成熟及自主血流调节功能差,易发生缺血-再灌注损伤。其发生机制主要是产生直接导致损伤活性氧化物及中性粒细胞趋化因子,引起组织损伤包括微脉管系的闭塞和通透性增加,活性氧物质代谢产物释放、细胞毒性酶释放及机械损伤等[26]。与此同时,目前普遍治疗新生儿贫血所使用的输血剂量为15~20 mL/kg红细胞,其液体量相当于1 kg的早产儿总循环量的17%,这可能会导致肠道处于过度充血状态,加重输血相关循环过载(TACO)的潜在风险[27]。近来越来越多的研究采用近红外光谱(NIRS)来测量肠道组织氧合情况,刘露等利用NIRS监测肠道组织氧饱和度(rSO2)发现,喂养耐受的患儿在输注红细胞过程中rSO2较红细胞输注前2 h明显升高[28]。
1.2 炎性细胞因子的产生和内皮细胞免疫活化:输血或者贫血引起NEC的发生可能是二次打击的结果,类似于输血相关性肺损伤(TRALI)[15],在TRALI中,潜在的病理因素(如创伤、感染)导致宿主的内皮细胞活化(第一次打击);输血和相关炎症介质的暴露可产生第二次打击,比如HLA抗体的活化、游离的血红蛋白及红细胞膜碎片均可能导致严重的炎症反应及相关的肺损伤。目前普遍认为早产儿肠道的免疫反应处于易于激活状态,一旦有些相关病因发生,如基底膜的暴露、缺氧、抗生素相关的肠道菌群失调及配方奶喂养等易产生炎症反应[29]。本文3例TANEC均发生在极低出生体重早产儿,考虑与该机制有关。在这样的背景下,加之红细胞在储存过程中可能产生一些生物反应修饰因子,比如供体抗体、存储在血液里的细胞因子、游离的血红蛋白、红细胞膜上的脂质及外源性生物反应调节剂等,均可能产生过度免疫反应,导致肠道黏膜的炎症和损伤[3,30]。DANI等通过研究20名胎龄小于32周的婴儿输血后血清细胞因子的改变,发现输血后干扰素-γ、单核细胞趋化蛋白-1、细胞内粘附分子-1和白细胞介素-1b、白细胞介素-8、白细胞介素-17均显著增加,从而进一步表明输血相关免疫调节(TRIM)的机制,输注红细胞可以触发免疫细胞活化并且对血管内皮细胞、上皮细胞及先天性免疫细胞产生促炎作用,导致相关细胞因子的释放[31]。HO等在临床观察性研究中发现47名早产儿在接受输血后,其来源于肠黏膜和管腔中活化的中性粒细胞的粪钙卫蛋白的水平增加,表明输血可导致新生儿肠道发生亚临床炎症反应,但是在易感的婴儿中,过度的粘膜反应可能在临床上表现为NEC[32]。
2 TANEC的预防
2.1 关于脐带结扎的时间:目前普通的共识认为延迟脐带结扎对新生儿有利,其可以增加出生时血红蛋白的水平,改善过渡时期的循环、减少输血的需求、降低NEC及脑室出血的发生率。因此,建议在条件允许的情况下,在新生儿出生后至少30 s~60 s后再行脐带结扎[33]。据文献报道接受脐带延迟结扎的患儿患NEC的风险比出生后立即行脐带结扎患儿的风险低[34]。CHIRUVOLU等在一项队列研究中发现,延迟脐带结扎60 s的新生儿NEC的发生率为0[35],这可能因为延迟脐带结扎可以使胎盘中血液更多的流入新生儿体内,可增加新生儿血容量,改善肠道缺氧症状[36]。
2.2 减少医源性失血:医源性失血是导致早产儿贫血及需要输血的主要原因。在NICU里常见的减少医源性失血的方法包括无创检测以及利用脐带血做入院检查[37]。减少医源性失血可以防止早产儿贫血的发生,间接减少输血的次数,从而对预防TANEC的发生具有积极作用。
2.3 促红细胞生成素的运用:存在母乳的促红细胞生成素可能在肠道发育、细胞修复及抑制炎症因子的产生方面起到重要作用[38,39]。LEDBETTER和JUUL首次报道了人重组红细胞生成素与NEC的相关性,对小于1250 g的新生儿身上使用人重组促红细胞生成素可以降低NEC的发病率,该研究提出促红细胞生成素与其受体的结合可引起相关信号通路的活化,激活抗凋亡基因,从而预防NEC的发生。EPO对早产儿发生NEC的保护作用还可以通过预防早产儿贫血而得到加强[40]。据文献报道在早期使用EPO(出生后小于8 d)和晚期使用EPO(在8~28 d内)的患儿中,前者与安慰剂组相比可以降低NEC的发病率,而后者NEC的发病率与安慰剂组及对照组无明显差异[41,42]。
2.4 输血中暂停喂养对TANEC的作用:在输血过程中暂停喂养可以减少NEC的发生[43]。王琦凡等研究中发现暂停喂养组输血后48 h内发生TANEC的比例低于喂养组(3.7%比17.3%)[44]。TERRI等利用NIRS监测输血期间喂养的婴儿肠系膜氧合(rSO2)情况时发现,输血期间喂养的婴儿在输血后喂养的15 h内餐后rSO2的水平降低[45],这与KRIMMEL等利用多普勒技术发现输血期间喂养的婴儿,其肠系膜血流速度下降相符合,表明输血期间喂养可能增加肠道氧需求从而导致输血后餐后肠道血液灌注延迟,增加肠道缺血风险[46]。
综上所述,TANEC常发生在极小早产儿,且发病时间较早,提示肠道发育不成熟及神经调节不良仍是早产儿易患TANEC的基础[46]。输注红细胞可能导致组织缺氧、肠系膜血流动力学紊乱以及过度的免疫反应,最终导致肠道黏膜损伤,发生NEC。使用EPO、延迟脐带结扎、减少医源性失血可以预防贫血,减少输注红细胞的次数,从而防止TANEC的发生,但是否与NEC的发病直接相关需要进一步前瞻性的临床研究及动物试验来证实。输血过程中暂停喂养可以减少TANEC发生,其相关机制可能与喂养导致肠系膜氧合改变有关,但其具体临床实践仍存在争议。
利益冲突 所有作者均声明不存在利益冲突

