吸附-缓释Se(IV)材料的吸附性能及机理初探
李佳媛,田欢,,徐峰,姚凌阳,魏昌华,,鲍征宇,,
(1.中国地质大学(武汉) 材料与化学学院,湖北 武汉 430078;2.安康国硒源科技有限公司,陕西 安康 725000; 3.中国地质大学(武汉)浙江研究院,浙江 杭州 311300)
硒是人体必需的微量元素,缺硒会导致人体内一些重要器官的功能失调,从而引发多种疾病[1]。统计显示,中国大部分地区和人群处于缺硒状态[1]。过量的无机硒具有极大的毒性,并不适用于人体吸收利用,植物可通过光合作用将无机硒转化为安全性较高的有机硒,成为人和动物摄入硒的主要来源[2-4]。然而,植物的含硒量并不高,只有0.05~1.5 mg/kg[1],难以满足人们对日常补硒的需求。因此,通过向土壤中施加外源硒,以提高其总硒和有效硒含量,是实现作物富硒最直接有效途径。
本文选择天然的吸附材料(如坡缕石、活性炭、膨润土、蛭石),通过pH、反应时间以及吸附质浓度的单因素实验[5],得出最适宜吸附硒的条件,旨在寻找一种具有高效吸附、缓慢释放特点的材料,以此调节土壤中硒的含量,进而提高作物硒含量,为缺硒人群补硒提供更多的选择。
1 实验部分
1.1 试剂与仪器
坡缕石、活性炭、膨润土、蛭石均为工业品;亚硒酸钠、盐酸、氢氧化钠、硼氢化钾、硒标准储备液均为分析纯;超纯水。
AFS-933原子荧光光谱仪;FT-IR-6700傅里叶红外光谱仪;ASAP 2020 PLUS HD88物理-化学吸附仪;PgUV-10-AS超纯水机;PHS-3C pH计;THZ-82A恒温水浴振荡器;TD5A医用离心机;UP电子分析天平。
1.2 硒的吸附实验
配制硒浓度50 mg/L的亚硒酸钠溶液,其初始pH为6.85。取15 mL硒溶液转入带密封盖的100 mL离心管中,加入0.500 0 g吸附材料,于25 ℃水浴中以200 r/min的转速振荡24 h。将离心管于4 000 r/min下离心20 min,取上清液,采用原子荧光光谱仪(AFS)测定[6-9]硒含量,计算材料对硒的吸附量。

式中C0——空白溶液平均浓度,mg/L;
Ct——吸附后溶液平均浓度,mg/L;
m——吸附质质量,g。
2 结果与讨论
2.1 坡缕石、活性炭、膨润土、蛭石粉的吸附性能 比较
坡缕石化学式为Mg5Si8O20(OH)2(H2O)4·nH2O,它是一种多孔且比表面积较大的天然矿物,坡缕石通过改性可制备净水剂,用于处理重金属超标的废水[10];活性炭主要成分为碳,活性炭表面具有无数细小孔隙,表面积很大,吸附容量相当高[11];膨润土的化学成分为(Na,Ca)0.33(Al,Mg)2[Si4O10](OH)2·nH2O,其主要矿物成分蒙脱石是一种片层结构的硅酸盐,由于膨润土晶包形成的层状结构中氧层与氧层的联系力比较小,容易致使水与其他极性分子通过、进入[12]。蛭石化学式为(Mg,Al,Fe)6[(Si,Al)8O20](OH)48H2O,属于三八面体和二八面体铝硅酸盐类,具有很强的吸附性[13],是一种廉价易得而且效果突出的吸附硒材料[14],实验结果见图1。

图1 膨润土、坡缕石、活性炭、 蛭石对Se(IV)的吸附量对比图Fig.1 Comparison diagram of adsorption capacity of Se(IV) by bentonite,palygorskite, activated carbon and vermiculite
由图1可知,4种天然材料对Se(IV)的吸附能力差异显著,其中活性炭和蛭石吸附量最大,其次是坡缕石,膨润土吸附能力最弱。50 mg/L的亚硒酸钠溶液初始pH为6.85,在该pH值时,Se(IV)主要以HSeO3-的形式存在[15],对比分析几种材料的结构,蛭石中的—OH相对较多,故存在更多的吸附位点[10],因此蛭石对Se(IV)的吸附能力较强。
综合考虑本实验结果和原料成本,选择蛭石作为后续研究材料。
2.2 pH值对蛭石吸附硒的影响
蛭石的平均吸附量与pH的关系见图2。

图2 溶液pH值对蛭石吸附性能的影响Fig.2 Effect of pH on adsorption of Se(IV) by vermiculite

图3 硒的pE-pH图[15]Fig.3 pE-pH diagram of selenium[15]
由图2可知,随着pH值升高,蛭石吸附硒的能力下降。由图3可知,溶液中Se(IV)的存在形态随pH值变化而异,pH<2.5时,硒主要为H2SeO3,pH=2.5~8时,硒主要为HSeO[3-15],因此,蛭石对Se(IV)的吸附类型以阴离子吸附交换为主。通常阴离子交换是由断面破键水解造成的,主要与结构层所带的正电荷有关,受溶液环境影响较大[16]。当pH值下降时,与阴离子基团竞争的氢氧根离子也减少,有利于蛭石吸附Se(IV)[17]。
蛭石吸附硒的能力之所以与pH值呈负相关,其机理可能为,当溶液pH值相对于结构层端等电点偏酸性一侧时,晶层边缘发生的反应为:M-(OH)+H+→[M-(OH2)]+(M为溶液中的Na+)[16],即边缘端面带正电,有利于对含Se(IV)阴离子的吸附;当溶液pH值相对于结构层端面等电点偏碱性一侧时,晶层边缘反应为:M-(OH)+(OH)-→[M-O]-+H2O[16],不利于对含Se(IV)阴离子的吸附。
2.3 蛭石的吸附动力学
配制50 mg/L的亚硒酸钠溶液,用盐酸调节其pH约为3。使用移液管吸取15 mL溶液,分别加到27根离心管中,将27根离心管置于恒温水浴振荡器中,温度为25 ℃,转数为200 r/ min,加盖后振荡。27只离心管分为9个组。每个组3份。每组振荡时间依次为5,10,20,30 min,1,2,4,8 h。每1组结束振荡后,立即取出,擦干管外壁的水珠,置于离心机中,4 000 r/ min离心分离20 min。取上清液0.1 mL,定容至10 mL离心管中。上机测试。实验数据用动力学一级方程和二级方程拟合[7]。
一级动力学方程:
ln(Ce-Ct)=ln(Ce)-kt
二级动力学方程:
式中k——动力学一级方程速率常数,L/min;
Ce——硒离子的平衡浓度,mg/L。
吸附过程一般包括三个阶段:颗粒外部扩散阶段、孔隙扩散阶段和吸附反应阶段[8]。一般情况下,孔隙扩散为速控步。根据Weber-Morris模型[9]:
式中KWM——孔隙扩散常数;
C——边界层、厚度对吸附过程的影响。
KWM值越大,表示吸附质在吸附剂中的扩散越容易。C越大,表示边界层对吸附过程的影响程度越大[9]。亚硒酸钠溶液Se(IV)浓度随时间变化趋势见图4。

图4 蛭石对Se(IV)的吸附速率图Fig.4 Rate of adsorption of Se(IV) by vermiculite
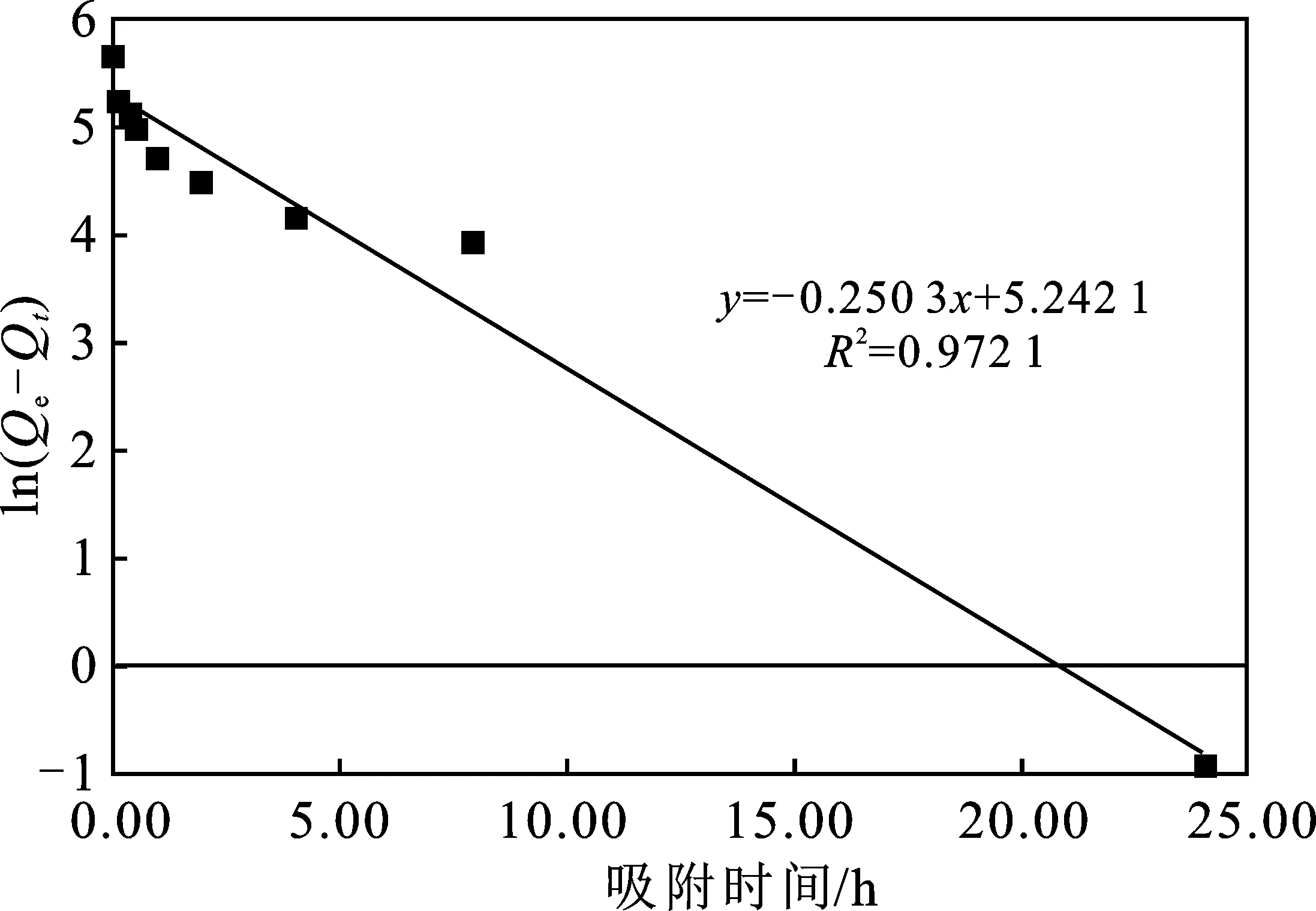
(a)一级动力学模型
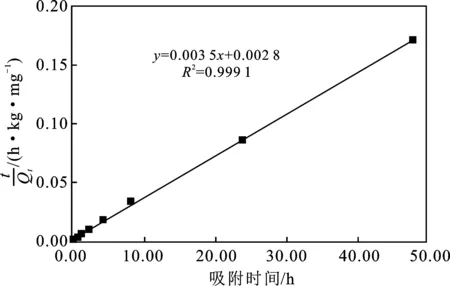
(b)二级动力学模型

图6 蛭石吸附Se(IV)的孔隙扩散模型Fig.6 A pore diffusion model for vermiculite adsorption Se(IV)
由图4,图5可知,二级反应方程回归的线性系数为0.999 1,一级反应方程回归的线性系数为0.972 1,所以蛭石吸附Se(IV)可能为二级反应[7]。由图6可知,Weber-Morris曲线拟合线性系数为0.984 6,说明孔隙扩散是吸附过程的速控步;但是Weber-Morris拟合直线并没有经过原点,C较大,说明除了孔隙扩散阶段,颗粒外部扩散阶段也不可忽略[9]。
2.4 蛭石的吸附等温曲线
配制50,40,30,20,10 mg/L的亚硒酸钠溶液,用盐酸分别调节其pH为1和3左右。固液比1∶30,称取蛭石粉0.500 0 g于100 mL离心管中,分别加入50,40,30,20,10 mg/L的亚硒酸钠溶液,每组3份,一份空白。将离心管置于恒温水浴振荡器中,设定温度为25 ℃,转数为200 r/min,加盖后振荡24 h。 将振荡后的30根离心管从振荡器中取出,擦干管外壁的水珠,置于离心机中,4 000 r/min离心分离20 min。上机测试,计算吸附容量qe,图7是不同pH值时,蛭石对Se(IV)的吸附等温线。
由图7可知,随着初始浓度的增加蛭石对Se(IV)的吸附量先增加后趋于平稳。对图7数据Langmuir和Freundlich 模型进行拟合[7],结果见表1。

图7 蛭石对Se(IV)的吸附等温线Fig.7 Adsorption isotherm for adsorption of Se(IV) by vermiculite

表1 蛭石吸附Se(IV)的Langmuir和Freundlich 模型参数Table 1 Parameters of Langmuir and Freundlich models for vermiculite adsorption of Se(IV)
由表1可知,蛭石吸附硒用Freundlich 模型拟合结果较好。
2.5 蛭石改性对硒吸附的影响
2.5.1 高温改性 高温改性蛭石对硒的吸附量见图8。

图8 高温改性蛭石对Se(IV)的 吸附量变化曲线Fig.8 Change curve of adsorption capacity of high temperature modified vermiculite
由图8可知,改性温度越高,蛭石对硒的吸附量越低。原因可以从两个方面进行解释:(1)蛭石高温易膨胀,比表面积增加,吸附量也应该增加;(2)蛭石晶格中其他金属阳离子的竞争[18],造成硒的吸附量下降。本研究中,可能是由于(2)的影响大于(1),总体表现出吸附量降低的趋势。
2.5.2 酸改性 强酸改性蛭石对硒的吸附量见图9。

图9 强酸改性蛭石对Se(IV)的 吸附量变化曲线Fig.9 Curve of adsorption capacity of vermiculite modified by strong acid
由图9可知,1 mol/L盐酸改性的蛭石对Se(IV)的平衡吸附量大于原始蛭石的平衡吸附量,而3,6,10,12 mol/L盐酸改性的蛭石吸附Se(IV)的能力均下降。这可能是因为高浓度的酸洗脱了蛭石上面的铁离子和铝离子,未能使蛭石携带更多的正电荷,从而减弱了对Se(IV)的吸附能力,也可能是高浓度的酸破坏了蛭石的晶体结构,使得蛭石不具备吸附能力。
2.6 蛭石的表征
2.6.1 物理特性 矿物学意义上的蛭石为两层硅氧四面体片(T)的活性氧相对中间结合一层镁氧八面体片(O)组成的TOT型层状硅酸盐矿物,其层间域含有可交换性水化阳离子与水分子[19]。原始蛭石、700 ℃高温改性蛭石和1 mol/L盐酸改性蛭石的表面物理特性见表2。

表2 改性前后蛭石的物理特性Table 2 Physical prosperities of unmodified and modified vermiculite
由表2可知,原始蛭石和改性蛭石的平均孔径均在6.01~6.43范围内,可归类为介孔材料,具有较强的物理吸附性能。高温改性蛭石的比表面积有所增加,微孔体积几乎没有变化;酸改性后蛭石的比表面积、微孔体积显著增加,因此酸改性蛭石的吸附量最高。
2.6.2 红外光谱表征 图10为改性蛭石红外光谱图。

图10 改性蛭石表面官能团的红外光谱图Fig.10 Infrared spectrogram of surface functional groups of modified vermiculite
由图10可知,3 400 cm-1左右为—OH伸缩振动,1 000 cm-1为O—Si—O伸缩振动,1 600 cm-1左右为H2O的伸缩振动,450 cm-1左右为Mg—O键。由图10可知,酸改性蛭石的—OH峰强度增强,高温改性蛭石的—OH峰强度减弱,酸改性后的蛭石中H2O含量明显上升,高温改性和酸改性后的蛭石O—Si—O伸缩振动均下降。
高温和酸均对蛭石的硅氧键造成破坏,低浓度的酸改性后,蛭石结构中—OH的含量显著上升,增加了吸附位点,对Se(IV)的吸附显著上升;高温改性后,蛭石中—OH结构减少,吸附位点减少,对于Se(IV)的吸附有所下降[10]。
2.7 蛭石的脱附实验
将3组0.500 0 g蛭石置于pH=3,15 mL 浓度50 μg/L亚硒酸钠溶液中,于25 ℃下吸附24 h。吸附后的蛭石分为3份,每份0.300 0 g,第1份中加入pH=7的中性溶液,第2份中加入pH=5的酸性溶液,第3份中加入pH=9的碱性溶液。北方土壤普遍偏碱性,南方土壤普遍偏酸性。本实验模拟吸附材料在pH值不同的土壤中的脱附能力,结果见表3。

表3 蛭石中Se(IV)随时间的脱附量(μg)Table 3 Desorption of Se(IV) over time in vermiculite (μg)
由表3可知,酸性条件有利于蛭石中吸附的Se(IV)被解吸下来,而碱性条件则不利于硒的脱附,因此酸碱性对硒的解吸附影响较大。同时,在不同酸性条件下,蛭石中硒的解吸附量均在第4 d时达到最大,这说明硒的脱附时间不受酸度控制。脱附过程是一个脱附-吸附同时进行的过程,反应初期,脱附速率大于吸附速率。从整体来看,溶液中Se(IV)浓度增加。同时,随着Se(IV)浓度增加,脱附速率会加快,而吸附速率减慢。当Se(IV)达到一定浓度时,脱附速率大于吸附速率,从整体来看,溶液中Se(IV)浓度减少。
3 结论
(1)对比坡缕石、活性炭、膨润土、蛭石吸附Se(IV)的能力,筛选出吸附性能佳、环境友好的吸附材料蛭石。蛭石在对Se(IV)符合吸附Freundlich模型,可能为二级反应,孔隙扩散过程是吸附反应的速控步。
(2)高温改性后,蛭石对Se(IV)的平衡吸附量均降低,随着改性温度的升高,蛭石对Se(IV)的平衡吸附量下降。较低浓度的1 mol/L盐酸改性后,蛭石对Se(IV)的吸附能力增强,盐酸的浓度增高,蛭石对Se(IV)的吸附能力减弱明显。
(3)蛭石的脱附量受pH值的影响较大,碱性条件下,蛭石的脱附性能明显减弱。但无论酸碱度如何,蛭石的脱附量均在4 d达到最大。

