针刺配合济生肾气丸治疗阴阳两虚糖尿病肾病的临床观察
刘瑞萍,张世超
(辽宁中医药大学附属医院,沈阳 110032)
糖尿病肾病(diabetic kidney disease, DKD)是糖尿病(diabetes mellitus, DM)最主要的微血管并发症之一,也是发达国家终末期肾脏病的首要病因[1]。DKD发病机制十分复杂,迄今尚未完全明确,发病较为隐匿,其主要临床表现为持续性白蛋白尿、高血压以及进行性肾功能受损[2]。DKD早期临床表现以微量白蛋白尿为主,若早期微量白蛋白尿未得到有效控制则可发展为大量蛋白尿,肾功能将迅速恶化,进入终末期肾脏病,需要肾脏替代疗法维持生命。因此,临床早期诊断DKD并干预治疗对延缓DKD病程进展具有重要意义[3]。目前临床DKD的治疗仍主要采用改变生活方式、控制血糖、控制血压、纠正脂质代谢紊乱、改善微循环等方面[4]。近20年来西医在治疗DKD方面不断研发新的药品,但在临床治疗上仍未达到满意疗效。大量临床试验和研究[5-6]表明,中医特色疗法治疗本病具有多靶点、多层次的治疗机制,而且具有不良反应小、安全性高等优势。本研究在西医常规治疗基础上采用针刺配合济生肾气丸治疗阴阳两虚 DKD患者,并与单纯西医常规治疗相比较,观察其临床疗效。
1 临床资料
1.1 一般资料
纳入88例阴阳两虚DKD患者均来自2018年10月至2019年10月辽宁中医药大学附属医院门诊及病房,采取随机数字表法分为观察组和对照组,每组 44例。观察组中男24例,女20例;平均年龄(66±5)岁;DM平均病程(12.85±3.14)年;DKD 平均病程(2.89±0.83)年;平均体质量指数(body mass index,BMI)为(25.94±3.71) kg/m2。对照组中男25例,女19例;平均年龄(65±5)岁;DM平均病程(13.25±3.29)年,DKD平均病程(3.11±0.57)年;平均 BMI为(26.46±3.73) kg/m2。两组患者性别、年龄、病程、BMI比较,差异无统计学意义(P>0.05)。两组患者依从性良好,未发生脱落病例。本研究已获得辽宁中医药大学附属医院医学伦理委员会批准。
1.2 诊断标准
1.2.1 西医诊断标准
参照《中国2型糖尿病防治指南(2017年版)》[7]相关标准制定Ⅱ型DM诊断标准;参照《糖尿病肾病防治专家共识(2014年版)》[8]相关标准制定DKD诊断标准。
1.2.2 中医诊断标准
参照《糖尿病肾病诊断、辨证分型及疗效评定标准(试行方案)》[9]和《糖尿病肾病中西医结合诊疗规范》[10]。主症为精神萎靡,形寒肢冷,大便泄泻,阳痿,遗精。次症为面色苍白无华,倦怠乏力,面目浮肿,腰酸耳鸣。舌淡、苔白,脉沉迟或沉细无力。凡具有主症表现及2个以上次症表现,符合舌脉者即可诊断。
1.3 纳入标准
①符合中西医诊断标准;②患者年龄 45~80岁;③自愿参与本试验并签署知情同意书。
1.4 排除标准
①Ⅰ型 DM或近期具有糖尿病酮症酸中毒及其他急性并发症者;②合并其他原发性或继发性肾脏疾病及肾毒性药物服用史者;③合并严重心、肺、肝、脑等重要脏器功能障碍者;④妊娠期或哺乳期妇女;⑤精神异常、意识障碍或不配合治疗及拒签知情同意书者;⑥对本试验药物过敏或不耐受者。
2 治疗方法
2.1 对照组
给予西医常规治疗,包括健康教育、适量运动、饮食调节、戒烟戒酒、控制体质量、控制血糖、控制血压、纠正脂代谢紊乱。根据患者血糖、血压、血脂及病情状况合理选用胰岛素制剂、降压药、降脂药。
2.2 观察组
在对照组西医常规治疗基础上,采用针刺配合济生肾气丸治疗。针刺取太溪(双)、太白(双)、脾俞(双)、肾俞(双)和足三里(双),穴位处常规消毒后,持毫针垂直进针,得气后留针30 min,每日治疗1次。济生肾气丸处方为熟地黄15 g,官桂15 g,牛膝15 g,山药30 g,山萸肉30 g,丹皮30 g,车前子30 g,茯苓30 g,泽泻30 g,附子 20 g。由辽宁中医药大学附属医院制剂中心统一煎制,每日1剂,分早、中、晚3次服用。
比较两组护士在自我管理、护理满意度以及护理质量方面的评分。观察组护士各项评分均优于对照组,差异显著(P﹤0.05),有统计学意义。详见表1:
两组患者均连续治疗12周。
3 治疗效果
3.1 观察指标
3.1.1 糖代谢指标、肾功能指标和炎性因子水平
治疗前后分别采用全自动生化仪测定空腹血糖(fasting plasma glucose, FPG)、餐后 2 h血糖(2-hour postprandial blood glucose, 2hPG)、糖化血红蛋白(glycosylated hemoglobin, HbA1c)、尿微量白蛋白(urinary microalbumin, mALB)、尿白蛋白排泄率(urinary albumin excretion rate, UAER)、血肌酐(serum creatinine, Scr)和血尿素氮(blood urea nitrogen, BUN),采用免疫荧光法检测超敏C反应蛋白(hypersensitive C-reactive protein,hs-CRP),采用酶联免疫吸附法检测肿瘤坏死因子(tumor necrosis factor, TNF)-α。
3.1.2 中医证候评分及单一症状评分
记录两组患者治疗前后中医证候评分及单一症状评分。参照《中药新药临床研究指导原则(试行)》[11],根据中医症状轻重程度进行评分,分为无(0分)、轻度(2分)、中度(4分)和重度(6分)。
3.2 疗效标准[11]
显效:临床症状、体征基本消失,疗效指数≥70%,血糖下降1/3及以上,UAER下降1/2及以上。
有效:临床症状、体征明显减轻,疗效指数≥30%,血糖下降不足1/3,UAER下降不足1/2。
无效:临床症状、体征无明显改善甚或加重,疗效指数<30%,血糖、UAER无变化或加重。
疗效指数=[(治疗前总积分-治疗后总积分)/治疗前总积分]×100%。
总有效率=[(显效例数+有效例数)/治疗总例数]×100%。
3.3 统计学方法
采用SPSS19.0统计软件进行统计分析。符合正态分布的计量资料以均数±标准差表示,比较采用t检验;计数资料比较采用卡方检验。以P<0.05表示差异有统计学意义。
3.4 治疗结果
3.4.1 两组临床疗效比较
两组患者治疗12周后,观察组总有效率明显高于对照组(P<0.05),详见表1。
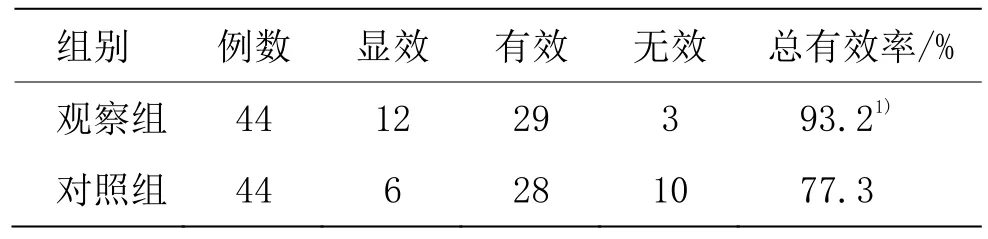
表1 两组临床疗效比较 (例)
3.4.2 两组治疗前后中医证候总评分及单一症状评分比较
表2 两组治疗前后中医证候总评分及单一症状评分比较(每组44例) (±s,分)
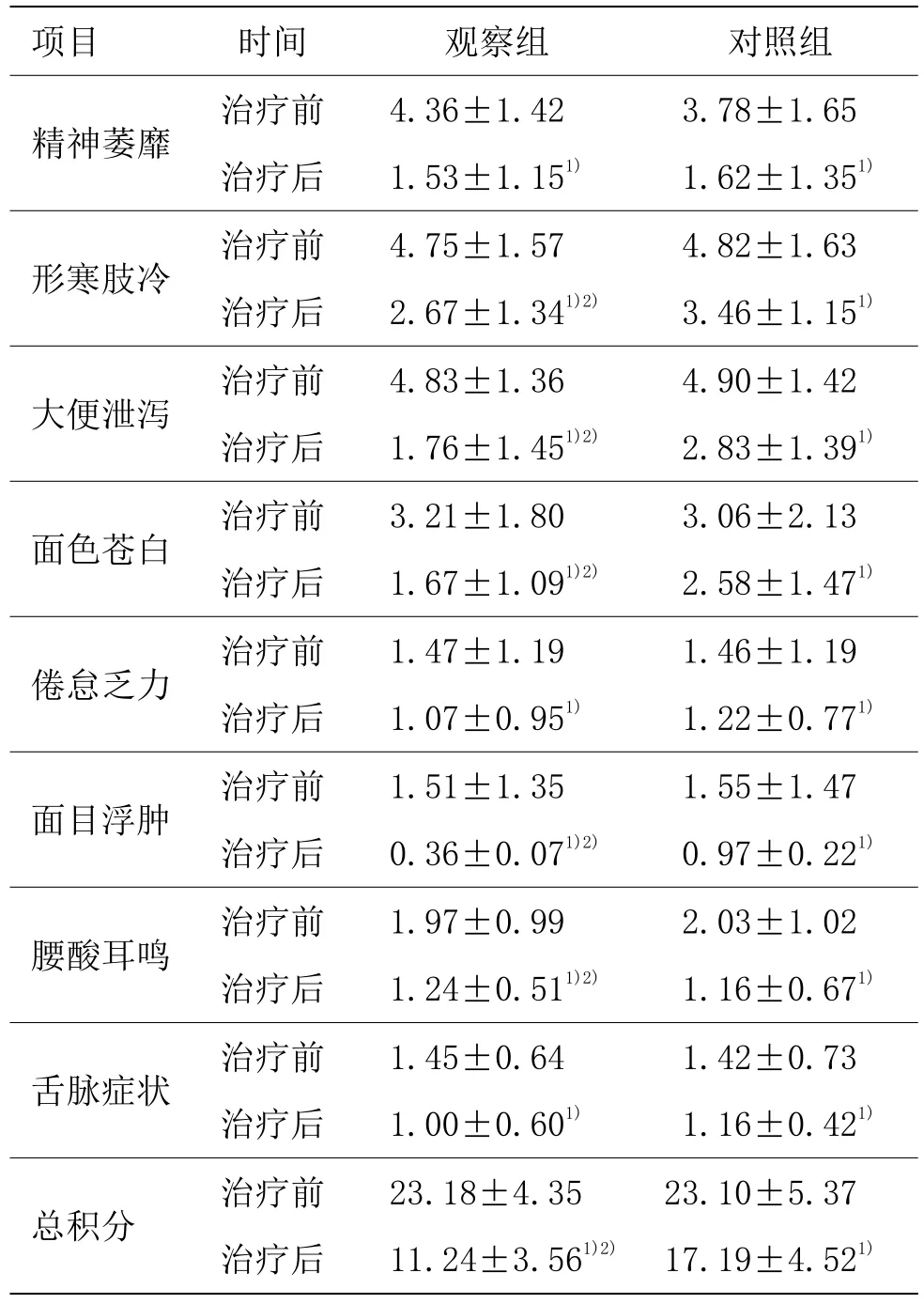
表2 两组治疗前后中医证候总评分及单一症状评分比较(每组44例) (±s,分)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05
项目 时间 观察组 对照组精神萎靡 治疗前 4.36±1.42 3.78±1.65治疗后 1.53±1.151) 1.62±1.351)形寒肢冷 治疗前 4.75±1.57 4.82±1.63治疗后 2.67±1.341)2) 3.46±1.151)大便泄泻 治疗前 4.83±1.36 4.90±1.42治疗后 1.76±1.451)2) 2.83±1.391)面色苍白 治疗前 3.21±1.80 3.06±2.13治疗后 1.67±1.091)2) 2.58±1.471)倦怠乏力 治疗前 1.47±1.19 1.46±1.19治疗后 1.07±0.951) 1.22±0.771)面目浮肿 治疗前 1.51±1.35 1.55±1.47治疗后 0.36±0.071)2) 0.97±0.221)腰酸耳鸣 治疗前 1.97±0.99 2.03±1.02治疗后 1.24±0.511)2) 1.16±0.671)舌脉症状 治疗前 1.45±0.64 1.42±0.73治疗后 1.00±0.601) 1.16±0.421)总积分 治疗前 23.18±4.35 23.10±5.37治疗后 11.24±3.561)2) 17.19±4.521)
两组患者治疗后中医证候总评分及单一症状评分均较同组治疗前显著降低(P<0.05)。观察组治疗后形寒肢冷、大便泄泻、面色苍白、面目浮肿、腰酸耳鸣症状评分及中医证候总评分均显著低于对照组(P<0.05),但在精神萎靡、倦怠乏力、舌脉症状方面,两组比较差异均无统计学意义(P>0.05)。详见表2。
3.4.3 两组治疗前后糖代谢指标、肾功能指标和炎性因子水平比较
两组患者治疗后糖代谢指标(FPG、2hPG和HbAlc)均较治疗前降低(P<0.05),且观察组显著低于对照组,两组差异均有统计学意义(P<0.05)。两组患者治疗后肾功能指标(Scr、BUN、UAER和mALB)均较治疗前降低(P<0.05),且观察组显著优于对照组,两组差异均有统计学意义(P<0.05)。两组患者治疗后炎性因子(hs-CRP、TNF-α)水平均较治疗前显著降低(P<0.05),且治疗后观察组炎性因子水平均明显低于对照组,两组差异均有统计学意义(P<0.05)。详见表3。
表3 两组患者糖代谢指标、肾功能指标和炎性因子水平比较(每组44例) (±s)
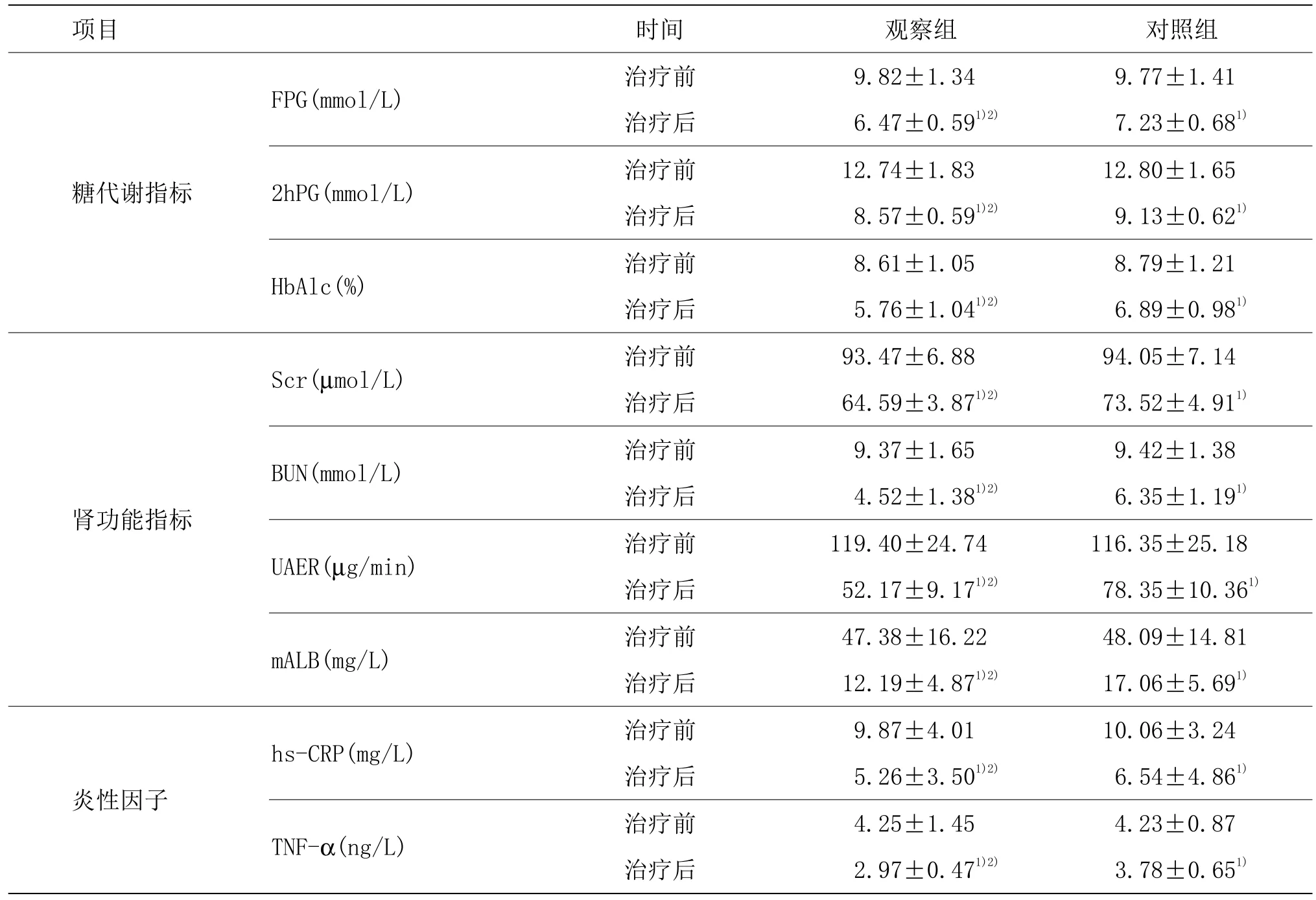
表3 两组患者糖代谢指标、肾功能指标和炎性因子水平比较(每组44例) (±s)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05
项目 时间 观察组 对照组糖代谢指标肾功能指标炎性因子治疗后 6.47±0.591)2) 7.23±0.681)2hPG(mmol/L) 治疗前 12.74±1.83 12.80±1.65 FPG(mmol/L) 治疗前 9.82±1.34 9.77±1.41治疗后 8.57±0.591)2) 9.13±0.621)HbAlc(%) 治疗前 8.61±1.05 8.79±1.21治疗后 5.76±1.041)2) 6.89±0.981)治疗后 64.59±3.871)2) 73.52±4.911)BUN(mmol/L) 治疗前 9.37±1.65 9.42±1.38 Scr(µmol/L) 治疗前 93.47±6.88 94.05±7.14治疗后 4.52±1.381)2) 6.35±1.191)UAER(µg/min) 治疗前 119.40±24.74 116.35±25.18治疗后 52.17±9.171)2) 78.35±10.361)mALB(mg/L) 治疗前 47.38±16.22 48.09±14.81治疗后 12.19±4.871)2) 17.06±5.691)治疗后 5.26±3.501)2) 6.54±4.861)TNF-α(ng/L) 治疗前 4.25±1.45 4.23±0.87 hs-CRP(mg/L) 治疗前 9.87±4.01 10.06±3.24治疗后 2.97±0.471)2) 3.78±0.651)
4 讨论
糖尿病肾病继发于消渴病,在古代文献并无明确记载,根据症状变化情况多归属于中医学“肾消”“尿浊”“水肿”“肾劳”“关格”等范畴[12-15]。DKD病机为阴津亏损,燥热偏盛,病程日久累及于肾,导致肾阴亏虚,阴损及阳,故致阴阳两虚证。肾脏功能失常,封藏之力不足,肾精外泄,发为蛋白尿;阴虚则肾脉不得以濡养,阳虚则气化失常,故症见精神萎靡、形寒肢冷、大便泄泻;男子又可伴阳痿、遗精等肾气不固之证。故立阴阳双补之法,予济生肾气丸以温补肾阳、滋补肾阴、利水消肿。方中附子温肾助阳而消阴翳,熟地黄归滋肾填精而阴中求阳,二药相须为用,同气相求能峻补阴阳;官桂温肾补火,以助膀胱气化;山茱萸滋肾益肝;泽泻、车前子利水渗湿,合桂、附温阳利水;牡丹皮寒凉清泄;山药、茯苓益气健脾,补土制水;牛膝益肝肾而引药下行,助达病位。全方补中寓泻,共奏温补肾阳、滋补肾阴、利水消肿之功,又无滋腻助邪之虞[16-18]。针刺疗法为中医特色疗法之一,具有整体调节、双向调节的作用特点,功用专于通经脉,调气血,平衡阴阳,调和脏腑,是中医学非药物治疗的重要手段之一。研究表明针刺疗法对于DKD的治疗不仅可以作为辅助疗法增加疗效,还可从根本上解决和缓解DKD临床症状,在控制DKD血糖、血脂,调节血流动力学,调节T淋巴细胞活性以及抗氧化应激反应等方面具有明显治疗优势[19-20]。黄迎峰[21]采用益气滋阴汤联合针刺(肾俞、关元、太溪、足三里、三阴交)对DKD气阴两虚证进行治疗,结果显示针药并用对DKD临床疗效良好,可明显改善患者的血糖、血脂水平状态和肾功能。张健豪等[22]研究显示,针刺治疗DKD以调补脏腑为原则,主要采用脏腑辨证和经络辨证,多选用肾俞、脾俞、太溪、关元、足三里、三阴交等穴位以标本兼治。《灵枢·九针十二原》:“五脏有疾也,当取之十二原。”太溪乃足少阴肾经之输穴,同时也是肾之原穴,故选用太溪穴以达补肾之力;太白乃脾之原穴,故针刺太白穴以达补脾之功;二穴互促互助,以补先后天之本。《难经·六十七难》:“阴病行阳,阳病行阴,故令募在阴,俞在阳。”脏病多与背俞穴相关。肾俞穴乃肾之背俞穴,为肾脏之气灌注之处,是治疗肾脏疾病的重要腧穴;脾俞穴乃脾之背俞穴,补益脾气,使脾能运化水液,补后天以养先天。故选用脾俞、肾俞以固护先后天之气。足三里为足阳明胃经之合穴,也是胃之下合穴,乃经脉之气与脏腑之气汇合之处,针刺足三里可通经调脏、强壮补益、平衡阴阳[23]。五穴合用共奏健脾补肾、养阴和阳之效。本研究结果显示,针刺疗法配合济生肾气丸可明显改善阴阳两虚DKD患者的形寒肢冷、大便泄泻、面色苍白、面目浮肿、腰酸耳鸣症状;能够控制阴阳两虚DKD患者血糖;可减少阴阳两虚DKD患者尿蛋白排泄、延缓肾脏功能进行性损害。
DKD发病机制十分复杂,迄今尚未完全明确。目前普遍认为,DKD的发生发展与遗传因素、代谢紊乱、血流动力学改变、炎症反应、氧化应激等诸多因素有关[24-25]。现代研究亦证实慢性持续性炎症反应是 DKD病情持续发展的关键因素[26-27]。hs-CRP为全身炎症标志物,其水平升高可影响肾小球微循环结构,从而造成DKD病情加重[28]。TNF-α是巨噬细胞诱导下产生的细胞因子,其水平升高可加速内皮细胞炎症损伤,影响肾小球毛细血管壁从而加重DKD进展[29]。本研究结果显示,在西医常规治疗基础上,针刺疗法配合济生肾气丸可降低阴阳两虚DKD患者炎性因子,抑制炎症反应,进而延缓肾小球微循环改变。
综上所述,在西医常规治疗基础上,针刺疗法配合济生肾气丸可明显改善阴阳两虚DKD形寒肢冷、大便泄泻、面色苍白、面目浮肿、腰酸耳鸣症状,调节糖代谢及肾功能,降低hs-CRP、TNF-α水平,临床疗效显著。

