2195铝锂合金在N2O4中的浸泡腐蚀研究
郭一,黄智勇,金国锋,田干
(火箭军工程大学 导弹工程学院,陕西 西安 710000)
2195铝锂合金在空气动力学领域被广泛认为是一种理想的轻质高强度结构材料[1]。在铝合金中,每添加1%的锂,可使铝合金密度降低3%,弹性模量提高6%[2]。
由于N2O4的蒸汽压大、沸点低(21.13 ℃)、极易挥发,并具有强烈的刺激性、毒性和腐蚀性,给材料的腐蚀研究工作带来了困难[3-6]。研究表明,N2O4对金属的腐蚀作用主要是其中的硝酸造成的[7]。1978年,美国AFRPL研究了推进剂中含水量对N2O4-HNO3体系的影响。结果表明,30%的硝酸溶液是铝合金的腐蚀的最高点[8-9]。本文以2195铝锂合金在液体推进剂的腐蚀为研究背景,探索2195铝锂合金在N2O4、含6%水N2O4以及30% HNO3中的耐蚀性。
1 实验部分
1.1 材料与仪器
N2O4,工业品;硝酸、乙醇均为分析纯;2195铝锂合金;去离子水。
VEGAIIXMUINCN型扫描电子显微镜;X’Pert Pro MPD型X射线粉末衍射仪;Instron 5569万能试验拉伸机。
1.2 实验方法
1.2.1 试件预处理 2195铝锂合金试件的形状为狗骨状,厚度为2 mm,试件形状及尺寸见图1。
试件除油,120#砂纸打磨,去离子水冲洗,酒精冲洗,试样编号,去离子水冲洗,酒精冲洗,置于烘箱中干燥(60 ℃),在通风状态下自然冷却。称重,将试件置入干燥器保存,实验时取出使用。

图1 试件形状及尺寸(单位:mm)Fig.1 Specimen shape and size
1.2.2 浸泡实验 将试件分别放入以304 L不锈钢为外壳,聚四氟乙烯为内衬的容器中,分别加入N2O4、含6%水N2O4以及30%稀硝酸,压紧,密封,将其浸入至水浴恒温槽,温度设定为20 ℃。以N2O4为腐蚀介质的每隔30 d取1次试件,含6%水N2O4以及30%稀硝酸为介质的每隔5 d取1次试件。将试件清洗处理后,进行称重,利用扫描电子显微镜观察其腐蚀形貌,并对腐蚀产物进行XRD分析,以确定其成分。
1.3 力学性能测试
以初始试件的力学性能为参考,分别将浸泡后的试件进行单向拉伸试验,测试2195铝锂合金的屈服强度(σs)和抗拉强度(σb)以及断裂延伸率,对比腐蚀前后试件力学性能的影响。
2 结果与讨论
2.1 浸泡腐蚀实验数据分析
由表1可知,2195铝锂合金浸泡在N2O4中,几乎没有腐蚀,失重数据可以忽略不计。由于N2O4中水分含量极少(≤0.4%)[10],其中的硝酸含量十分稀少,试件在N2O4中的腐蚀也是非常轻微的,所以在短时间内很难得到结果,也表明了N2O4与2195铝锂合金具有良好的相容性。
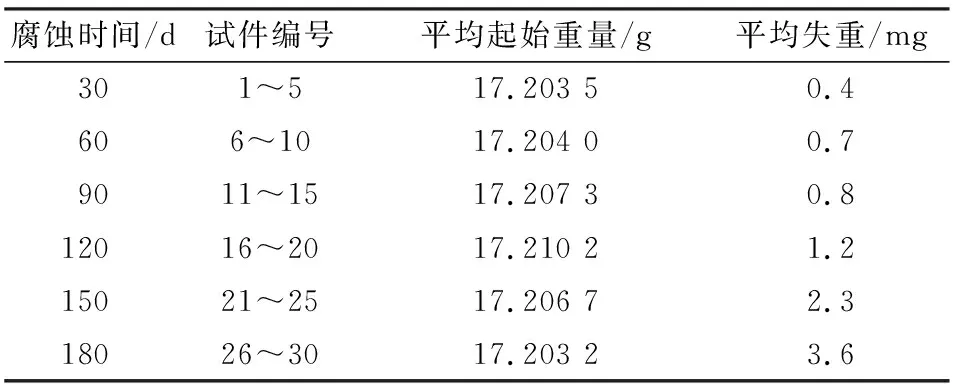
表1 N2O4浸泡实验腐蚀失重数据Table 1 The corrosion weight loss of 2195 Al-Lialloy with N2O4 immersed
由图2可知,2195铝锂合金在含6%水的N2O4中的腐蚀速率远远大于在N2O4中的腐蚀速率。由于在N2O4中加入了6%含量的水,相当于此时HNO3的含量约为30%(见表2),随着腐蚀时间的增长,腐蚀越严重,试件的重量越小。但由于N2O4与水是有限的互溶,必然会造成生成的HNO3在腐蚀介质中分布不均匀,会造成局部腐蚀。通过计算发现,随着时间的增长,腐蚀介质中硝酸的成分逐渐减少,腐蚀失重率呈下降趋势。

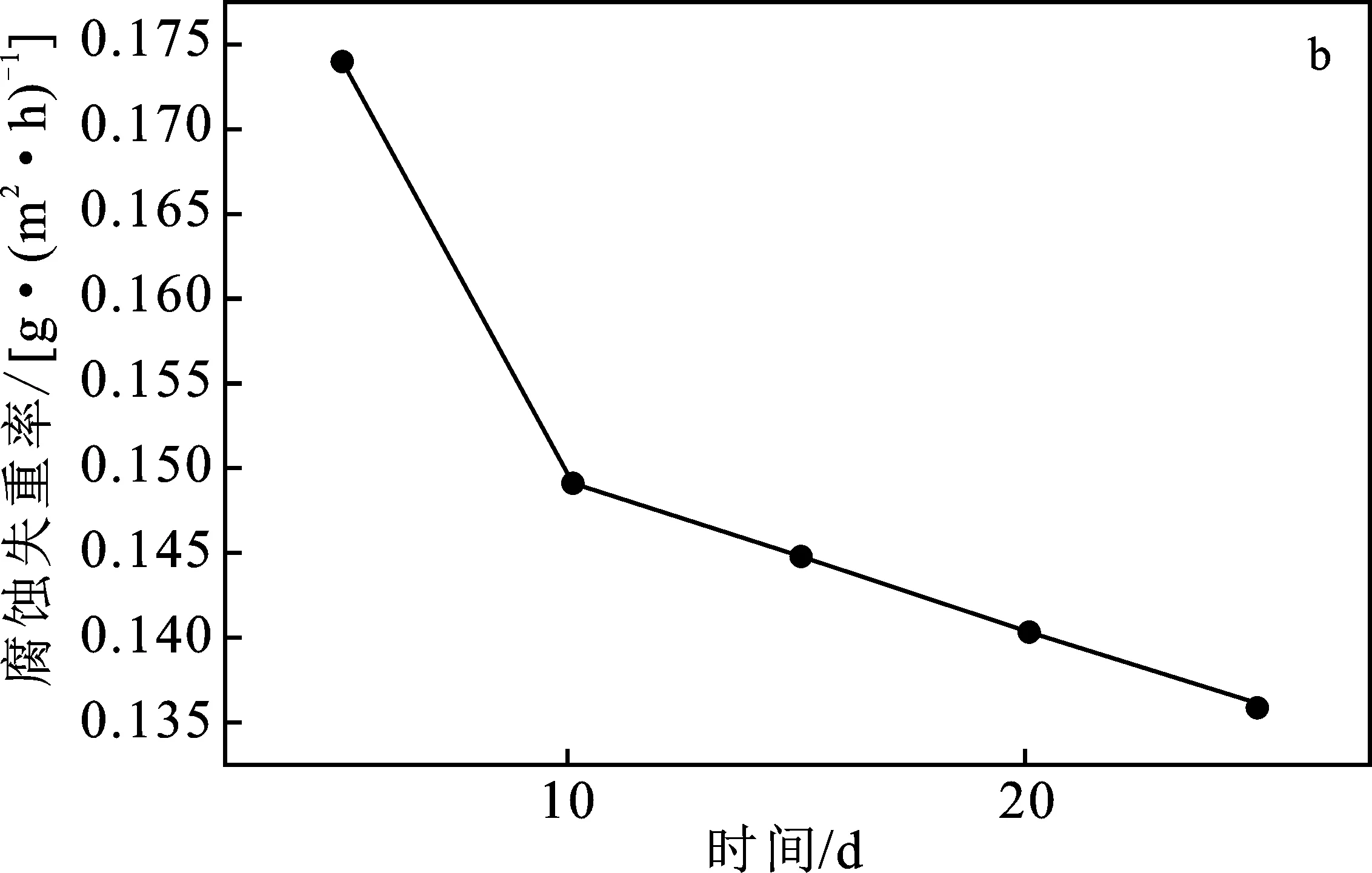
图2 试件在含水6%的N2O4中的失重及腐蚀率随时间的变化Fig.2 Variation of weight loss and corrosion rate ofspecimens with time in N2O4 with 6% watera.腐蚀失重;b.腐蚀率
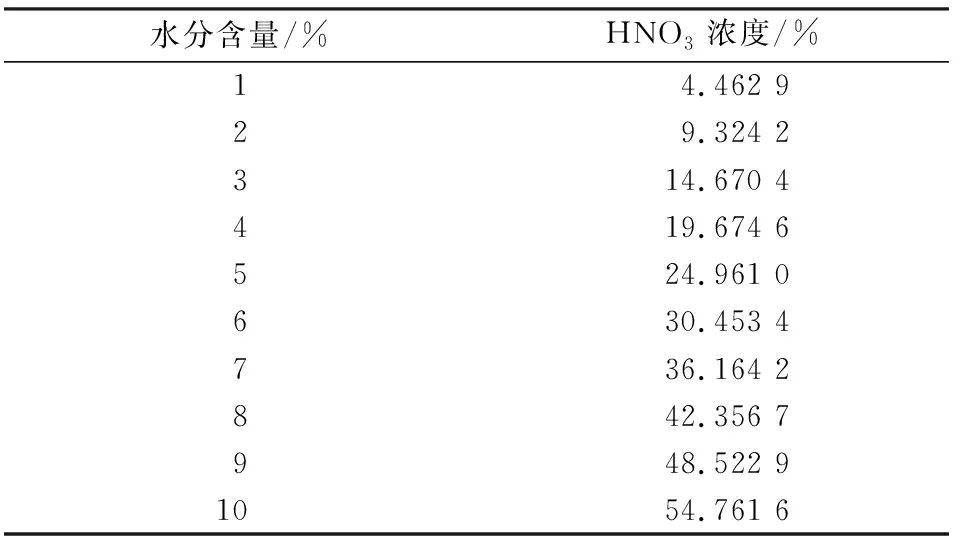
表2 含水量与HNO3的浓度Table 2 Relationship between of wateramount and HNO3 content
由图3可知,2195铝锂合金在30% HNO3中腐蚀速度十分迅速,随着腐蚀时间的增长,腐蚀程度不断加重。通过计算发现,腐蚀率维持在 0.76 g/(m2·h)附近波动,腐蚀失重呈线性增长,腐蚀反应趋于稳定,表明2195铝锂合金在30% HNO3中以恒定的腐蚀速率被侵蚀。
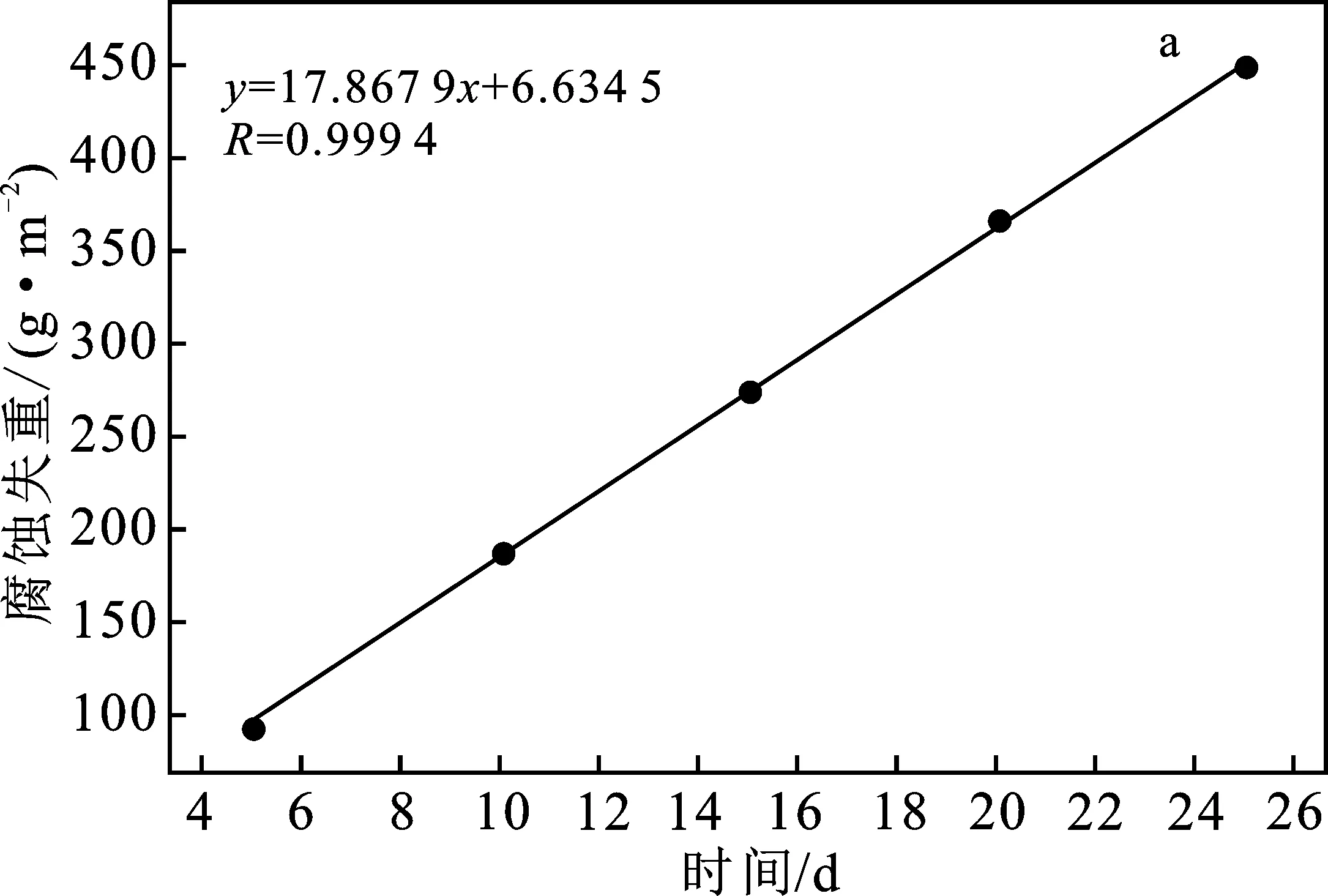
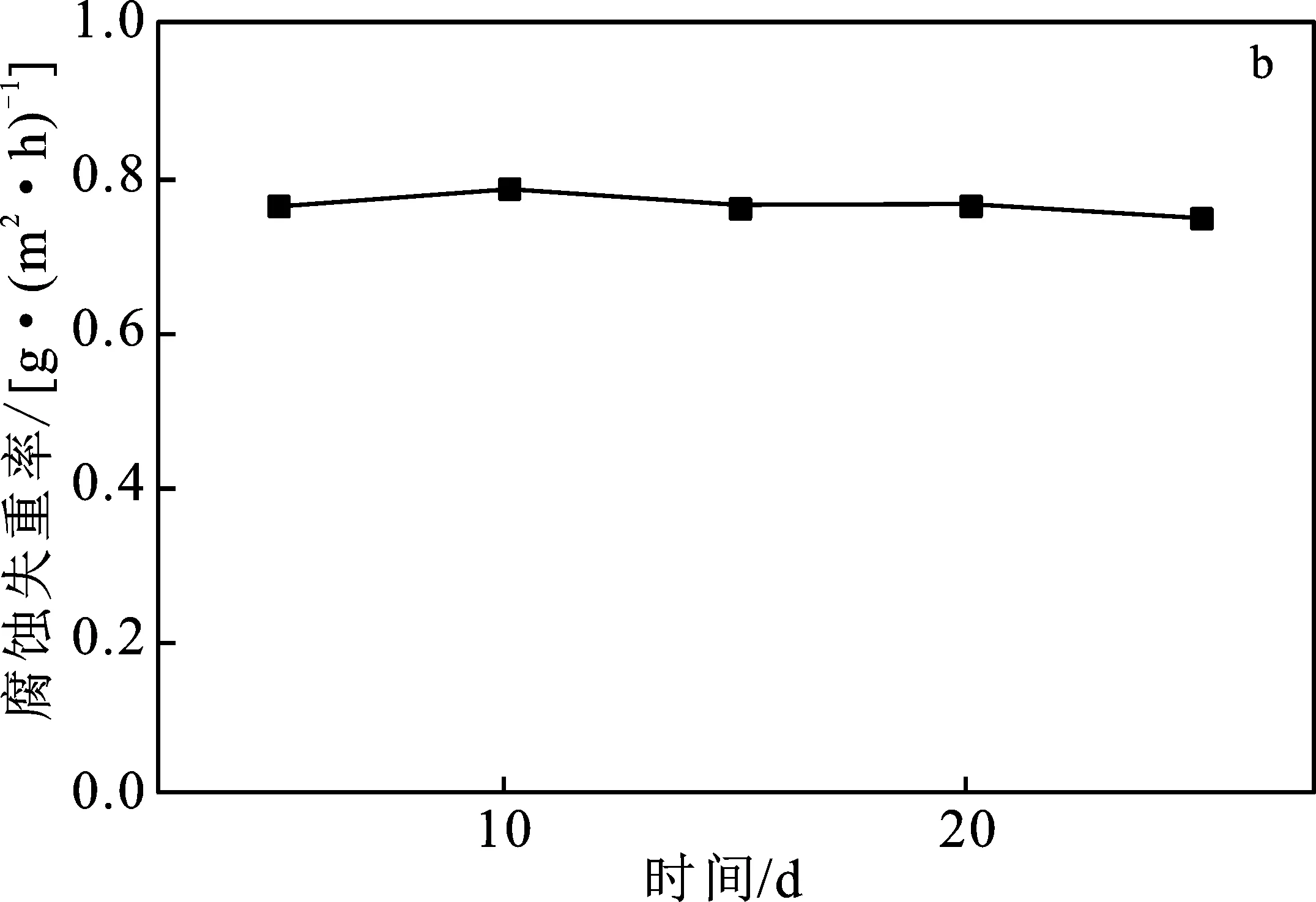
图3 试件在30%HNO3中的失重及腐蚀率随时间的变化Fig.3 Variation of weight loss and corrosion rate ofspecimens with time in 30% HNO3a.腐蚀失重;b.腐蚀率
由腐蚀失重拟合曲线对比可知,2195铝锂合金在30% HNO3中的腐蚀更加剧烈,在30% HNO3中的腐蚀1 d相当于其在含水6%的N2O4中腐蚀6 d。
2.2 腐蚀形貌分析
由图4可知,2195铝锂合金在N2O4中几乎不发生腐蚀,随着浸泡时间的增长,试样表面附着了一些块状物,但是表面仍可看到打磨痕迹。而表面产物则是由于材料中不均匀的夹杂相在溶解过程中生成附着物沉积在合金表面;同时,在取出试件过程中,附着在表面的N2O4与空气中的水分相结合,对基体进一步腐蚀,产生的附着物。

图4 N2O4浸泡试件的表面腐蚀形貌图Fig.4 Surface corrosion morphology of N2O4 immersed specimensa.30 d;b.90 d;c.180 d
由图5可知,2195铝锂合金在含6%水的N2O4中腐蚀现象明显。由于铝锂合金在用砂纸打磨的过程中,不可避免的会造成划痕、边缘斜面等缺陷,会使接触件表面产生微小的腐蚀间隙,形成明显的腐蚀凹坑。浸泡5 d时,即在表面发现了一些不规则的点蚀坑,推测是由于氧化膜的局部破坏形成的局部的微电池从而造成腐蚀;随着浸泡时间的增长,点蚀坑的密度增加,相邻蚀坑由于扩展而相互交错结合,形成面积更大的腐蚀坑;在腐蚀的初期阶段,腐蚀坑的发展以横向为主,点蚀坑聚集在一起;随着腐蚀程度的加剧,增速在逐渐减缓。

图5 含6%水的N2O4浸泡试件的表面腐蚀形貌图Fig.5 Surface corrosion morphology of N2O4 immersed specimens containing 6% watera.5 d;b.10 d;c.15 d;d.20 d;e.25 d
由图6可知,2195铝锂合金在30%HNO3中腐蚀速度很快。浸泡5 d时,腐蚀坑就布满了整个表面;10,15 d时,腐蚀坑的面积及密度不断增大,大片聚集,扩展连成一片,腐蚀坑的深度也在不断增加,局部范围内伴随着片状剥落的现象。而在20,25 d时,表面形貌没有较大的变化,说明2195铝锂合金在30%HNO3中是均匀腐蚀,这与腐蚀失重数据也吻合。

图6 30% HNO3浸泡试件的表面腐蚀形貌图Fig.6 Surface corrosion morphology of 30% HNO3 immersed specimensa.5 d;b.10 d;c.15 d;d.20 d;e.25 d
2.3 腐蚀产物分析
在三组浸泡腐蚀实验中,2195铝锂合金试件表面均有晶体生成。其中在N2O4中,出现黄绿色晶体;含6%水的N2O4中,出现淡黄绿色晶体;在30% HNO3中,出现白色半透明状晶体。XRD衍射分析结果见图7。
由图7可知,腐蚀产物的主要成分为Al(H2O)6-(NO3)3(H2O)3,是Al(NO3)3的一种水合物,即三种介质下的腐蚀产物是一致的,说明了2195铝锂合金在三种介质中的腐蚀为铝与硝酸的反应,最终生成硝酸盐。
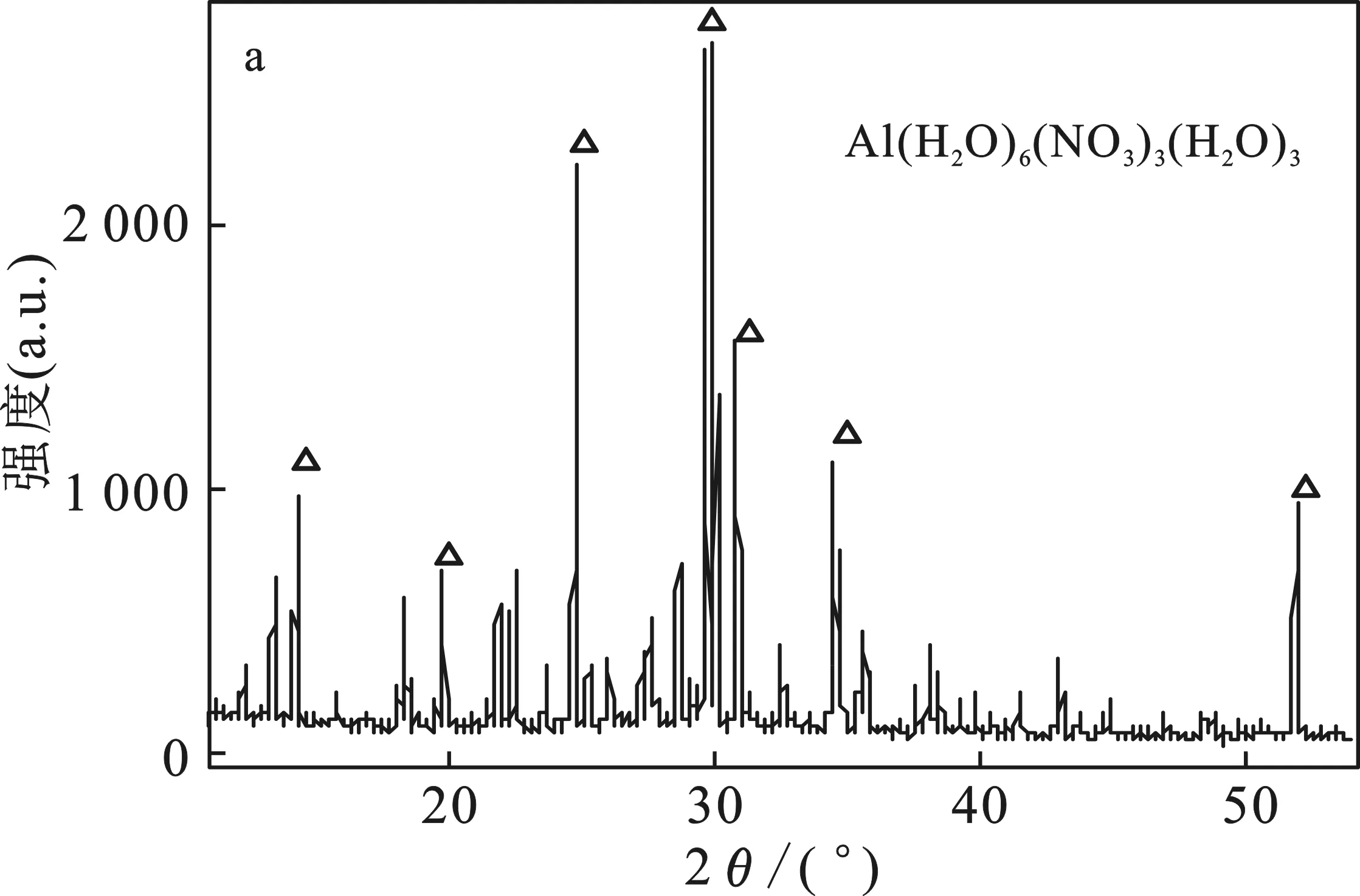
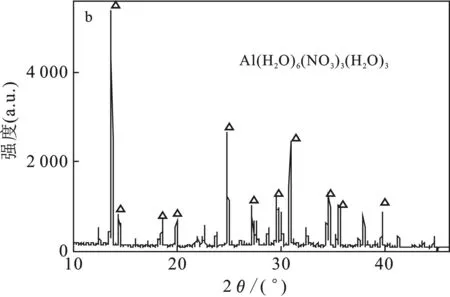
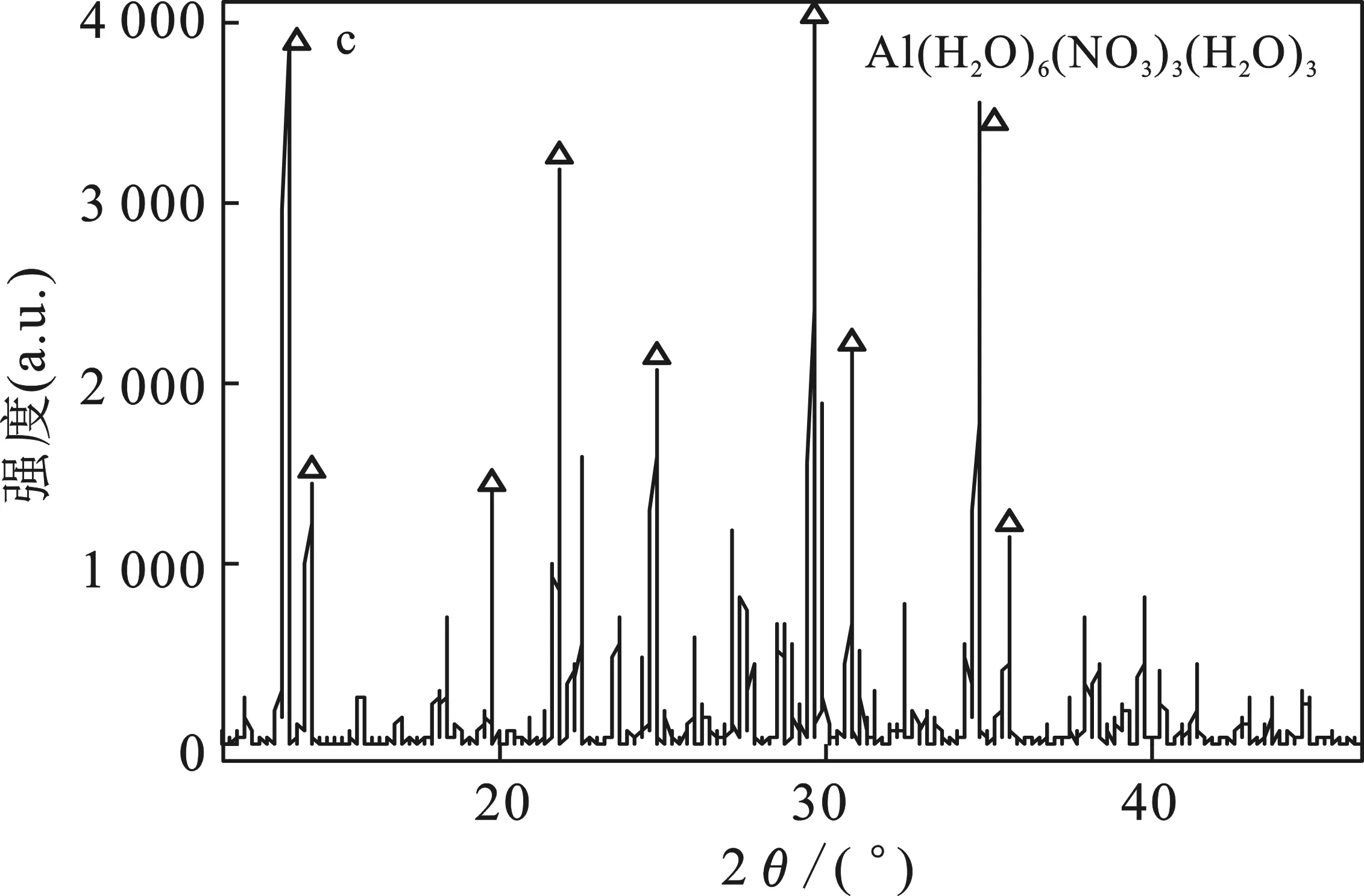
图7 N2O4(a)、含6%水的N2O4(b)及30% HNO3(c)腐蚀试验产物的XRD图Fig.7 XRD of corrosion products of N2O4(a),N2O4 containing 6%H2O(b) and 30% HNO3(c)
2.4 力学性能测试
2195铝锂合金的力学性能测试见图8。

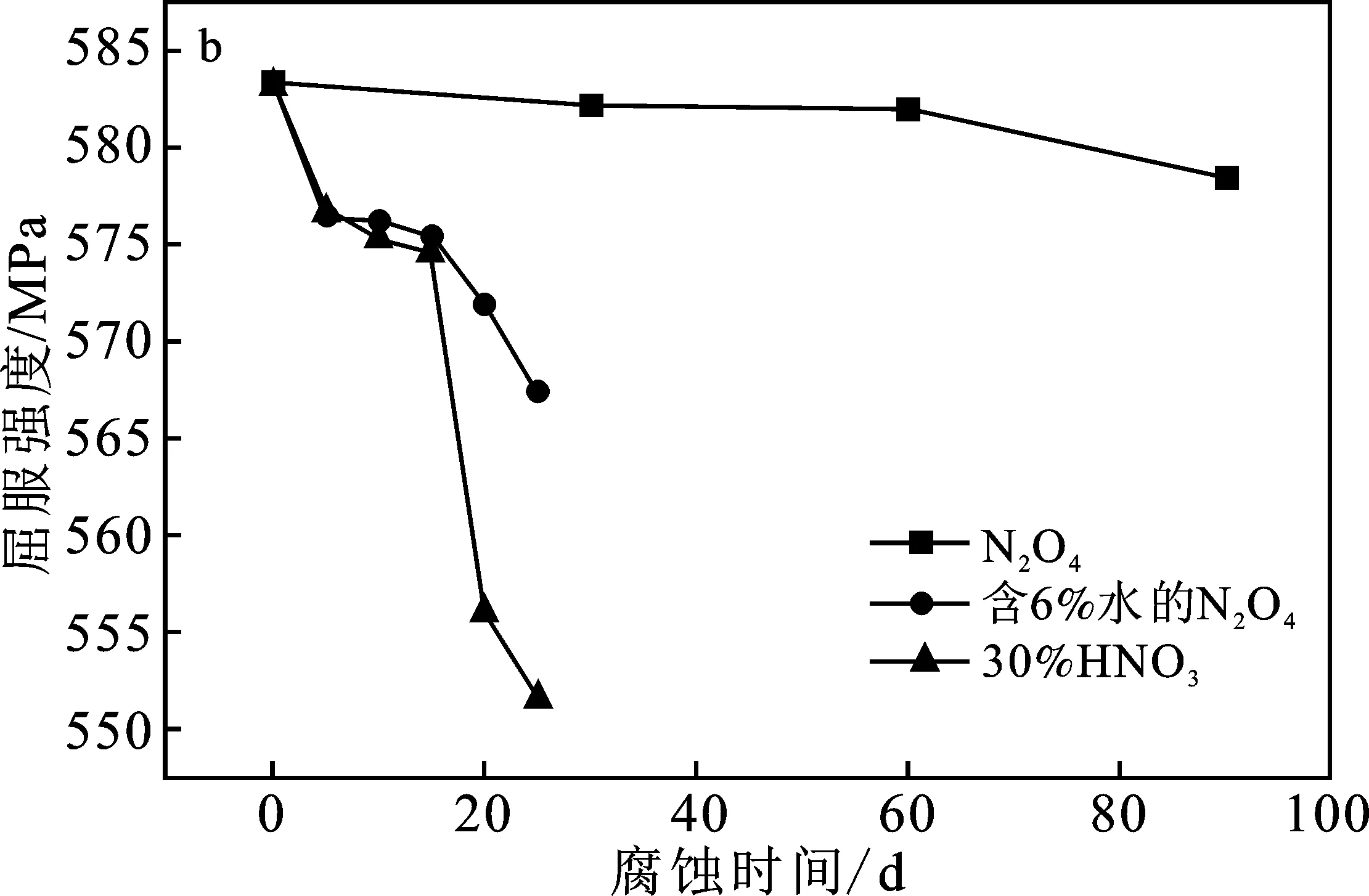

图8 试件腐蚀后的抗拉强度(a)、屈服强度(b)和延伸率(c)Fig.8 Tensile strength (a),yield strength (b) andelongation (c) of corroded specimens
由图8可知,2195铝锂合金在N2O4中腐蚀后的力学性能几乎不发生变化,也印证了其腐蚀失重数据,表明2195铝锂合金与N2O4有着良好的相容性;而在含6%水的N2O4以及30%HNO3中,力学性能下降明显,这也与2195铝锂合金在三种腐蚀介质中腐蚀的程度相关。在含水6%的N2O4中,尽管力学性能不断下降,但是整体保持一个稳定的趋势。而在30% HNO3中,其力学性能下降的更为剧烈,在第20~25 d时,拉伸强度、屈服强度以及延伸率均有较大幅度的下降,推测此时2195铝锂合金的腐蚀层已经在不断剥落,进而腐蚀下一层基体。
3 结论
(1)2195铝锂合金与N2O4的相容性良好,而在含水6%的N2O4中与30%HNO3中,腐蚀现象明显,在30% HNO3中腐蚀速度最快,相当于在含水6%的N2O4中腐蚀速率的6倍。
(2)在含6%水的N2O4中,2195铝锂合金的腐蚀由点蚀引起,逐渐扩展成较大的腐蚀坑连结成面;在30%HNO3中,表面腐蚀形貌变化不大,为剥落腐蚀。
(3)2195铝锂合金在三种介质中腐蚀产物均为Al(H2O)6(NO3)3(H2O)3,为Al(NO3)3的一种水合物,说明了2195铝锂合金在三种介质中的腐蚀为铝与硝酸的反应,最终生成硝酸盐。
(4)随着腐蚀程度的加剧,其力学性能也不断下降。在30%HNO3中,试件在20 d后,力学性能有了一个较大的下降幅度,推测此时2195铝锂合金的腐蚀层已经在不断剥落,进而腐蚀下一层基体。

