鼠李糖脂与多孔介质对天然气水合物生成影响
黄仙智,马贵阳,王 平
(辽宁石油化工大学 石油天然气工程学院,辽宁 抚顺 113001)
天然气水合物(以下简称“水合物”)是由天然气和水在低温高压下形成的非化学计量的笼型络合物[1-2],分布于深海和永久冻土带,约以1:170的体积比释放出甲烷气体[3]。 水合物在储运方面均具有巨大的发展潜力。 因此,研究提高水合物生成速率和储气密度的影响因素就显得尤为重要。
研究表明,加入表面活性剂是促进水合物生成的有效方法,其中,阴离子表面活性剂十二烷基硫酸钠(SDS)的应用最为广泛[4]。 然而,SDS作为化学合成表面活性剂,具有一定的毒性,在水合物的后续解离过程中, 释放出的SDS水溶液通过食物链到达生物体,破坏生物大分子,对生物体造成侵害。 这一缺点将会对环境造成污染,因此,寻找一种能促进水合物生成的无毒无害表面活性剂成为解决问题的首要途径。
鼠李糖脂表面活性剂是从铜绿假单胞菌中提取出的一种天然的阴离子表面活性剂,可进行生物降解,不会污染环境。Arora等[5]发现鼠李糖脂可以降低水的表面张力, 且临界胶束浓度仅为SDS溶液的百分之一。 Jadva等[6]认为水合物是以鼠李糖脂溶液中存在的胶束为中心成核。 由于目前生物型表面活性剂的研究较少,对于鼠李糖脂促进水合物生成的最优浓度的研究也并不全面。 因此,本实验采用不同浓度(100~1500 mg/L)的鼠李糖脂溶液,研究实验条件下最适宜水合物生成的鼠李糖脂浓度,以及加入多孔介质后对水合物生成的影响,为水合物工业化应用提供必要的理论参考。
1 实验部分
1.1 实验装置
本实验采用KDSD-II型水合物动力学实验装置,装置简图如图1所示。 主要包括:气瓶和气体增压装置;Pt 100/Φ3铂热电偶2个, 温控范围为-10~+90 ℃,精度为±0.1 ℃;压力传感器,测量范围为0~30 MPa,精度为±0.01 MPa;带视窗的不锈钢反应釜容积为350 mL、最高工作压力为25 MPa;电脑及工作台。

图1 KDSD-II型水合物动力学实验装置
1.2 实验材料
甲烷(CH4)气体,沈阳科瑞特种气体有限公司制造,物质的量纯度为99.9%;鼠李糖脂,西安瑞捷生物科技有限公司制造,纯度95%;十二烷基硫酸钠(SDS), 天津市致远化学试剂有限公司制造, 纯度86%; 去离子水, 实验室自制; 多孔介质为直径为6 mm的铜及二氧化硅颗粒;5.5 cm×6.5 cm的塑料容器,材质为聚对苯二甲酸乙二醇酯(PET)。
1.3 实验步骤
(1)实验之前,用去离子水对反应釜内壁以及塑料容器反复清洗, 避免杂质混入而影响实验结果。
(2)将塑料容器放入反应釜,采用氮气反复吹扫直至干燥;反应釜安装完毕后采用真空泵将釜内抽成真空, 并检查气密性是否良好。 将配制好的100 mL溶液通过进料系统注入到反应釜内,随后打开进气阀向反应釜内充入甲烷气体直至压力达到6 MPa。 最后将反应釜浸于2 ℃恒温水域系统中。
(3)通过数据采集系统记录压力、温度等数据,待反应时间达到600 min时,停止实验。
2 数据处理
气体消耗量采用式(1)、(2)计算[7]:

储气密度采用式(3)计算:
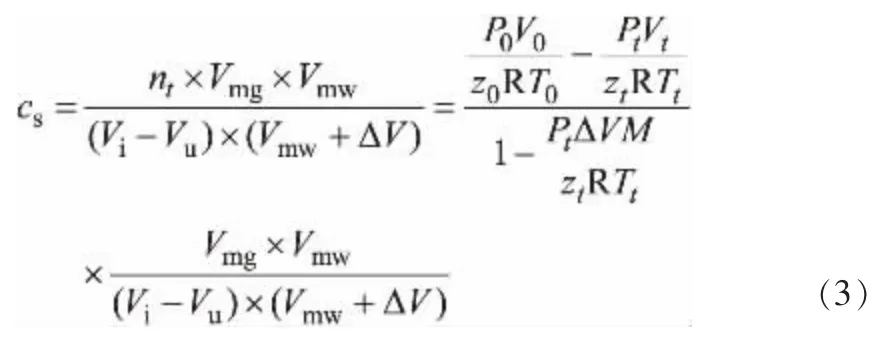
式中,cs为储气密度(单位体积的天然气水合物中所含有的气体体积),Vg/Vw;M为水合数, 无量纲;nt为t时刻甲烷气体的消耗量,mol;P0和Pt分别为0时刻和t时刻的压力,MPa;R为气体状态常数,8.314 J/(mol·K);T0和Tt分别为0时刻和t时刻的温度,K;V0和Vt分别为0时刻和t时刻的气体体积,m3;ΔV为水合物与水之间的摩尔体积差,m3;Vmg和Vmw分别为气体和水的摩尔体积,m3/mol;Vi和Vu分别为初始反应溶液的体积和未反应溶液的体积,m3;z0和zt分别为0时刻和t时刻的压缩因子, 无量纲;Tc、Pc和ω分别为临界温度、临界压力和偏心因子,对于甲烷气体分别为190.6 K、4.599 Pa和0.012。
3 结果与讨论
实验研究了不同浓度的鼠李糖脂溶液以及与多孔介质复配体系下对促进水合物生成的影响。 在水合物生成实验期间,以30 s为时间间隔记录数据。
3.1 鼠李糖脂溶液浓度对促进水合物生成的影响
图2为水合物形成过程的压降曲线, 随着溶液浓度增大,反应的剩余压力呈现上升的趋势。 其中,100 mg/L鼠李糖脂溶液条件下, 水合物生成的剩余压力最低,为3.22 MPa。这种现象的原因可能由于胶束的影响。 Zhong等[8]最早提出了胶束理论,认为胶束的存在促进了水合物的生成。 鼠李糖脂大体分为4个结构, 由于鼠李糖脂是从铜绿假单胞菌中培养获得,因此生成的产物具有不确定性,可能为单一结构,也可能为几种结构的混合体。 鼠李糖脂结构不同,其CMC值也存在一定变化。 Lang等[9]得出结论,鼠李糖脂在浓度为5~200 mg/L时,降低水表面张力的效果最好。实验采用的鼠李糖脂主要包括R1和R3两种结构,质量浓度为100 mg/L。 因此,在此浓度下,鼠李糖脂将溶液的表面张力降至最低,使甲烷气体更易溶解进入液相, 从而增大水合物的生成量,直观表现为剩余压力最低。

图2 不同浓度鼠李糖脂溶液与500 mg/L SDS溶液中水合物生成压降曲线
Fazlali等[10]发现,SDS溶液浓度为500 mg/L时对水合物促进效果最佳。因此,实验采用500 mg/L SDS溶液与鼠李糖脂溶液体系进行对比。 研究发现,500 mg/L SDS溶液的剩余压力为3.49 MPa,100 mg/L鼠李糖脂溶液的剩余压力较其减少了7.7%。 图3为水合物形成过程的储气密度曲线。 100 mg/L鼠李糖脂溶液条件下水合物的储气密度最大,为104.3 Vg/Vw,相较于SDS溶液条件下水合物94.8 Vg/Vw的储气密度, 增大了10%。 这可能是因为, 鼠李糖脂溶液的CMC值小于SDS溶液的CMC值。也就是说,在低浓度下,鼠李糖脂溶液具有更多的胶束。 由于水合物以胶束为中心成核,因此胶束越多,成核数量也越多,促进了水合物的生长,储气密度也呈现出更大的趋势。 在两种表面活性剂的最优浓度下,鼠李糖脂的浓度仅为SDS浓度的五分之一, 大大节省了表面活性剂的用量。 同时,鼠李糖脂作为天然生物型表面活性剂,对环境起到保护作用,节省了后续对水合物解离时分离出的水溶液进行污水处理的成本,具有更广泛的应用前景。

图3 不同浓度鼠李糖脂溶液与500 mg/L SDS溶液中水合物生成储气密度曲线
3.2 鼠李糖脂溶液和SDS溶液促进水合物生成机理分析

图4 鼠李糖脂结构图:(a)R1型;(b)R3型
如图4所示, 实验中采用的鼠李糖脂主要包含R1、R3两种结构。 鼠李糖脂中由1~2分子的鼠李糖环作为亲水基团,1~2分子的不同碳链长度的饱和或不饱和脂肪酸作为疏水基团。 在实验过程中,亲水性的鼠李糖环与水结合,疏水性的脂肪酸与甲烷气体结合,均匀的分布在气液接触面上,降低了溶液的表面张力, 使气体更易进入到液相形成水合物。 两亲物在溶液中易形成胶束,由于其排列方式的不同,鼠李糖脂溶液中的胶束呈现出棒状、蠕虫状等不同形态。Bai等[11]认为鼠李糖脂结构中含有两个疏水基团, 且这些疏水基团的碳链较为复杂,占据了较大的空间。 活性基团均匀排列在溶液的表面,降低了溶液的表面张力。 尾部数量较多的疏水基团将气相中的甲烷气体分子更多的带入到液相,使溶液中溶解了更多的甲烷气体,促进水合物的生成。而SDS只带有一个疏水基团,且疏水基团的碳链较为简单,因此在空间占据上处于劣势,与鼠李糖脂溶液相比也溶解了更少的甲烷气体。 所以,在实验结果中,SDS溶液的效果低于一定浓度下的鼠李糖脂溶液。 同时,鼠李糖脂作为阴离子表面活性剂,在水溶液中电离出的阴离子基团中含有羧酸盐。 由于羧基碳原子为sp2杂化,键长更趋于平均化,更有利于水合物的生成。

图5 100 mg/L鼠李糖脂溶液条件下水合物生成形态
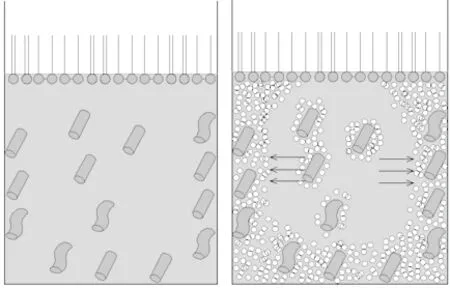
图6 水合物生成过程原理图
图5为水合物完全生成的状态, 在容器的内壁上,厚度不均的分布了一层水合物,而容器中间部分为中空状态。可以看出,水合物为贴壁生成。这可能是由于水合物在溶液中的两种生长位置导致的。图6为水合物生成过程原理图。 由于反应釜被放置在2 ℃的恒温水浴中,壁面处温度较低,利于达到水合物的生成条件,因此,水合物在气液接触表面上贴容器壁逐渐生长。 另一种是在溶液中,以胶束为中心, 将吸收进液相的甲烷气体牵引在胶束周围,不断成核生长。 由于水合物在成核时会释放大量热量,导致温度升高,温度升高又会导致表面张力降低。 容器壁处接近水浴装置,温度更低,所以表面张力较大,这就形成了表面张力梯度。 气液就会从表面张力低的位置被拉拽到表面张力高的位置,也就是从溶液内部的高温区走向壁面处的低温区,为生成水合物提供物质条件。 因此,在容器壁处的胶束优先成核生成水合物。 贴壁处出现水合物之后,由于表面张力作用,气液又进一步被牵引到贴壁处[12],在宏观条件下就形成了水合物贴壁生成的现象。
3.3 多孔介质对鼠李糖脂溶液促进水合物生成的影响
图2中各浓度下的鼠李糖脂溶液在促进水合物生成的过程中,均出现了较长的诱导时间。 为了提高水合物的生成速率,缩短诱导时间,本文增加了多孔介质进行实验。将直径为6 mm的球形二氧化硅颗粒和铜颗粒分别等量放入100 mg/L鼠李糖脂溶液中,以相同温压条件进行实验。 图7为加入多孔介质后水合物的压降曲线。 可以看出,在加入多孔介质后,诱导时间明显缩短。 在铜颗粒中,诱导时间缩短为纯鼠李糖脂溶液的51%, 在二氧化硅颗粒中甚至观察不到诱导期的存在。 这表明表面活性剂与多孔介质的复配作用对缩短诱导时间有一定的积极影响。 这是因为多孔介质具有较大的表面积,与溶液接触后,存在了更多的气-固-液三相成核位点,相比于纯鼠李糖脂溶液中的同相成核,异相成核能够加快水合物的成核速度, 因此有效的缩短了诱导时间[13]。图8为加入多孔介质后水合物的储气密度曲线,从图中可以发现,虽然诱导时间均有缩短,但不同种类的多孔介质对水合物的储气密度却有较大的影响。 在二氧化硅颗粒中,水合物的储气密度比纯鼠李糖脂溶液中的储气密度增加了2%,而在铜颗粒中,水合物的储气密度却大幅度减少,甚至低于纯鼠李糖脂溶液中的储气密度。 造成这种现象的原因可能是因为多孔介质表面特性的不同。

图7 多孔介质与鼠李糖脂复配体系中水合物生成压降曲线
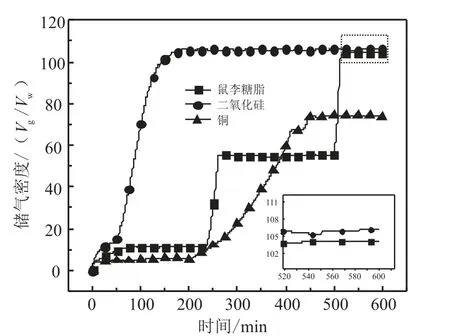
图8 多孔介质与鼠李糖脂复配体系中水合物生成储气密度曲线
二氧化硅为亲水性材料,表面具有羟基,与水接触后形成氢键。 同时,水为极性分子,又与二氧化硅表面的羟基之间形成较强的库仑力。 在氢键与库仑力的双重作用下,二氧化硅颗粒与周围溶液之间形成了较为紧密的接触,同时,由于水分子之间的强相互作用力,二氧化硅颗粒周围的水分子又将稍远部分的水分子向内吸引[14]。正是由于这种吸附力,甲烷气体进入液相后,不断地被牵引到二氧化硅颗粒周围,增强了传质作用,为水合物的生成提供了大量的物质条件,因此,促进了水合物的生成速率,也增加了水合物的储气密度。
Kashchiev等[15]认为,物质的亲水性越强,其表面越易于成核。 亲水性的强弱可以通过测量接触角的大小获得,接触角越小,说明物质的亲水性越强。二氧化硅润湿后的接触角约为8°[16], 而铜润湿后的接触角则约为52°[17],远大于二氧化硅的接触角。 也就是说,铜的亲水性相比于二氧化硅更弱。 因此,以铜颗粒为多孔介质时,水合物的成核速率小于二氧化硅颗粒, 与二氧化硅颗粒作为多孔介质相比,出现了相对较长的诱导时间。 铜作为金属单质,表面不具有化学键,且亲水性较低,因此,铜颗粒在溶液中与水分子之间的作用力小于二氧化硅颗粒与水分子之间的作用力,对溶液中溶解的甲烷气体的吸附力也相对下降。 这就导致了液相下部的铜颗粒周围聚集的甲烷气体分子较少,传质作用低于二氧化硅颗粒。 铜颗粒作为多孔介质,提供了成核位点,水合物率先在铜颗粒表面成核,晶核达到一定的临界尺寸之后,开始形成水合物。 随着水合物的生成,多孔介质之间的缝隙逐渐减小甚至发生堵塞,阻碍了甲烷气体进入到溶液底部,导致溶液底部剩余一部分液体不能与甲烷气体分子结合生成水合物,仍然为液态存在。 图9分别为二氧化硅与铜颗粒下水合物底部生成形态。 溶液不能完全发生反应,并且铜颗粒周围的甲烷气体吸附量较少, 两种原因叠加后,导致了甲烷气体消耗量减少,水合物的储气密度降低。

图9 二氧化硅与铜颗粒下水合物底部生成形态
4 结论
(1)鼠李糖脂的浓度与水合物的储气密度呈负相关性。 由于鼠李糖脂具有较多的疏水基团,且疏水基团间存在sp2杂化方式,因此,在较低浓度下,对水合物生成的促进效果较好。其中,100 mg/L鼠李糖脂溶液的效果最佳,剩余压力为3.22 MPa,储气密度为104.3 Vg/Vw。
(2)鼠李糖脂溶液与多孔介质复配体系可显著降低水合物生成的诱导时间,其中,二氧化硅颗粒效果最优,已经观察不到诱导期的存在。 铜颗粒的加入阻止了甲烷气体进入溶液底部,降低了水合物的储气密度。 二氧化硅颗粒表面的羟基与水分子之间形成的氢键及库仑力,增加了传质作用,使水合物的储气密度增至106.2 Vg/Vw。

