超高效液相色谱-串联三重四极杆质谱法测定塑料食品接触材料中9种荧光增白剂
张丽妮,邹 孝,余文琴,但家宇,唐加利,高亚凯
(1.重庆市计量质量检测研究院,重庆 401121;2.重庆大学化学化工学院,重庆 401331)
近年来,食品接触材料迁移带入的食品安全问题已经引起了食品安全监管部门的注意。这些食品接触材料常使用的一些化学染料,如荧光增白剂,它在塑料材料中大量使用,是一种容易残留并迁移到食品中的有毒有害物质。据医学实验报道,荧光增白剂可使细胞产生变异,会通过与接触的食品迁移进入人体或直接与人体表面皮肤接触[1]。虽然食品接触材料中批准使用的适量荧光增白剂属低毒风险,但违规添加及过量使用则会对人体健康构成威胁,同时也是潜在的致癌因素之一[2-3]。我国GB 9685—2016《食品接触材料及制品用添加剂使用标准》标准,欧盟2002/72/EC号指令及美国联邦法规21CFR178.3297均制定了允许用于生产食品接触材料和制品的荧光增白剂清单,同时还规定了最大使用量和特定迁移限量,如荧光增白剂FWA184,我国标准和欧盟标准一致,均规定其特定迁移限量为0.6 mg/kg,美国联邦法规则规定其加入量不得超过0.015%[4-7]。
目前,关于洗涤用品、纺织用品、塑料制品中荧光增白剂的检测技术多有报道[8-9],国内外学者针对荧光增白剂的研究主要有紫外分光光度法[10]、荧光光度法[11-12]、高效液相色谱法和超高效液相色谱法[13-20]、液相色谱-串联质谱法[21-29]等。紫外分光光度法和荧光分光光度法设备简单、操作易行、检测速率较快,但是干扰因素多、灵敏度不高,只能测定单一荧光增白剂或荧光增白剂总量,无法分析具体种类,而且环境因素对结果有影响;高效液相色谱法是目前技术相对成熟的一种检测手段,对于较为复杂的基质易受杂质干扰,检测结果准确性难以保证,且在分析多化合物时,不易分离或者分析时间过长;液相色谱-串联质谱法则是结合了液相色谱和质谱的优点,通过保留时间与特征离子对目标物进行定性与定量分析,具有其他分析方法无可比拟的优势,对于复杂化合物的定性定量更为准确,因此,近些年学者开始研究开发液相色谱-串联质谱法同时测定食品接触材料多种荧光增白剂的检测方法。如吕水源等[30]建立了高效液相色谱-串联三重四极杆质谱同时测定塑料食品接触材料中OB、OB-1、EBF、KCB 4 种荧光增白剂含量的检测方法;许健等[31]建立了采用液相色谱-串联质谱法测定发泡聚苯乙烯餐具中FWA135、FWA184、FWA185、FWA199、FWA367、FWA368、FWA378、FWA393 8 种荧光增白剂的含量。
虽然超高效液相色谱-串联三重四极杆质谱法测定塑料食品接触材料中荧光增白剂已有报道,但目前仍没有超高效液相色谱-串联三重四极杆质谱法测定塑料食品接触材料中荧光增白剂的检测标准,前人在研究时存在一些不足,一是研究选择的材质比较单一,二是对于多种荧光增白剂同时检测的论述较少。本实验在前人研究的基础上,以市场上常见的食品接触材料为对象,在提取溶剂选择和色谱条件优化方面进行了大量的工作,以期建立一种适合多种塑料食品接触材料材质中9 种荧光增白剂同时检测的超高效液相色谱-串联三重四极杆质谱法,为市场监管部门调查食品接触材料中的荧光增白剂含量提供技术支持,同时也为相关标准的制定提供依据。
1 材料与方法
1.1 材料与试剂
塑料食品接触材料样本购自本地超市、甜品店、饭店;FWA199、FWA135、FWA378标准品(纯度>98%) 上海安谱实验科技股份有限公司;FWA184、FWA52、FWA393 标准品(纯度>98%) 北京百灵威科技有限公司;FWA367标准品(纯度>98%) 英国Fluorochem化学有限公司;FWA185、FWA368对照品(纯度>95%) 济南塑邦精细化工有限公司;甲醇、乙腈(均为色谱纯) 德国Merck公司;甲酸(色谱纯) 成都科隆化学品有限公司;乙酸铵(色谱纯) 美国Fisher Chemical公司;三氯甲烷(分析纯) 重庆川东化工(集团)有限公司。
1.2 仪器与设备
UPLC 1290/API 4000型超高效液相色谱-串联三重四极杆质谱仪(配有电喷雾离子源(electrospray ion source,ESI)) 美国Agilent公司/美国Sciex公司;Quintix224-1CN电子天平 德国Sartorius公司;PP020XXM1&PF2XXXXM1超纯水机 英国Elga公司;VORTEX3旋涡混合器 德国IKA公司;3K15离心机德国Sigma公司;KH5200DE超声波清洗器 昆山禾创超声仪器有限公司;MD200-2氮吹仪 杭州奥盛仪器有限公司。
1.3 方法
1.3.1 色谱条件
色谱柱:Waters ACOUITY UPLC®HSS T3(2.1 mm×100 mm,1.8 μm);流动相;A为0.1%甲酸-乙腈溶液,B为0.1%甲酸-5 mmol/L乙酸铵溶液;柱温:40 ℃;流速:0.4 mL/min;进样量:5 μL;梯度洗脱程序见表1。

表1 梯度洗脱程序Table 1 Mobile phase gradient elution procedure
1.3.2 质谱条件
ESI正离子模式;多反应监测(multiple reaction monitoring,MRM)模式;电喷雾电压5 500 V;离子源温度600 ℃;碰撞气(N2)压力6 psi;气帘气(N2)压力30 psi;雾化气(N2)压力60 psi;辅助加热气(N2)压力60 psi;碰撞室出口电压14 eV。监测离子对、定量离子、去簇电压、碰撞能量见表2。
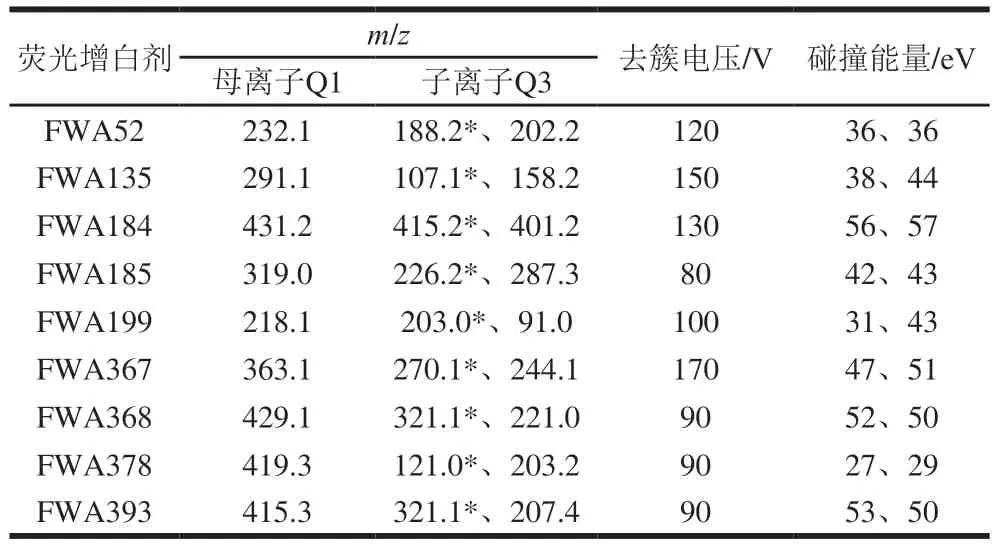
表2 9 种荧光增白剂的质谱参数Table 2 Mass spectrometric parameters for nine fluorescent whiteners
1.3.3 标准曲线的绘制
精密称取各标准品25 mg,分别置于25 mL棕色容量瓶中,用三氯甲烷溶解并定容至刻度,混匀,配制成质量浓度为1 000 mg/L的单标储备溶液,-18 ℃保存;将FWA52、FWA135、FWA184、FWA185、FWA367配成混合标准中间溶液,用甲醇逐级稀释为线性范围0.5~100 ng/mL,将FWA199、FWA368、FWA378、FWA393配成混和标准中间液,用甲醇逐级稀释为线性范围5~1 000 ng/mL。以待测物质量浓度为横坐标,以定量离子质量色谱峰面积为纵坐标,绘制标准曲线。
1.3.4 样品处理
选取食品接触类塑料包装,如:饮用水瓶(聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET))、密胺餐具(密胺树脂(melamine resin,MF))、一次性餐盒(聚丙烯(polypropylene,PP))、方便面桶(聚乙烯(polyethylene,PE)内膜)、复合膜包装袋(双向拉伸尼龙/低密度聚乙烯(biaxially oriented polyamide(nylon) film/low-density polyethylene,BOPA/LDPE)复合)、镀层塑料包装(CPP镀铝膜)6 种材质17 个代表性样品,剪成小于5 mm×5 mm的碎片,混匀后分别装入洁净容器作为试样,密封并做标识。
样品前处理:称取0.5 g(精确至0.1 mg)已混匀的样品于25 mL具塞棕色玻璃比色管中,加入10 mL三氯甲烷,涡旋0.5 min,于40 ℃超声提取30 min,以6 000 r/min离心5 min,转移上清液至氮吹管中,继续加入10 mL甲醇至比色管中,涡旋0.5 min,于40 ℃超声提取30 min,以6 000 r/min离心5 min,转移并合并2 次提取的上清液,于40 ℃氮吹至近干,残渣用1.0 mL甲醇复溶,过0.22 μm微孔有机滤膜后供超高效液相色谱-串联三重四极杆质谱测定。
加标样品制备:称取0.5 g(精确至0.1 mg)经前期检测为阴性的试样于25 mL具塞棕色玻璃比色管中,加入适量混合标准溶液,室温放置,待样品吸收标液至干后,按上述步骤进行前处理。
1.3.5 提取溶剂选择
本实验以提取回收率为指标,以6 种材质为基质,对甲醇、乙腈、二氯甲烷、三氯甲烷、N,N-二甲基甲酰胺(N,N-dimethylformamide,DMF)溶剂进行比较研究,并确定合适的提取溶剂。
1.3.6 检出限与定量限
按照1.3.4节样品提取条件,以经前期测试不含本研究9 种荧光增白剂的样品为本底,用阴性样品加标实验,以3 倍信噪比计算检出限,以10 倍信噪比计算定量限。1.3.7 回收率与精密度
按照1.3.4节样品提取条件,以经前期测试不含本研究9 种荧光增白剂的样品为本底,取样品0.5 g,分别添加定量限的1、2 倍和10 倍3 个水平进行回收率实验和精密度实验,每个添加量进行6 次平行实验,同时做空白实验,均扣除本底值后计算加标回收率和相对标准偏差。
1.4 数据处理
实验结果统计分析采用WPS 2019表格,图像处理方法采用Origin 2018。
2 结果与分析
2.1 液相色谱条件的优化
据文献报道,液相色谱-质谱法检测荧光增白剂主要使用的流动相通常为0.1%甲酸-乙腈(A)和水(B)[21];0.1%甲酸-甲醇(A)和0.1%甲酸(B)[30];乙腈(A)和乙酸铵缓冲溶液(B)[31]。实验在借鉴前人使用流动相的基础上对色谱条件进行优化,发现对本实验的9 种目标荧光增白剂的分离效果不佳,峰形差。为了达到良好的分离效果和峰形,从流动相pH值稳定性和离子强度进行改进。对比研究0.1%甲酸-乙腈(A)和0.1%甲酸溶液(B)、0.1%甲酸-甲醇(A)和0.1%甲酸溶液(B)、0.1%甲酸-乙腈(A)和0.1%甲酸-5 mmol/L乙酸铵溶液(B)、0.1%甲酸-甲醇(A)和0.1%甲酸-5 mmol/L乙酸铵溶液(B)4 种流动相组合。首先使用0.1%甲酸-乙腈(A)-0.1%甲酸(B)和0.1%甲酸-甲醇(A)-0.1%甲酸(B)作为流动相时,分离度因个别峰的峰形宽及拖尾严重造成总离子流图分离效果不佳,而后考虑加入5 mmol/L乙酸铵缓冲盐使流动相保持一定的离子强度以改善峰形,使用0.1%甲酸-甲醇(A)-0.1%甲酸-乙酸铵(B)流动相时效果明显,分离效果好、峰形好、响应高,但检测时间稍长,考虑到这9 种荧光增白剂的极性偏弱,选择0.1%甲酸-乙腈(A)-0.1%甲酸-乙酸铵(B)流动相时,洗脱能力增强,9 种荧光增白剂的保留时间减少,经过梯度程序优化,同样能达到很好的分离效果,响应更高,尤其是FWA378、FWA367、FWA184,比0.1%甲酸-甲醇(A)-0.1%甲酸-乙酸铵(B)流动相体系高3~5 倍。最终选择0.1%甲酸-乙腈(A)-0.1%甲酸-5 mmol/L乙酸铵(B)溶液作为流动相,并优化梯度洗脱程序。9 种荧光增白剂色谱分离的总离子流图见图1。
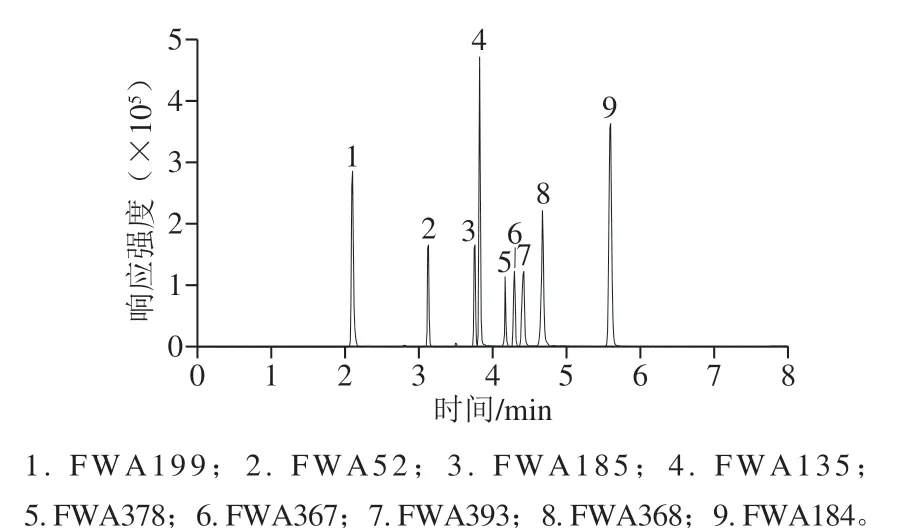
图1 9 种荧光增白剂色谱分离的总离子流图Fig. 1 Total ion current chromatograms for chromatographic separation of nine fluorescent whiteners
2.2 提取溶剂的选择
考虑到本实验的9 种目标荧光增白剂属于脂溶性荧光增白剂,提取溶剂需选择有机溶剂。在前人的研究中,刘杰等[13]研究了三氯甲烷和甲醇对脂溶性荧光增白剂的提取效果,结果表明三氯甲烷-甲醇(4∶1,V/V)能够兼顾回收率和峰形,吴钟玲等[32]研究了甲醇、甲苯、二氯甲烷、三氯甲烷、DMF对脂溶性荧光增白剂的提取效果,结果表明三氯甲烷是最佳提取剂。叶玲等[33]比较研究三氯甲烷、甲醇、乙腈对荧光增白剂的提取效果,结果显示三氯甲烷为最佳提取剂。本实验选取甲醇、乙腈、二氯甲烷、三氯甲烷、DMF为提取剂,在相同条件下(室温超声提取30 min,料液比0.5 g/10 mL),对6 种不同材质的自制阳性样品进行测试,比较不同材质食品接触材料中荧光增白剂在不同提取溶剂中的提取效果,由图2可以看出,和前人研究结果一致,三氯甲烷和甲醇对6 种材质的食品接触材料中荧光增白剂的提取效果均优于其他试剂,但二者对不同的荧光增白剂有着不同提取效率,前人的研究以使用三氯甲烷为主,甲醇的作用多为沉淀高聚物以减少杂质的干扰[31],并没有考虑甲醇对个别荧光增白剂的萃取作用。本实验在探索过程中发现甲醇对FWA52、FWA185、FWA368、FWA378的提取效果优于三氯甲烷,刘杰等[13]研究发现,三氯甲烷和甲醇作为提取溶剂时,甲醇含量超过三氯甲烷的1/4会导致目标荧光增白剂和高聚物一起析出,影响回收率,因此本实验尝试采用前人未曾摸索的两种溶剂分两步提取法,先用三氯甲烷超声提取30 min,再用甲醇超声提取30 min,合并2 次提取溶液,氮吹至近干后用1 mL甲醇溶解残渣,过0.22 μm有机滤膜,上机检测,图3表明,分2 次提取6 种材质食品接触材料中的9 种荧光增白剂,虽然FWA52回收率较甲醇单独提取有所降低,但9 种荧光增白剂整体回收率明显优于甲醇和三氯甲烷单独提取的效果,说明三氯甲烷和甲醇分别提取荧光增白剂能够起到互补作用。
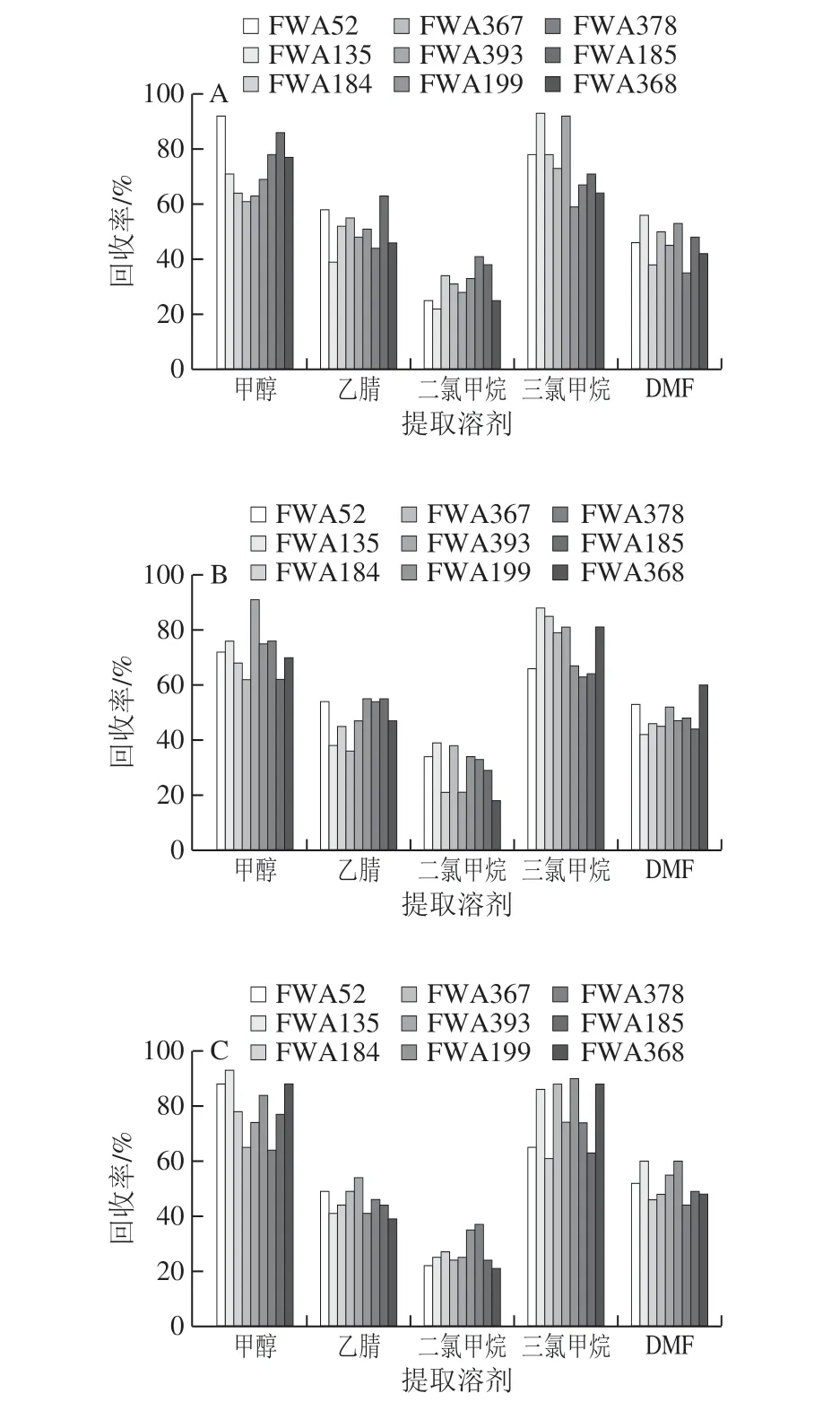
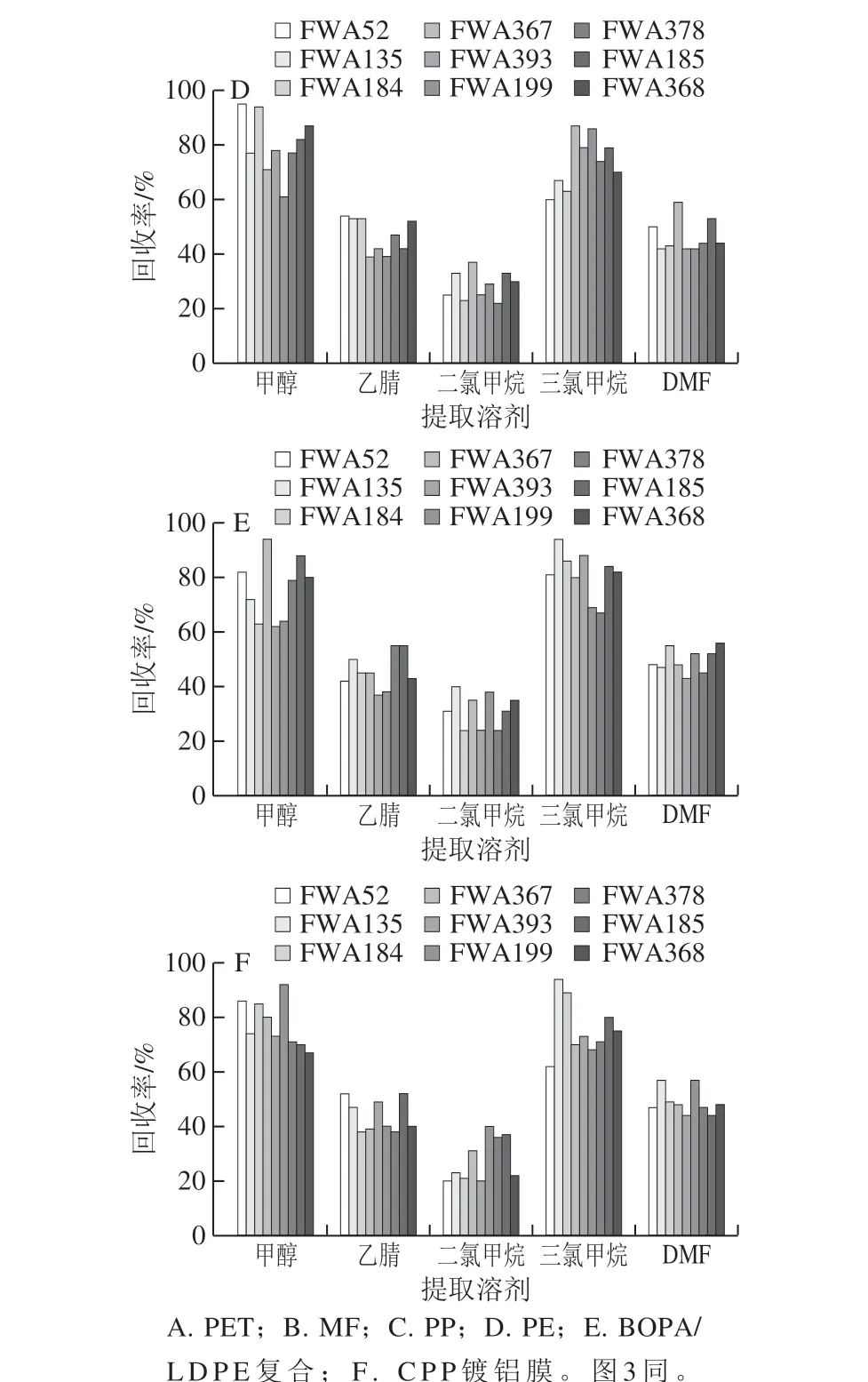
图2 提取溶剂对6 种食品接触材料中9 种荧光增白剂回收率的影响Fig. 2 Effect of extraction solvents on the recovery of nine fluorescent brighteners in six food contact materials
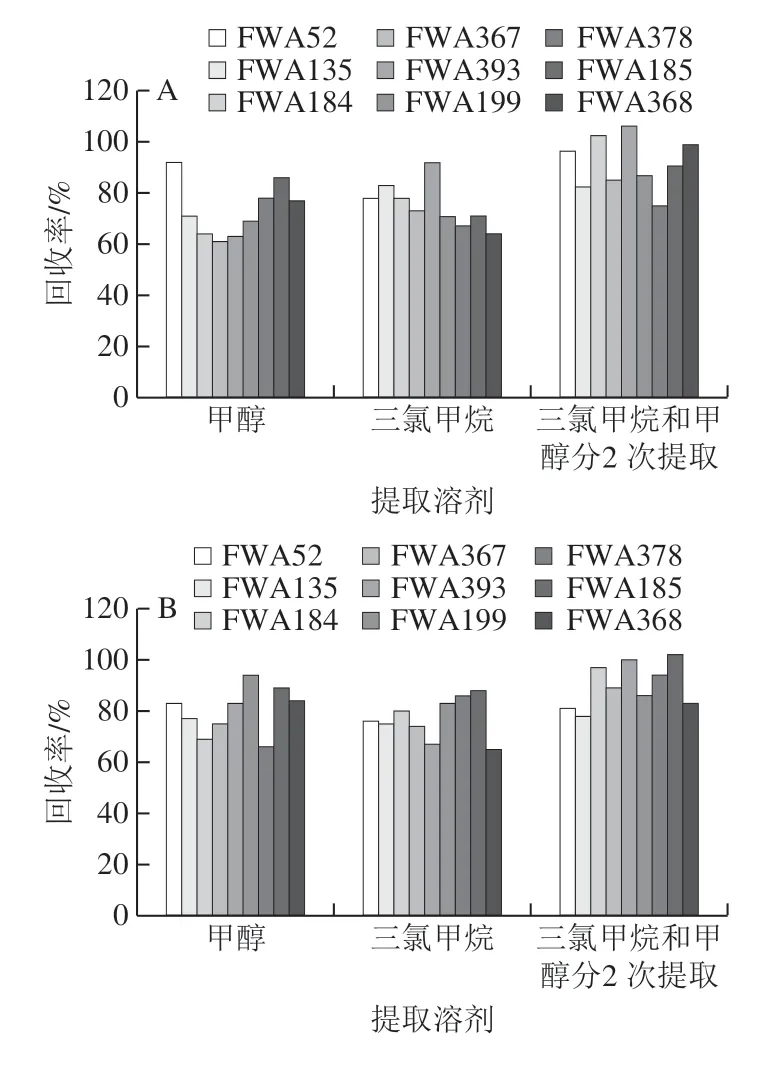
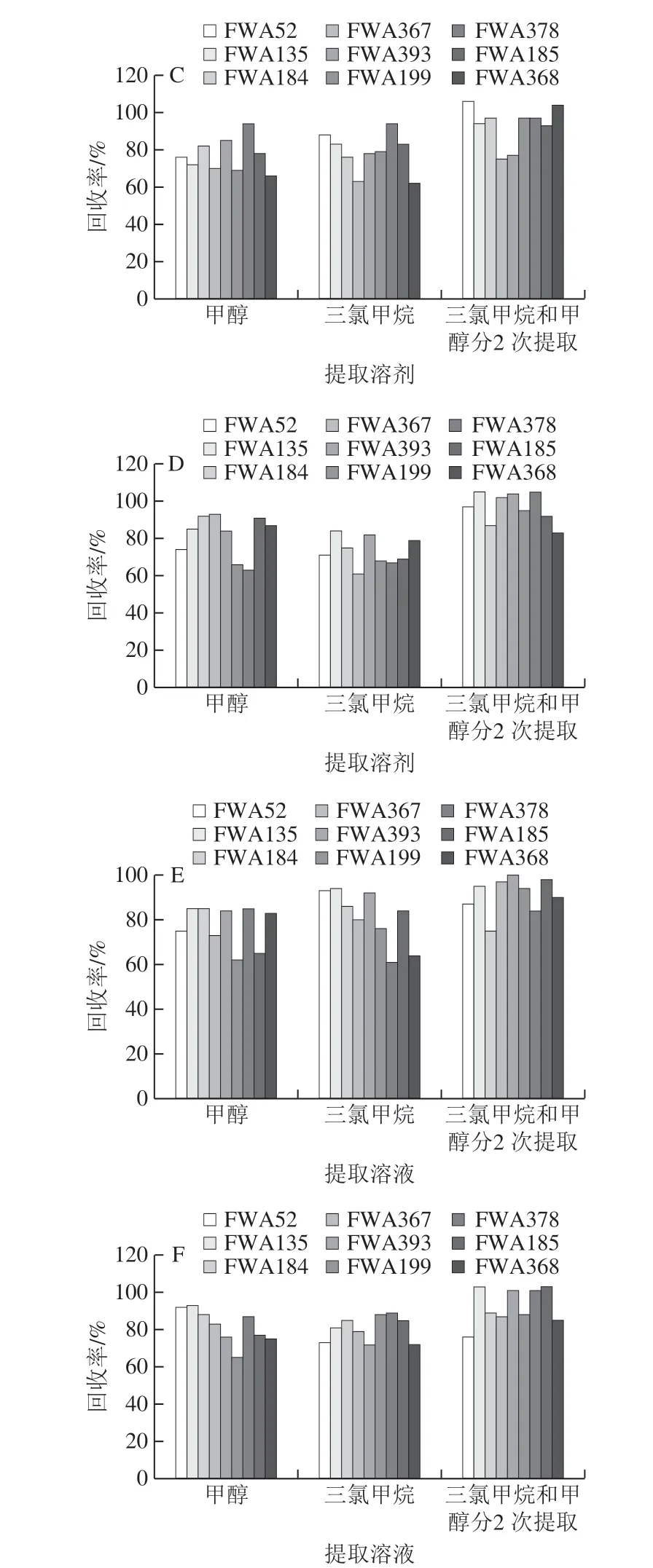
图3 甲醇、三氯甲烷、三氯甲烷和甲醇分2 次提取对6 种食品接触材料中9 种荧光增白剂回收率的影响Fig. 3 Effects of individual and sequential extraction with chloroform and methanol on on the recovery of 9 fluorescent whitening agents in six food contact materials
2.3 质谱条件的优化
质谱条件的优化通过在流动注射模式下对1.0 μg/mL的9 种荧光增白剂单独进样完成。根据9 种荧光增白剂的化合物结构,选择在正离子模式下进行优化。采用一级质谱对目标化合物进行母离子全扫描,分析得到[M+H]+分子离子峰;再采用二级质谱,以分子离子为母离子,优化去簇电压、碰撞能量参数,对目标化合物的子离子进行全扫描,每种荧光增白剂选择2 个信号稳定且强度高的m/z为定性离子对,选着其中信号强度高且受基质干扰小的m/z为定量离子对,结果见表2。9 种荧光增白剂提取离子色谱见图4。
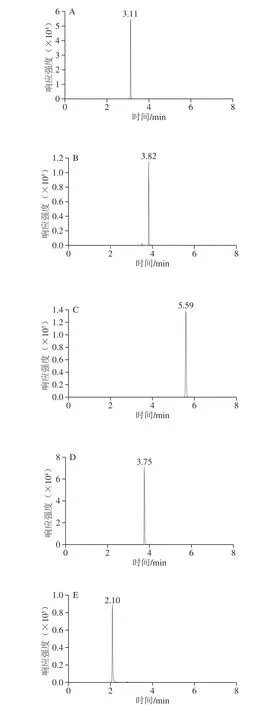
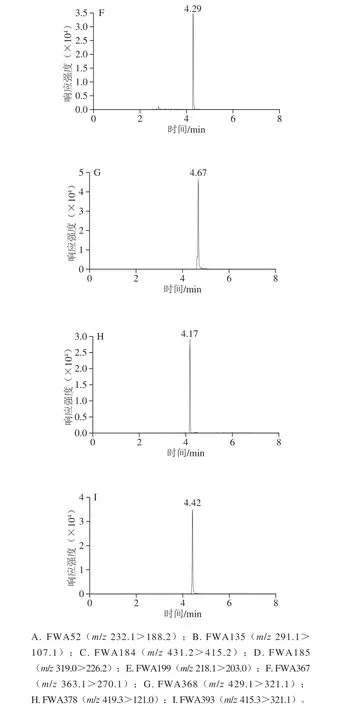
图4 9 种荧光增白剂提取离子MRM色谱图Fig. 4 Extracted ion MRM chromatograms of nine fluorescent whiteners
2.4 线性范围、检出限和定量限测定结果
根据1.3.3节方法配制混合标准系列,经测试分析后得出标准曲线,用阴性样品加标实验,计算检出限和定量限,结果见表3。9 种荧光增白剂在0.5~1 000 ng/mL范围线性良好,相关系数均大于0.9 9 9,检出限为0.05~3.2 μg/kg,定量限为0.2~10 μg/kg,本方法线性范围宽、灵敏度高。
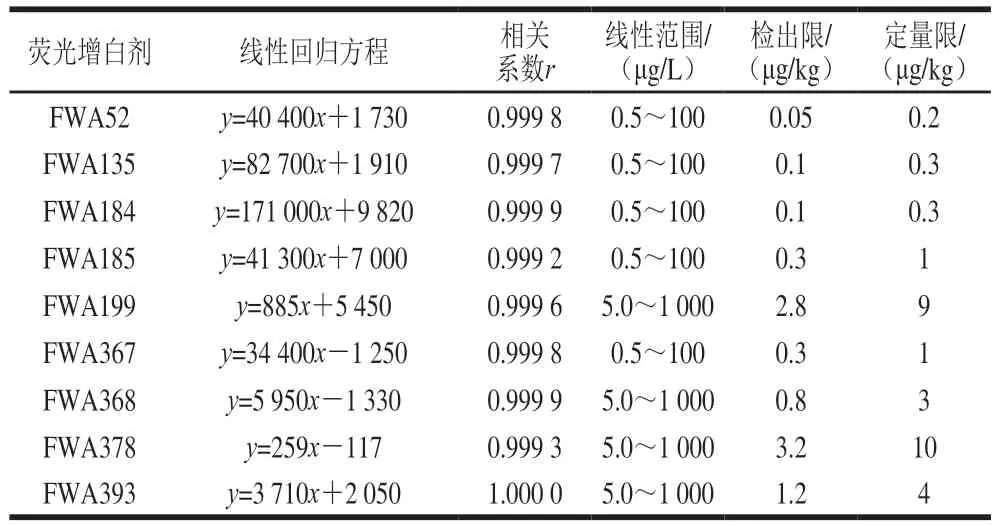
表3 9 种荧光增白剂的线性回归方程、相关系数、线性范围、检出限和定量限Table 3 Linear regression equations, correlation coefficients,linear ranges, detection limits and quantitative limits for nine fluorescent brighteners
2.5 加标回收率和精密度实验结果
如表4 可知,9 种荧光增白剂的平均回收率在76.11%~106.55%之间,相对标准偏差在1.97%~8.31%之间,表明本方法回收率稳定,可满足实际样品的检测要求。
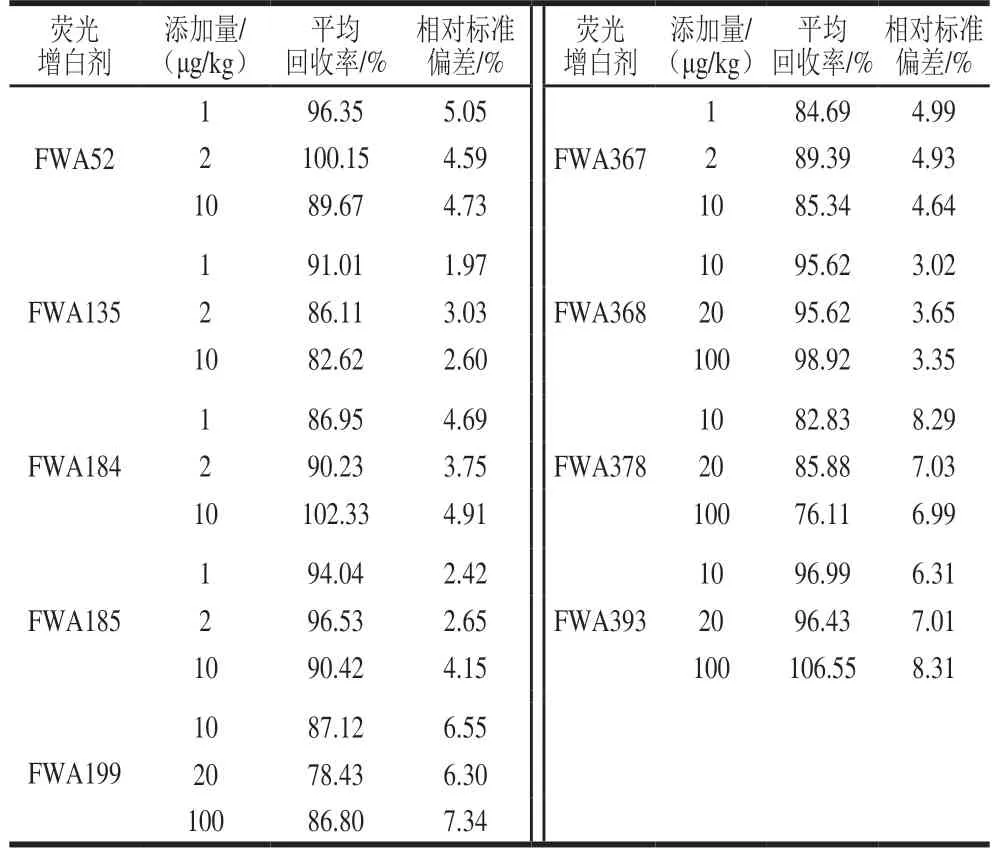
表4 9 种荧光增白剂的加标回收率和精密度(n=6)Table 4 Recoveries and precision of nine fluorescent brighteners from spiked samples (n= 6)
2.6 实际样品分析结果
采用最优条件下的实验方法对从超市、甜品店、饭店购买的17 个样品进行测试,结果见表5,图5为典型阳性样品(YP-16)中检出荧光增白剂(FWA393)的总离子流图和质谱图。由表5可看出,有15 个样品检出不同程度的荧光增白剂,主要集中在FWA135、FWA184、FWA378、FWA393,FWA393最高检出含量1 380 μg/kg,而FWA135、FWA184、FWA378并不允许在食品接触用塑料材料及制品中使用,由此可见,检出样品可能是由于污染带入,或者是人为在塑料制品中违规使用禁用荧光增白剂,需要市场监管部门加强监督管理。同时本课题在接下来的研究中会对特定迁移量的模拟实验进行研究。
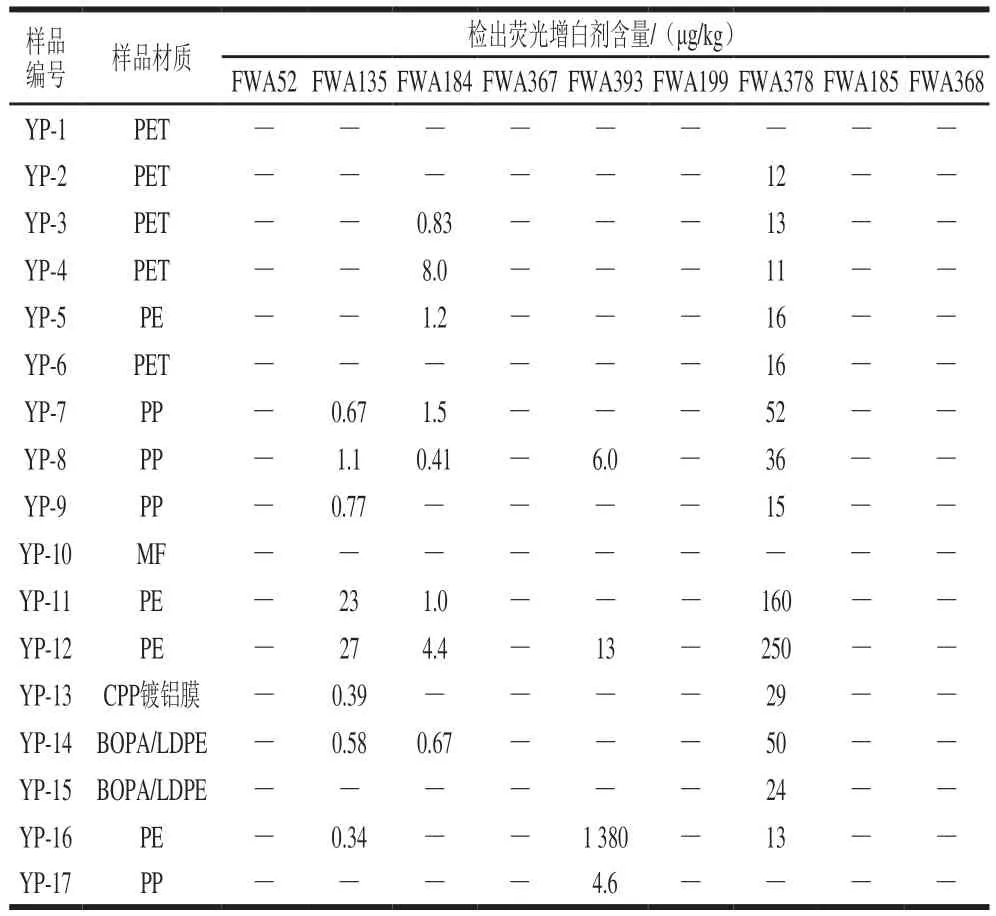
表5 塑料食品接触材料实际样品中9 种荧光增白剂的含量Table 5 Contents of nine FWAs in actual samples of plastic food contact materials determined by the proposed method
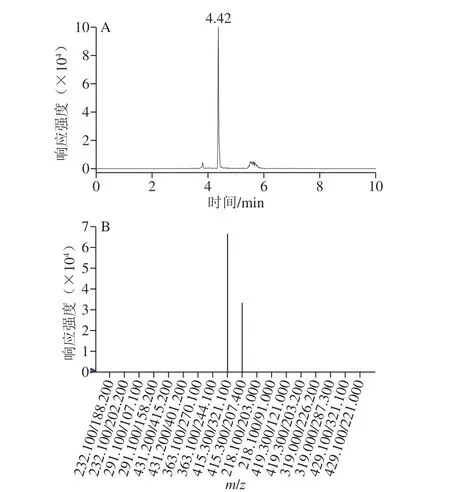
图5典型阳性样品(YP-16)中检出荧光增白剂(FWA393)的总离子流图(A)和质谱图(B)Fig. 5 Total ion current chromatogram (A) and mass spectrum (B) of fluorescent brightener (FWA393) in typical positive samples (YP-16)
3 结 论
本实验建立了同时测定塑料食品接触材料中FWA52、FWA135、FWA184、FWA185、FWA199、FWA367、FWA368、FWA378、FWA393 9 种荧光增白剂含量的超高效液相色谱-串联三重四极杆质谱检测方法。该方法条件下9 种荧光增白剂检出限为0.05~3.2 μg/kg,定量限为0.2~10 μg/kg,在0.5~1 000 ng/mL范围线性良好,相关系数均大于0.9 9 9,加标回收率范围为76.11%~106.55%,相对标准偏差(n=6)为1.97%~8.31%,均符合方法确认的要求,本方法成功应用于塑料食品接触材料中9 种荧光增白剂的快速定性定量分析,为检测方法标准的制定提供依据,同时为食品安全监管提供技术支持。

