安罗替尼三线治疗广泛期小细胞肺癌的疗效评价
刘晓文
小细胞肺癌是起源于支气管黏膜或腺体的一类肺恶性肿瘤,属于神经内分泌癌,具有疾病进展快、自然病程较短、早期易转移、易复发、预后差的特点,在我国发病率高[1]。它对于初始的放化疗敏感,但一旦耐药,后续治疗较困难。肿瘤的生长离不开新生血管,安罗替尼是由我国自主研究多靶点抗血管药物,除了对血管内皮生长因子受体2(VEGFR2)有较强的抑制作用,对于参与肿瘤血管生成的其他信号通路如血小板衍生生长因子受体(PDGFR)、成纤维细胞生长因子受体(FGFR)等同样具有强烈的抑制,对介导多条信号通路的c-kit 也表现较强的抑制作用[2]。鉴于此,本次共纳入46 例小细胞肺癌患者,探究最佳治疗方式,报告如下。
1 资料与方法
1.1 一般资料 选取2018 年7 月~2019 年5 月46 例既往接受两种化疗方案后疾病进展的广泛期小细胞肺癌患者为研究对象,美国东部肿瘤协作组(ECOG)活动状态(PS)评分0~2 分。采用整群随机化方式分为对照组和研究组,每组23 例。对照组:年龄59~79 岁,平均年龄(69.0±3.4)岁,男∶女=13∶10;研究组:年 龄60~79 岁,平均年龄(69.5±3.2) 岁,男∶女=12∶11。两组患者的一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1 研究组 予以患者盐酸安罗替尼胶囊(正大天晴药业集团股份有限公司,国药准字H20180004)治疗,12 mg/次,1 次/d,连续用药14 d,停药7 d,为1 个周期,每42 天做1 次疗效评估。疗效评估标准根据实体瘤疗效评价标准(RECIST) 1.1 进行,在控制疾病的同时,如果患者可以耐受,则可继续用药,疾病进展或是不能耐受的患者应立即停止用药。
1.2.2 对照组 予以患者安慰剂治疗,选择空白药片,1 片/次,1 次/d,连续用药14 d,停药7 d,为1 个周期,每21 天进行1 次评估。
1.3 观察指标及判定标准
1.3.1 比较两组患者治疗前后的KPS 评分及体重①体重变化<1 kg,生存质量稳定;体重增加>1 kg,生存质量增加;体重减少>1 kg,生存质量降低。②KPS评分变化<10 分,生存质量稳定;KPS 评分提升>10 分,生存质量改善;KPS 评分下降>10 分,生存质量降低。
1.3.2 比较两组患者的不良反应发生情况 包括高血压、腹泻、乏力、皮疹、蛋白尿。
1.3.3 比较两组患者的无进展生存时间 治疗后,统计两组患者的无进展生存时间。
1.4 统计学方法 采用SPSS21.0 统计学软件进行统计分析。计量资料以均数±标准差()表示,采用t 检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组患者治疗前后的KPS 评分及体重比较治疗前,两组患者的KPS 评分、体重比较,差异均无统计学意义(P>0.05);对照组患者治疗后的KPS 评分、体重均低于本组治疗前,差异均具有统计学意义(P<0.05) ;研究组患者治疗后的KPS 评分、体重与本组治疗前比较,差异均无统计学意义(P>0.05);研究组患者治疗后的KPS 评分、体重均高于对照组,差异均具有统计学意义 (P<0.05)。见表1。
2.2 两组患者的不良反应发生情况比较 研究组患者的不良反应发生率为78.26%,与对照组的69.57%比较,差异无统计学意义(P>0.05)。见表2。
表1 两组患者治疗前后的KPS 评分及体重比较()
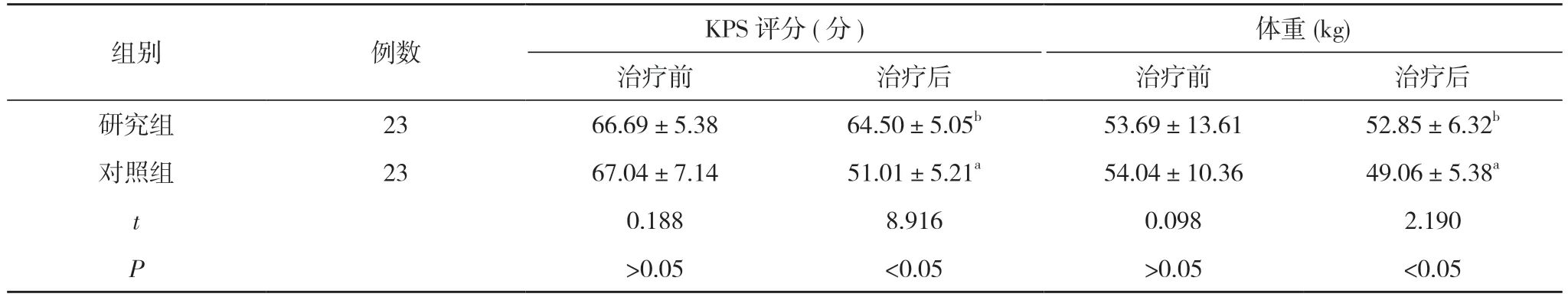
表1 两组患者治疗前后的KPS 评分及体重比较()
注:与本组治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05

表2 两组患者的不良反应发生情况比较[n(%)]
2.3 两组患者的无进展生存时间比较 研究组患者的无进展生存时间为(4.1±1.13)个月,长于对照组的(0.7±1.01)个月,差异具有统计学意义(t=10.759,P=0.000<0.05)。
3 讨论
小细胞肺癌恶性程度极高,约95%归因于吸烟,空气污染,有少数早期的患者首选手术治疗,但诊断时广泛期占2/3,具有生存期短、易复发、易转移等特点[3]。肺癌领域的顽疾小细胞肺癌的治疗模式在近30 年中经过屡屡尝试,一直没有明显改变,治疗进展较慢,当前仍需进一步探索,尽可能将小细胞肺癌患者的生存期延长。最近随着基础和临床研究的推进,随着医学技术的不断进步和发展,在抗血管治疗等领域的探索终于给小细胞肺癌的治疗带来了转机,建立了小细胞肺癌新的治疗模式,成为小细胞肺癌治疗的里程碑,特别是多靶点抗血管药物的应用[4]。
安罗替尼属于一种多靶点抗肿瘤血管生成的药物,它全面作用于血管生成通路中VEGFR、PDGFR和FGFR 等各相关靶点,且IC50 低,且靶点集中,选择性强,与治疗无关的药物作用少,所以抗血管生成治疗强效、单药有效且副作用低。同时抑制c-Kit(增殖)、Ret(增殖)、FGFR(增殖/转移)、c-Met(转移)等靶点,控制肿瘤细胞增殖和转移,并能解除免疫抑制状态,增加T 细胞活性及浸润,开启血管正常化窗口,提高药物递送效率,并增加局部氧分压和氧含量[5]。众所周知,肿瘤区别于正常组织具有这十大特征,其中血管形成,持续的增殖,侵袭转移,免疫逃逸等,其中安罗替尼可以通过抑制血管新生、肿瘤增殖和调节微环境来达到抑制肿瘤的目的。肿瘤的发生发展是以微环境中的血管为基础的,初期的肿瘤,微环境的营养和氧气就可以供应他的生存,但是当肿瘤体积逐步增大到两立方毫米以上的时候,原有的血管系统营养供应不足,此时的肿瘤会上调微环境促血管生成相关信号,急需要发展独立的血管系统来维持肿瘤的生长[6]。肿瘤血管主要是由内皮细胞,周细胞和平滑肌细胞按照一定的排列次序组合而成的,调控三者细胞增殖的主要相关因子就是VEGFR、PDGFR 和FGFR,这三个受体是安罗替尼作用的主要抗血管靶点。肿瘤细胞或者是肿瘤相关的成纤维细胞,也是主要的分泌细胞,在接收到外界缺氧的信号后,会促使VEGF、FGF、PDGF 相关蛋白的表达,这些是配体,配体表达上调后,会与血管结构细胞膜上定位的受体对应结合,配体受体结合,构象会发生变化,进而激活了下游相关的增殖信号,实现细胞的增殖,增殖了的血管细胞,进而形成新的血管组织[7]。血管由内皮细胞,外围周细胞,还有平滑肌细胞构成,这些细胞膜上都有对应的受体,也是安罗替尼的作用靶点,血管的新生为肿瘤进展提供了营养氧气和转移的通道,而安罗替尼通过抑制这些血管结构细胞膜上的受体信号通路,抑制血管细胞的增殖,使得肿瘤因为缺乏血供饥饿而死,最终达到治疗肿瘤的目的[8,9]。本次研究组患者三线治疗采用安罗替尼,结果显示,治疗前,两组患者的KPS 评分、体重比较,差异均无统计学意义(P>0.05);对照组患者治疗后的KPS评分、体重均低于本组治疗前,差异均具有统计学意义(P<0.05);研究组患者治疗后的KPS 评分、体重与本组治疗前比较,差异均无统计学意义(P>0.05);研究组患者治疗后的KPS 评分、体重均高于对照组,差异均具有统计学意义 (P<0.05)。研究组患者的不良反应发生率为78.26%,与对照组的69.57%比较,差异无统计学意义(P>0.05)。研究组患者的无进展生存时间为(4.1±1.13)个月,长于对照组的(0.7±1.01)个月,差异具有统计学意义(t=10.759,P=0.000<0.05)。表明安罗替尼在广泛期小细胞肺癌三线治疗中具有较高的安全性,且患者生存质量稳定,其用药时采用连续口服用药14 d停药7 d的方式,使其具有极好的耐受性和便捷性。
综上所述,广泛期小细胞肺癌三线治疗中,采用安罗替尼可提升患者的治疗效果,延长无进展生存时间,对提升患者生存质量具有重要意义,不良反应低。

