天然气脱除硫化氢的研究
谭更彬,王志泉,吴钟旺
(1.青岛科技大学 机电工程学院,山东 青岛 266061;2.山东省化工研究院,山东 济南 250014)
天然气中含有大量酸性气体、重烃、水、汞等杂质,进行液化处理时易形成水合物,导致储罐腐蚀,管道堵塞[1]。硫化氢作为天然气中主要有害杂质[2],在工业生产中会使大部分的催化剂失效,并且其燃烧后的产物排放到大气中会形成酸雨,必须予以脱除[3]。
某采油厂采用二乙醇胺(DEA)工艺对天然气进行脱硫处理,随着脱硫剂的使用,该厂发现二乙醇胺由于本身特性,使用时间到达一定年限,设备对硫化氢的吸收不足,导致天然气验收时出现硫含量超标的现象,考虑升级为甲基二乙醇胺(MDEA)。本文对甲基二乙醇胺脱硫化氢工艺进行研究,对比二乙醇胺与甲基二乙醇胺的脱硫效果,为采油厂工艺换代提供实验数据。
1 实验部分
1.1 材料与仪器
天然气,硫含量23 mg/L、二乙醇胺、甲基二乙醇胺、CdCl2、冰乙酸、碘化钾均为分析纯;正丙硫醇,化学纯;硫化氢标准样(纯度99.99%);氮气(纯度99.99%);实验用水为去离子水。
WY-WK2000型微库仑综合分析仪。
1.2 实验方法
实验流程见图1。
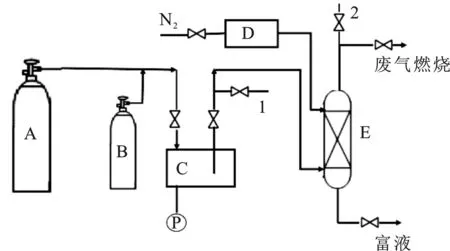
图1 溶剂吸收法实验流程图Fig.1 Solvent absorption method experiment flow chart1.天然气进料取样处;2.净化天然气出料取样处;A.天然气钢瓶;B.硫化氢钢瓶;C.配气罐;D.脱硫剂储罐;E.吸收塔;P.压力表
钢瓶A内装有标准天然气气样,钢瓶B中装有硫化氢标准气样,通过调节钢瓶A和钢瓶B的阀门,将两种气样通入配气罐C,配制实验所需要浓度的含硫天然气气样,通过分析配气罐内气样浓度,调节前端阀门,直到配气罐检测气样为实验所需气样浓度。配气罐中的天然气经过流量计进入吸收塔E底部,脱硫剂储罐D采用氮气加压将输送罐中溶液至吸收塔顶部,在吸收塔E内部,天然气与脱硫剂逆流接触脱除硫化氢气体,吸收塔出口设计取样点,检测天然气中硫含量。
1.3 分析方法
1.3.1 硫化氢定性分析 利用CdCl2检测天然气中是否含有硫化氢组分[4]。在250 mL的玻璃吸收管中加入100 mL浓度为0.1 mol/L的CdCl2溶液,加入直径为3 mm的洁净玻璃珠,以增大气液接触面积。将天然气流速调整为100 mL/min,通入玻璃吸收管底部,与溶液进行混合,将反应后气体进行放空处理,通气10 min,结束实验。观察CdCl2溶液中是否存在黄色沉淀,若存在,则说明天然气中含有硫化氢气体,进行硫含量测定[5-8]。

1.3.2 总硫含量测定 参照标准《天然气含硫化合物的测定第4部分:用氧化微库仑法测定总硫含量》(GB/T 110604—2010)测量总硫含量。
2 结果与讨论
2.1 温度对脱硫反应的影响
以MDEA溶液为脱硫剂,浓度为20%,10 mL,硫含量为23 mg/L的天然气为原料气,空速为1.5 h-1,进行温度对脱硫影响的研究,以5 h为间隔,当净化气高于二类气要求,即0.2 mg/L时,停止实验,结果见图2。
由图2可知,温度为20 ℃时,脱硫效果最好,并且随着温度上升,脱硫剂工作时间变短,酸性气负荷也降低。因为酸碱中和过程为放热反应,温度上升导致正向反应速率下降,不利于脱硫剂对硫化氢的吸收。15~30 ℃为理想反应条件,取20 ℃为后续实验条件。
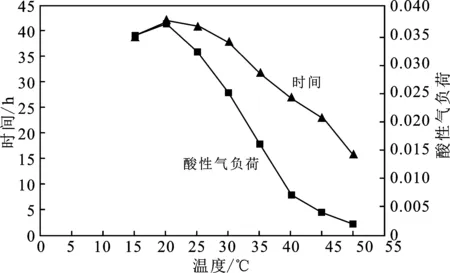
图2 温度对脱硫效果的影响Fig.2 Effect of temperature on desulfurization effect
2.2 脱硫剂浓度对脱硫反应的影响
以MDEA溶液为脱硫剂,硫含量为23 mg/L的天然气为原料气,进行脱硫浓度对脱硫反应的影响。实验温度为20 ℃,原料气空速为1.5 h-1,工业用MDEA浓度一般为20%~50%,因此选取20%,25%,30%,35%,40%,45%,50%七个实验浓度,体积为10 mL,进行实验。每隔5 h分析一次硫含量,当净化气H2S高于二类气要求,即0.2 mg/L时,停止实验,结果见图3。
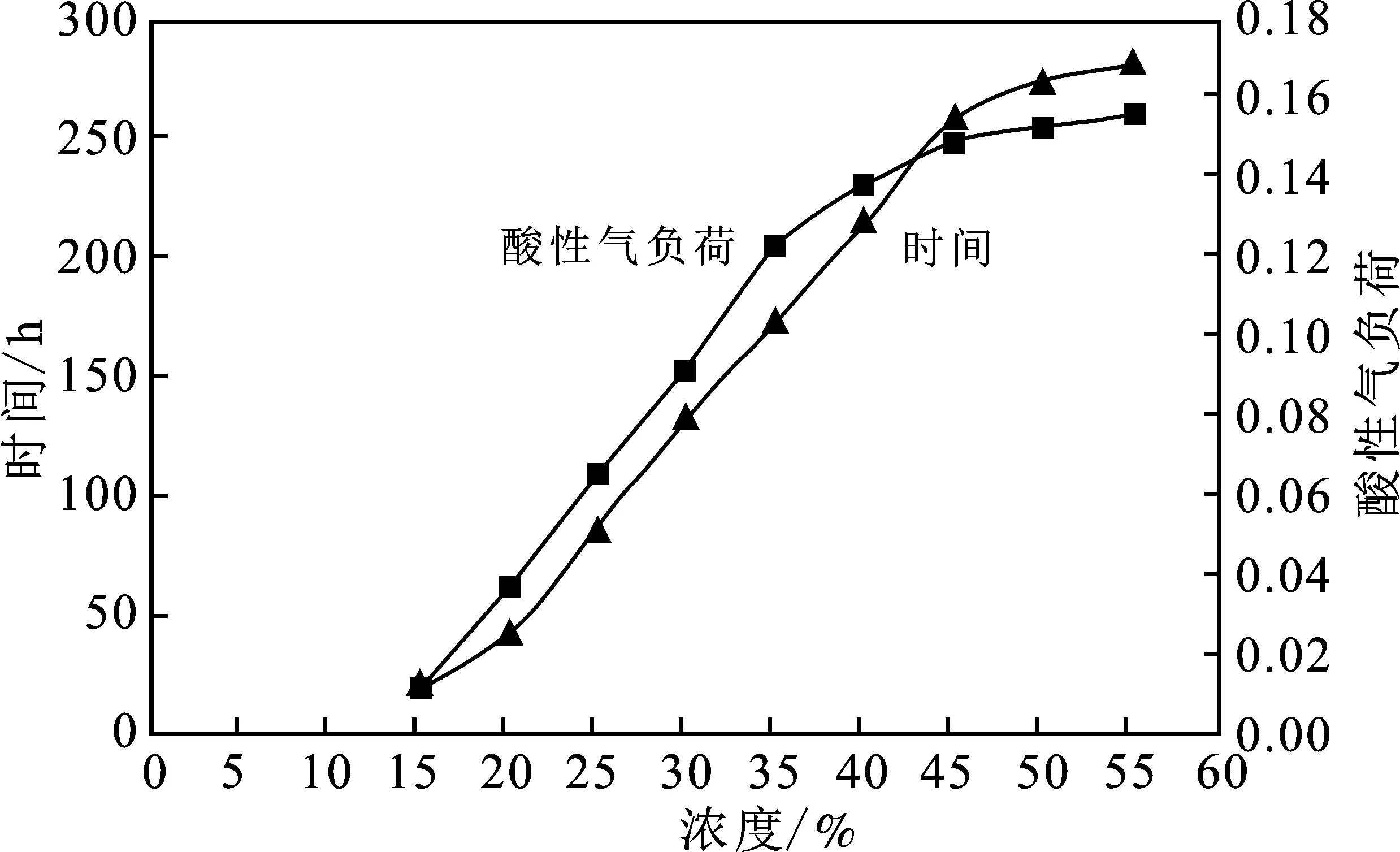
图3 溶液浓度对脱硫效果的影响Fig.3 Effect of solution concentration on desulfurization effect
由图3可知,(1)当MDEA浓度增加时,脱硫时间逐步增加,浓度为15%~45%区间时,脱硫时间呈线性增加,在45%以后,时间增速放缓,说明在50%浓度之后,再增加溶液浓度,并无明显效果。因此,脱硫剂理想浓度范围为40%~50%;(2)在浓度>45%之后,酸性气负荷增速大幅降低,虽然此时脱硫时间增速只是小幅降低,但考虑到经济价值,选择MDEA溶液浓度为45%。
2.3 空速对脱硫效果的影响
2.3.1 天然气空速对脱硫效果的影响 以MDEA溶液为脱硫剂,硫含量为23 mg/L的天然气为原料气,进行原料气空速对脱硫效果影响实验。实验条件:20 ℃,脱硫剂浓度45%,脱硫剂空速为1.0 h-1,原料气空速由1.0 h-1,以0.5 h-1为步长,增加原料气空速。脱硫剂与原料气逆向接触,调整空速至设定值,反应持续25 min,当净化气H2S高于二类气要求,即0.2 mg/L时,停止实验,结果见图4。
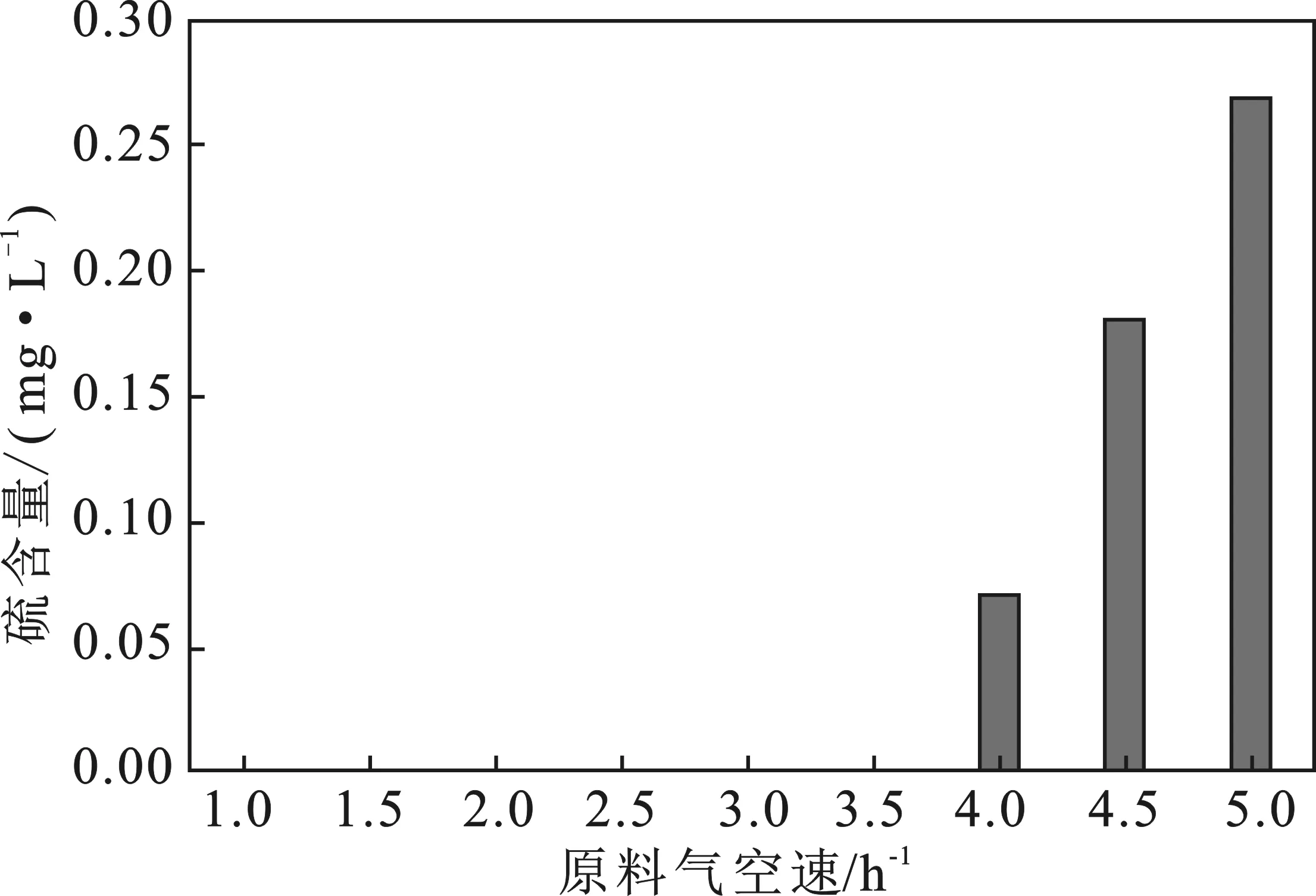
图4 原料气空速对脱硫效果的影响Fig.4 Effect of raw material space velocity on desulfurization effect
由图4可知,当脱硫剂空速为1.0 h-1时,原料气空速至4.5 h-1前都可进行正常脱硫反应,当空速>4.5 h-1后,由于原料气在脱硫剂中存留时间过短,脱硫效果较差,考虑采油厂实际情况,选择1.5~3.5 h-1为理想原料气空速。
2.3.2 脱硫剂空速对脱硫效果的影响 以MDEA溶液为脱硫剂,硫含量为23 mg/L的天然气为原料气,进行天然气空速对脱硫效果影响实验。实验条件:20 ℃,脱硫剂浓度45%,原料气空速选择1.5 h-1,脱硫剂空速由0.3 h-1,以0.05 h-1为步长,进行实验。脱硫剂与原料气逆向接触,调整空速至设定值,反应持续25 min,当净化气H2S高于二类气要求,即0.2 mg/L时,停止实验,结果见图5。
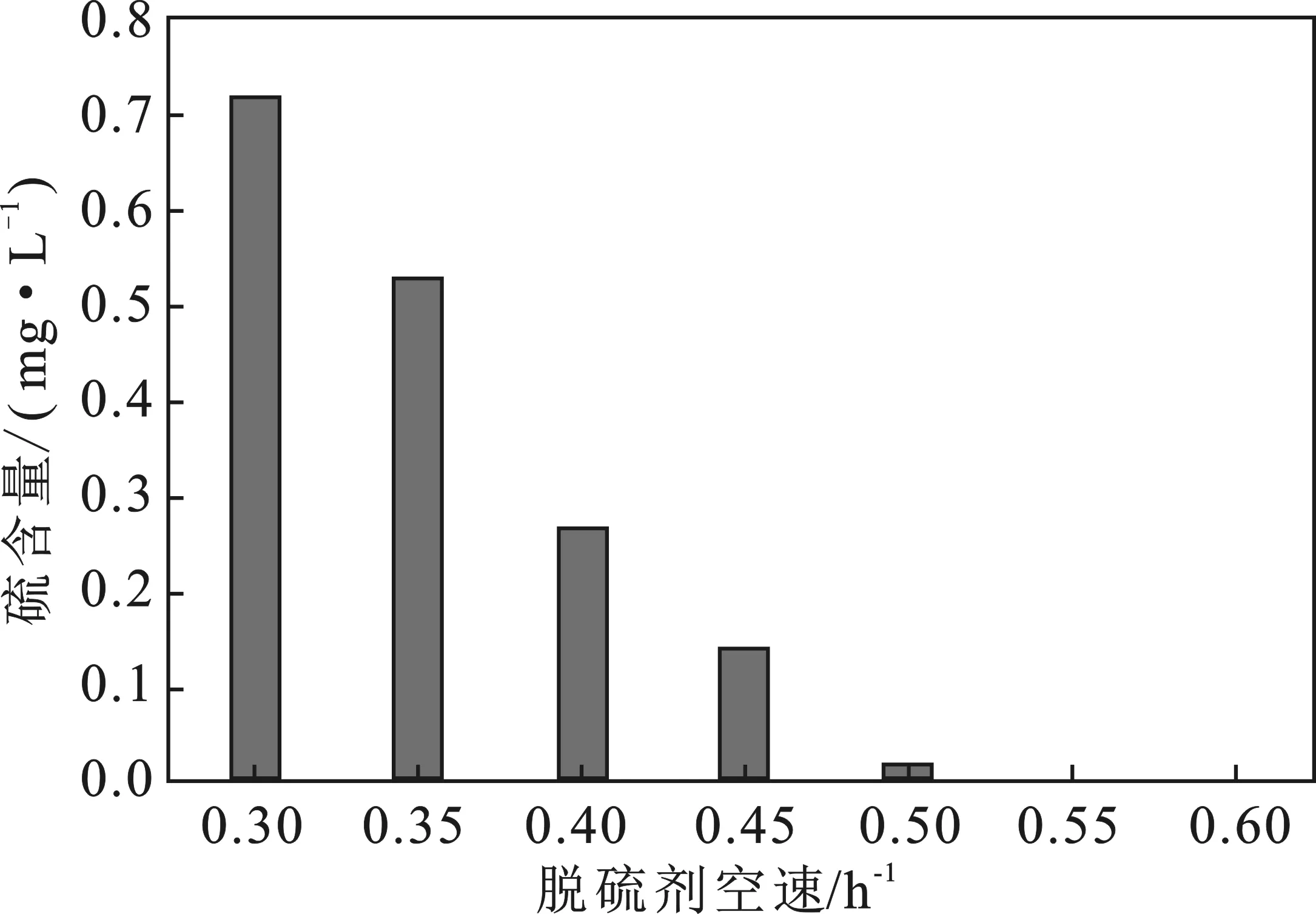
图5 脱硫剂空速对脱硫效果的影响Fig.5 Effect of space velocity of desulfurizer on desulfurization effect
由图5可知,(1)当脱硫剂空速增大时,脱硫剂对硫化氢负荷提高;(2)当脱硫剂空速低时,参与反应的脱硫剂较少,不能完成脱硫反应,当脱硫剂空速>0.45h-1时,即可达到天然气二类气标准。综合考虑,结合采油厂实际情况,可选择0.55~1.2 h-1为脱硫剂理想空速。
2.4 对比实验
利用甲基二乙醇胺(MDEA)与二乙醇胺(DEA)两种脱硫剂对原料气进行脱硫实验。实验中若考虑再生系统,则工序较为复杂,且不易实现,因此以净化后天然气质量与脱硫剂工作时间为标准,对MDEA与DEA进行对比实验。当考虑脱硫剂空速时,此时需不断加入脱硫剂,导致脱硫时间大大上升,净化后的天然气将会一直为合格气,因此将脱硫剂定量为10 mL,进行实验,探究两种脱硫剂的脱硫效果对比。
实验条件:吸收温度20 ℃,MDEA与DEA溶液浓度质量百分数45%,体积10 mL,原料气空速2.5 h-1。每隔12 h分析一次硫含量,当净化后天然气的硫含量高于0.2 mg/L,即高于二类气要求时,停止实验,结果见图6。
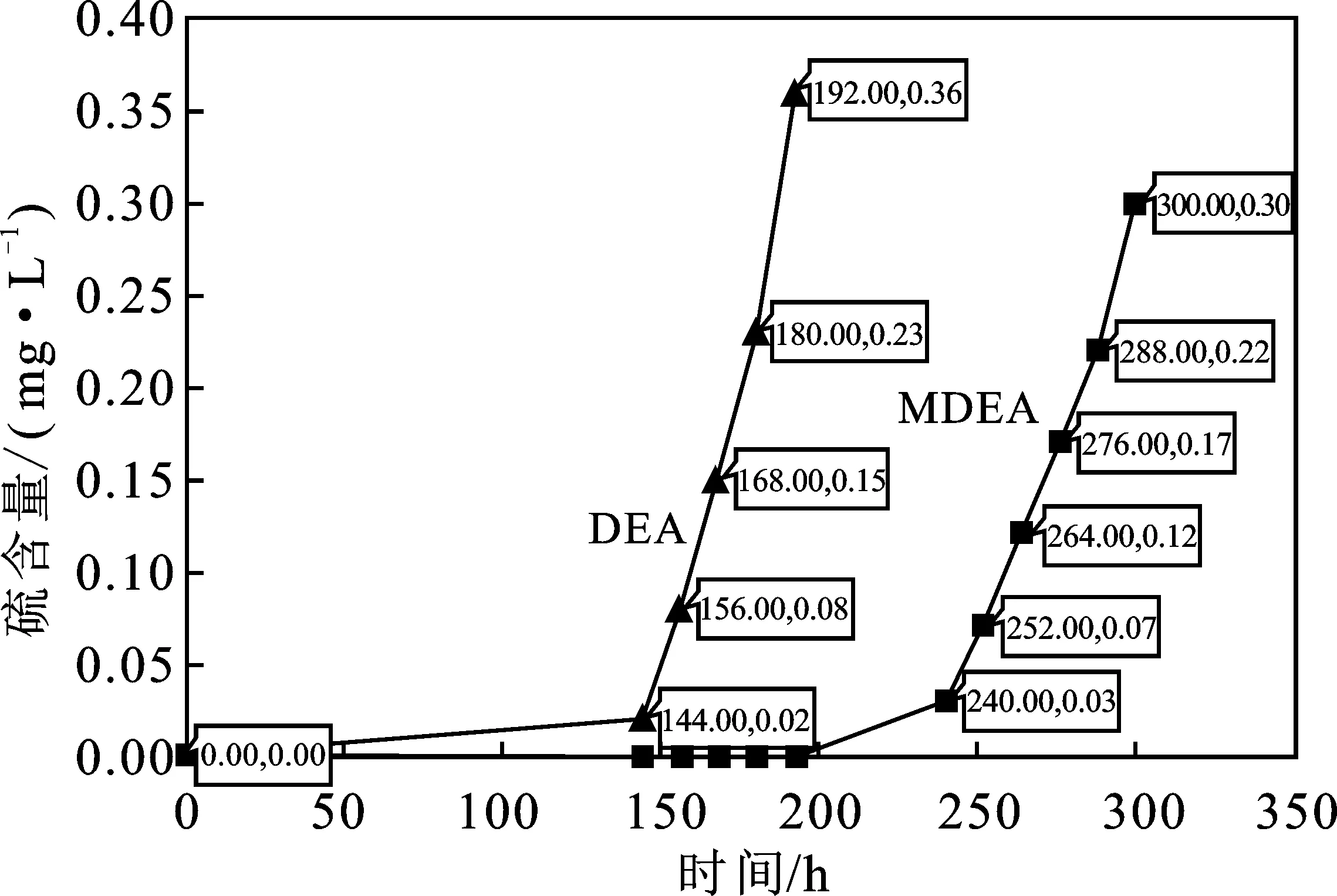
图6 两种脱硫方法脱硫效果对比Fig.6 Comparison of desulfurization effect between two desulfurization methods
由图6可知,前144 h,两种脱硫剂都能完成工作,在第144 h时,二乙醇胺(DEA)首次检测出硫含量,并且在随后的48 h中,硫含量逐步上升,第180 h时,硫含量>0.2 mg/L,超过二类气标准。第240 h时,在甲基二乙醇胺(MDEA)中首次检测出硫含量,并在随后的48 h中逐步上升,在第276 h时,硫含量>0.2 mg/L。
实验说明,甲基二乙醇胺的耐用时间,即第1次监测出硫含量的时间比二乙醇胺增加了67%,最终持续时间,即硫含量大于二类气要求的时间增加了53%,为采油厂由二乙醇胺工艺升级为甲基二乙醇胺工艺,提供了参考。
3 结论
根据某采油厂由二乙醇胺工艺迭代为甲基二乙醇胺的工艺需求,对甲基二乙醇胺进行实验研究,得出以下结论:
(1) 甲基二乙醇胺为脱硫剂时,最佳工作温度范围为15~30 ℃,最佳浓度范围为40%~50%,原料气空速范围为1.5~3.5 h-1,脱硫剂空速范围为
0.55~1.2 h-1。工作条件为上述范围时,可将脱硫剂性能最大化利用。
(2)对甲基二乙醇胺与二乙醇胺进行对比,证明甲基二乙醇胺工作效果大于二乙醇胺,相较于二乙醇胺,甲基二乙醇胺初次测得硫化氢时间增加了96 h,增加了67%,最终持续时间,增加了108 h,整体脱硫效果增加了53%。

