新生儿毛细血管渗漏综合征临床特点与治疗体会
高耸云
毛细血管渗漏综合征是指由各种原因引发的人体毛细血管内皮出现损伤以及血管通透性大幅度增加进而导致的组织间隙被小分子蛋白渗入,从而发生低血压、急性肾缺血、低蛋白血症以及患儿全身水肿现象的综合征[1]。毛细血管渗漏综合征的临床表现多为患儿胸腔及腹腔发生渗液、低蛋白、少尿、皮肤和黏膜水肿等,容易累及机体多处器官,且该病是引发新生儿病死的疾病之一,临床表现极其复杂,死亡率较高,预后效果差[2]。新生儿患有毛细血管渗漏综合征的原因较多,如脓毒症、缺血缺氧以及药物原因均可引发该病,治疗不当很有可能导致器官衰竭或内环境紊乱,给新生儿生命安全带来严重威胁[3]。本研究将2015 年1 月~2019 年5 月期间本院接收的8 例新生儿毛细血管渗漏综合征患儿作为研究对象,针对新生儿毛细血管渗漏综合征的临床特点与治疗方法进行分析,现报告如下。
1 资料与方法
1.1 一般资料 将2015 年1 月~2019 年5 月期间本院接收的8 例新生儿毛细血管渗漏综合征患儿作为研究对象,其中男5 例,女3 例;胎龄35~41 周,平均胎龄(36.67±2.25)周;<37 周5 例,≥37 周3 例;体重1210~3641 g,平均体重(2325.76±440.22)g;患病时间2~8 d,平均患病时间(4.82±1.15)d;正常分娩3 例,剖宫产5 例;所有患儿均为单胎,经临床检查与诊断确诊为新生儿毛细血管渗漏综合征,均符合2012 年版《毛细血管渗漏综合征》中的相关诊断标准;患儿家属均同意参加本研究,并在知情同意书上签字确认;本研究取得医院伦理委员会的批准。排除凝血功能障碍者,遗传性代谢疾病者,严重器质性疾病者;对研究中涉及药物存在禁忌证者;合并其他并发症者。
1.2 方法
1.2.1 诊断方法 新生儿毛细血管渗漏综合征的临床诊断金标准为将白蛋白输入,对细胞外液菊粉的分布容量进行测量,并利用电学方法对人体水分进行测定,即予以患儿生物电阻抗分析,其方法虽具有较高的临床诊断价值,但检测价格昂贵,无法在临床上推广[4];因此,临床上对于新生儿毛细血管渗漏综合征的诊断方式主要为常规实验室检查、临床症状以及分析病史等,其诊断依据为:存在严重感染、脓毒血症、严重创伤、低氧血症等;少尿,全身皮肤黏膜、球结膜出现水肿情况,眼泪溢出物呈现血浆状,血压和中心静脉压呈降低趋势,体重呈上升趋势,且胸腔和腹腔均存在积液;影像学X 线检查显示肺内出现间质渗出性变化;实验室检查显示血浆蛋白降低[5]。
1.2.2 治疗方法 以治疗原发病为主,对患儿施以抗感染、抗休克以及机械通气等基础性治疗;给予乌司他丁,剂量为2000 U/(kg·次),2 次d,以患儿病情发展情况为依据,连续治疗5 d[6];同时给予患儿白蛋白,剂量为1 g/(kg·次),2 h 后再次给予患儿同样剂量的白蛋白,其后续治疗需要根据患儿的实际情况酌情增加;严格把控患儿的出入量,如患儿尿量(24 h)大于生理需求量,则第2 天补液的剂量为生理需求量,如患儿尿量(24 h)小于生理需求量,则第2 天进行补液的剂量为前1 d 的尿量(24 h)[7]。
1.3 观察指标 分析患儿的临床表现与临床诊断结果,对比患儿治疗前后白蛋白水平;对患儿进行3 个月的随访,记录并分析患儿的生存情况。
1.4 统计学方法 采用SPSS22.0 统计学软件进行数据统计分析。计量资料以均数±标准差()表示,采用t 检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 临床表现与临床诊断结果 8 例患儿均出现全身水肿、体重增加以及低血压情况,且出现少尿患儿6 例(75.0%),低蛋白血症患儿5 例(62.5%);引起新生儿毛细血管渗漏综合征的主要因素为脓毒血症(87.5%)、机械通气(75.0%)、新生儿呼吸窘迫综合征(62.5%)、严重感染(37.5%)。见表1。
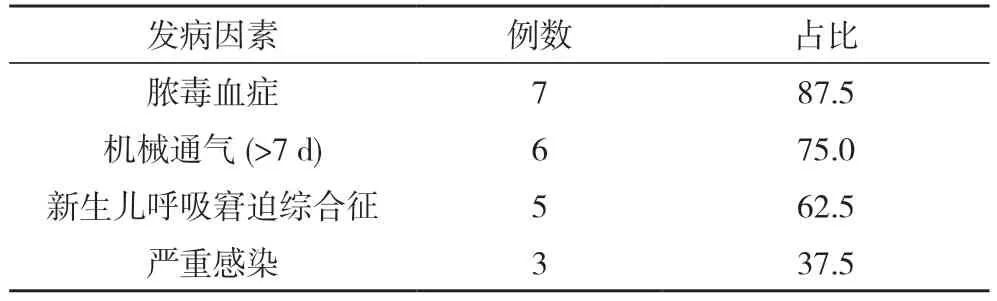
表1 临床表现与临床诊断结果(n,%)
2.2 治疗前后白蛋白水平比较与生存情况 治疗后,患儿白蛋白水平(31.75±2.61)g/L 高于治疗前的(23.42±2.15)g/L,差异有统计学意义(P<0.05)。随访3 个月,患儿死亡率为25.0%(2/8),生存率为75.0%(6/8)。
3 讨论
因早产等原因,新生儿极易发生休克、组织缺氧等现象,进而引起毛细血管渗漏,毛细血管渗漏综合征已成为近几年导致新生儿死亡的重要因素之一,由于新生儿器官尚未发育成熟,免疫系统不健全,所以病情更为严重[8]。有关新生儿毛细血管渗漏综合征的发病机制临床至今没有明确定论,有研究显示,在炎症介质的作用下机体毛细血管的内皮受到伤害,细胞逐渐发生分离现象,最终血管通透性变得更高,导致其无法阻止较小质量的分子[9]。另外,大量水分渗漏至组织间隙会引发新生儿全身皮肤发生水肿,继而导致循环血量受到干扰,全身器官因此发生缺血、缺氧症状,毛细血管渗漏综合征发生时肺部会出现渗出现象,加重组织缺氧,使新生儿发生呼吸窘迫,进而形成循环障碍[10]。这种疾病往往是从局部炎症开始,最后发展至大范围炎症蔓延,严重者还可能出现多器官功能衰竭。对于毛细血管渗漏综合征的治疗临床以往多使用羟乙基淀粉,羟乙基淀粉属于人工胶体,其能够降低炎症带来的反应,减少血管内皮损害程度,改善机体微循环
[11]。乌司他丁是一种蛋白酶抑制剂,能够调节白细胞与炎症反应,被广泛应用于急性肺损伤、胰腺炎等治疗中,同时还可以维护血管内皮细胞[12]。根据相关研究[13,14]表明,与羟乙基淀粉类型药物比较,乌司他丁在临床治疗上的效果更为显著,其能够更加明显的降低炎性反应,降低血管通透性与白蛋白的渗漏情况,还可以促进水分回流,缓解休克等其临床症状,控制新生儿出入量,有利于减轻患儿肺水肿情况,并对改善呼吸困难状态具有积极意义。
本次研究中通过对8 例新生儿毛细血管渗漏综合征患儿进行临床分析,可知引起新生儿毛细血管渗漏综合征的因素分别为脓毒血症(87.5%)、机械通气(75.0%)、新生儿呼吸窘迫综合征(62.5%)、严重感染(37.5%),因此,面对新生儿时要注意其个体性,考虑新生儿身体机能与正常儿童的差别,重点监护并予以优质护理,最大限度的降低新生儿毛细血管渗漏综合征的发生,为患儿的生命安全提供保障。在原发病治疗的基础上予以患儿乌司他丁,治疗后,患儿白蛋白水平(31.75±2.61)g/L 高于治疗前的(23.42±2.15)g/L,差异有统计学意义(P<0.05)。随访3 个月,患儿死亡率为25.0%(2/8),生存率为75.0%(6/8)。由此表明蛋乌司他丁能够有效改善患儿临床指标,有利于促进患儿的康复。
综上所述,新生儿毛细血管渗漏综合征与脓毒血症、机械通气、新生儿呼吸窘迫综合征以及严重感染等具有密切关系,患儿经乌司他丁、白蛋白以及调控出入量等临床治疗,其临床症状明显改善,对于患儿的生存质量具有重要意义。

