羟考酮复合罗哌卡因硬膜外分娩镇痛的临床效果
王春梅, 费 青, 吴周全
(南京医科大学附属常州第二人民医院, 江苏 常州, 213003)
分娩镇痛是指应用理疗、心理安慰以及药物镇痛等方式缓解产妇分娩痛苦,具体方法包括针灸、导乐、按摩、静脉给药及硬膜外给药等[1-2]。硬膜外镇痛是一种较安全且效果确切的分娩镇痛方法,具有易操作调控、不良反应少、产妇满意度高等特点,已成为临床首选的分娩镇痛方法[3-4]。目前,硬膜外分娩镇痛用药方案仍以低浓度局部麻醉药与阿片类药物联合应用为主,可起到协同镇痛作用,并降低不良反应发生率。羟考酮是一种半合成μ、κ双受体兴奋药,与吗啡相比,起效速度更快,镇痛时间更长[5], 且在治疗内脏痛方面比其他阿片类药物优势更明显[6-7]。分娩第一产程的疼痛主要是由子宫收缩以及胎头下降压迫直肠引起的内脏牵涉痛,故羟考酮更适用于分娩镇痛。本研究比较了羟考酮复合罗哌卡因与舒芬太尼复合罗哌卡因在硬膜外分娩镇痛中的应用效果,现报告如下。
1 资料与方法
1.1 一般资料
纳入80例22~35岁产妇作为观察对象。纳入标准: 孕周≥37周,单胎妊娠,经评估能够进行阴道分娩者。排除标准: 严重心、肺疾病患者,宫颈扩张>3 cm、明显头盆不称者,脊柱畸形侧弯或有脊柱手术史者,凝血功能异常及穿刺部位感染者。采用计算机生成的随机数编码,将80例产妇随机分为对照组和观察组,每组40例。本研究获得本院伦理委员会审核批准,且所有产妇知情同意。
1.2 方法
进入产房后,常规监测产妇生命体征,建立静脉注射通路,静脉滴注乳酸钠林格氏液500 mL。当产妇宫颈扩张约2 cm时,由从事麻醉工作5年以上的麻醉科医生进行硬膜外穿刺。嘱产妇取左侧卧位,定位L3~4间隙并行硬膜外穿刺,将硬膜外导管经硬膜外针向头侧置入4 cm。将试验剂量1.5%利多卡因3 mL注入硬膜外导管,判断未进入血管或蛛网膜下腔之后,对照组采用0.5 μg/mL舒芬太尼复合0.08%罗哌卡因8 mL初始剂量行硬膜外分娩镇痛,观察组采用0.2 mg/mL羟考酮复合0.08%罗哌卡因8 mL初始剂量行硬膜外分娩镇痛。硬膜外给药30 min后疼痛视觉模拟评分法(VAS)评分>3分视为置管失败,予以剔除。2组分别将镇痛药溶液100 mL连接电子镇痛泵,设置背景剂量8 mL/h泵入药液。若产妇自觉疼痛,则每次自控追加剂量8 mL, 锁定时间20 min。整个分娩过程中,应用超声多普勒系统监测胎儿心率,应用宫缩监测仪监测产妇宫缩强度及频率。产妇宫缩减弱、产程进展慢需增强子宫收缩力时,予2.5 U催产素稀释至500 mL静脉滴注。当宫颈完全扩张后,硬膜外电子镇痛泵泵注终止[8-9]。
1.3 观察指标
① 采用VAS评分评估2组产妇镇痛前、镇痛后1 h、镇痛后4 h以及分娩时的疼痛程度,分为无痛(0分)、轻度疼痛(1~3分)、中度疼痛(4~7分)、严重疼痛(8~9分)。② 比较2组产妇满意度评分(0分为极不满意, 10分为完全满意)、配合度评分(0分为非常不配合, 10分为非常配合)。③ 硬膜外给药后每30 s测试感觉阻滞最高平面,比较2组镇痛起效时间(硬膜外给药开始到麻醉平面达到T10的时间)、首次镇痛持续时间(镇痛后首次出现VAS评分>3分,需要追加剂量的时间)、自控镇痛泵追加给药次数、产程持续时间、催产素使用情况、会阴侧切缝合时局麻药使用情况以及中转剖宫产情况。④ 比较2组新生儿1 min Apgar评分和5 min Apgar评分,并在胎儿娩出后1 min收集脐动脉血进行血气分析。⑤ 比较2组产妇高血压(收缩压比基础值增高20%)、低血压(收缩压比基础值降低20%)、心动过缓(心率<60次/min)、恶心呕吐、皮肤瘙痒、呼吸抑制[血氧饱和度(SpO2)<93%或呼吸频率<10次/min]、爆发痛等不良反应发生情况。
1.4 统计学分析
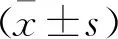
2 结 果
2.1 产妇一般资料比较
对照组有1例产妇硬膜外穿刺给药后镇痛效果不佳,予以剔除。2组产妇孕周、年龄、身高、体质量、出血量、总产程、催产素使用率以及中转剖宫产率比较,差异均无统计学意义(P>0.05), 见表1。
2.2 镇痛效果及产妇满意度、配合度比较
2组镇痛起效时间比较,差异无统计学意义(P>0.05)。镇痛后, 2组VAS评分均低于镇痛前,差异有统计学意义(P<0.05); 镇痛前和镇痛后1 h时, 2组间VAS评分差异无统计学意义(P>0.05); 镇痛后4 h时和分娩时,观察组VAS
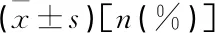
表1 2组产妇一般资料比较
评分均低于对照组,差异有统计学意义(P<0.05)。观察组会阴侧切缝合时局麻药使用率、爆发痛发生率低于对照组,首次镇痛持续时间长于对照组,自控镇痛泵追加给药次数少于对照组,产妇满意度和配合度高于对照组,差异均有统计学意义(P<0.05)。见表2。
2.3 产妇不良反应比较
2组产妇分娩期间均未发生低血压、呼吸抑制和心动过缓; 2组恶心呕吐发生率比较,差异无统计学意义(P>0.05); 观察组高血压发生率低于对照组,皮肤瘙痒发生率高于对照组,差异有统计学意义(P<0.05)。见表3。
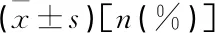
表2 2组镇痛效果及产妇满意度、配合度比较

表3 2组产妇不良反应比较[n(%)]
2.4 新生儿相关指标比较
本研究中,胎儿心率为120~160次/min, 新生儿1 min Apgar评分均>7分, 5 min Apgar评分均>8分,脐动脉血pH值均≥7.2。2组新生儿脐动脉血pH值、Apgar评分比较,差异无统计学意义(P>0.05), 见表4。
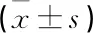
表4 2组新生儿脐带血气分析结果及Apgar评分比较
3 讨 论
硬膜外分娩镇痛具有易于实施、便于调控、并发症少且满意度高等优点,已成为临床分娩镇痛的首选方法[10]。低剂量罗哌卡因具有独特的“感觉与运动分离”优势,可明显降低运动阻滞的发生率[11]。与单一使用局麻药相比,低剂量罗哌卡因复合阿片类药物应用于硬膜外分娩镇痛中对产妇血流动力学的影响更小[12]。相关研究[13]显示,复合镇痛可以增强镇痛效果,减少局麻药用量,缩短第二产程,并提高新生儿1 min Apgar评分。
与芬太尼相比,舒芬太尼具有易通过血脑屏障及细胞膜、亲脂性高等优点,药物作用时间长,常被作为硬膜外分娩镇痛用药[14]。羟考酮主要通过激活μ受体和κ受体产生镇静和镇痛效果[15-16]。静脉注射羟考酮的镇痛起效时间为2~3 min, 镇痛维持时间为3.5~5.0 h[17-18]。张莹等[8]认为,硬膜外分娩镇痛中联合应用0.2 mg/mL羟考酮具有很好的的镇痛效果。本研究中,与对照组相比,观察组镇痛时间更长,爆发痛发生率更低,镇痛泵追加用药次数减少,会阴侧切缝合时局麻药使用率更低,这可能与羟考酮镇痛时间较长有关。羟考酮可显著减轻内脏牵涉痛,这与κ受体激活有关[19], 其良好的内脏镇痛作用可有效减轻产妇第一产程中的直肠压迫不适感,避免过早用力屏气排便,并可随意变换体位,促进产程顺利进展,减少不良反应的发生。本研究还显示,观察组孕妇的满意度更高,再次验证了复合羟考酮镇痛相比舒芬太尼更具优势。2组产程、中转剖宫产率及缩宫素使用率比较,差异无统计学意义(P>0.05), 提示羟考酮复合罗哌卡因在增强分娩镇痛效果的同时并没有延长产程时间,也不影响分娩方式。观察组皮肤瘙痒的发生率较高于对照组,但皮肤瘙痒主要发生于给药初期,且是一过性的,本研究产妇通过听音乐的方式分散注意力后均表现出较好的耐受性,无需另行用药。
KOKKI M等[20]研究表明,与未孕妇女相比,在第一产程中静脉注射羟考酮的产妇消除半衰期显著更短,且新生儿未发生严重不良反应。KINNUNEN M等[21]分别在母羊的静脉血管和硬膜外腔注射羟考酮注射液,并测试脐血与母体血浆的羟考酮血药浓度,发现硬膜外注射组脐血与母体的血药浓度均远低于静脉注射组。SEATON S等[22]采集剖宫产术后行羟考酮静脉镇痛产妇的母乳及新生儿血液检测羟考酮含量,发现产后72 h的母乳中虽含有羟考酮,但因新生儿母乳摄入量较少,故风险很小。羟考酮静脉给药可引发呼吸抑制,但本研究中所有新生儿Apgar评分均较高,且无1例胎儿脐动脉血pH值低于7.2, 表明羟考酮应用于硬膜外分娩镇痛中不会引起新生儿呼吸抑制,安全性较高。
综上所述,相较于舒芬太尼复合罗哌卡因,羟考酮复合罗哌卡因硬膜外分娩镇痛能延长镇痛时间,改善镇痛效果,且不会增加产妇不良反应,也不会引发新生儿呼吸抑制,是一种可在临床推广应用的分娩镇痛新方法。

