18F-FDG PET/CT显像对宫颈癌放疗后骶骨不全骨折与转移瘤的鉴别诊断
张杰平,林端瑜,李生栩,蔡志华,唐明灯
福建省肿瘤医院,福建医科大学附属肿瘤医院,福建福州 350014;
骶骨不全骨折(sacral insufficiency fracture,SIF)与创伤性骶骨骨折不同,是指发生于生理性应力或轻微外力于骨组织减少或弹性抵抗力降低的骶骨所发生的不完全骨折。骨的弹性抵抗力减低可由多种因素引起,而放疗是重要的诱发因素,可加剧骨折的发生。骨盆放疗后并发 SIF 并不罕见,其发生率为4.4%~18.0%[1-3]。骨折的炎症反应及修复过程均不同程度地摄取18F-FDG。随着18F-FDG PET/CT 在恶性肿瘤诊断、分期、监测等中的广泛应用,如何将这些良性病变的18F-FDG 摄取与肿瘤复发转移相鉴别至关重要。目前临床对放疗后SIF 认识不足,具有恶性肿瘤病史患者发生SIF 极易误诊为骨转移瘤[4]。SIF 会严重影响患者的生活质量,并具有一定的致残、致死率[5]。因此,正确认识SIF 并与骶骨转移瘤鉴别对指导临床治疗至关重要。本研究拟探讨盆腔放疗后SIF 的18F-FDG PET/CT 表现及其在鉴别诊断SIF 与骶骨转移瘤中的价值。
1 资料与方法
1.1 研究对象 收集2011年10月—2018年12月福建省肿瘤医院因宫颈癌盆腔放疗后行18F-FDG PET/CT检查患者660 例。SIF 纳入标准:结合病史、症状、治疗经过及影像学检查共同诊断。影像学诊断标准:放疗结束后放疗区域内骨盆新出现的病灶,CT 表现为骨皮质连续性中断,骨小梁受压变形,同时可能出现骨痂形成的硬化区域。随访至少6 个月,影像复查和(或)临床判断病情好转或稳定,无可疑肿瘤复发转移。最终纳入SIF 患者29 例,平均年龄(61±10)岁,发现SIF 距放疗结束时间(17±15)个月。29 例患者均无明显外伤史,其中17 例有下腰背部或大腿内侧疼痛,12 例无明显症状。随访6~60 个月,中位时间37 个月。收集同期我院确诊的28 例骨转移仅限骨盆并累及骶骨的患者作为对照组,其中男13 例,女15 例,平均年龄(56±14)岁;原发灶:肺癌8 例,宫颈癌7 例,乳腺癌、鼻咽癌、食管癌各3 例,直肠癌、肝癌各2 例。本研究经我院伦理审查委员会批准,免除患者知情同意。
1.2 检查方法 采用Philips PET/CT 仪(GEMINITF64);回旋加速器(HM-10);显像剂18F-FDG 放化纯度>95%。注射显像剂前,患者空腹6 h 以上,血糖控制在7.0 mmol/L 以内。按0.10~0.15 mCi/kg 静脉注射18F-FDG,静息60 min 后显像。先行CT 扫描,扫描范围自颅顶至股骨中段,扫描参数:管电压120 kV,管电流100~110 mA,螺距0.829;重建层厚5.0 mm;腰椎及骨盆局部重建层厚1.0 mm,间隔1.0 mm。PET图像采集范围同CT,采集时间1.0~2.0 min/床位,采集层厚4.0 mm。PET 图像重建采用迭代法重建,利用CT 透射扫描数据对PET 图像进行衰减校正。在EBW 2.0 工作站上进行图像融合,获得横断面、矢状面和冠状面PET、CT 以及融合图像。
1.3 图像分析 由2 名具有多年骨关节影像学诊断经验的医师采用盲法进行图片分析,意见不同时协商达成一致。测量及观察指标包括:①放疗区域腰椎椎体CT 值、邻近放疗区域外椎体CT 值;测量方法:选取相应区域密度均匀椎体,设置尽可能大的感兴趣区,并避开骨岛、硬化、骨皮质、椎后静脉入口处骨小梁缺少区,2 名医师独立测量后取平均值。②骨折类型:参考Linstrom 等[6]关于无外伤史SIF 分型,将骨折分为:骶骨翼双侧纵行骨折(A1 型),若进一步加重则出现横行骨折(A2 型);骶骨翼单侧纵行骨折(B1 型),若进一步加重则出现横行骨折(B2 型),并记录有无合并胸腰椎及骨盆其他部位骨折。③病灶区域FDG 摄取模式包括SUVmax、弥散或局灶性、结节/团块状或条带状。④CT 骨质改变:弥散或局灶性、成骨、溶骨或混合改变、有无骨折线(骨质透亮线/硬化)。⑤有无软组织肿块。
1.4 统计学方法 采用SPSS 25.0 软件,正态分布的计量资料比较采用成组资料t检验;分类变量组间比较使用χ2检验或Fisher 确切概率法。采用受试者工作特征(ROC)曲线分析SIF 与骶骨转移瘤的最佳SUVmax 临界值。P<0.05 为差异有统计学意义。
2 结果
2.1 SIF 组和转移瘤组的CT 表现 SIF 组放疗区域内、外椎体CT 值分别为(25.1±26.6)Hu 和(90.3±32.5)Hu,差异有统计学意义(t=8.354,P<0.001;图1);骨折类型:B1 型9 例,B2 型2 例,A1 型11 例,A2 型7 例,合并骶骨外骨折11 例,其中耻骨骨折9 例。骨质改变分布:弥漫性21 例,局限性8 例;骨质破坏类型:成骨性24 例,混合性5 例。29 例均显示骨折线;29 例均无软组织肿块(图2)。
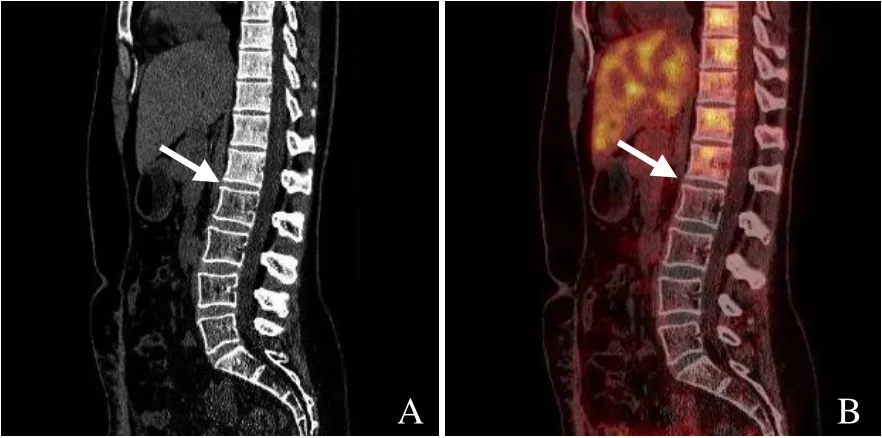
图1 女,39 岁,宫颈癌放疗后7 个月SIF。矢状位CT 示以L1~2 椎间隙为分界线,照射野内腰椎密度明显低于照射野外(箭,A);PET/CT 融合图示以L1~2 椎间隙为分界线,照射野内腰椎放射性摄取明显低于照射野外(箭,B)
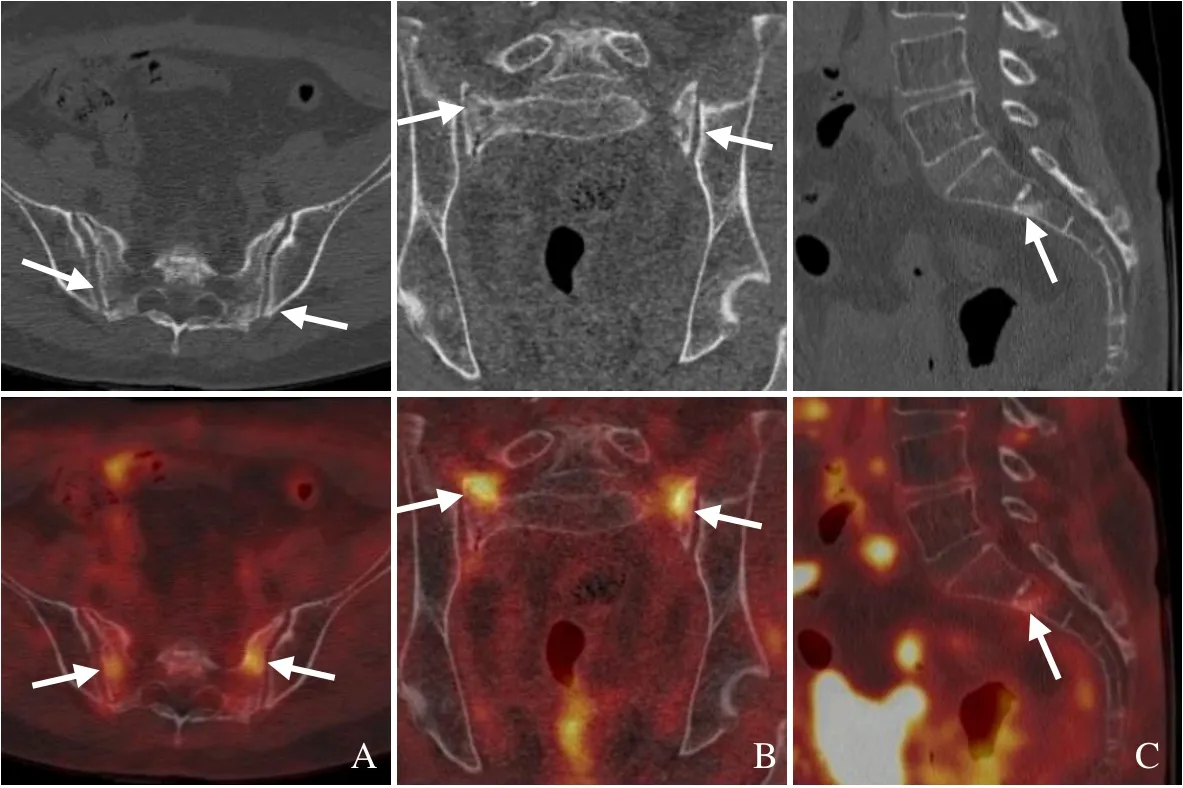
图2 女,55 岁,宫颈癌放化疗后5年SIF。PET/CT 骶骨横断面(A)、冠状面(B)显示双侧骶骨翼平行于骶髂关节骨折线,放射性摄取弥漫性轻度增高,沿骨折线处为著(箭);矢状面(C)显示骶骨体横行硬化骨折线,轻度FDG 摄取(箭)
转移瘤组骨质改变分布:弥漫性2 例,局限性22 例;骨质破坏类型:溶骨性16 例,成骨性3 例,混合性5 例,无骨质破坏4 例;骨折线2 例;20 例合并软组织肿块(图3)。
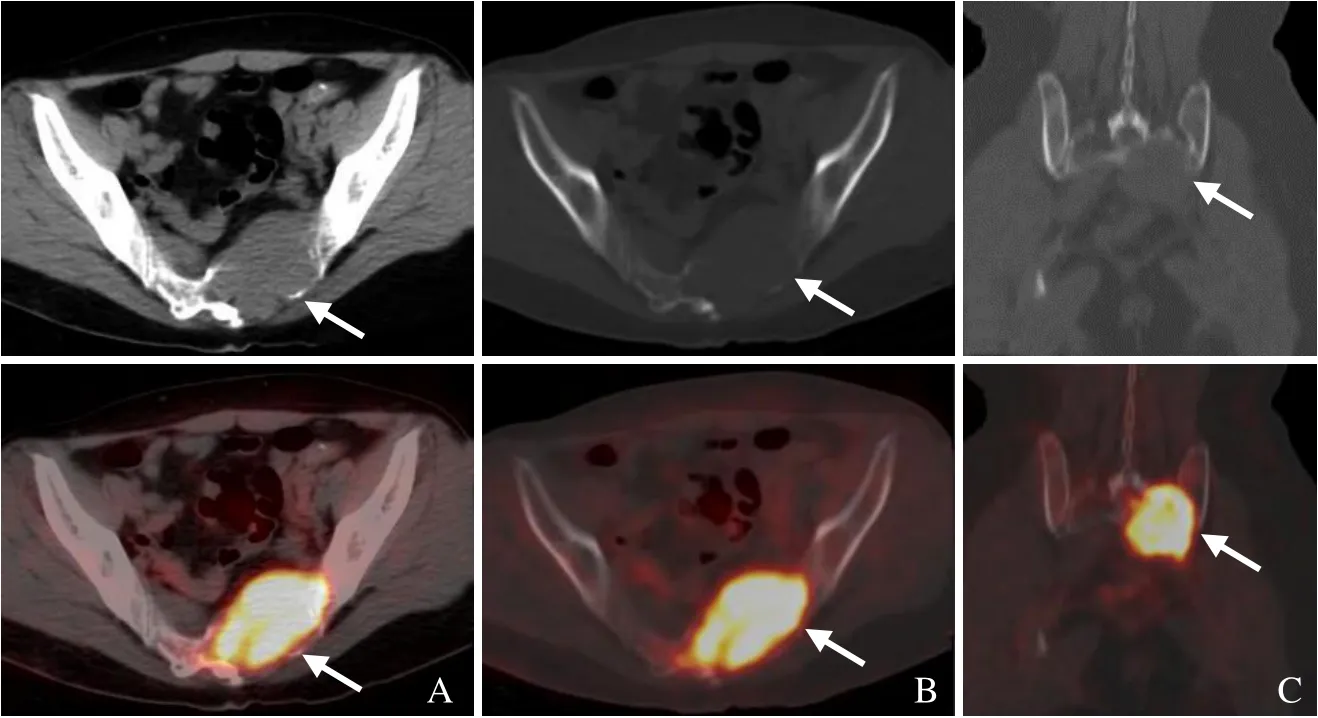
图3 女,54 岁,宫颈癌骶骨转移。PET/CT 示骶骨溶骨性破坏,骨破坏区可见软组织肿块,放射性摄取增高(箭),SUVmax为8.4。横断面软组织窗显示骨质破坏区软组织肿块,FDG 高摄取(A);横断面骨窗显示骶骨体及左侧翼溶骨性破坏,FDG 高摄取(B);冠状面骨窗显示骶骨体及左侧翼溶骨性破坏,FDG 高摄取(C)
2.2 SIF 组和转移瘤组的FDG 摄取特征 SIF 组病灶SUVmax 为3.0±1.2;18F-FDG 浓聚分布:弥漫性20 例,局灶性6 例,无摄取3 例。26 例浓聚形态均为条带状。转移瘤组SUVmax 为9.1±4.2;18F-FDG 浓聚分布:弥漫性2 例,局灶性26 例。2 例浓聚形态为条带状,26 例为结节状/团块状。
2.3 SIF 组与转移瘤组PET/CT 特征比较 两组SUVmax、FDG 摄取范围、浓聚形态、CT 骨质密度改变分布、骨质破坏形式构成比、骨折线检出及有无软组织肿块比较,差异均有统计学意义(P均<0.001);骨质破坏4种类型中混合性骨质破坏检出率差异无统计学意义(P>0.05),成骨性、溶骨性及无骨质密度改变检出率差异均有统计学意义(P<0.001,表1)。
ROC 分析显示,区分SIF 与转移瘤的SUVmax最佳阈值为5.0,敏感度为83.2%,特异度为98.5%(图4)。
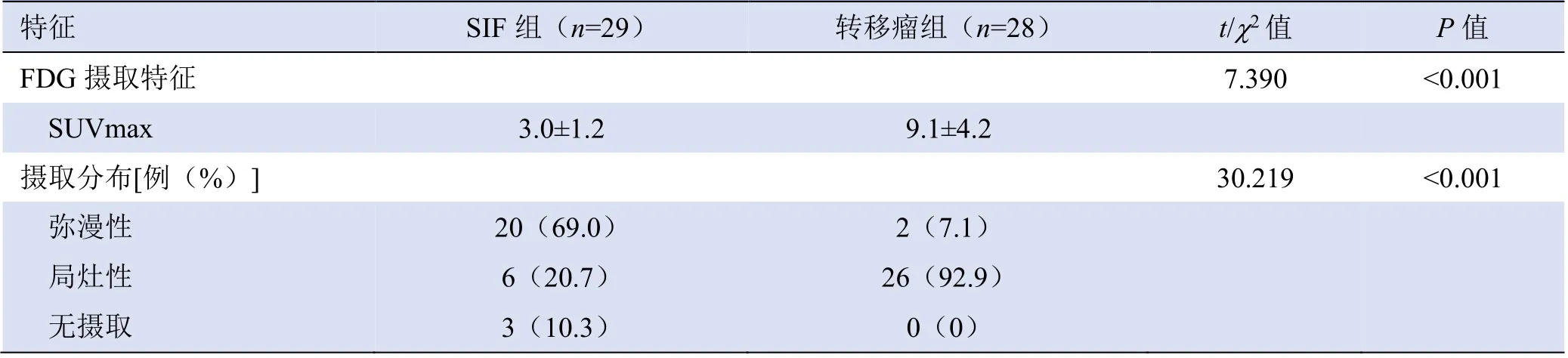
表1 SIF 组与骶骨转移瘤组的PET/CT 特征
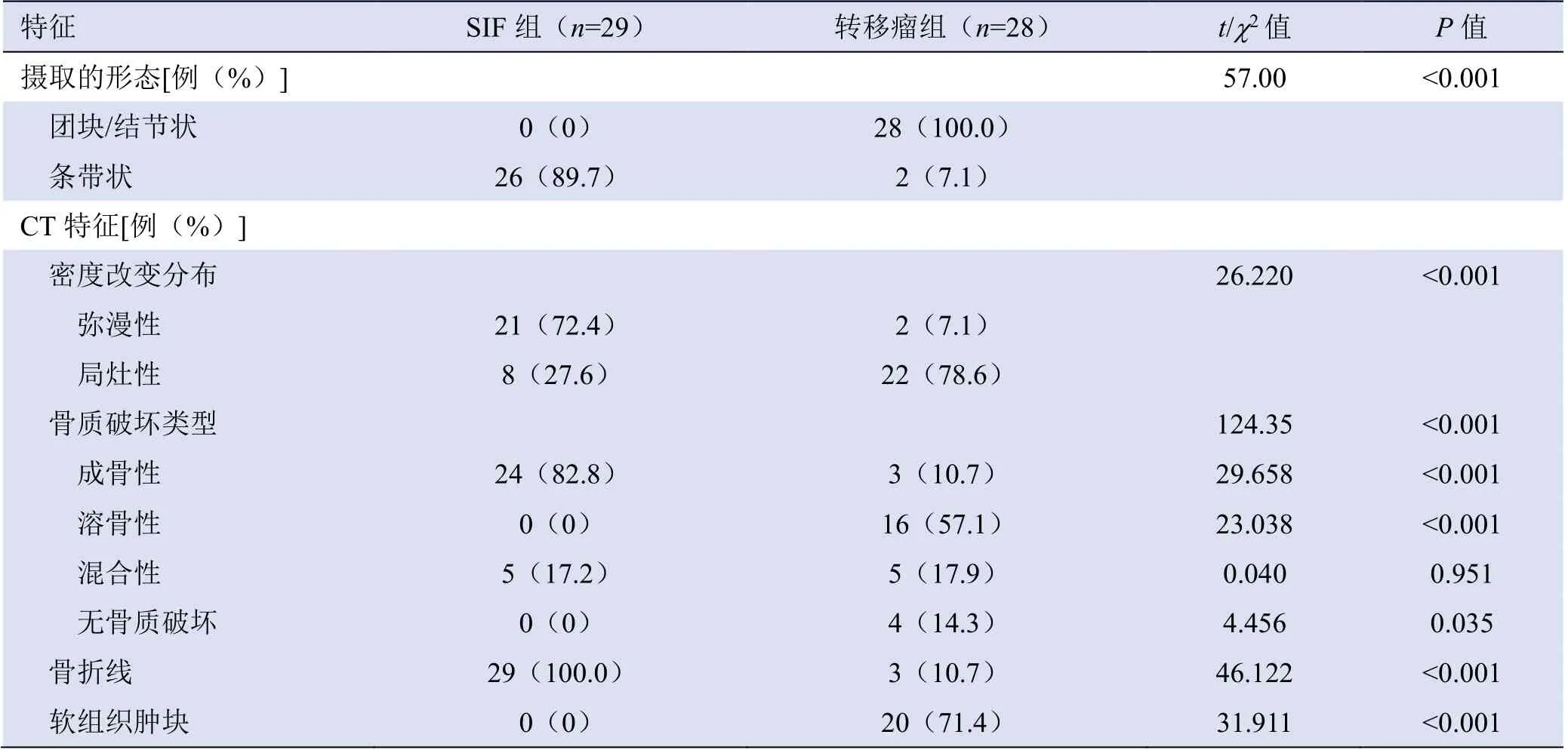
续表1
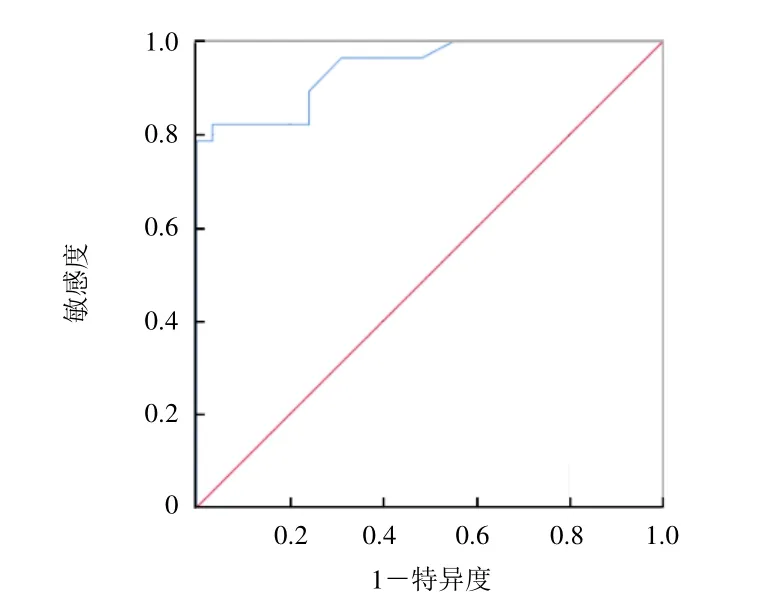
图4 SUVmax 诊断骶骨转移瘤的ROC 曲线
3 讨论
宫颈癌的发病率居女性恶性肿瘤第二位,仅次于乳腺癌。放疗是治疗宫颈癌的重要方法,特别是中晚期(ⅡB 期以上)宫颈癌,大多数选择同步放化疗。接受盆腔放疗宫颈癌患者的骨盆暴露于照射野内。放疗可杀死成骨细胞、骨细胞和破骨细胞,导致骨基质减少,还可以引起小血管闭塞,导致骨坏死、骨萎缩,继发骨质疏松,而骨质疏松是发生SIF 的根本原因[7]。CT 和MRI 是宫颈癌随访的常规影像技术,也是其放疗后SIF 检出的重要方法。CT 为断层成像,能有效避免结构重叠,并具有较高的密度及空间分辨率,有利于显示骨折线及骨折修复形成的硬化性改变。CT值能定量分析骨骼密度的改变,判断骨质疏松的程度。CT 既能反映SIF 易发因素,又能有效检出骨折部位,在SIF 诊断中具有一定的价值。然而对于早期的隐匿性骨折CT 通常不能有效检出。本组SIF 患者中FDG 摄取增高的范围常超出骨折线,部分FDG 摄取增高的区域CT 并未发现骨折,而在后期复查该区域出现成骨性修复,推测其原先为CT 未能检出的隐匿性骨折。当骨折线与扫描线平行时,CT 轴位扫描图像也很容易漏诊[8]。MRI 具有高软组织分辨率,骨折引起的骨髓水肿及出血均能引起MRI 信号改变,因此MRI 诊断SIF 的灵敏度高,但其信号改变与其他疾病重叠较多,当表现不典型时难以鉴别。
18F-FDG PET/CT 实现了功能影像与解剖影像的同机融合,不仅能提供病变椎体形态及密度改变,还可以根据其代谢状态进行鉴别诊断。为了验证放疗对骨骼的改变,本研究对比放疗区域内、外椎体的CT值,发现放疗区域内椎体的CT 值显著低于放疗区域外,平均达65.2 Hu,两者差异有统计学意义。腰椎椎体松质骨CT 值与骨密度呈高度正相关,因而直观地反映了放疗继发骨质疏松这一SIF 的根本原因。检出骨折线是诊断SIF 的重要依据,Meixel 等[9]报道PET/CT 对SIF 的误诊率较高,未能发现骨折线可能是一个重要因素,因为既往研究中PET/CT 中CT 扫描通常采用低剂量、大视野、厚层、软组织重建,其空间分辨率低,不利于检出骨折线。本研究在腰椎及骨盆区域采取局部1 mm 层厚、小视野、骨算法重建以提高图像分辨率;29 例SIF 均清晰显示骨折线,表现为骶骨翼一侧或双侧出现平行于骶髂关节的透亮线或硬化带,部分可伴有骶骨体横行骨折线;11 例骶骨外出现骨折,其中耻骨是最常见的部位,与Zhang 等[10]的研究结论相符。
骨折线外骶骨不同程度及不同范围的骨质密度增高也是本组SIF 的典型表现,29 例均出现该征象,推测其原因为骶骨应力隐匿性损伤修复过程的表现,损伤发生距检查的时间点不同,反映不同的修复阶段,表现为不同程度的骨质密度增高。转移瘤以溶骨性病灶为主,即使成骨性转移其密度改变也较局灶。18F-FDG PET/CT 对部分无骨质密度改变的转移灶更有优势,本组4 例转移瘤仅表现为局灶性放射性浓聚而无骨质密度改变,单纯CT 扫描极易漏诊。29 例SIF中,26 例(89.7%)摄取FDG,SUVmax 为3.0±1.2,转移瘤100%摄取18F-FDG,SUVmax 为9.1±4.2,SIF 组显著低于转移组,差异有统计学意义;区分SIF 与转移瘤的最佳阈值为5.0,其敏感度为83.2%,特异度为98.5%;与Choi 等[11]在椎体良、恶性骨折的阈值4.25 相仿。良性骨折的18F-FDG 摄取主要由于骨折致使局部组织缺血坏死,导致大量中性粒细胞、巨噬细胞等炎症细胞聚集,反映炎症细胞的18F-FDG 摄取[12-13],其摄取程度一般低于恶性肿瘤[11-12]。本研究中两组18F-FDG 浓聚形态存在显著差异;丁浩源等[14]报道SIF 患者SPECT/CT 表现为骶骨“H”形显像剂浓聚,沿骨折线条带状浓聚伴骶骨弥散性轻度浓聚也是 SIF PET/CT 的摄取特点,占18F-FDG 阳性病例的76.9%(20/26)。骶骨转移瘤的18F-FDG 浓聚多呈局灶性,表现为结节状或团块状浓聚。
除骨折线相应部位的条带状放射性摄取增高外,骨折线外骶骨骨质正常区域弥散性轻度放射性浓聚也是SIF 的特有表现,其原因可能是细微隐匿性骨折或骨挫伤;张峰等[15]报道18 例脊椎骨挫伤均摄取18F-FDG;本组SIF 复查病例中,部分患者在原先轻度浓聚而无骨质密度改变区域新出现骨质密度增高影,推测其可能为原先隐匿性损伤修复的表现。而转移瘤大多不伴有骶骨应力隐匿性损伤,故肿瘤以外区域无浓聚。本组SIF 病变椎体周围均无软组织肿块影;转移瘤组71.4%(20/28)出现软组织肿块,多为溶骨性转移。软组织肿块出现情况差异有统计学意义,与吴增杰等[16]的报道一致。良性压缩性骨折椎体周围软组织影可能是因少量出血、软组织水肿所致,SIF 多为自发或仅受轻微外伤,故软组织肿块的发生率很低。
总之,平行于骶髂关节的骨折线伴轻中度18F-FDG 摄取是宫颈癌放疗后SIF 的典型表现;18F-FDG PET/CT 显像中病变的SUVmax、18F-FDG 摄取模式、CT 骨质破坏模式、有无骨折线及软组织肿块等在SIF 与转移瘤的鉴别诊断中有重要价值。本研究的不足之处在于,多数病例未能明确SIF 发生距18F-FDG PET/CT 检查的时间跨度,无法判断骨折的新旧程度与FDG 摄取程度是否相关。18F-FDG PET/CT显像在SIF 治疗中的指导价值有待于进一步研究。

