中空微结构合金Pt/Cu的制备及其对氨硼烷水解释氢的催化活性
刘全兴,刘亚伟,张 军,杜西刚,李 想
(河南科技大学 化工与制药学院,河南 洛阳 471023)
0 引言
氨硼烷(ammonia borane,AB)是一种新型化合物储氢材料,理论含氢量高达19.6%,借助于适当的催化剂能够实现可控化释氢[1-2],因而近年来AB的研究引起广泛关注,应用潜力无限[3]。
涉及AB水解释氢的催化剂大多集中在贵金属领域[4-6],如Pd、Pt、Rh、Ru的单质及其化合物,虽然贵金属基催化剂的催化效果较好,但其高昂的价格依然是其应用发展的主要障碍。近年来,将某些催化能力较低的过渡金属(如Fe、Co、Ni和Cu等)与贵金属进行复合,通过特殊的合成途径,使金属间形成电子和物相结构有效协同的多形貌合金微纳米粒子,可较大幅度地提升其催化性能[7-9]。过渡金属Cu的储量丰富、价格低廉、导电性强、性能稳定,但其对AB水解释氢的催化活性很低,将Cu与贵金属Pt融合成为独特微结构(如中空、纳米线、核壳结构等)的合金微粉[10-11],可有效降低催化剂的制备和应用成本。制备特殊微结构合金的方法已有多种[12],其中,牺牲模板(或伽伐尼置换)法已被证明具有良好的形貌调控能力,文献[13-14]分别采用此类工艺制备了具有中空结构的多种金属纳米晶,但产物形貌不够规整,且团聚较严重。由于中空结构微粒可为反应物的传输提供便捷通道,且具有较大的比表面积,因而可以形成更多的活性位点,有效提升其催化效能。现阶段Pt/Cu中空合金的制备,大多采取溶剂热工艺路线,需要高压条件,而且还要用到较多的有机溶剂,产物不易分离,产率较低,且易造成一定程度的污染[15],因而亟待寻求新的合成途径,以利于制备更多种类、更为高效的合金催化剂。本文采用水作为溶剂,水合肼为还原剂,将铜快速置换出来,然后加入氯铂酸,使铜与氯铂酸之间发生伽伐尼置换反应,从而以“一锅烩”的方式,制成了具有中空结构的Pt/Cu微纳米合金粒子,并借助AB水解释氢反应科学评价了合金的催化性能。
1 试验部分
1.1 原料及仪器
氯化铜(CuCl2·2H2O,99.0% (质量分数,下同))、氯铂酸(H2PtCl6·6H2O,98.2%)、十六烷基三甲基溴化铵(C16H33(CH3)3NBr,CTAB,99.0%)、水合肼(N2H4·H2O,99.9%)、乙醇(C2H6O,99.7%)和丙酮(CH3COCH3,99.5%)均为国产分析纯试剂,用前未作进一步纯化。氨硼烷(NH3BH3),购于郑州聚硼公司,标称质量分数大于98%;试验用水为自制的二次蒸馏水。产物的物相结构用X射线粉末衍射仪(X-ray diffraction,XRD) (Bruker D8-Advance,德国)分析,Cu 靶Kα射线 (λ=0.154 nm);用透射电子显微镜(transmission electron microscope,TEM) (JEM-2100,日本)对产物形貌进行了表征。
1.2 Pt/Cu双金属合金催化剂的制备
对于Pt/Cu物质的量比为0.5∶1.0的情况,制备方法如下:室温下,取37 mg的CTAB加入20 mL水中,搅拌使之溶解,再加100 μL、0.1 mol·L-1的Cu2+水溶液,搅拌10 min后,逐滴滴加浓氨水,调节混合溶液的pH = 10,然后将溶液转移到100 mL圆底烧瓶中。此外,将37 mg CTAB固体和280 μL质量分数为85%的水合肼,依次加入20 mL水中,搅拌均匀,得到水合肼溶液。在强烈搅拌下,将20 mL水合肼溶液逐滴(约1.0 mL·min-1)加入圆底烧瓶中,室温下不断搅拌,连续反应3 h,反应过程中溶液颜色逐渐由天蓝色转化为酒红色。
取300 μL浓度为17.0 mmol·L-1的PtCl62-水溶液,加入20 mL水中,搅拌后形成Pt溶液,将此Pt溶液用酸式滴定管逐滴(约1.0 mL·min-1)滴加到前述步骤所得酒红色含Cu粒子的混合体系中,继续搅拌反应3 h。将产物移出,高速(约10 000 r/min)离心分离,依次用丙酮、50 ℃热水反复洗涤数次,充分洗去残余的还原剂和表面活性剂,取出产物封存于无水乙醇中,备用,标记为Pt/Cu-0.5。需要制成固态微粒时,可通过冷冻干燥而获得。
调控前驱体H2PtCl6与CuCl2的物质的量比分别为1.00∶1.00、0.75∶1.00、0.50∶1.00、0.25∶1.00和0.15∶1.00,按照上述制备方法,可获得一系列双金属催化剂Pt/Cu,依次标记为Pt/Cu-1.00、Pt/Cu-0.75、Pt/Cu-0.50、Pt/Cu-0.25、Pt/Cu-0.15。
1.3 Pt/Cu双金属合金的催化活性评价
选用50 mL体积的厚壁耐压玻璃瓶作为AB水解反应器,置于恒温水浴槽内,采用水下磁力搅拌装置对溶液进行搅拌。耐压玻璃瓶上端出口与立式冷凝管连接,用273 K深冷循环水进行冷凝;经冷凝后导出的气体通入气体捕集阱,阱内装有足量的无水固体氯化钙,用以脱除杂质气体,之后把气体导入排水集气定量装置,汇聚氢气,适时测定产氢量。水浴温度控制在预定值,控温精度为±0.5 K。将10 mL浓度为100 mmol/L的AB溶液注入反应器,快速加入5 mg的Pt/Cu双金属催化剂,开始搅拌、计时,定时记录AB水解过程中的释氢体积[16]。
2 结果与讨论
2.1 Pt/Cu双金属合金的物相表征
控制双金属的物质的量之比,所得系列产物的XRD图谱见图1。由图1可知:对于单一金属Cu和Pt,分别在2θ位于43.29°、50.43°、74.13°、89.93°以及39.76°、46.24°、67.45°、81.28°的位置,各自均出现了4个比较清晰的衍射峰,经与粉末衍射标准联合委员会数据库比对,这两组衍射峰分别对应于面心立方晶相的Cu (PDF:04-0836)和Pt (PDF:04-0802),分别归属于金属Cu和Pt的(111)、(200)、(220)和(311)晶面。对于其余5个双金属产物,即Pt/Cu-0.15、Pt/Cu-0.25、Pt/Cu-0.50、Pt/Cu-0.75和Pt/Cu-1.00,相应的XRD图谱明显呈现出一定程度的规律性变化。当Pt/Cu较低(n(Pt)∶n(Cu)=0.15∶1.00)时,其XRD图中主要显示Cu的特征衍射峰(43.29°、50.43°),但已能看到Pt的两个特征峰(39.76°、46.24°)略微凸起。继续增大Pt/Cu至0.25∶1.00和0.50∶1.00时,Cu的特征峰进一步弱化,而Pt的特征峰逐步增大。当Pt/Cu为0.75∶1.00和1.00∶1.00时,Cu的衍射峰已非常微弱,几乎难以辨识,而对应于Pt的4个衍射峰则已全部清晰地显现。也就是说,随着双金属组分物质的量之比的变化,分别代表着面心立方晶相Cu和Pt的衍射峰强度发生了此消彼长的变化。除此之外,未见其他不明物相的衍射峰出现,表明产物中不含杂质或其他物种。经过液相还原生成Cu晶粒,再与PtCl62-发生伽伐尼置换反应,所得到的双金属Pt/Cu产物并未形成新相,即没有生成新的化合物,其赋存状态仍是相互独立的单一金属Cu和Pt。
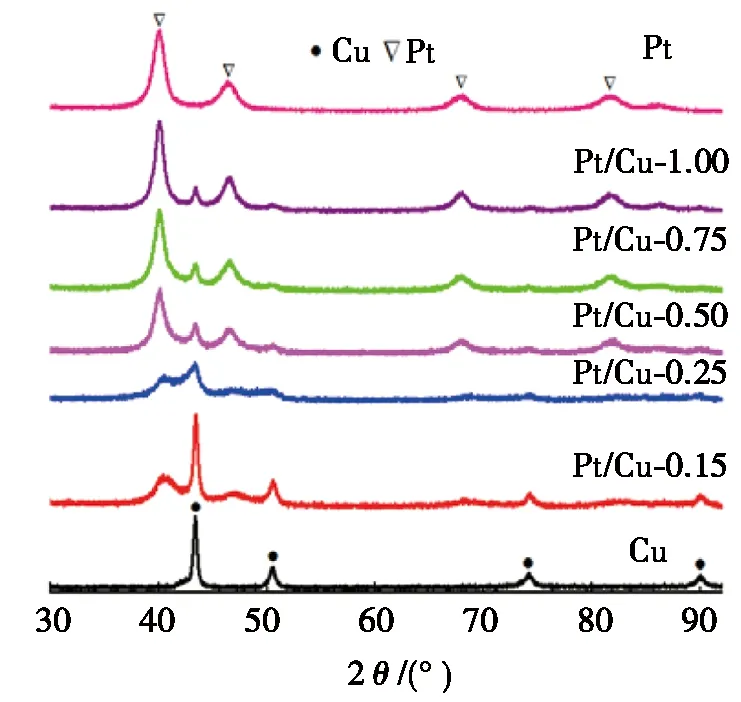
图1 不同Pt/Cu合金产物的XRD图谱
2.2 Pt/Cu双金属合金粒子的形貌分析
改变金属的物质的量配比,不但对双金属产物Pt/Cu的物相结构产生影响,而且还能使产物的形貌发生较大改变。图2为3种典型产物样品的TEM分析结果。金属Pt含量较低(n(Pt)∶n(Cu)=0.15∶1.00)时,所得产物Pt/Cu-0.15的形貌明显呈微球状,平均粒径约为48 nm,微球表面粗糙,由大量的次级微粒附着和集聚而成,结构比较紧凑致密,如图2a所示。而当n(Pt)∶n(Cu)=0.75∶1.00时,产物微球表面呈现约20 nm厚度的薄壳层(见图2b中红线标记),球心部位为中空结构,平均粒径基本保持不变,如图2b所示。单金属Pt呈现高分散的超微颗粒,粒径为5~10 nm,如图2c所示。

(a) n(Pt)∶n(Cu)=0.15∶1.00(b) n(Pt)∶n(Cu)=0.75∶1.00 (c) 单金属Pt
2.3 Pt/Cu双金属合金对AB水解释氢的催化性能

图3 不同Pt/Cu双金属合金和单金属催化水解氨硼烷的释氢曲线
把不同物质的量比的Pt/Cu双金属复合微纳米粉用作催化剂,在298 K温度下对AB水解释氢的催化活性进行了系统性评价,结果如图3所示。由图3可以看出:单质Cu纳米粒子的催化能力非常微弱,而单质Pt纳米粒子的催化能力较强,反应9.8 min即可达到最大释氢量(70.8 mL),即释氢完毕。除此之外,其余5个双金属合金催化剂的催化能力均超过单金属Cu纳米粒子。含Pt量较高的3个双金属催化剂(Pt/Cu-0.50、Pt/Cu-0.75和Pt/Cu-1.00)的催化能力明显高于单金属Pt纳米粒子,达到最大释氢量所需要的时间依次为8.5 min、7.0 min和8.0 min,也就是说Pt/Cu-0.75的催化能力最强,Pt/Cu-1.00次之。另外两个含Pt量较低的双金属合金(Pt/Cu-0.15、Pt/Cu-0.25)的催化能力均弱于单金属Pt纳米粒子,达到最高释氢体积所需要的水解时间分别为22.3 min和21.0 min。基于上述分析可知,这些Pt基合金催化剂催化能力的顺序为:Pt/Cu-0.75>Pt/Cu-1.00>Pt/Cu-0.50>单质Pt纳米粒子>Pt/Cu-0.25>Pt/Cu-0.15>单质Cu纳米粒子。通过试验数据计算[16]得知:催化能力最强的双金属合金Pt/Cu-0.75对AB水解释氢反应的转化频率(turnover frequency,TOF)为67.22 min-1。Pt/Cu双金属合金良好的催化活性主要归因于Cu和Pt之间的协同效应,同时独特的中空微结构可以提供更大的比表面积,生成更多更有效的活性位点,这些积极因素的正向协同可有效提升双金属合金的催化性能。
2.4 Pt/Cu双金属合金催化水解AB的动力学分析
按照化学动力学理论,温度对于化学反应速度具有重要影响,同时也会在很大程度上影响催化剂的性能。因此,以Pt/Cu-0.75作为催化剂,设定不同的温度(298 K、303 K、308 K、313 K和318 K),保持上述AB水解反应的其他条件(催化剂投加量、AB浓度和体积)不变,详细地考察了温度对AB催化释氢反应的影响,不同温度下Pt/Cu-0.75催化AB水解反应的动力学拟合曲线如图4所示。由图4a可以清楚地看到:温度对于释氢速率具有比较显著的正向促进作用,升高温度有助于提高释氢速率。借助试验数据可以计算得出:水解释氢反应至2 min时,在从低到高(298 K→318 K)的5个温度条件下,平均产氢速率依次为18.25 mL·min-1、22.65 mL·min-1、25.90 mL·min-1、29.80 mL·min-1和31.85 mL·min-1。显然,释氢速率随着温度的升高而快速递增,Pt/Cu-0.75的催化能力随着温度的提升而逐步得到强化,但不同温度对于改善释氢速率的幅度有一定差异。

(a) 释氢速率 (VH2-t) (b) 阿伦尼乌斯方程 (ln k-1/T)
文献[17]分析表明:该类水解反应属于准一级反应。根据不同温度下所获得的释氢反应速率,可以通过试差法求得各温度下的反应速率常数k。按照一级反应的动力学模型,基于阿伦尼乌斯方程(lnk=-Ea/RT+lnA)对试验数据进行关联,以lnk对水解反应温度的倒数(1/T)作图,可得到如图4b所示的线性关系,由直线的斜率可以获得反应的表观活化能Ea=35.75 kJ·mol-1。经与文献对比研究发现,该活化能低于已报道的其他Pt基双金属催化剂[18]。
3 结论
(1)试验所得的系列化Cu/Pt双金属合金微纳米粒子,对于储氢材料氨硼烷的水解释氢具有较高的催化活性。
(2)在室温条件下,Pt/Cu纳米粒子对氨硼烷水解的催化活性均高于Cu纳米粒子,其中Pt/Cu-0.75的催化活性显著高于Pt纳米粒子,其释氢反应的催化转化频率为67.22 min-1,表观活化能为35.75 kJ·mol-1。

