全腹腔镜全胃切除Uncut Roux-en-Y吻合与π形吻合的对比分析
陈洪义,张新生,张乾世,冯 震,闫恩俊,马浩日,孙志威,任双义
(大连医科大学附属第二医院 胃肠外科,辽宁 大连 116027)
胃癌(gastric carcinoma, GC)是最常见的消化系统恶性肿瘤之一,在我国胃癌的发病率及病死率均位于全部消化道恶性肿瘤的第2位[1]。1991年,Kitano等[2]完成了第1例腹腔镜胃癌手术治疗,自此胃癌手术进入腹腔镜时代。近年来,腹腔镜手术在成像技术,手术适应范围,腹腔镜下消化道重建方式等方面均取得了巨大的进步,基于腹腔镜手术微创、视野优化、患者术后痛苦小等优势,国内外众多医疗中心纷纷开始开展全腹腔镜下全胃切除手术(totally laparoscopic total gastrectomy, TLTG),但何种手术方式最佳却无法达成共识[3-4]。TLTG比较经典的两种吻合方式是借助管型吻合器行食管空肠端侧吻合和借助直线切割闭合器行食管空肠侧侧吻合。有研究指出,全腹腔镜下行管型吻合时置入抵钉座的难度较大,且部分病例有吻合口狭窄的可能,而应用直线切割闭合器行食管空肠侧侧吻合时,其吻合口直径大,吻合区域血运好,可以降低术后吻合口狭窄、吻合口漏的发生[5-6]。所以,本中心自2016年1月开始,在TLTG施行食管空肠侧侧吻合的基础上,尝试应用Uncut Roux-en-Y吻合与π形吻合两种不同的消化道重建方式,以期探究TLTG的安全性及可行性,对比两种吻合方式的围手术期指标及术后疗效。
1 资料与方法
1.1 一般资料
收集2016年1月至2019年6月大连医科大学附属第二医院胃肠外科施行TLTG的75例胃癌患者的病例资料。根据消化道重建方式的不同,分为Uncut RY组(39例,52%)和π形吻合组(36例,48%)。两组患者的年龄、性别、身高、体重、肿瘤位置等一般资料相比,差异均无统计学意义,P>0.05。见表1。
纳入标准:(1)所有患者术前均行电子胃镜检查,并经病理确诊为胃癌;(2)术前影像学检查提示无远处转移;(3)行3D全腹腔镜根治性全胃切除,无中转开腹;(4)手术由同一高年资医师团队施行。排除标准:(1)合并其他恶性肿瘤者;(2)有严重心肺肝肾功能不全不能耐受手术者;(3)既往有腹部大手术史;(4)急诊手术及(或)姑息性手术患者。

表1 两组患者一般临床资料比较
1.2 手术方法
两组患者均依据第4版《日本胃癌治疗指南》行根治性全胃切除和D2淋巴结清扫术[7]。消化道重建方式如下:(1)Uncut Roux-en-Y吻合:先行食管离断,标本游离,装入标本袋。牵拉食管下段,于食管右侧壁切开小孔,预置吻合口A;距Treitz韧带约25 cm提起空肠至食管下端,检查确保系膜无张力,于对系膜缘切开肠壁全层,长约0.5 cm,预置吻合口B;经A、B置入吻合器两臂(图1A),将食管下端与空肠行侧侧吻合,再闭合共同开口(图1B),完成食管-空肠吻合重建。而后提起输入、输出袢肠管,自食管-空肠吻合口至输出袢远端约45 cm将输入、输出袢行侧侧吻合,再闭合共同开口。距食管空肠吻合口约5 cm处闭合输入袢肠管(不离断)(见图1C)。(2)π形吻合:先用束带结扎阻断食管胃结合部,牵拉束带,自贲门上食管右侧壁切开小孔,预置吻合口A;距Treitz韧带约25 cm提起空肠至食管下段,检查确保系膜无张力,于对系膜缘切开肠壁全层,长约0.5 cm,预置吻合口B;经A、B置入吻合器两臂,将食管下端与空肠行侧侧吻合(图2A),于侧侧吻合口近端小肠系膜无血管区电勾钻孔(图2B),自此孔置入直线切割闭合器离断肠管,闭合食管空肠共同开口(图2C),完成食管-空肠吻合重建。标本游离,装入标本袋。而后提起输入、输出袢肠管,自食管-空肠吻合口至输出袢远端约45 cm将输入、输出袢行侧侧吻合,再闭合共同开口。
1.3 观察指标
(1)患者一般资料:年龄、性别、身高、体重、肿瘤位置。(2)围手术期指标:术后病理标本情况、手术时间、术中出血量、术后住院时间、总住院费用。(3)术后早期并发症:术后食管空肠吻合口漏、术后腹腔出血、术后肺炎和(或)胸腔积液、切口感染。
1.4 术后随访
对所有入组患者进行术后随访,随访方式采用电话随访及门诊登记随访,随访时间选取患者手术3个月以后。主要记录患者术后出现的临床症状、体征、术后并发症发生情况及术后相关辅助检查结果。根据患者手术3个月以后的随访情况,制定术后远期疗效观察指标:反流性食管炎、倾倒综合征、吻合口溃疡、Roux滞留综合征。
1.5 统计学方法
采用SPSS 24.0统计学软件对临床数据进行分析统计。计数资料以例数(百分比)表示,采用χ2检验或Fisher精确检验。计量资料先行正态分布与方差齐性检验,符合正态分布、方差齐性,以均数±标准差表示,采用t检验;不符合正态分布、方差齐性,以中位数及四分位间距表示M(P25,P75),采用秩和检验。P<0.05认为差异具有统计学意义。
2 结 果
两组患者均顺利完成全腹腔镜下全胃切除手术,无中转开腹,无二次手术,无围手术期死亡。
2.1 两组患者围手术期指标比较
两组患者的手术时间比较,Uncut RY组与π形吻合组患者的手术时间分别为(215.10±35.71)min和(191.58±36.43)min,术后首次进食时间分别为3(2,4)d 和4(3,6)d,差异具有统计学意义,P<0.05;患者肿瘤最大径、术后病理分化情况、术后病理TNM分期、术中出血量、术后住院时间、总住院费用,两组比较差异无统计学意义,P>0.05。见表2。
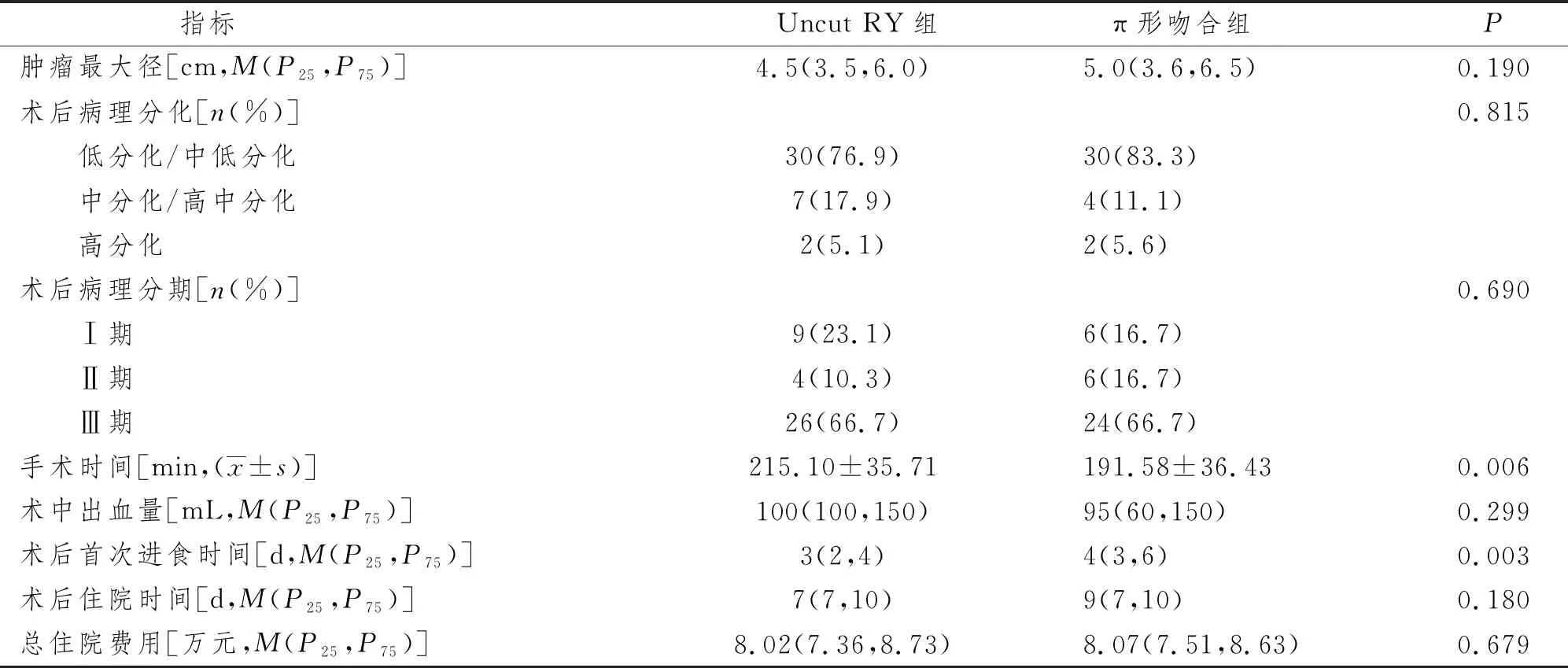
表2 两组患者围手术期指标比较
2.2 两组患者术后并发症比较
两组患者中,Uncut RY组Roux滞留综合征发生2例(5.1%),π形吻合组发生8例(22.2%),差异具有统计学意义(P<0.05)。术后食管空肠吻合口漏、腹腔出血、术后肺炎或胸腔积液、切口感染、反流性食管炎、倾倒综合征、吻合口溃疡发生情况两组无明显差异,P>0.05。见表3。
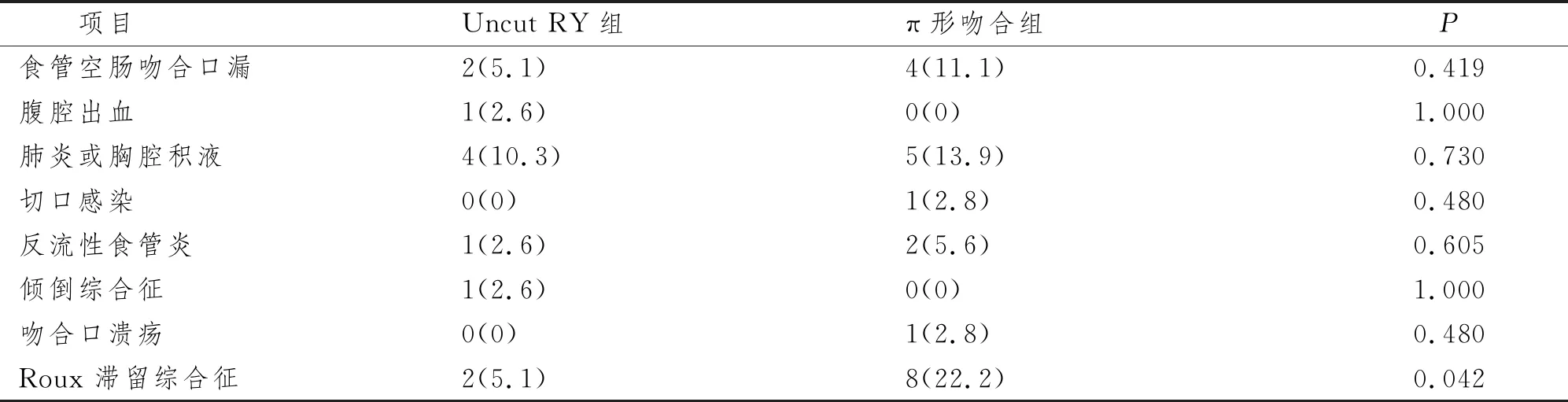
表3 两组患者术后并发症比较
3 讨 论
全腹腔镜根治性全胃切除是指在全腹腔镜下完成胃癌手术的淋巴结清扫、全胃切除,和食管空肠消化道吻合重建,而食管空肠吻合重建是手术的重点及难点。本研究中,两组患者均在全腹腔镜下完成淋巴结清扫及消化道重建,术中无中转开腹,无围手术期死亡。入组患者术后病理标本远近断端切缘无癌组织残留,淋巴结清扫均达到根治要求。75例患者中,Uncut RY组平均手术时间为(215.10±35.71)min,术中出血量为100(100,150)mL;π形吻合组的平均手术时间为(191.58±36.43)min,术中出血量为95(60,150)mL;均优于国内腹腔镜辅助全胃切除手术中关于手术时间及术中出血量的报道[8-9]。3D腹腔镜系统在微创手术的基础上,定位更准确,视野更清晰,对胃周血管及解剖层次的显现更加精准立体,可以提高术者的实际操作能力,减少手术时间,降低术中出血量[10]。术中消化道重建在全腹腔镜下进行,节省了小切口辅助开腹时间及吻合时寻找判断肠管方向的时间。两组患者的手术时间相比,差异具有统计学意义(P<0.05),分析原因如下:π形吻合在行消化道重建过程中,先不做食管离断,在束带牵拉食管的作用下,将食管下端与空肠行侧侧吻合,在行共同开口闭合时,可以一并离断食管和空肠,达到三合一的吻合目的[11],很大程度上降低了手术操作难度,节省手术时间。但此种吻合方式有一缺陷,在消化道重建之前检查近端切缘困难,一旦切缘阳性,弥补过程费时费力。Uncut Roux-en-Y吻合在行消化道重建时,先行食管离断,在近端切缘距肿瘤距离的判断上优于π形吻合,但由于食管离断后容易回缩,全腹腔镜下食管空肠侧侧吻合的操作难度增加。在食管空肠侧侧吻合后,完成共同开口的闭合过程中,为了避免闭合器误夹过多空肠破坏肠管连续性,防止闭合器闭合过多吻合口后壁空肠系膜影响吻合血运,需要精准调整并反复观察直线切割闭合器的角度,对术者及助手的配合要求高,吻合难度要高于π形吻合,所以手术时间花费相对较长。
全胃切除术后,食管空肠吻合口漏是较为严重的并发症之一,国内外均缺乏对TLTG食管空肠吻合口漏多中心大样本量的报道。2018年,日本Oshi等[12]收集了131例行腹腔镜辅助胃癌全胃切除患者的临床资料,对其食管空肠吻合口漏的危险因素进行分析,此项研究中,食管空肠吻合口漏的发生率为9.9%。本中心参阅Clavien-Dindo系统[13]吻合口漏的分级标准,对吻合口漏的诊断制定严格评级,本研究中,经临床表现及影像学检查证实的术后食管空肠吻合口漏共发生6例(8%),低于日本学者腹腔镜辅助胃癌全胃切除术后吻合口漏的报道,以上6例患者经保守治疗后好转。
两组患者均行Roux-en-Y消化道重建,此重建方式可以有效降低十二指肠残端压力,预防反流性食管炎、倾倒综合征等并发症的发生[14-15],但一部分患者会出现Roux滞留综合征(Roux stay syndrome, RSS)。RSS是指患者手术3个月以后,排除梗阻、吻合口狭窄等机械性原因出现的进食后上腹部疼痛、腹胀、恶心呕吐等症状反复发生的情况。国外关于RSS发病率的报道为11.6%~30%[16-17],但全腹腔镜全胃切除术后RSS的发生报道较少。本研究结果显示:75例患者中,Uncut RY组RSS发生2例(5.1%),π形吻合组发生8例(22.2%),差异具有统计学意义(P<0.05)。RSS的发生原因考虑和迷走神经离断及十二指肠存在优势电位的控制有关[18],正常小肠受自身慢波节律的控制,在十二指肠部位存在优势电位,能保证小肠自近端到远端的正常节律性运动。π形吻合在行消化道重建时需要离断空肠,破坏肠管的连续性,即电位节律的连续性也相应受到破坏。Roux肠袢及远端小肠脱离了十二指肠优势电位的控制,仅依靠远端肠管的节段性慢波节律,因此远端小肠出现脱离十二指肠优势电位后慢波电位引起的蠕动减弱或逆蠕动,从而导致RSS的发生。Uncut Roux-en-Y吻合仅闭合输入袢肠管,不做离断,一定程度上保证了小肠的连续性,故其RSS的发生率相对π形吻合低。两组患者首次进食时间差异具有统计学意义(P<0.05),同样考虑与肠管连续性及电位节律的连续性破坏有关。全胃切除的患者,因无胃的储备功能,进食后很难即刻适应无胃状态,多表现为腹胀,大部分患者活动后可自行缓解。在饮食调整上,本研究遵照加速康复外科(enhanced recovery after surgery,ERAS)[19]的指导,遵循先进水后进流食,少食多餐,逐日递增,肠内肠外联合营养的方式进行调整,对于术后第2天的全胃切除患者开始试进水,耐受者可进全流质饮食,无法耐受者推迟进食时间,患者会慢慢适应这种状态。因小肠连续性被完全破坏,π形吻合小肠蠕动减弱或逆蠕动强于Uncut Roux-en-Y吻合,会引起患者饮水后上腹部不适,其进水后的适应过程较Uncut Roux-en-Y吻合用时较长,所以术后首次进食时间也较晚。
目前,腹腔镜手术的开展已经使腹部手术的切口越来越小;镇痛方式的多种选择降低了患者术后疼痛带来的痛苦;加速康复外科指导下的术前肠道准备、术中麻醉诱导、围手术期饮食管理等减轻了患者的主观不适,但由于消化道重建引起的并发症及不适,却往往难以解决。在全腹腔镜全胃切除发展的近几年,对于消化道重建方式的探索层出不穷,π形吻合因其吻合方式简单,学习曲线相对较短等优势被各大中心尝试与推广。在追求手术速度,手术质量的同时,了解术后患者的主观不适也尤为重要,Uncut Roux-en-Y吻合在全腹腔镜下的开展很好地弥补了这一点。本研究结果可协助手术医师在进行TLTG选择手术方式时提供依据,但本研究是单中心研究,患者入组数量有限,在入组过程中剔除了残胃癌以及患有严重内科合并症的患者,今后仍需大样本量多中心的前瞻性研究分析。
综上所述,TLTG应用Uncut Roux-en-Y吻合与π形吻合均安全可行。两者相比,应用π形吻合手术时间更短,应用Uncut Roux-en-Y吻合进食更早,RSS发生率更低。

