利用离子掺杂固相法煅烧立方晶型硫铝酸钙
宋 飞, 吕忆农, 殷 悦, 刘文娟, 彭美勋
(1.湖南科技大学 材料科学与工程学院, 湖南 湘潭 411100;2.湖南科技大学 新能源储存与转换先进材料湖南省重点实验室, 湖南 湘潭 411100;3.南京工业大学 材料科学与工程学院, 江苏 南京 210009)
硫铝酸盐水泥(CSA)具有早强、高强、低碱度等一系列优点,这主要源于其中的高活性矿物—无水硫铝酸钙(C4A3$)[1-3].相对于普通硅酸盐水泥而言,C4A3$具有烧成温度低、钙含量低、更易粉磨的优点,特别是在其生产和水化过程中可充分利用各种工业废渣和混合材[4-6].
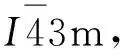
C4A3$结构中存在多元环骨架及巨大的“β笼”空腔,可允许较大程度的离子取代或扭转[14].例如C4A3$中的Ca(占据孔道中位置)可被Na、K、Sr、Ba等取代,Al(占据四面体位置)可被Fe、Si、B等取代,SO4(占据“β笼”中心)则可被Cl、CrO4、WO4等取代[11,15-16].理论分析表明,借助离子掺杂可支撑C4A3$骨架结构,使其处于非坍缩状态,从而可在室温下获得C4A3$立方结构[12].最近,Liu等[17]利用Ga3+取代Al3+制备C4A3$固溶体,当Ga3+取代量达到14%(摩尔分数)时,立方结构C4A3$可在室温下稳定存在.在含C4A3$水泥工业生产过程中,原料引入的微量元素可能导致C4A3$的微结构发生改变.宋飞等[18]通过透射电子显微镜(TEM)发现贝利特-硫铝酸盐水泥(BCSA)中C4A3$存在超结构,并同时以立方和正交晶型存在.部分研究者利用Na+、B3+、Fe3+等离子的掺杂,促使较多C4A3$在室温下以立方结构存在,但详细的变化规律尚不明晰[16,19].
材料性能主要取决于其微结构,离子掺杂可改变C4A3$晶体结构及形貌特征等,进而影响C4A3$的水化历程及浆体结构.本文通过掺杂适量水泥原料中常见的Na+、Fe3+、Si4+,基于固相法制备c-C4A3$,以明晰常见离子对C4A3$晶型结构、含量、微观形貌的影响规律,探讨晶型结构转变的作用机制.相关研究有利于探索具有不同微结构特征的C4A3$水化性能,并为含C4A3$水泥的开发和应用提供科学依据.
1 试验
1.1 样品制备
试验采用分析纯碳酸钙、二水硫酸钙、氧化铝、碳酸钠、氧化铁及二氧化硅试剂,通过固相法制备Na+、Fe3+、Si4+掺杂的C4A3$,且为保持电价平衡,掺杂化学计量比相同的Na+、Si4+.相应的Ca4-xNaxAl6-x-yFeySixO12SO4名义化学计量比(x=0.1、0.2、0.3、0.4;y=0.1、0.2、0.3)如表1所示.按表1比例称取各粉体原料共40g,于研钵中充分混合均匀,并全部通过0.075mm方孔筛.粒度合格的粉体在400kN压力下制得直径5cm、厚5mm的试块.参考文献[19]中的煅烧制度,将试块置于1250℃ 高温炉中煅烧4h后,冷却至室温.将获得的样品破碎后,选取0.5mm颗粒用于电镜分析;再粉磨通过0.075mm方孔筛,供X射线衍射测试.
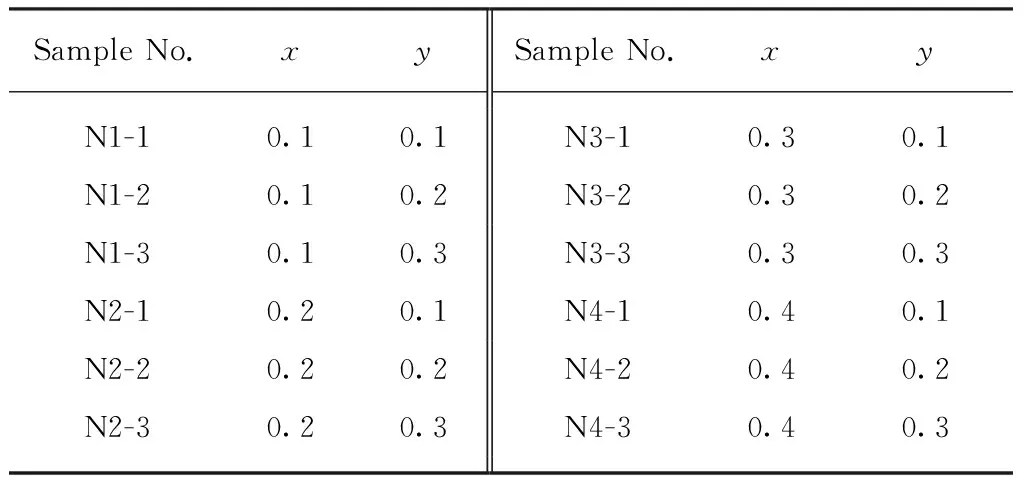
表1 Ca4-xNaxAl6-x-yFeySixO12SO4名义化学计量比
1.2 表征方法
采用布鲁克公司的D8 ADVANCE型X射线衍射仪(XRD)表征样品物相结构.使用Cu靶Kα线作为X线源,θ/θ扫描方式,管电压为40kV,管电流为40mA.此外还利用日本理学公司的Smart Lab-9kW型X射线衍射仪进行Rietveld精修定量分析.以Cu靶Kα1线作为X线源,θ/θ扫描方式,管电压为45kV,管电流为200mA.衍射仪扫描步长为0.02°,扫描范围为5°~45°,扫描速率为5(°)/min.
采用日本电子公司JSM-6380型扫描电镜(SEM)观察样品形貌和尺寸大小,加速电压为20kV,辅以牛津NCA350型能谱仪(EDS)对其进行化学组成分析.产物微结构在日本电子公司JEM-2100F UHR型透射电子显微镜(TEM)上进行分析测试,加速电压200kV,球差系数0.5mm,同时借助美国热电公司NS7型能谱仪分析产物化学组成.
运用JADE软件的检索功能,选择与衍射图谱最为接近的PDF/ICSD卡片用于Rietveld精修定量分析.利用GSAS软件进行精修,主要拟合参数包括标度因子、背底函数、晶胞参数、样品偏移、样品吸收、峰形函数、半高宽函数及不对称函数等[20].
2 结果分析与讨论
2.1 物相结构分析
首先对Na+掺杂量x=0.1(掺杂等量Si4+)的N1系列样品进行XRD物相结构分析(见图1(a)),发现Fe3+掺杂量在一定范围内变化(y=0.1~0.3)时,合成的物相主要组成为C4A3$及少量铝酸一钙(CA)和铁铝酸四钙(C4AF).少量铁铝酸盐形成原因可能为:(1)原料中二水石膏高温分解,导致S含量不足,进而生成副产物;(2)原料混合不够均匀,局部存在偏析;(3)少量碱金属在高温下形成液相,促进了铁铝酸盐的形成.进一步对衍射图谱局部进行观察(见图1(b)),可以看出属于o-C4A3$的18°左右衍射峰峰强较高,即C4A3$主要以正交晶型存在,故少量的掺杂离子无法稳定c-C4A3$.此外,当Fe3+掺杂量y=0.2时,12°左右出现鼓包,说明此时结晶度不高的C4AF含量增多.
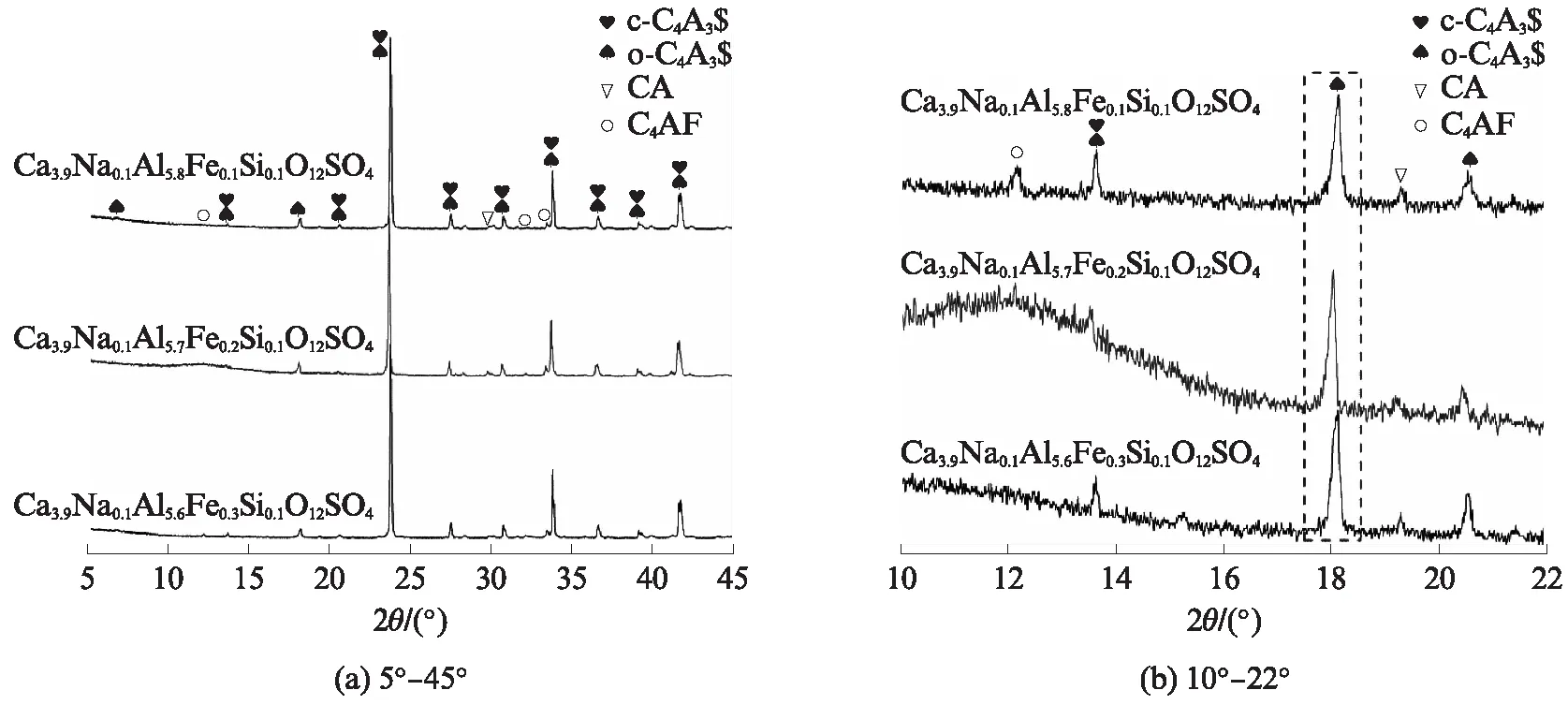
图1 N1系列样品的XRD谱Fig.1 XRD patterns of N1series sample
Na+掺杂量x=0.2(掺杂等量Si4+)时,N2系列样品的XRD图谱如图2(a)所示.可以看出,其物相组成同样为C4A3$及少量CA、C4AF.观察局部衍射图谱(见图2(b))发现:当Fe3+掺杂量y=0.1时,N2-1中C4A3$主要以正交晶型存在;当Fe3+掺杂量增至0.2或0.3时,o-C4A3$的18°左右衍射峰强度显著降低,说明N2-2、N2-3中C4A3$大部分以立方晶型存在.因此,当Na+掺杂量x=0.2、复掺等量Si4+及适量Fe3+(y=0.2、0.3)时,可稳定c-C4A3$,使其能够在室温下大量存在.

图2 N2系列样品的XRD谱Fig.2 XRD patterns of N2series sample
Na+掺杂量增至x=0.3(掺杂等量Si4+)时的N3系列样品XRD图谱如图3(a)所示.可以发现,合成的样品物相组成依然为C4A3$及少量CA、C4AF.从局部衍射图谱(见图3(b))可以看出,Fe3+掺杂量y=0.1~0.3时,o-C4A3$的18°左右衍射峰强度始终较弱,即N3系列样品中C4A3$均主要以立方晶型存在.此结果说明Na+掺杂量x=0.3、复掺等量Si4+时,较大范围内的Fe3+含量波动(y=0.1~0.3)均可稳定c-C4A3$.
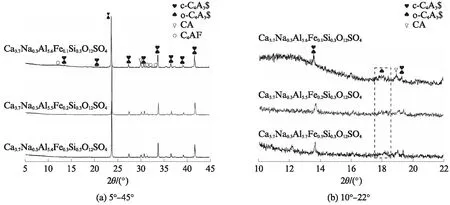
图3 N3系列样品的XRD谱Fig.3 XRD patterns of N3 series sample
进一步将Na+掺杂量提升至x=0.4(掺杂等量Si4+),获得的N4系列样品XRD图谱见图4(a).由图4(a)可见,尽管N4系列样品的主要物相仍然为C4A3$,但其中的少量矿物发生了明显变化.各样品中均未出现CA,并且Fe3+掺杂量较低的N4-1中几乎无C4AF形成,而Fe3+掺杂量较多的N4-2、N4-3中存在一定量C4AF.由于N4系列样品中Na+含量较高,故复掺的等量Si4+浓度也相应升高,然而C4A3$体系无法容纳较多的Si4+,导致样品中出现了β型硅酸二钙(β-C2S).同时,额外Ca2+的消耗促使富余的S元素形成了游离硬石膏(C$).N4系列样品的局部衍射图谱如图4(b)所示,显然,其中的C4A3$主要以正交晶型存在.因此,Na+掺杂量较高时,不仅无法稳定c-C4A3$,而且较多的掺杂离子会生成其他物相.
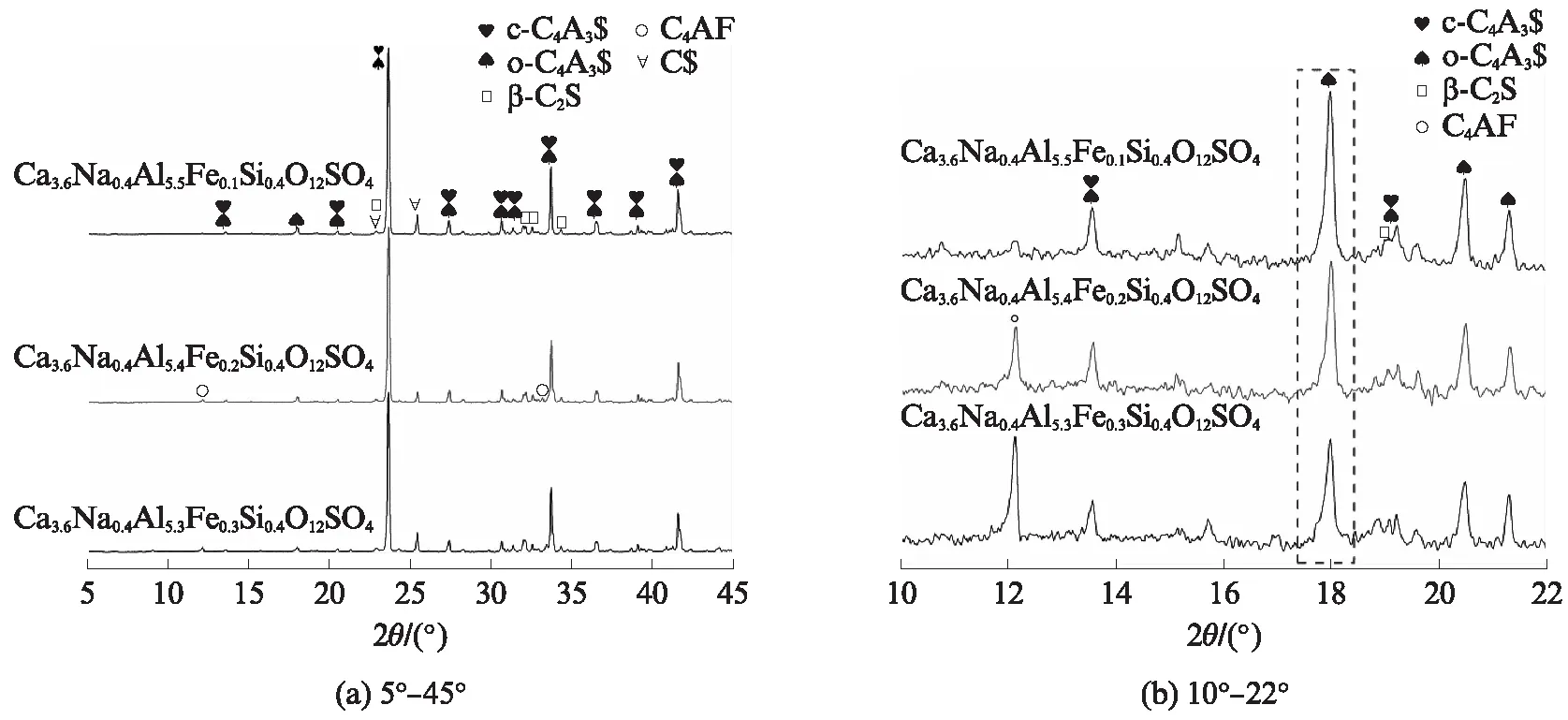
图4 N4系列样品的XRD谱Fig.4 XRD patterns of N4 series sample
综上所述,Na+掺杂量对c-C4A3$的形成和稳定具有重要影响,当Na+掺杂量过低或过高时,无法稳定C4A3$立方结构,甚至会形成较多副产物.仅当适量Na+取代Ca2+、Si4+或Fe3+占据Al3+位置时,方可在室温下稳定c-C4A3$的骨架结构.
2.2 Rietveld精修分析
为掌握主要组成为立方结构的Ca4-xNaxAl6-x-yFeySixO12SO4系列样品中晶胞参数及物相含量变化,进行了Rietveld精修分析.图5显示了N2-2样品Rietveld精修拟合图谱(剩余方差因子Rwp=6.99%),可以看出图谱拟合较好,差值曲线(Differential line)平滑,分析结果可信度高.分别对各样品(N2-2、N2-3、N3-1、N3-2、N3-3)进行精修拟合(Rwp均小于10%),所获得的立方结构C4A3$ 晶胞参数如表2所示.可以看出,离子掺杂后的C4A3$晶格尺寸均略小于纯相C4A3$的晶格尺寸(a=0.9205nm),结合C4A3$ 所属方钠石结构特征,说明离子半径较小的Na+和Si4+分别占据了C4A3$ 晶格中Ca2+和Al3+的位置,支撑了其多元环骨架结构,促使立方结构C4A3$在室温下稳定存在[21].这与前文分析得出的Na+掺杂量(复掺等量Si4+)对c-C4A3$ 形成和稳定具有重要影响的结论一致.

图5 N2-2样品的Rietveld拟合谱Fig.5 Refinement pattern of sample N2-2

表2 立方结构Ca4-xNaxAl6-x-yFeySixO12SO4的晶胞参数a
各样品Rietveld精修定量分析结果如表3所示,其中c-C4A3$含量均大于60%(质量分数,下同),o-C4A3$含量均低于8%.N3系列样品中的铁铝酸盐含量高于N2-2、N2-3中的铁铝酸盐含量,说明Na+掺杂量的增加可能形成较多液相,有利于铁铝酸盐的形成.通过Rietveld精修分析证实Na+、Si4+、Fe3+的掺杂可稳定c-C4A3$晶格,且产物中c-C4A3$ 含量最高可达80%以上,为C4A3$晶型结构调控提供了新思路.

表3 Ca4-xNaxAl6-x-yFeySixO12SO4的定量结果
2.3 微观形貌分析
为了解主要组成为立方结构的Ca4-xNaxAl6-x-yFeySixO12SO4系列样品中产物微观形貌,对N2-2、N2-3、N3-1、N3-2、N3-3进行二次电子像分析,如图6所示.由图6(a)可见:当Na+掺杂量x=0.2(掺杂等量Si4+)、Fe3+掺杂量y=0.2时,产物结构疏松多孔,颗粒呈现不规则的多角形,晶界较为明显,粒径1~3μm,此结果与C4A3$单矿物形貌较为类似[22].进一步对颗粒上P1点进行EDS分析(见图6(f)),可以发现其主要元素组成为Al、S、O、Ca及少量Na、Fe、Si,并且主要元素或次要元素的比例基本接近Ca3.8Na0.2Al5.6Fe0.2Si0.2O12SO4的化学计量比.说明C4A3$通过固溶少量Na+、Fe3+、Si4+,其晶格尺寸发生了变化,并可在室温下稳定c-C4A3$.当Fe3+掺杂量升至y=0.3时,颗粒整体尺寸减小,同时结构中孔洞体积降低,如图6(b)所示.
当Na+掺杂量增至x=0.3(掺杂等量Si4+)、Fe3+掺杂量y=0.1时,产物微观形貌发生了明显变化,N3-1结构相对致密,颗粒棱角消失,呈现近球形形貌特征,粒径1μm左右(见图6(c)).近球形颗粒间晶界较为模糊,表面可能有高温熔融相存在,此结果与Rietveld定量分析得出铁铝酸盐含量较多的结论吻合.当Fe3+掺杂量y=0.2或y=0.3时,N3-2、N3-3微观形貌整体无明显变化,依然呈现近球形特征,仅尺寸略有增大,如图6(d)、(e)所示.产物微观形貌的变化可能源于碱金属在高温下形成了相对较多的液相,从而影响了晶体的生长和发育.因此,C4A3$ 中掺杂的Na+不仅可占据晶体结构中Ca2+的位置,而且能够改变C4A3$的生长环境,有利于球状c-C4A3$的形成.
2.4 微结构分析


图6 Ca4-xNaxAl6-x-yFeySixO12SO4的二次电子像Fig.6 Secondary electronimages of Ca4-xNaxAl6-x-yFeySixO12SO4
3 结论
(1)通过掺杂适量Na+、Fe3+、Si4+进入C4A3$晶格,占据Ca2+和Al3+位置时,可在室温下稳定具有超结构的立方晶型C4A3$(伪立方),其含量最高可达80%以上.其中掺杂的Na+不仅占据C4A3$晶格中Ca2+的位置,还可改变C4A3$的生长环境,促进球状c-C4A3$的形成.
(2)Na+掺杂量x=0.2、复掺适量Si4+和Fe3+时,固相法合成的C4A3$主要以立方晶型存在,呈现多角形微观形貌.升高Na+掺杂量至x=0.3(复掺等量Si4+)时,较大范围内的Fe3+掺杂量波动(y=0.1~0.3)均可稳定c-C4A3$,并呈现近球形形貌特征.当Na+掺杂量较低或较高时(x=0.1或x=0.4)时,不仅无法稳定c-C4A3$,还会形成较多副产物.
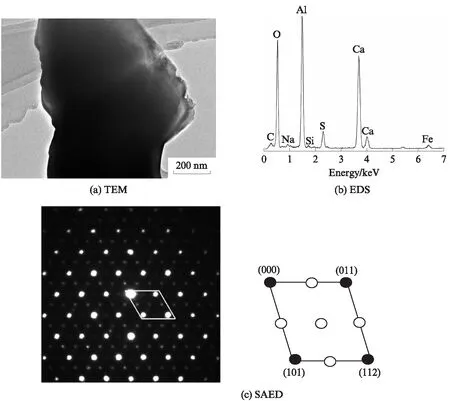
图7 N2-2样品的TEM分析Fig.7 TEM analysis of sample N2-2

