聚L-谷氨酸/石墨烯修饰电极测定对苯二酚
耿 明,朱庆仁,汝冬冬,董 笑①
(淮北师范大学 信息学院,安徽 淮北235000)
0 引言
对苯二酚(HQ)为有毒的白色针状结晶,易溶于热水、酒精和乙醚等物质,化学性质不活泼. 对苯二酚广泛应用于生活领域及化工领域[1],如染发剂、洗涤剂等. 由于对苯二酚具有很强的毒副作用[2],过量使用易造成头晕、耳鸣等症状,且该物质难降解而不易除去,严重破坏环境[3],因此,对对苯二酚进行测定是很有必要的. 目前,对苯二酚的研究检测方法主要包括分光光度法[4]、高效液相色谱法[5]、电化学法[6]、化学发光法[7]和荧光法[8]等. 由于电化学方法灵敏度高,操作简单且成本低[9]而备受人们的关注. 目前,研究人员对对苯二酚在修饰电极上的电化学行为已进行一些研究[10-12]. 近些年来,石墨烯[13-15]因其良好的导电性能及电催化效果被用于修饰电极的制备来测定对苯二酚. 因此,本文通过电化学方法制备聚L-谷氨酸/石墨烯修饰电极,并用该修饰电极测定对苯二酚,结果令人满意.
1 实验部分
1.1 仪器与试剂
仪器:KQ-250B型超声波清洗器(昆山超声波仪器有限公司);pHS-3C型酸度计(上海康仪仪器有限公司);LK2006A电化学工作站(天津市兰力科化学电子高技术有限公司);电化学实验采用三电极系统:玻碳电极为工作电极,铂丝为对电极,Ag/AgCl电极为参比电极.
试剂:5.00×10-4mol·L-1对苯二酚溶液;氧化石墨烯分散液;2.50×10-3mol·L-1L-谷氨酸溶液;磷酸盐缓冲液(PBS):pH 0.5~7.0,用0.1 mol·L-1H3PO4、NaH2PO4、Na2HPO4、Na3PO4溶液按常规方法配制并通过酸度计校准.
1.2 聚L-谷氨酸/石墨烯修饰电极的制备
用添加少量Al2O3粉末并滴加适量蒸馏水的抛光纸对玻碳电极下表面(Ф=3.0 mm)进行打磨抛光至镜面,超声波清洗仪对其污垢进行清洗,晾干待用. 将晾干后的玻碳电极作为工作电极,铂丝电极作为辅助电极,Ag/AgCl电极作为参比电极,放进10 mL氧化石墨烯及L-谷氨酸混合液中,通过循环伏安法进行扫描,从而制得聚L-谷氨酸/石墨烯修饰电极(PLG-ERGO/GCE). 将其取出用蒸馏水冲洗,再用滤纸轻轻擦干表面蒸馏水,等待备用.
1.3 实验方法
用移液管移取2.0 mL 5.00×10-4mol·L-1对苯二酚溶液、2.0 mL PBS(pH值为2.0)、蒸馏水定容10 mL于电解池中,将铂丝电极作为辅助电极,石墨烯谷氨酸修饰过的玻碳电极作为工作电极,Ag/AgCl电极作为参比电极的三电极系统放入电解池中,静置100 s,在初始电位为0.0 V,终止电位为0.6 V的条件下,对对苯二酚的电化学行为进行探究,记录并保存每次循环伏安曲线上的数据. 扫描结束后,用蒸馏水冲洗电极,晾干,再进行下一次的操作.
2 结果与讨论
2.1 聚L-谷氨酸/石墨烯修饰电极的最佳制备条件
采用单一控制变量法,利用循环伏安法,对混合均匀的氧化石墨烯及L-谷氨酸溶液进行扫描,每次仅改变一个条件,最终结果表明,当参数设定电位范围在-1.8~2.2 V,扫描速度为0.12 V·s-1,循环次数为11次,等待时间为7 s时,制备的聚L-谷氨酸/石墨烯修饰电极测定对苯二酚的效果最佳,得到的电化学信号最强.
2.2 电化学阻抗图谱分析
利用电化学阻抗技术(EIS)通过不同修饰电极,对K3[Fe(CN)6]以及KCl溶液进行测定表征,表征图谱如图1. 由图1可明显看出,在3-谷氨酸修饰电极上,会有一个比2-石墨烯修饰电极以及1-聚L-谷氨酸/石墨烯修饰电极稍大的圆弧,而圆弧越大,表明电极的电阻率越大,电子传递速率越低. 因此,从图1中可知,聚L-谷氨酸/石墨烯修饰电极的电阻率最小,电子传递速率最佳,这与文献[16]描述一致.
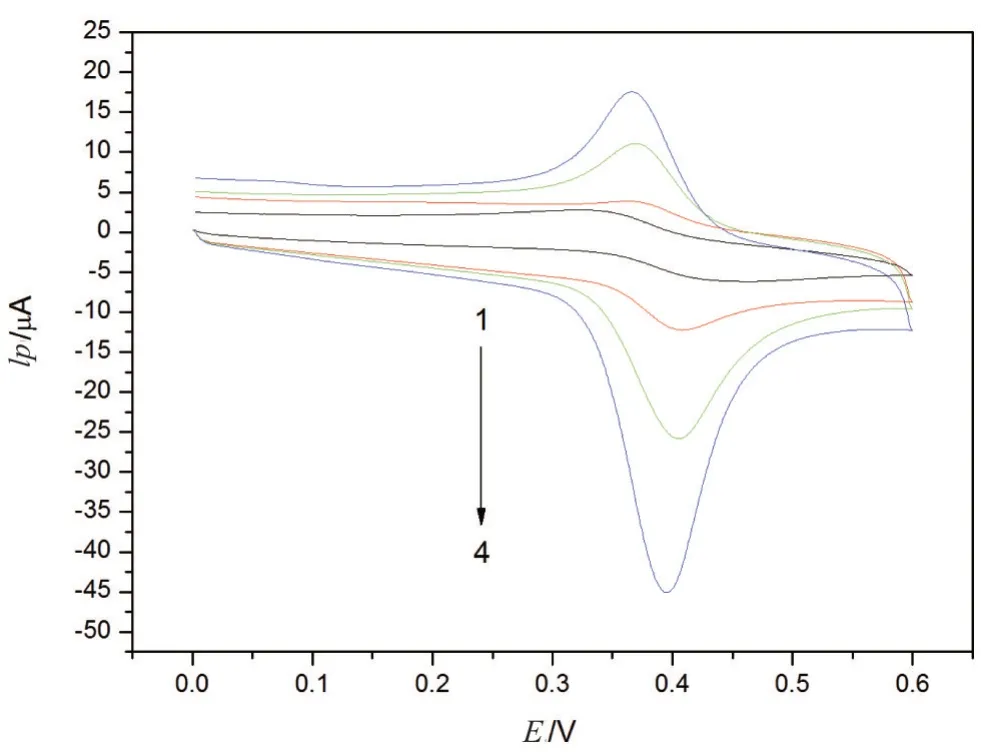
图2 对苯二酚在不同电极循环伏安特性曲线
2.3 对苯二酚在修饰电极上的电化学行为
2.3.1 对苯二酚的循环伏安曲线
用循环伏安法研究测定对苯二酚,图2 为初始电位0.0 V,终止电位0.6 V 条件下,在pH 值为1.0 的PBS中的1.00×10-4mol·L-1的对苯二酚分别在1-裸电极(GCE)、2-谷氨酸修饰电极、3-石墨烯修饰电极以及4-聚L-谷氨酸/石墨烯修饰电极上的循环伏安曲线图. 由图2可知,在GCE上,对苯二酚有一较低峰,而在聚L-谷氨酸/石墨烯修饰电极上峰电流比在其他3种电极上明显增加. 因此,表明聚L-谷氨酸/石墨烯修饰电极具备良好的导电性能,以及对对苯二酚的催化作用.
2.3.2 不同酸度条件对对苯二酚测定的影响
只改变底液酸度,采用循环伏安法来探究不同pH 值对1.00×10-4mol·L-1对苯二酚测定的影响. 如图3,由实验结果得知,在pH值为0.5~7.0的酸度区域内,随着酸度的增加,聚L-谷氨酸/石墨烯修饰电极对对苯二酚测定的氧化还原峰电流先降低后增加,对苯二酚在pH值为1.0的磷酸盐介质内中,测定所得到氧化还原峰电流最大且峰形最佳. 因此选择的底液最佳酸度为pH值为1.0. 且峰电位随之向右发生位移,其氧化还原峰电位和底液酸度成线性关系,ɑ氧为氧化峰电位:E=0.518 4-0.055 62 pH,r=0.991 6;b还为还原峰电位:E=0.414 4-0.584 0 pH,r=0.994 1. 说明对苯二酚有质子参与反应.
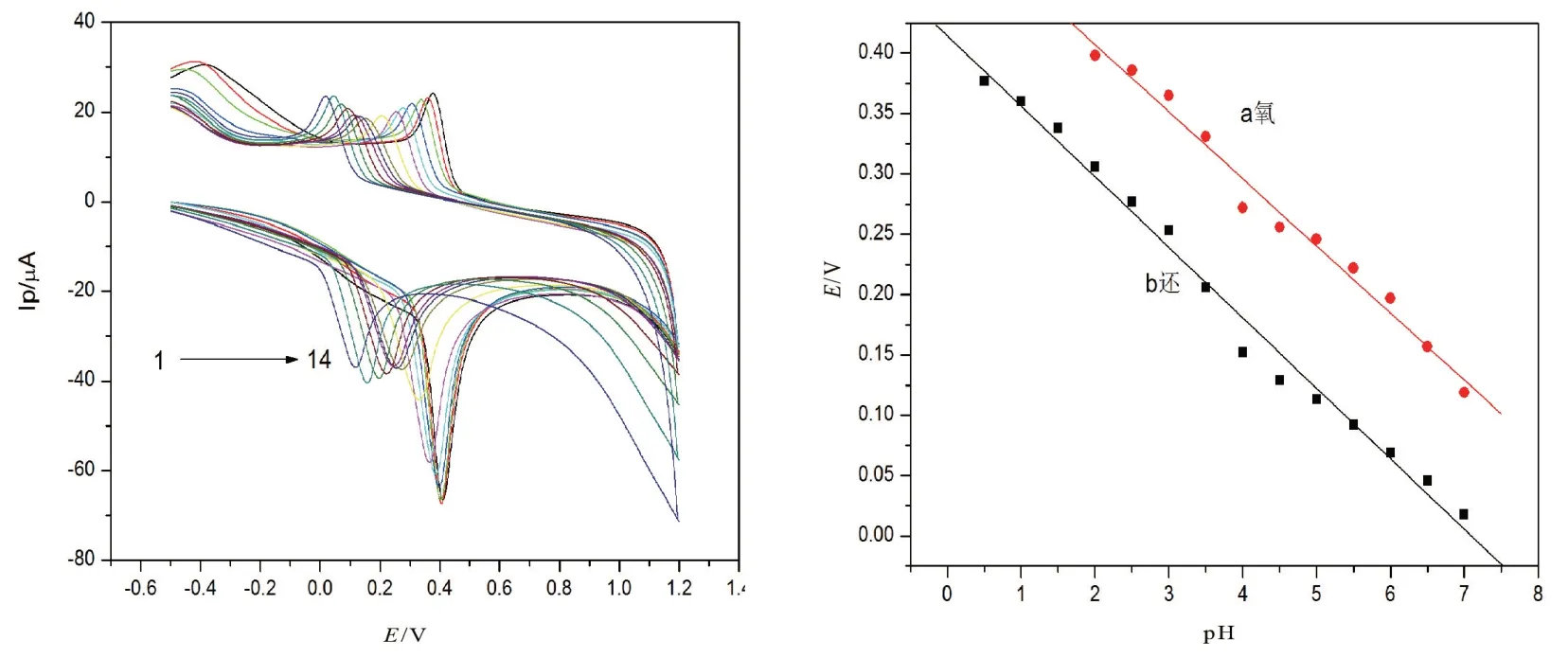
图3 对苯二酚在不同底液酸度下的循环伏安叠加图及E与pH值的关系曲线
2.3.3 不同扫描速度对对苯二酚测定的影响
图4显示其他参数条件不变,探究扫速的改变对1.00×10-4mol·L-1对苯二酚的电化学行为的影响. 在扫速为0.02~0.40 V·s-1范围内,随着扫速的增加,氧化还原峰电流也随之不断增大,然而峰形和可逆效果却随着扫速的变大而变差. 综合两者进行考虑,本实验选用的最佳扫描速度为0.12 V·s-1. 在0.02~0.40 V·s-1扫速范围内,对苯二酚的氧化还原峰电流均与扫速呈对数线性关系,其氧化峰回归方程为:lgIp=2.041 7+0.584 7 lgν,r=0.999 1;还原峰对应的回归方程为lgIp=1.714 4+0.547 1 lgν,R=0.990 5,二者所对应的斜率值均接近0.5,因此,对苯二酚的电化学反应过程中主要受扩散控制.

图4 不同扫速叠加图及扫速对数和峰电流对数的线性关系
2.3.4 扩散系数的研究
扫速研究表明,对苯二酚主要在电极上受到扩散控制. 因此,将采用计时电流法研究不同电极对于对苯二酚的扩散系数的影响. 图5为2.50×10-3mol·L-1的对苯二酚在玻碳电极、谷氨酸修饰电极、石墨烯修饰电极以及聚L-谷氨酸/石墨烯修饰电极上的计时电流曲线. 表1为根据Cottrell相关方程计算所得各个电极上的扩散系数. 由图5及表1可知,对苯二酚在聚L-谷氨酸/石墨烯修饰电极上的扩散系数最大,这也足以说明,聚L-谷氨酸/石墨烯修饰电极对于对苯二酚测定的电催化活性最强.

表1 对苯二酚在4种电极上的扩散系数
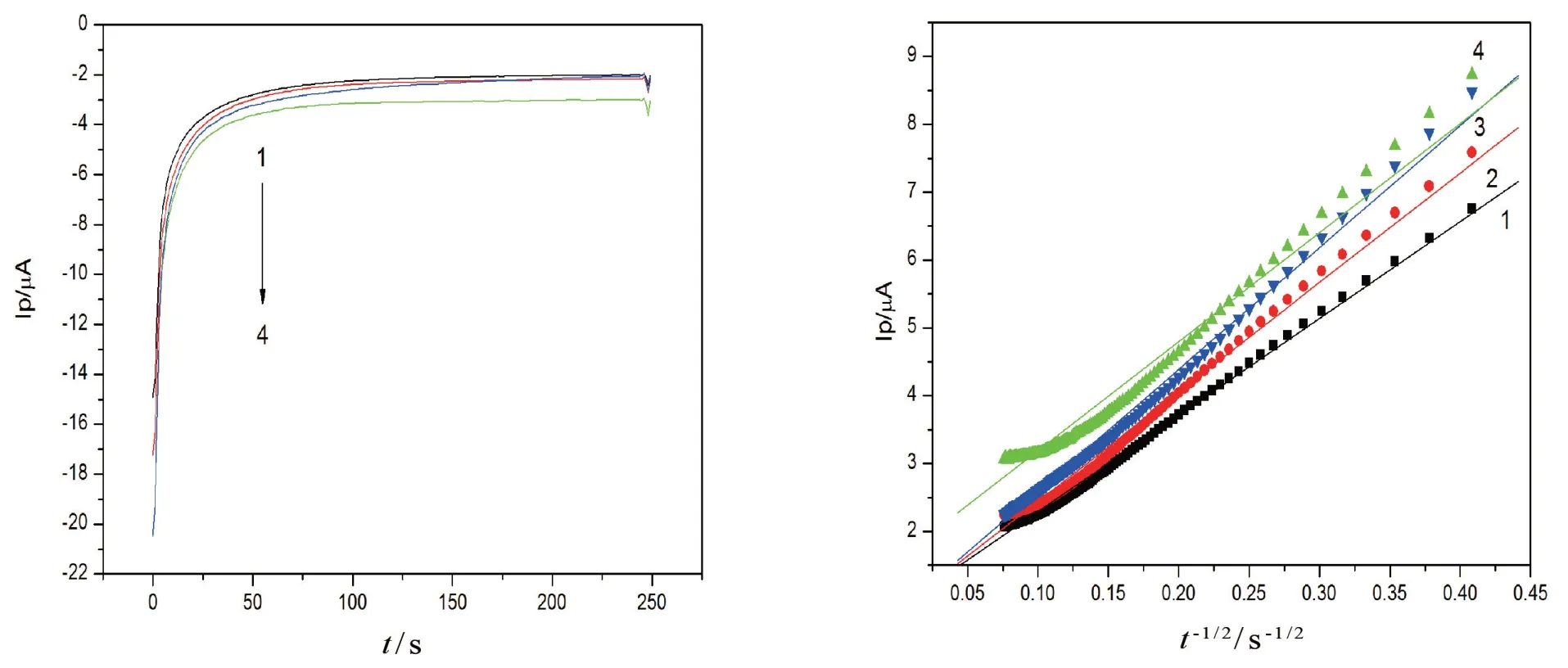
图5 对苯二酚在4种电极上的计时电流曲线以及I~t-1/2关系曲线
2.3.5 不同浓度对苯二酚的循环伏安曲线
采用循环伏安法,在上述最佳优化条件下,对不同浓度的对苯二酚进行扫描. 扫描的最优电位范围为0.0~0.6 V,在底液酸度pH值为1.0的磷酸盐缓冲溶液中,静置100 s后,以0.12 V·s-1的扫描速率进行扫描,测定结果如图6所示. 实验结果显示,在4.00×10-6~4.00×10-4mol·L-1范围内呈现良好的线性关系,线性方程见表2.2.3.6 精密度及稳定性

表2 测定对苯二酚的线性范围、回归方程以及相关系数
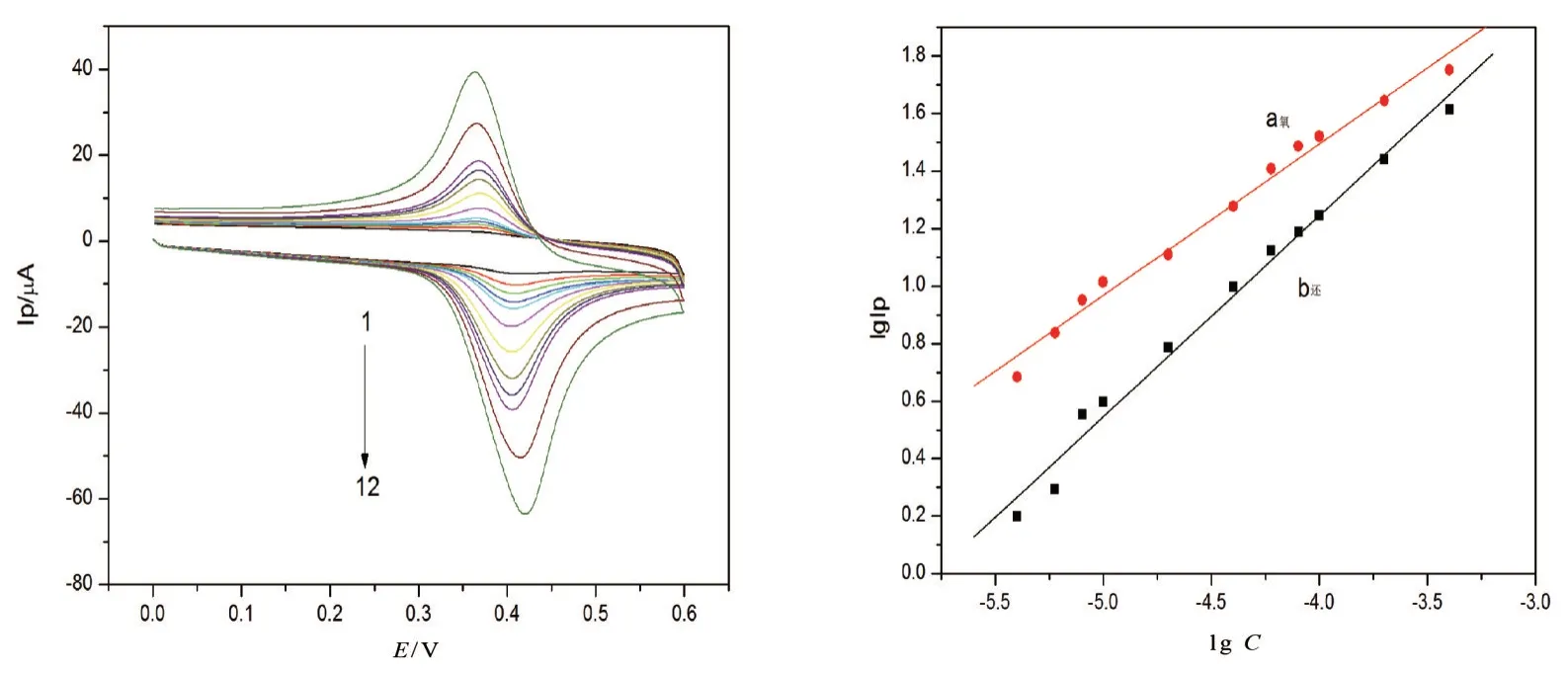
图6 不同浓度对苯二酚的循环伏安曲线及线性关系图
将浓度为1.00×10-4mol·L-1对苯二酚溶液在最佳条件下进行10次平行实验,计算所得RSD为3.4%.测定结果显示,聚L-谷氨酸/石墨烯修饰电极的测定具良好的精密度. 室温下,将聚L-谷氨酸/石墨烯修饰电极放置15 d,在条件不变情况下重复上述实验进行测定,峰电位和峰电流基本上处于稳定状态,未发生明显偏差,由此证明聚L-谷氨酸/石墨烯修饰电极具有很好的稳定性.
2.4 干扰离子实验
在上面实验测得的最佳实验条件下,误差不超过±5%的范围内,研究测定一些共存离子对1.00×10-4mol·L-1对苯二酚的干扰. 结果显示:1 000倍的Ni+、NH4+、Mn2+、Cd2+、Co2+、Ag、IO4-、CO32-;200倍的Pb2+、Zn2、+Cl-;100倍的Al3+;10倍的苯酚、邻苯二酚均不干扰测定.
2.5 样品分析
取污水样品,加入浓度不相同的对苯二酚,采用标准加入法,测定污水中对苯二酚的浓度,测定结果如表3所示.
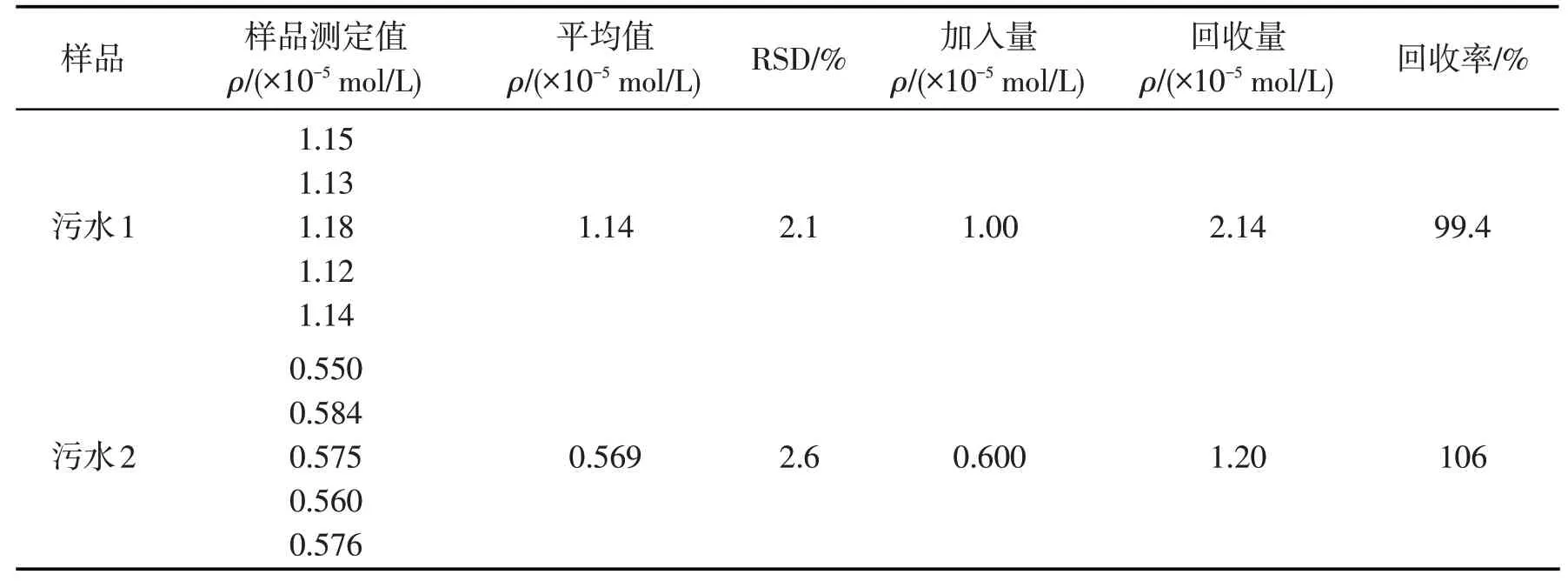
表3 污水样品中对苯二酚(HQ)的分析结果
3 结论
本实验利用循环伏安法制备聚L-谷氨酸/石墨烯修饰电极,并以此修饰电极为工作电极对对苯二酚的电化学行为进行研究. 根据实验结果得知,聚L-谷氨酸/石墨烯修饰电极显著提高对苯二酚的电催化活性,且电极有较强的稳定性,实验结果令人满意.

