二烷基二硫代氨基甲酸酯钼和银配合物的合成与结构表征
张彩霞,方多文,钱冰峯,贾爱铨,张千峰
(安徽工业大学分子工程与应用化学研究所,安徽马鞍山243002)
过渡金属硫化物在自然界中广泛存在,其具有酶的催化活性,可参与多相催化过程[1-2]。在共面结构中硫原子可与金属离子发生相互作用,形成稳定的金属硫化物。二烷基二硫代氨基甲酸酯(DTC)[3]是常见的含硫配体,具有一定的还原性,且廉价易得。自Akerstrom(1959)首次描述DTC与过渡金属银(Ag)形成配合物以来[4],这类含Ag S键的配合物在发光材料等领域受到广泛关注[5-6]。DTC上取代烷基的不同以及反应条件的变化,可导致生成不同结构的配合物[7-8]。过渡金属钼(Mo)配合物的合成方法大致为两种途径:将金属氧化到更高的氧化态;在不改变金属氧化态的情况下,将作为配体的DTC直接活化成可配位螯合的硫化物[9]。对于不同结构的过渡金属硫化物,结构差异会导致其催化活性、光致发光特性等性质有所不同。因此,采用不同方法合成更多结构的过渡金属硫化物,对开发更高效的催化剂和发光材料具有重要意义。鉴于此,文中将过渡金属银和钼作为研究对象,将其与不同结构的DTC 在不同条件下反应得到两种配合物,即单核Mo[S2CN(iPr)2]4PF6(1)和Ag6[S2CN(nPr)2]6(2),利用紫外-可见吸收光谱、X 射线单晶衍射表征配合物1和2的结构,为探索更多的应用前景提供依据。
1 实验部分
1.1 试剂与仪器
三氧化钼、硝酸银、六氟磷酸购自Alfa Aesar 化学试剂有限公司,其他试剂购自中国上海国药化学试剂有限公司,使用前均采用常规蒸馏方法对试剂进行纯化和脱气。Na(iPr-DTC)和Na(nPr-DTC)采用文献[10]中描述的方法制备。
实验仪器为Perkin-Elmer 2400 CHN元素分析仪、Bruker SMART APEX 2000 CCD 面探测衍射仪、岛津UV-2600紫外可见分光光度计。
1.2 配合物的合成
1.2.1 配合物Mo[S2CN(iPr)2]4PF6
氮气条件下,将二异丙胺(4.86 g,0.05 mol)和乙醇(8 mL)置于100 mL的圆底烧瓶,冰水浴下,先后逐滴缓慢加入CS2(3.8 g,0.05 mol)和配制好的NaOH(2 g,0.05 mol)水溶液。反应液在0 ℃搅拌4 h后得到淡黄色溶液,后加入20 mL正己烷并充分震荡,至有白色沉淀析出,过滤干燥即得Na(iPr-DTC)。取适量Na(iPr-DTC)(0.16 g,0.8 mmol)作为配体与HPF6(0.17 g,1.5 mmol)和MoO3(30 mg,0.2 mmol)在脱氧乙腈(20 mL)中加热回流5 h。冷却至室温,用旋转蒸发仪浓缩溶液体积约至2 mL,乙醚重结晶得到红棕色固体,过滤,用乙醚洗涤固体3次,干燥,在乙腈/乙醚的液相扩散体系中得到适合于单晶衍射的红黑色块状晶体Mo[S2CN(iPr)2]4PF6(1)。
产量65 mg,产率35%。分子式为Mo[S2CN(iPr)2]4PF6,元素分析理论值(质量分数,%)为C 35.51,H 0.16,N 0.14;实测值(质量分数,%)为C 35.24,H 0.18,N 0.12。
1.2.2 配合物Ag6[S2CN(nPr)2]6
用上述方法制备Na(nPr-DTC)。取适量的Na(nPr-DTC)(0.20 g,1.0 mmol)溶于脱氧乙腈(15 mL),搅拌条件下缓慢加入AgNO3(0.17 g,1.0 mmol)的甲醇溶液,室温搅拌30 min,形成淡黄色溶液。用旋转蒸发仪浓缩溶液体积约至2 mL,用乙醚重结晶得到淡黄色固体,过滤、用乙醚洗涤3次、干燥,在二氯甲烷/正己烷的液相扩散体系中得到适合于单晶衍射的淡黄色块状晶体Ag6[S2CN(nPr)2]6(2)。
产量89 mg,产率32%。分子式为Ag6[S2CN(nPr)2]6,元素分析理论值(质量分数,%)为C 28.64,H 0.15,N 0.22;实测值(质量分数,%)为C 28.21,H 0.18,N 0.25。
1.3 配合物结构的测定
采用Bruker SMART APEX 2000 CCD 面探测衍射仪测定配合物1和2的晶体结构。选取尺寸合适且透光度良好无裂缝的晶体,采用封管法以稍微倾斜的角度将晶体固定在毛玻璃管顶端并用凡士林封口,Mo−Kα射线为光源(λ=0.071 073 nm),由装有影像板面的探测器收集衍射数据,测试温度为(296±2)K。晶体结构数据可采用直接法或重原子法解得,收集的单晶衍射点数据由SAINT程序还原,再使用SADABS程序进行经验吸收校正,采用基于F2的全矩阵最小二乘法用SHELXTL软件包进行精修[11]。非氢原子均经各向异性修正,氢原子坐标采用理论加氢得到。
将配合物1和2配制成10-4mol/L的乙腈溶液,采用岛津UV-2600紫外可见分光光度计测定配合物的紫外-可见光谱。
2 结果与讨论
图1 为二烷基二硫代氨基甲酸酯钼/银配合物的合成路线。DTC 作为配体与过渡金属银和钼在不同条件下生成相应的配合物,其中Na(iPr-DTC)与三氧化钼以乙腈为溶剂,加热回流5 h 后生成钼配合物Mo[S2CN(iPr)2]4PF6(1),需要注意的是三氧化钼在反应前需用六氟磷酸进行质子化处理。而Na(nPr-DTC)和硝酸银在乙腈中室温下反应30 min就可得到银簇合物Ag6[S2CN(nPr)2]6(2)。
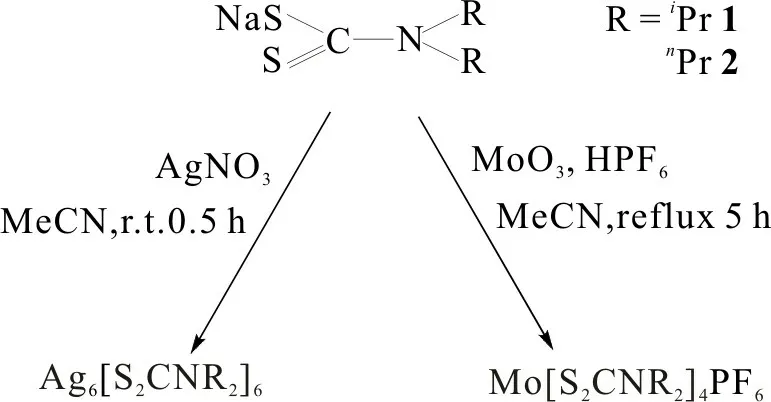
图1 配合物1和2的合成路线Fig.1 Synthetic route of complexes 1,2
2.1 配合物的晶体数据
表1为配合物1和2的晶体数据。由表1可看出:配合物1属于单斜晶系,长为1.690 nm,宽为0.769 nm,高为1.905 nm,晶体密度为1.271 g·cm-3,结晶在P2/n 空间群且单胞个数为2,是一种离子型配合物,包含Mo[S2CN(iPr)2]4+阳离子和一个六氟磷酸根阴离子;配合物2属于三斜晶系,长为1.138 nm,宽为1.237 nm,高为1.292 nm,晶体密度为1.713 g·cm-3,结晶在P-1 空间群且单胞个数为1,是一种分子型配合物。

表1 配合物1和2的晶体数据Tab.1 Crystallographic data of complexes 1,2
2.2 配合物的晶体结构
图2 为钼配合物的分子结构。由图2 可看出:4个二乙胺基硫代甲酸根的8个S原子在Mo周围组成十二面体,中央离子Mo采取4d45s15p8杂化轨道与配体成键;8 个S 原子和Mo 并非是独立的单齿配位,而是4 个双齿硫螯合配位;两个包含S(1),S(2),S(1A),S(2A)原子的配体位于同一平面(标准偏差,0.005 nm),与另外两个配体包含S(3),S(4),S(3A),S(4A)原子(标准偏差,0.004 nm)定义的平面接近垂直(89.3°),这两个平面之间的夹角接近正十二面体的 理 想 值(90°),与 配 合 物[Mo(S2CNMe2)4]+[9],[Ta(S2CNMe2)4]+[12],[Re(S2CN(CH3)2)4][Cl][13]等结构相似。由表2可知:Mo—S的平均键长约0.251 nm,二异丙胺基二硫代甲酸根中一对S 原子S(1)与S(6)之间的距离与十二面体的价键方向及Mo—S键长相匹配;S—C 键的平均键长为0.171 nm,低于正常值0.182 nm,反映S—C 键中有共轭双键成分;Mo—S—C 键角的平均值为91.4°,表明S 原子以纯的p轨道与相邻原子形成化学键;C—N键的平均键长为0.132 nm,低于正常值0.148 nm,此键介于单双键之间,表明N原子上的孤对电子参与共轭体系;Mo S的平均键长约0.251nm,这与文献[9]中报道的类似。

图2 配合物1的分子结构Fig.2 Molecular structure of complex 1
图3为配合物2的分子结构。由图3可看出:配合物2中,存在理想的三重对称轴,3个双重对称轴均垂直于三倍轴,且将整个分子一分为二[7];配合物2由两个类似环己烷的Ag3S3环组成,银原子位于一个扭曲的八面体顶点,每个银原子均与二丙基二硫代氨基甲酸酯配体中的3个硫原子配位。S原子有两种类型:[S(1),S(3),S(5),S(1A),S(3A),S(5A)],在末端仅与一个银原子配位;[S(2),S(4),S(6),S(2A),S(4A),S(6A)],在两个Ag原子之间起桥梁作用。由表2可知:Ag—S平均键长为0.251 nm;两个分别由3个Ag和3个S原子形成的六元环通过6个Ag—Ag键连接在一起,平均键长为0.297 nm,比Ag的金属键(0.289 nm)长,但仍比两个Ag原子的范德华半径之和(0.344 nm)短[14],这意味着它们之间的相互作用较弱。另一方面,螯合配体充当夹子,将两个六元环与单配位硫原子S(1),S(3)和S(5)(及其对称等价物)结合在一起,这也是两个六元环能够紧密接触的原因[15]。

图3 配合物2的分子结构Fig.3 Molecular structure of complex 2
2.3 配合物的紫外-可见光谱
图4 为配合物1和2的紫外-可见光谱(UVvis)。图4表明,配合物1在300 和450 nm处有吸收峰,配合物2仅在300 nm处有吸收峰。配合物1和2在300 nm 处的最大吸收峰为配体到过渡金属的特征峰(LMCT 跃迁),配合物1在450 nm 处的吸收峰可归属于Mo—S键电子跃迁的结果,为过渡金属到配体的特征峰(MLCT跃迁),表征双齿型的4个巯基阴离子与过渡金属钼配位螯合。

图4 配合物1和2的紫外-可见吸收光谱Fig.4 UV-vis absorption spectra of complex 1,2
3 结 论
将三氧化钼和硝酸银分别与DTC 在不同条件反应,合成配合物Mo[S2CN(iPr)2]4PF6(1) 和Ag6[S2CN(nPr)2]6(2),通过X射线单晶衍射和紫外-可见吸收光谱对配合物1和2的结构进行表征,所得主要结论如下:
1) 配合物1是一种离子型配合物,包含Mo[S2CN(iPr)2]4+阳离子和一个六氟磷酸根阴离子,属于单斜晶系,结晶在P2/n空间群、单胞个数为2;配合物2是一种分子型配合物,属于三斜晶系,结晶在P-1空间群、单胞个数为1。
2)配合物1为由以钼原子为中心周围连接8个S原子形成的十二面体结构;配合物2为由两个类环己烷Ag3S3六元环组成的六核结构。
3)配合物1在乙腈溶液中的紫外吸收光谱在300,450 nm处有吸收峰;配合物2在乙腈溶液中的紫外吸收光谱在300 nm处有吸收峰。

